Содержание статьи
Введение
Подагра — системное аутовоспалительное тофусное заболевание, которое характеризуется отложением кристаллов моноурата натрия в тканях и развитием в связи с этим воспаления у лиц с гиперурикемией, обусловленной внешнесредовыми и/или генетическими факторами [1, 2]. Важнейшим компонентом терапии подагры является прием уратснижающих препаратов, рациональное и длительное применение которых направлено на достижение и поддержание уровня урикемии ниже определенных значений, что является основой полного контроля над заболеванием, включающего отсутствие приступов артрита и связанной с заболеванием боли, полное рассасывание имеющихся в организме отложений кристаллов уратов и предотвращение образования новых [3, 4].
Любые действующие рекомендации по лечению подагры непременно включают положение о необходимости достижения целевого уровня мочевой кислоты (МК) сыворотки крови. Этот уровень определен как величина <360 мкмоль/л для всех пациентов и <300 мкмоль/л для пациентов с тяжелой подагрой (наличие подкожных и/или внутрикостных тофусов, хронического артрита, подагрической артропатии) как в национальных, так и в некоторых зарубежных и межнациональных рекомендациях [5–9]. Достижение целевых уровней МК, таким образом, считается основной целью лечения и базовым методом оценки эффективности терапии, поскольку отражает постепенное рассасывание кристаллов уратов, включая тофусы, снижение частоты острых приступов подагрического артрита вплоть до их полного исчезновения [10–14]. Препаратом первой линии терапии подагры, как постулируют все основные рекомендации [5–9, 15], является ингибитор ксантинксидазы аллопуринол, который, исходя из длительного в сравнении с другими уратснижающими средствами опыта его применения, доказанной эффективности [12, 16, 17], предполагаемого кардиопротективного действия [18, 19] и экономической целесообразности [20], рассматривают в качестве препарата первой линии терапии подагры [21].
Максимально допустимая доза аллопуринола весьма высока — 900 мг/сут, однако в клинической практике дозы выше 300 мг/сут назначаются редко, что осложняет реализацию таргетного принципа терапии подагры [22]. Более того, насколько оправдан метод титрования дозы аллопуринола до максимально возможной, практически не изучено; и даже в сравнительных исследованиях применяемые дозы препарата, как правило, не превышали 300 мг/сут, предопределяя относительно редкое (36–42%) достижение целевого уровня МК при использовании низких доз препарата [23–25]. При этом одной из причин плохого контроля над заболеванием считается неоптимальная лекарственная, прежде всего уратснижающая, терапия [26].
Цель исследования: определение вероятности достижения целевого уровня МК сыворотки крови у пациентов с подагрой при последовательном титровании дозы препарата до максимально возможной в соответствии со стратегией «лечение до цели».
Материал и методы
В одноцентровом проспективном 6-месячном исследовании эффективности аллопуринола при назначении в соответствии со стратегией «лечение до цели» приняли участие 78 пациентов с подагрой, наблюдаемых в ФГБНУ НИИР им. В.А. Насоновой в период с января 2017 г. по январь 2021 г.
Критерии включения:
установленный диагноз подагры (критерии ACR/EULAR 2015) [27];
возраст старше 18 лет;
уровень МК сыворотки крови >360 мкмоль/л;
неиспользование уратснижающих препаратов на момент включения в исследование;
наличие двух и более приступов артрита за последний год;
подписанная форма информированного согласия.
Критерии невключения:
наличие любых других ревматических заболеваний, характеризующихся воспалительным артритом, включая системные заболевания соединительной ткани, спондилоартриты, другие микрокристаллические артриты;
наличие соматических или психических заболеваний, препятствующих выполнению процедур исследования;
расчетная скорость клубочковой фильтрации (рСКФ) <30 мл/мин/1,73 м2;
наличие противопоказаний к приему аллопуринола, перечисленных в инструкции по медицинскому применению, включая аллергические реакции и реакции гиперчувствительности [28], а также анамнестические данные о нежелательных явлениях и/или неэффективности предшествующего приема аллопуринола, по мнению врача и/или пациента;
двукратное превышение верхней границы нормативного показателя уровней трансаминаз (АЛТ и АСТ) крови, печеночная недостаточность;
злокачественные новообразования в анамнезе в течение предшествующих 5 лет;
потребность в назначении терапии любым другим препаратом, снижающим уровень МК, помимо аллопуринола;
отказ от приема уратснижающей терапии.
Исследование проведено в соответствии с Хельсинкской декларацией и одобрено локальным этическим комитетом.
Всем включенным в исследование пациентам инициировали терапию аллопуринолом в начальной дозе 100 мг 1 р/сут, каждые 2–3 нед. проводилось измерение сывороточного уровня МК крови, при сохранении уровня МК выше целевого дозу увеличивали на 100 мг/сут вплоть до достижения целевого уровня МК, при необходимости титрование дозы проводилось до максимально допустимой — 900 мг/сут. У пациентов с наличием ХБП 3-й степени (рСКФ в пределах 30–59 мл/мин/1,73 м2) максимальная доза аллопуринола составила 300 мг/сут. У пациентов с подагрой, характеризующейся наличием подкожных тофусов, целевой уровень МК сыворотки крови был принят за величину <300 мкмоль/л, у остальных пациентов — <360 мкмоль/л.
По достижении целевого уровня МК титрование дозы прекращали, и пациент принимал препарат в подобранной дозе вплоть до завершения исследования. Через 6 мес. от начала приема препарата вновь проводилось исследование сывороточного уровня МК с целью определения стабильности достигнутого результата (целевого уровня МК сыворотки). Период наблюдения за каждым пациентом составил 6 мес. (26 нед.) непрерывного применения аллопуринола.
В качестве профилактики приступов артрита препаратом выбора был колхицин в дозе 0,5 мг/сут, при противопоказаниях и/или плохой переносимости — НПВП в минимальной эффективной противовоспалительной дозе, при их непереносимости или наличии противопоказаний — глюкокортикоиды (преднизолон 7,5 мг/сут). Выбор конкретного препарата проводился индивидуально, с учетом имеющихся противопоказаний к длительному применению этого препарата. Пациенты, у которых развились непереносимость или нежелательные явления при приеме одного препарата, могли перейти на прием другого лекарственного средства или полностью прекратить профилактический прием.
Лабораторные исследования включали в себя определение уровня МК, АЛТ, АСТ и креатинина на каждом визите. На первом и последнем визитах проводились общий анализ крови, общий анализ мочи, ЭКГ. СКФ рассчитывалась по формуле CKD-EPI — креатинин (eGFR, Estimated Glomerular Filtration Rate, CKD-EPI creatinine equation).
Первичной конечной точкой было достижение целевого уровня МК сыворотки при применении аллопуринола путем титрования до максимально возможных доз (первичную конечную точку определяли у всех пациентов, включенных в исследование). Вторичными конечными точками являлись влияние проводимой терапии аллопуринолом на показатели, отражающие функцию почек и печени, и эффективность терапии через 6 мес. от начала исследования, также определяемая при помощи вычисления доли пациентов с целевым уровнем МК (вторичные конечные точки определяли у пациентов, завершивших исследование).
Статистический анализ осуществляли с помощью пакета прикладных программ Statistica 12.0 (StatSoft Inc., США) описательной статистики. Результаты представлены в виде средних значений и средних квадратичных отклонений (М±δ) для количественных признаков, имеющих нормальное распределение, в остальных случаях — в виде медианы и интерквартильного интервала (Ме [25-й; 75-й перцентили]). Для сравнения признаков двух зависимых групп использовали тест Вилкоксона. Различия считали статистически значимыми при р<0,05.
Результаты исследования
Исходная клиническая характеристика включенных в исследование пациентов с подагрой представлена в таблице 1.
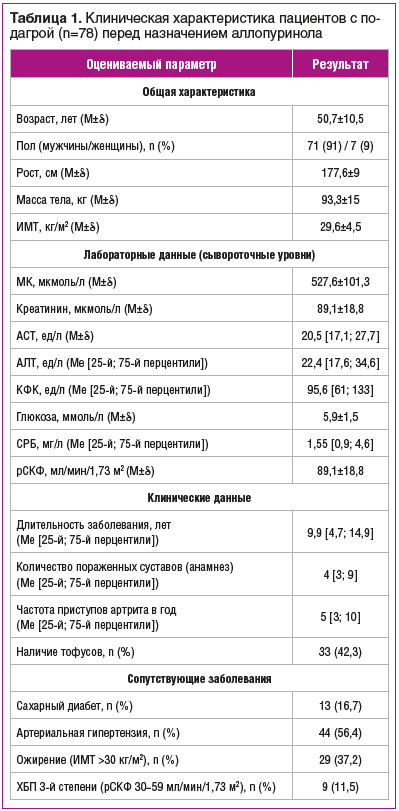
Уровень МК <360 мкмоль/л был определен как целевой для 45 (57,7%) пациентов, уровень <300 мкмоль/л — для 33 (42,3%) пациентов.
У 9 (11,5%) из 78 пациентов с наличием ХБП 3-й степени (рСКФ в пределах 30–60 мл/мин/1,73 м2) максимально используемая доза аллопуринола составила 300 мг/сут.
В процессе титрования дозы аллопуринола целевой уровень МК был достигнут у 67 (86%) из 78 пациентов. По мере увеличения дозы аллопуринола число пациентов, достигших искомого уровня МК сыворотки, проспективно увеличивалось (см. рисунок). В дальнейшем доза аллопуринола оставалась неизмененной в течение всего оставшегося периода исследования, при этом уровень МК сыворотки от момента завершения титрования дозы препарата вплоть до завершающего визита не определялся.
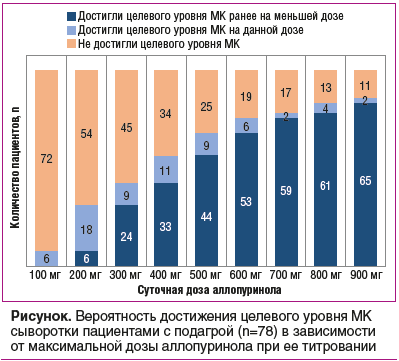
Так, за время наблюдения из исследования были исключены 7 (9%) из 78 пациентов. В 3 случаях пациенты были исключены по причине прекращения приема аллопуринола в связи с развитием нежелательных реакций: у 2 пациентов — аллергической реакции по типу крапивницы при приеме аллопуринола в дозах 100 и 300 мг/сут (в обоих случаях симптомы быстро и полностью регрессировали на фоне приема антигистаминных препаратов) и у одного пациента было зафиксировано увеличение сывороточного уровня креатинина (166 мкмоль/л) и снижение рСКФ <30 мл/мин/1,73 м2 (доза аллопуринола на этот момент составляла 200 мг/сут). Четыре пациента не явились на запланированные визиты и также были выведены из исследования. При этом все 67 пациентов, у которых в процессе титрования дозы был достигнут целевой уровень МК сыворотки, завершили исследование.
Таким образом, исследование завершил 71 пациент, все они были обследованы через 6 мес. от начала приема аллопуринола. Из них вторичная конечная точка (сохранение целевого уровня МК сыворотки) была достигнута у 52 (73%), т. е. сывороточный уровень МК оставался в пределах установленных нормативных значений на момент завершающего визита (6 мес. от начала терапии).
У 15 (22%) из 67 пациентов, достигших целевого уровня МК, уровень МК на момент завершающего визита превысил целевой, хотя и был ранее достигнут в процессе титрования дозы аллопуринола. Дозы аллопуринола на момент прекращения титрования (при достижении целевого уровня МК сыворотки) у этих пациентов распределились следующим образом: 100 мг/сут — 1 пациент, 200 мг/сут — 3 пациента, 300 мг/сут — 1 пациент, 400 мг/сут — 2 пациента, 500 мг/сут — 2 пациента, 600 мг/сут — 1 пациент, 700 мг/сут — 1 пациент, 800 мг/сут — 3 пациента и 900 мг/сут — 1 пациент. Пять из 15 указанных пациентов принимали на момент прекращения титрования низкие дозы препарата (≤300 мг/сут), еще 5 пациентов — средние (400–600 мг/сут) и оставшиеся 5 пациентов — высокие (700–900 мг/сут). Таким образом, возможность эскалации дозы препарата оставалась у 14 из тех 15 пациентов, у которых исходно целевой уровень МК был достигнут, однако на момент окончания исследования уровень МК вновь превышал целевой.
У 5 (56%) из 9 пациентов с рСКФ в пределах 30–59 мл/мин/1,73 м2 к концу исследования сывороточный уровень МК соответствовал целевому, причем в 6 из 9 случаев отмечалось значимое увеличение рСКФ до величин, превышающих 60 мл/мин/1,73 м2 (табл. 2).
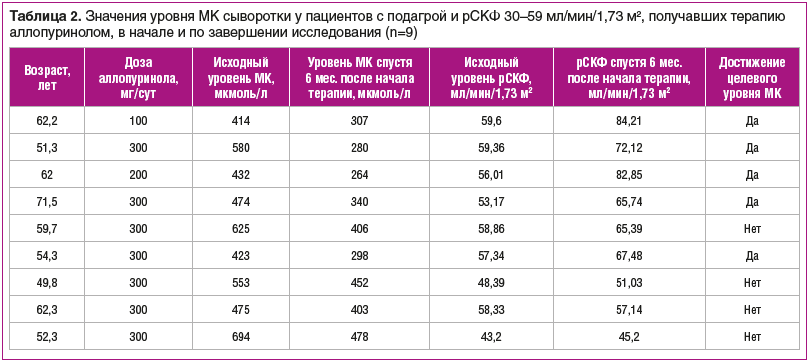
Также у завершивших исследование пациентов (n=71) было отмечено снижение среднего сывороточного уровня креатинина и увеличение медианы уровня АСТ, не имевшее клинического значения. Средние значения рСКФ не изменились (табл. 3).
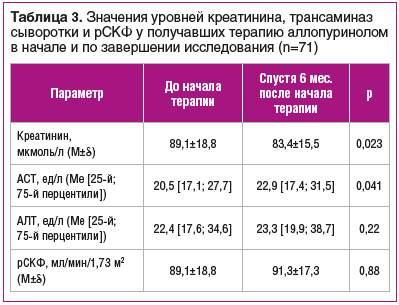
Прием высоких доз (700–900 мг/сут) аллопуринола пациентами с подагрой (n=14) также не приводил к значимым изменениям исследуемых показателей (табл. 4).
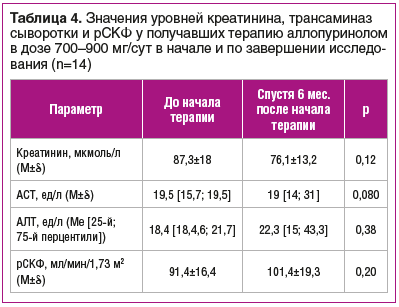
Ни у одного пациента, независимо от принимаемой дозы аллопуринола, сывороточные уровни АСТ и АЛТ не достигли двукратного превышения верхней границы нормы.
Обсуждение
Хотя аллопуринол используется для лечения подагры на протяжении более полувека и признан препаратом первой линии уратснижающей терапии, значительная часть пациентов, его принимающих, не достигают необходимого уровня МК сыворотки, что предопределено использованием низких доз, тогда как данные об эффективности высоких (>600 мг/сут) и средних (400–600 мг/сут) доз аллопуринола весьма ограничены [29–31]. Еще меньше данных о практическом применении методики индивидуального подбора дозы аллопуринола путем постепенной ее эскалации, но и в этом случае используемая суточная доза, как правило, не превышает 600 мг/сут [32], тогда как инструкцией лимитировано назначение значительно большей дозы (>900 мг/сут) [5]. В российской популяции проспективные исследования, посвященные изучению возможности практического применения высоких доз аллопуринола пациентами с подагрой, до настоящего момента вовсе не проводились. Данная работа является одной из немногих проспективных работ, где одновременно проводились и титрование дозы препарата до максимально возможной, и последовательная оценка достижения целевого уровня МК исходя из существующих рекомендаций.
Главный результат нашей работы — подтверждение того, что таргетное лечение аллопуринолом, осуществляемое в полном соответствии с действующими федеральными рекомендациями, позволяет реализовать желаемую цель терапии у большинства пациентов с подагрой [5]: первичная конечная точка была достигнута у 86% из включенных в исследование пациентов, причем почти у половины из них целевой уровень МК, исходя из тяжести подагры, был определен как величина <300 мкмоль/л, а не <360 мкмоль/л, что является отличительной особенностью нашего исследования.
В настоящий момент есть данные всего двух рандомизированных контролируемых исследований, в которых сравнивали эффективность стратегии «лечение до достижения цели» с лечением подагры без определенного уровня МК, которого необходимо добиться [32, 33]. В одном из них приняли участие 517 пациентов, из которых 255 пациентов основной группы получали терапию под наблюдением медицинской сестры строго в соответствии с таргетным принципом терапии (в качестве первой линии терапии назначался аллопуринол 100 мг/сут, доза которого увеличивалась каждые 3–4 нед. в зависимости от концентрации уратов сыворотки, вплоть до максимальной — 900 мг 1 р/сут; при недостижении целевого уровня МК (<360 мкмоль/л) вместо аллопуринола назначался фебуксостат в дозе 80 мг/сут (при необходимости доза увеличивалась до 120 мг/сут) или бензбромарон в дозе 50 мг/сут (с возможным титрованием до 200 мг/сут) [33]. Остальные 262 пациента получали терапию под руководством врача общей практики, без строгого контроля. При строгом контроле за терапией через 2 года от начала лечения продолжали получать уратснижающие препараты 96% пациентов, тогда как в группе сравнения — только 47% пациентов. И в основной группе, и в группе сравнения наиболее часто применяемым препаратом был аллопуринол (84% и 96% пациентов соответственно). То есть, практически как и в нашем случае (86% пациентов), у 84% пациентов основной группы подобная терапия была достаточной для достижения целевого уровня МК сыворотки, при этом у 80% из них доза препарата была больше 300 мг/сут (в среднем — 460 мг/сут). Оставшиеся 16% принимали либо фебуксостат (14%), либо, крайне редко (2%), урикозурики, и ни одному из пациентов не потребовалась комбинированная терапия (ингибитор ксантиноксидазы + урикозурик), что крайне важно, так как и монотерапия урикозуриками, и комбинированное лечение (ингибитор ксантиноксидазы + урикозурик) в РФ затруднительны по причине отсутствия зарегистрированных в нашей стране препаратов этой группы.
Таким образом, данные M. Doherty et al. [33] показали, что даже спустя 2 года от начала терапии при должном контроле у 95% пациентов сывороточный уровень МК можно поддерживать на уровне меньшем, чем 360 мкмоль/л, тогда как таковых в группе сравнения было всего 30% (отношение рисков 3,18, 95% доверительный интервал 2,42–4,18). В сопоставимом по времени проведения отечественном исследовании доля пациентов, которые поддерживали сывороточный уровень МК в указанном пределе и в большинстве своем воздерживались от динамического наблюдения у ревматолога и, следовательно, от титрования дозы аллопуринола, также была низкой, составив всего 24% [34]. Достижение желаемой цели лечения в случае неэффективности аллопуринола, применяемого в максимальных дозах, или при наличии противопоказаний к его использованию возможно при назначении фебуксостата, по нашим данным, почти в ¾ от всех случаев [35], что подтверждает оптимальное как с точки зрения клинической практики, так и с точки зрения медико-экономического анализа применение подобной схемы терапии (эскалация дозы аллопуринола с последующей заменой на фебуксостат при неэффективности первого) [20, 33]. Наконец, интересным результатом работы M. Doherty et al. [33] было отсутствие нарастания частоты нежелательных явлений при титровании дозы аллопуринола у пациентов со сниженной функцией почек, что согласуется с результатами исследования L.K. Stamp et al. [32]: титрование, при необходимости, дозы аллопуринола до 600 мг/сут при умеренном снижении рСКФ не привело к увеличению частоты нежелательных эффектов, связанных с приемом аллопуринола, но увеличило долю пациентов, достигших и длительно, на протяжении периода наблюдения поддерживающих целевой уровень МК сыворотки, более чем в 2 раза (с 32% до 69%). В нашей работе мы сознательно лимитировали дозу аллопуринола у пациентов с рСКФ<60 мл/мин/1,73 м2, учитывая возможные риски токсико-аллергических реакций [36], однако по результатам наблюдения у 5 из 9 таких пациентов проводимая терапия способствовала улучшению показателя, что, во-первых, косвенно подтверждает возможность нефропротективного действия аллопуринола при подагре [37], а во-вторых, позволяет вкупе с отсутствием иных нежелательных эффектов рассматривать в перспективе возможность дальнейшего нарастания суточной дозы препарата вплоть до достижения целевого уровня МК сыворотки. Последний постулат находит подтверждение и в крупном исследовании LASSO, основной задачей которого было изучение безопасности применения различных доз аллопуринола пациентами с подагрой (n=1735) при ежемесячных визитах [38]. Исследователям рекомендовали (но не требовали) титровать дозу препарата до достижения уровня МК сыворотки <360 мкмоль/л. Анализ проводился в 3 группах: принимавших аллопуринол в дозе <300 мг/сут (таковых было 14,4%), в дозе 300 мг/сут (большинство (65,4%) принимало препарат в указанной дозе) и в дозе >300 мг/сут (20,2% пациентов, причем 1,1% пациентов принимали препарат в дозе ≥700 мг/сут). Вероятность частоты нежелательных явлений и обусловленной ими отмены препарата была обескураживающей: доза до 300 мг/сут вызывала нежелательные явления у 15,2%, доза 300 мг/сут — у 9,5%, доза >300 мг/сут — у 11,4%. Частота нежелательных явлений, приведших к отмене аллопуринола или выводу из исследования, — 10,8, 3,6 и 1,7% соответственно. То есть вероятность нежелательных явлений не нарастала с увеличением дозы препарата, а вероятность прекращения терапии и вовсе снижалась. В нашем случае у всех 4 пациентов, которым пришлось отменить аллопуринол, нежелательные реакции развивались при приеме низких доз препарата, что, как и нарастающая в зависимости от дозы аллопуринола вероятность достижения целевого уровня МК крови, согласуется с данными исследования LASSO. Тем более не понятны опасения исследователей, участвующих в LASSO, легко титровавших суточную дозу аллопуринола до 300 мг, но редко назначавших бóльшие дозы.
Доступность терапии аллопуринолом в РФ максимально высока: аллопуринол независимо от фирмы-производителя входит в число жизненно важных препаратов, что предопределяет его низкую стоимость. Помимо аллопуринола, выпускаемого отечественными производителями, в РФ также зарегистрирован и доступен препарат Милурит® (Венгрия), единственный европейский аллопуринол в нашей стране, опыт применения которого исчисляется десятилетиями.
Заключение
Таким образом, результаты нашего исследования позволяют сделать очевидный вывод о высокой эффективности применения аллопуринола в качестве первой линии терапии подагры путем титрования дозы согласно стратегии «лечение до цели». Учитывая, что у части пациентов с уже подобранной дозой аллопуринола при динамическом наблюдении было зафиксировано повышение сывороточного уровня МК выше лимитированного, целесообразно оценивать уровень МК в динамике и тогда, когда целевой уровень МК достигнут. Следует констатировать также, что вероятность отмены аллопуринола из-за развития нежелательных явлений низка и не зависит от принимаемой дозы препарата. Источник финансирования
Работа выполнена в рамках научной темы № 0397-2020-0007 «Оптимизация методов симптоматической противовоспалительной терапии у пациентов с микрокристаллическими артритами (подагра, болезнь депонирования кристаллов пирофосфата кальция)».
Информация с rmj.ru






