Введение
Инфекции мочевыводящих путей (ИМП) — одно из самых часто встречающихся заболеваний и требующих особо-го внимания при ведении беременных. Распространенность ИМП у беременных достигает 10%: бессимптомной бактериурии (ББ) — 2–10% [1], острого цистита — 1–2% [2], острого пиелонефрита — 1% [3]. При этом в 80% наблюдений ИМП регистрируют во II триместре беременности (на сроке 22–28 нед.), реже — в III и I триместрах [4].
При беременности существенно возрастает риск развития заболеваний почек, что обусловлено нарушениями уродинамики в верхних мочевыводящих путях по мере увеличения размеров матки и снижения тонуса и амплитуды сокращений мочеточников начиная со II триместра беременности вследствие воздействия прогестерона и простагландинов на их рецепторы [5].
Таким образом, нарушения уродинамики могут иметь место в течение всего гестационного периода, родов и послеродового течения. И хотя адаптивные изменения мочевыделительной системы начинаются в ранние сроки беременности и продолжаются на протяжении всего гестационного периода, достигая максимума перед родами, ряд факторов могут способствовать возникновению ИМП:
повышение почечного кровотока (50–80%) и клубочковой фильтрации до 30–50%;
задержка выделения натрия, воды, солей;
снижение тонуса и перистальтики мышц мочевыводящих путей;
повышение нагрузки (обеспечивается выведение продуктов обмена и матери и плода);
механическое сдавление мочевыводящих путей, снижение скорости продвижения мочи;
увеличение рН мочи, глюкозурия, протеинурия (до 0,3 г/л);
увеличение мочеточника в диаметре, преимущественно в верхней и средней трети, чаще справа;
удлинение мочеточника, приобретение извилистой формы;
тенденция к неполному опорожнению мочевого пузыря;
развитие цистоуретрального рефлюкса;
повышение экскреции кальция и скорости клубочковой фильтрации [6].
«Инфекция мочевыводящих путей» — общий термин, связанный с инфекцией мочевого тракта, начиная с мочеиспускательного канала и заканчивая почками.
Риск развития цистита увеличивается в период беременности, и его пик приходится на ІІ триместр. Циститы во время беременности часто ассоциируются с различными осложнениями, влияющими на течение беременности. Преэклампсия возникает в 35–42% случаев, отслойка плаценты — в 5% случаев, часто (до 66% случаев) развивается анемия беременных, риск преждевременных родов возрастает в 1,5–2 раза [5, 7, 8]. Отдельные авторы считают, что ИМП, вызвавшие развитие указанных осложнений, не всегда сопровождаются выраженными клиническими симптомами [9]. В отечественных клинических рекомендациях ББ рассматривается, наряду с острым циститом и пиелонефритом, в числе основных нозологических форм ИМП у беременных [10]. Согласно результатам ряда исследований, проведенных в разных странах, частота ББ у беременных варьирует от 2% до 10% [9, 11].
В связи с этим лечению цистита во время беременности в современном акушерстве уделяется особое внимание. Общепринятым лечением ИМП, в т. ч. и ББ,
у беременных является антибактериальная терапия [10]. А с учетом патогенетических факторов на протяжении беременности возможны рецидивы, которые требуют многократного использования антибактериальной терапии. Потому актуален поиск альтернативных путей терапии и профилактики циститов во время беременности. На сегодняшний день безопасность фитотерапии делает привлекательным ее применение в акушерстве, где приоритетом является безвредность препарата для плода и матери [12].
В настоящее время в комплексной терапии и профилактике ИМП широко применяются препараты, содержащие в своем составе экстракт клюквы. В плодах клюквы содержатся фруктоза и проантоцианидины, которые связываются с белками на фимбриях E. coli, препятствуя адгезии бактерий на эпителиальной выстилке мочевыводящих путей [13, 14].
Биологически активная добавка (БАД) к пище Цистениум II («Аквион», Россия) в форме таблеток, содержащая экстракт плодов клюквы (Vaccinium oxycoccos), D-маннозу и витамин С, оказывает противомикробное, противовоспалительное, спазмолитическое и диуретическое действие, снижает риск обострений хронического цистита, улучшает функциональное состояние почек и мочевыводящих путей, способствует нормализации мочеиспускания и уменьшению почечных отеков. Входящий в состав Цистениума II моносахарид D-манноза препятствует адгезии бактерий к уротелию мочевого пузыря за счет увеличения клиренса бактерий с мочой [15, 16]. БАД Цистениум II разрешена беременным и детям старше 7 лет [17].
Цель исследования: оценить эффективность БАД Цистениум II в комплексной противомикробной терапии острого и рецидивирующего цистита в стадии обострения и ББ у беременных.
Материал и методы
В исследовании приняли участие 65 беременных с ИМП, 5 из которых были в I триместре, 22 и 38 соответственно во II и III триместрах, в возрасте от 21 до 43 лет (средний возраст 24,5±4,3 года). Из них было сформировано 3 группы. Первую группу составили 22 пациентки с острым циститом и обострением хронического цистита, 2-ю группу — 20 беременных с ББ (диагностически значимый титр для острой, рецидивирующей ИМП и ББ — более 103 КОЕ/мл). Контрольную группу составили 23 беременные (средний возраст 22,8±3,2 года) с острым циститом и обострением хронического рецидивирующего цистита, а также с ББ.
Критерии включения: беременность; верифицированный диагноз острого цистита или хронического рецидивирующего цистита в стадии обострения, ББ; подписанное информированное согласие на участие в программе.
Критерии невключения: тяжелая сопутствующая соматическая патология; злокачественные новообразования; тяжелые аллергические реакции или указание на развитие тяжелых нежелательных реакций на лекарственные препараты в анамнезе; злоупотребление алкоголем; гиперчувствительность к компонентам БАД; противопоказания к применению БАД Цистениум II.
Пациентки 1-й и 2-й групп получали комплексное лечение, которое включало антимикробную терапию фосфомицина трометамолом в дозе 3 г, а также БАД Цистениум II по 1 таблетке 2 р/сут во время еды в течение 14 дней. Все беременные контрольной группы получали только стандартную терапию (фосфомицина трометамол в дозе 3 г однократно). Всем пациенткам на первом визите выполняли УЗИ почек для исключения обструкции верхних мочевыводящих путей и выраженного гидронефроза.
Общее соматическое состояние пациенток, данные общего анализа мочи и бактериологическое исследование мочи оценивали через 14 дней и через 2 мес. после начала лечения.
Статистическую обработку данных проводили с помощью программы Statistica 6.0. Различия между показателями считали статистически значимыми при р≤0,05.
Результаты исследования
Все пациентки с клиникой ИМП отметили положительную динамику на фоне проводимого лечения. Однако у получавших монотерапию фосфомицина трометамолом полное исчезновение симптомов цистита наступало на 4–5-е сутки от начала приема препарата. В то же время у женщин, получавших комплексную терапию с включением Цистениума II, клиническое улучшение (исчезновение симптомов) отмечено на 2-е и 3-и сутки.
Через 14 дней после начала лечения количество лейкоцитов в общем анализе мочи снизилось до нормы у пациенток всех трех групп. Эрадикацию возбудителя констатировали у 77,3% пациенток 1-й группы, 70% пациенток 2-й группы и 61% пациенток 3-й группы (р<0,05; табл. 1).
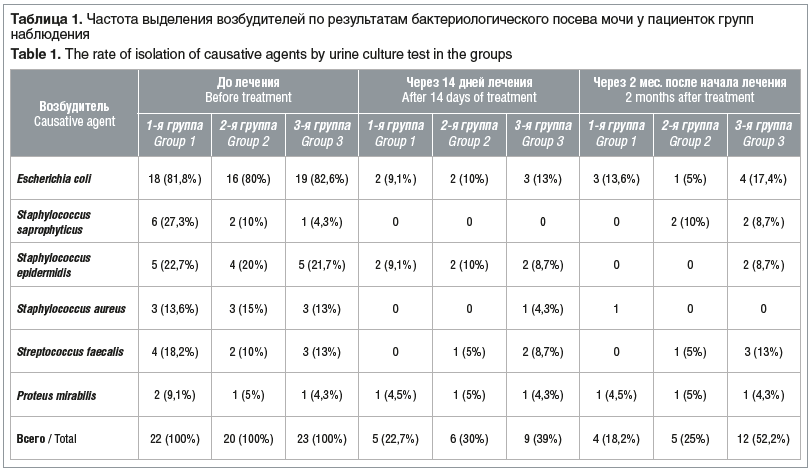
В основных группах (1-й и 2-й) в 2-месячный срок наблюдения (у некоторых женщин до полного вынашивания беременности, включая послеродовой период) признаки обострения хронического цистита были выявлены у 3 (13,6%) из 22 пациенток, ББ — у 2 (10%) из 20 пациенток, и лишь у 1 (4,5%) пациентки из 1-й группы развился острый пиелонефрит (р<0,05; см. табл. 1).
Несмотря на достигнутый ранее положительный эффект лечения, у 6 (26%) пациенток 3-й, контрольной, группы клинически констатировали обострение цистита в 2-месячный срок наблюдения, а у 4 (17,4%) пациенток течение болезни осложнилось острым пиелонефритом. При этом показатели содержания лейкоцитов и микроорганизмов в моче у пациенток 3-й группы также статистически значимо (р<0,05) превышали аналогичные данные у первых двух групп.
Переносимость Цистениума II все пациентки оценили как хорошую. Побочных реакций на фоне приема не было.
Обсуждение
Подготовка женщины с рецидивирующей ИМП к беременности предусматривает тщательное урологическое и гинекологическое обследование с целью выявления риска рецидивов во время беременности [9]. Профилактика развития и лечение ИМП занимают важное место в медицинской программе наблюдения за беременными и требуют комплексного подхода. В комплекс мер по профилактике ИМП у беременных могут быть включены:
прием жидкости не менее 1,2–1,5 л/сут (при нормальном диурезе);
обеспечение ежедневного опорожнения кишечника;
клюквенный, брусничный морсы;
применение про- и пребиотиков, например лактулозы, для нормализации биоценоза кишечника [18].
В настоящее время в научной литературе имеется множество публикаций, посвященных лечению ИМП у женщин с использованием фитопрепаратов, про- и пребиотиков [19–24]. При этом отмечается их высокая эффективность, сопоставимая с эффективностью антибиотикотерапии. С учетом того, что при беременности, особенно в ранние сроки, применение антибиотиков крайне нежелательно, использование фитопрепаратов с сопоставимым противомикробным эффектом является вполне обоснованной альтернативой при лечении ИМП.
Согласно результатам нашего исследования использование Цистениума II в терапии цистита, а также ББ у беременных не только повысило успешность лечения, но и способствовало поддержанию достигнутого эффекта.
Целесообразность включения Цистениума II в комплекс мер по профилактике и лечению ИМП в период беременности обусловлена его воздействием на основные звенья патогенеза за счет активных компонентов, обладающих противовоспалительным, спазмолитическим и диуретическим действием. Проантоцианидины, содержащиеся в экстракте плодов клюквы, препятствуют адгезии микробов на поверхности уротелия мочевого пузыря, моносахарид D-манноза увеличивает клиренс бактерий с мочой. Положительные результаты применения Цистениума II в отношении эрадикации возбудителя подкреплены данными проведенных бактериологических исследований мочи на флору (см. табл. 1).
Таким образом, применение Цистениума II позволило уменьшить количество повторных курсов антибактериальной терапии в период беременности за счет снижения частоты рецидивов мочевой инфекции, а также снижения числа случаев осложненного течения ИМП.
Удобство применения Цистениума II (таблетки допустимо разжевывать), отсутствие побочных эффектов, принадлежность к фитотерапевтическим средствам — эти характеристики способствуют повышению комплаентности беременных.
Выводы
Отмечена высокая терапевтическая эффективность БАД Цистениум II, которая составила 81,9% у беременных с острым циститом и обострением рецидивирующего цистита и 90% у беременных с ББ (контрольная группа показала эффективность 56,5%).
Полученные данные о клинической и бактериологической эффективности препарата, а также отсутствие побочных эффектов указывают на целесо-
образность широкого клинического применения БАД Цистениум II в комплексной терапии острого и рецидивирующего цистита, а также ББ у беременных.
Результаты исследования позволяют рекомендовать Цистениум II в комплексном лечении беременных с ИМП как средство, способствующее снижению бактериальной обсемененности мочи. За счет поддержания микробной чистоты мочевыводящих путей повышается эффективность профилактики рецидивов ИМП.
Сведения об авторах:
Нашивочникова Наталья Алексеевна — к.м.н., доцент кафед-
ры урологии им. Е.В. Шахова ФГБОУ ВО «ПИМУ» Минздрава России; 603950, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; ORCID iD 0000-0002-1138-1174.
Крупин Валентин Николаевич — д.м.н., профессор, заведующий кафедрой урологии им. Е.В. Шахова ФГБОУ ВО «ПИМУ» Минздрава России; 603950, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; ORCID iD 0000-0002-4887-4888.
Леанович Виктория Егурбиевна — медицинский директор АО «Аквион»; 123112, Россия, г. Москва, Пресненская наб., д. 8, стр. 1; ORCID iD 0000-0001-7653-797Х.
Контактная информация: Нашивочникова Наталья Алексеевна, e-mail: dom17.doctor@mail.ru. Прозрачность финансовой деятельности: исследование выполнено при поддержке АО «Аквион». Конфликт интересов: Леанович Виктория Егурбиевна является сотрудником АО «Аквион». Статья поступила 17.03.2021, поступила после рецензирования 08.04.2021, принята в печать 23.04.2021.
About the authors:
Natal’ya A. Nashivochnikova — Cand. of Sci. (Med.), associate professor of E.V. Shakhov Department of Urology, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky sq., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0002-1138-1174.
Valentin N. Krupin — Doct. of Sci. (Med.), Professor, Head of E.V. Shakhov Department of Urology, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky sq., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0002-4887-4888.
Viktoriya E. Leanovich — medical director of JSC “Akvion”; 8 build. 1, Prechistenskaya emb., Moscow, 123112, Russian Federation; ORCID iD 0000-0001-7653-797Х.
Contact information: Natal’ya A. Nashivochnikova, e-mail: dom17.doctor@mail.ru. Financial Disclosure: the study was supported by JSC “Akvion”. Conflict of interest: Viktoriya E. Leanovich is an employee of JSC “Akvion”. Received 17.03.2021, revised 08.04.2021, accepted 23.04.2021.
.
Информация с rmj.ru





