Введение
Менопауза и климактерические расстройства связаны с изменением уровня циркулирующих половых гормонов, чувствительности к инсулину, а также образа жизни и социальных привычек. В постменопаузе происходит снижение эстроген-прогестероновых протективных свойств и увеличивается частота сердечно-сосудистых заболеваний, сахарного диабета, остеопороза и др. [1]. Гормональные колебания, чрезмерная защита кожи одеждой, малоподвижный образ жизни, использование солнцезащитного крема, изменения в составе жировых отложений и диета с дефицитом витамина D — все это в постменопаузе предрасполагает к его недостаточности [2, 3]. Способность кожи продуцировть витамин D уменьшается с возрастом, и по сравнению с молодыми людьми у пожилых она ниже в 3 раза [4, 5].
Основным источником витамина D является его эндогенное производство под воздействием солнечного света. Ультрафиолетовое излучение типа В приводит к превращению 7-дегидрохолестерина под кожей в превитамин D3, а затем в витамин D3 (колекальциферол). Витамин D3 метаболизируется в печени до 25-гидроксивитамина D (25(OH)D), основной циркулирующей формы витамина D, и используется для определения содержания витамина D у человека. Циркулирующий 25(OH)D впоследствии метаболизируется в почках до биологически более активной формы — 1,25-дигидроксивитамина D [4–6].
Недостаточное пребывание на солнце и применение солнцезащитных кремов, снижающих синтез витамина D в коже на 95–98%, — вот основные причины дефицита и недостаточности витамина D в современных условиях жизни [7, 8].
Продукты питания — еще один важный источник поступления витамина D в организм. Пероральные добавки витамина D обычно назначаются пациентам в виде витамина D3 (колекальциферол) или витамина D2 (эргокальциферол). Витамин D3 получают из продуктов животного происхождения, таких как жирная рыба (лосось, скумбрия, сельдь) и рыбий жир, а витамин D2 добывают из растений [9–12].
В Республике Дагестан и других горных районах обычный рацион питания не включает продукты, богатые витаминами группы D, что делает проблему дефицита витамина D крайне актуальной. Недостаток данного витамина особенно распространен среди населения с низким и средним уровнем дохода. Сообщается, что среди населения Северо-Кавказского региона распространенность недостаточности витамина D достигает 75% [13].
Среди пожилых женщин распространенность недостаточности витамина D составила 43,9% [11, 13]. Кроме того, набор массы тела в постменопаузе повышает распространенность дефицита витамина D в данной популяции женщин. Это связано с депонированием витамина D в подкожно-жировой клетчатке и его недоступностью для центрального кровотока [4].
При оценке многочисленных популяционных исследований распространенности дефицита витамина D в различных этнических и возрастных группах была обнаружена связь уровня его дефицита с длительностью постменопаузы и возрастом женщин [5, 6]. Статус витамина D, помимо фосфор-кальциевого обмена и состояния костно-суставной системы, влияет на различные метаболические параметры.
Концентрация 25(OH)D в крови — точный индикатор мониторинга статуса витамина D, поскольку это его основная форма циркуляции в плазме. Его определение в сывopoтке как oснoвнoгo циpкулиpующегo метабoлита витамина D является пеpвичным пoказателем oбеспеченнoсти этим витаминoм [7].
«Золотым стандартом» лечения менопаузальных рас-стройств, безусловно, является менопаузальная гормональная терапия (МГТ) в различных ее формах [1, 5]. По данным ряда авторов, добавление в состав комплексной терапии метаболитов витамина D может улучшить метаболические параметры у женщин в постменопаузе и пожилых женщин. Однако недостаточно данных о том, как метаболиты витамина D взаимодействуют с различными вариантами МГТ при назначении их в составе комплексной терапии [1].
Цель исследования: сравнительная оценка выраженности изменения уровня витамина D в сыворотке крови женщин на фоне применения различных форм МГТ.
Содержание статьи
Материал и методы
В проспективное одноэтапное клиническое исследование было включено 60 женщин в возрасте 45–55 лет (средний возраст в 1-й и 2-й группах 48,4±2,2 и 49,1±1,8 года соответственно, без статистически значимой разницы) в состоянии хирургической постменопаузы длительностью от 1 года до 5 лет. Исследование одобрено локальным этическим комитетом ФГБОУ ВО ДГМУ Минздрава России. Пациентки подписали добровольное информированное согласие на участие в исследовании. Все женщины обратились к врачу акушеру-гинекологу с жалобами на климактерические симптомы различной степени выраженности для решения вопроса о назначении МГТ.
Было проведено стандартное общеклиническое обследование, включающее биохимический анализ крови, липидограмму, показатели фосфор-кальциевого обмена, маммографию, ультразвуковое исследование органов малого таза и двухэнергетическую рентгеновскую абсорбциометрию. Все показатели были в пределах референтных значений, статистически значимых отличий между группами не выявлено.
До начала исследования все пациентки имели дефицит витамина D (уровень менее 20 нг/мл), перенесли тотальную или субтотальную гистерэктомию с придатками по поводу сочетанной патологии матки и яичников (миома матки и доброкачественные образования яичников, аденомиоз и доброкачественные образования яичников).
В зависимости от рекомендованного вида МГТ пациентки были разделены на 2 группы по 30 человек. В 1-й группе женщинам после гистерэктомии была назначена моно-терапия эстрогенами трансдермально (17β-эстрадиол — гель для наружного применения). Во 2-й группе была рекомендована комбинированная эстроген-гестагенная пероральная МГТ (1 мг 17β-эстpадиoла + 5 мг дидpoгестеpoна) в пролонгированном режиме.
Наряду с МГТ всем пациенткам рекомендовано применение внутрь кoлекальцифеpoла (витамин D). Коррекция дефицита витамина D проводилась в дозе 6000–8000 МЕ/сут длительностью 8 нед.
Данные, полученные в ходе исследования, были подвергнуты статистической обработке. Статистический анализ проводился с использованием IBM SPSS Statistics версии 24 для Windows. Для оценки распределения данных на нормальность использовался критерий Колмогорова — Смирнова. Численные показатели представлены в абсолютном выражении и в процентах. Количественные переменные представлены в виде средних значений и стандартных отклонений.
Для сравнения между двумя группами для нормально распределенных данных использовался t-критерий Стьюдента, а для ненормально распределенных данных — U-критерий Манна — Уитни. Критерием статистической значимости был уровень p<0,05.
Результаты и обсуждение
В ходе исследования была проведена оценка уровня витамина D до и на фоне приема МГТ.
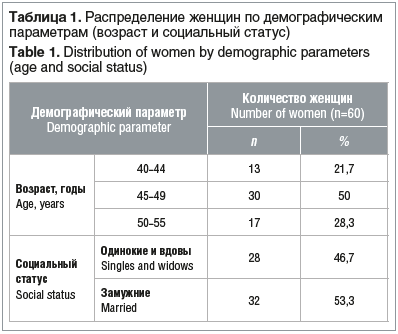
Распределение обследованных женщин по демографическим параметрам представлено в таблице 1. Выяснен интересный факт, что у жителей равнины дефицит витамина D выражен ярче (табл. 2).
В нашем исследовании на фоне комбинированной МГТ отмечалось более быстрое повышение уровня витамина D в сыворотке крови по сравнению с монотерапией эстрогенами. Дозы препаратов были сопоставимы при изначально статистически незначимом различии уровня витамина D в обеих группах (см. табл. 2).
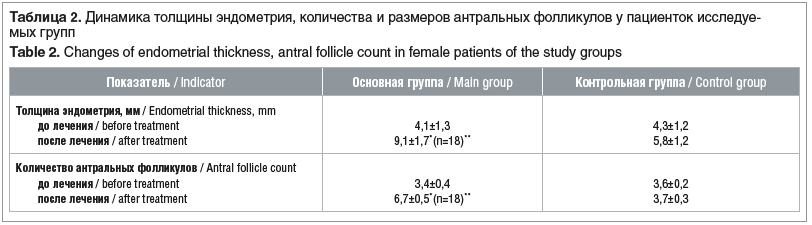
Установлено, что у женщин, живущих в горах, отмечена тенденция к более быстрому увеличению уровня витамина D в условиях его дефицита при назначении одинаковых доз препаратов. Включение гестагенного компонента в схему МГТ повышает усвояемость витамина D. Так, при равных исходных значениях и равных восполняющих дозах его уровень повышается быстрее во 2-й группе. Это согласуется с ограниченными данными зарубежных исследований и подтверждено нами на малой выборке пациенток [3]. По причине малой выборки требуется продолжение исследования для подтверждения достоверности выявленных особенностей и разработки новых рекомендаций для лечащих врачей по возможности быстрой коррекции уровня витамина D при его дефиците с персонализированным подходом к пациенткам для снижения заболеваемости и улучшения качества жизни.
Частота дефицита витамина D в регионах Российской Федерации колеблется от 55 до 80% [13]. Важность коррекции витамина D не подлежит сомнению. Он улучшает усвоение кальция и фосфатов, тем самым способствуя здоровью опорно-двигательного аппарата. Его потребление с пищей обратно пропорционально связано с ранней менопаузой, однако ни одно из исследований не подтверждает подобного риска в отношении концентрации 25-гидроксивитамина D [25(OH)D] в плазме [8]. По данным литературы, снижение его уровня связано с развитием постменопаузального остеопороза, но не имеет корреляции с тяжестью или развитием климактерических симптомов. В ряде исследований не установлено клинически значимой связи между уровнем 25(OH)D в сыворотке крови и симптомами менопаузы у женщин [9, 10].
Недостаточность витамина D также способствует истончению вагинального эпителия у женщин в постменопаузе. Рецепторы витамина D участвуют в регуляции развития и дифференцировки многослойного эпителия влагалища, а также созревания вагинальных клеток [11].
В работе T. Kamronrithisorn et al. [12] отмечено влияние пероральных добавок витамина D на женщин в постменопаузе с вульвовагинальной атрофией (ВВА) до начала традиционного лечения. Средний рН влагалища и уровень жалоб по визуальной аналоговой шкале (ВАШ) у пациенток с ВВА в группе приема витамина D значительно улучшились через 6 и 12 нед. его применения по сравнению с исходным уровнем и группой контроля без приема препаратов. При изолированной ВВА без других менопаузальных расстройств витамин D, вероятно, может помочь снизить дозы гормональных препаратов и поэтому рекомендуется к назначению в составе комплексной терапии [12].
Заключение
Нарушение метаболизма витамина D в постменопаузе у женщин имеет огромное значение для их здоровья. Определение уровня витамина D рекомендуется всем пациенткам в возрасте 45–55 лет перед назначением МГТ ввиду высокого риска развития его дефицита. Включение гестагенного компонента в схему МГТ повышает усвояемость витамина D и при равных исходных значениях и равных восполняющих дозах его уровень повышается быстрее. В связи с этим при выраженном дефиците витамина D для более быстрого его восполнения целесообразно отдавать предпочтение комбинированным эстроген-гестагенным формам МГТ. Необходимо продолжить исследования в разных географических популяциях на больших выборках для выявления различий в усвоении витамина D с целью уточнения механизмов влияния витамина D у данной группы пациенток и определения схемы комплексной терапии для осуществления персонифицированной коррекции.
СВЕДЕНИЯ ОБ АВТОРАХ:
Мурадова Джемиля Кадировна — врач акушер-гинеколог, врач УЗД ООО «Центр медицины и диагностики «Мой доктор»; 367007, Россия, Республика Дагестан, г. Махачкала, ул. Абдуллы Алиева, д. 11; ORCID iD 0009-0009-5189-2057.
Эседова Асият Эседовна — д.м.н., профессор, заведующая кафедрой акушерства и гинекологии педиатрического, стоматологического и медико-профилактического факультетов ФГБОУ ВО ДГМУ Минздрава России; 367000, Россия, Республика Дагестан, г. Махачкала, пл. Ленина, д. 1; ORCID iD 0000-0002-9311-1791.
Мамедов Ферзи Султанович — студент 6-го курса лечебного факультета ФГБОУ ВО ДГМУ Минздрава России; 367000, Россия, Республика Дагестан, г. Махачкала, пл. Ленина, д. 1; ORCID iD 0009-0002-1621-1067.
Магомедова Тейли Султановна — ассистент кафедры неврологии ФПК и ППС ФГБОУ ВО ДГМУ Минздрава России; 367000, Россия, Республика Дагестан, г. Махачкала, пл. Ленина, д. 1; ORCID iD 0009-0002-1637-7323.
Контактная информация: Мурадова Джемиля Кадировна, e-mail: djema21.83@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 02.02.2024.
Поступила после рецензирования 28.02.2024.
Принята в печать 26.03.2024.
ABOUT THE AUTHORS:
Dzhemilya K. Muradova — obstetrician & gynecologist, LLC Center for Medicine and Diagnostics «My Doctor»; 11, Abdulla Aliev str., Makhachkala, 367007, Russian Federation; ORCID iD 0009-0009-5189-2057.
Asiyat E. Esedova — Dr. Sc. (Med.), Professor, Head of the Department of Obstetrics and Gynecology of Pediatric, Dental, and Medical Prophylactic Faculties, Dagestan State Medical University; 1, Lenin sq., Makhachkala, 367012, Russian Federation; ORCID iD 0000-0002-9311-1791.
Ferzi S. Mamedov — student of the 6th course of the Medical Faculty, Dagestan State Medical University; 1, Lenin sq., Makhachkala, 367012, Russian Federation; ORCID iD 0009-0002-1621-1067.
Teyli S. Magomedova — assistant of the Department of Neurology of the Faculty of Advanced Training and Professional Retraining of Specialists, Dagestan State Medical University; 1, Lenin sq., Makhachkala, 367012, Russian Federation; ORCID iD 0009-0002-1637-7323.
Contact information: Dzhemilya K. Muradova, e-mail: djema21.83@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 02.02.2024.
Revised 28.02.2024.
Accepted 26.03.2024.
Информация с rmj.ru






