Введение
Сердечно-сосудистые заболевания (ССЗ) — ведущая причина смертности в мире [1]. Ключевой задачей здравоохранения является своевременное выявление пациентов с наличием кардиоваскулярного риска и проведение соответствующих профилактических мероприятий. Немало исследований посвящено выяснению механизмов взаимосвязи кардиоваскулярной патологии с аутоиммунными заболеваниями, некоторые из которых представляют собой специфические факторы риска для появления субклинического и клинически значимого атеросклероза. Одним из таких заболеваний является язвенный колит (ЯК) [2]. В рамках гипотез, объясняющих механизмы, лежащие в основе ассоциации ЯК с патологическими состояниями сердечно-сосудистой системы, обсуждаются системное воспаление, нарушение проницаемости кишечного барьера и изменение состава микробиоты кишечника, дисфункция эндотелия, тромбогенный сдвиг показателей системы гемостаза, дисрегуляция иммунной системы, кардиотоксическое действие ряда лекарственных препаратов [3, 4].
Исследования последних лет благодаря развитию и большей доступности методов секвенирования 16s рРНК направили вектор поиска возможных причин развития атеросклероза к изучению кишечной микробиоты (КМ). Рабочая группа Европейского общества кардиологов по коронарной патологии и микроциркуляции обсуждает теорию атеросклеротического микробиома, которая отражает связь атерогенеза с особенностями КМ [5].
Цель исследования: оценить вклад КМ у пациентов с ЯК в формирование кардиоваскулярного риска.
Содержание статьи
Материал и методы
В открытом исследовании методом поперечного среза изучен состав КМ у больных ЯК (n=40), из которых 6 больных имели АГ, у пациентов с ССЗ (n=20) и здоровых добровольцев (n=20). Исследование одобрено этическим комитетом ФГБОУ ВО ОмГМУ Миндрава России (протокол № 6 от 11.05.2023). Все участники исследования подписали добровольное информированное согласие.
Демографические характеристики и индекс массы тела (ИМТ) участников исследования по группам представлены в таблице.
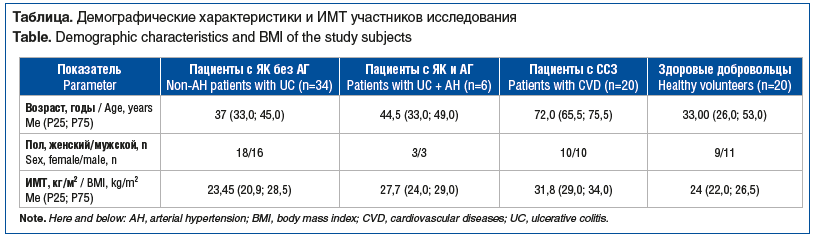
Пациенты с ЯК и ССЗ набраны в исследование из числа госпитализированных в профильные отделения (гастроэнтерологии и кардиологии) БУЗОО «ОКБ». Диагнозы ЯК, ишемическая болезнь сердца (ИБС) и АГ были установлены в соответствии с действующими клиническими рекомендациями[1],[2][6].
Критерии невключения в исследование: возраст младше 18 лет; беременность и период лактации; отказ или отсутствие возможности дать информированное согласие; терапия генно-инженерными биологическими препаратами; участие в клиническом исследовании незарегистрированных лекарственных препаратов; наличие кишечной инфекции, болезни Крона, туберкулеза, онкологических заболеваний и любых других серьезных сопутствующих заболеваний, которые могли исказить результаты исследования.
У пациентов с ЯК установлена по данным колоноскопии протяженность макроскопического поражения (Монреальская классификация): тотальный ЯК у 14 пациентов, левостороннее поражение — у 26. Тяжелая атака заболевания по классификации Truelove — Witts диагностирована у 10 пациентов, атака средней степени тяжести — у 20, легкая — у 10. Все пациенты с ЯК получали стандартную терапию в соответствии со степенью тяжести текущей атаки и локализацией поражения. Гормональная зависимость / резистентность на момент включения в исследование выявлена у 14 больных.
Пациентам с ИБС определен функциональный класс (ФК) стенокардии — ФК II у 5 пациентов, ФК III — у 11, ФК IV — у 4. Нарушение ритма сердца отмечалось у 17 больных: фибрилляция предсердий — у 9, трепетание предсердий — у 1, предсердная экстрасистолия — у 5, желудочковая экстрасистолия — у 3. В анамнезе инфаркт миокарда (ИМ) у 6 пациентов. Реваскуляризация коронарных артерий (чрескожное коронарное вмешательство или аортокоронарное шунтирование) была выполнена у 6 больных. Диа-гноз АГ был установлен у 20 пациентов: 1-я степень — у 2, 2-я — у 12, 3-я степень — у 6. Все больные имели III стадию АГ и 4 (очень высокий) риск сердечно-сосудистых событий.
Оценка таксономического состава и характеристик образцов микробиоты проведена в ООО «Нобиас Технолоджис». Образцы собирали в пробирки с транспортной средой (Nobias Technologies, Россия). Выделение ДНК проводилось с использованием наборов для выделения ДНК из кала с этапами гомогенизации твердотельными микрочастицами и стадией деплеции ингибиторов (Nobias Technologies, Россия). Оценка количества копий гена 16S в растворе выделенной ДНК проводилась с использованием наборов для контроля качества преаналитического этапа метагеномных исследований (Nobias technologies, Россия). Секвенирование полноразмерного гена 16S было выполнено с помощью технологии Oxford Nanopore. Для амплификации полноразмерного гена 16S рРНК были использованы праймеры F27 и R1492 (AGAGTTTGATYMTGGCTCAG и GGTTACCTTGTTAYGACTT соответственно) и амплификатор C1000 (Bio-Rad, США). Очистка полученных ПЦР-продуктов проводилась с использованием магнитных частиц Agencourt AMPure XP (Beckman Coulter In., США). Качество полученных ампликонов оценивали с помощью электрофореза в 1,5% агарозном геле. Дальнейшую подготовку библиотек ампликонов и секвенирование осуществляли с использованием реактивов фирмы NE: репарации одноцепочечных разрывов и концов НК NEBNext FFPE Repair Mix (M6630), NEBNext End repair / dA-tailing Module (E7546) и лигирование адаптеров NEBNext Quick Ligation Module (E6056). Все ферментативно-зависимые (промежуточные) стадии приготовления библиотеки сопровождались необходимой очисткой образца при помощи магнитных частиц Agencourt AMPure XP (Beckman Coulter Inc). Концентрацию полученных библиотек 16S рРНК в растворе измеряли с помощью флуориметра Qubit (Invitrogen, США) с использованием набора для высокочувствительного анализа dsDNA Quant-iTTM (Thermo Fisher Scientific). Очищенные библиотеки смешивали эквимолярно в соответствии с оцененными концентрациями. Секвенирование осуществляли с использованием наборов от производителя Oxford Nanopore Technologies: Ligation Sequencing Kit (SQK-LSK109), Flow Cell Priming Kit (EXP-FLP002) и набора для PCR-free мультиплексирования Native Barcoding Expansion 96 (EXP-NBD196). Секвенирование проводилось на приборе MinION с использованием чипа серии R9 (FLO-MIN106). Для бейзколлинга использовалась программа Guppy (версия 5.1.13), в качестве модели использовался режим High-accuracy basecalling, минимальная отсечка по качеству qscore=7.
Индекс Chao 1 и Shannon использованы для оценки α-разнообразия, данные показатели были вычислены с помощью пакета vegan в среде разработки R [7, 8]. Более высокое значение указанных индексов соответствует большему разнообразию.
Для превалирующих микробов был проведен количественный анализ пропорций — вычислено β-разнообразие — различия в видовом разнообразии КМ между отдельными индивидами [9]. Визуализация β-разнообразия выполнена методом анализа главных координат (PCoA).
Статистический анализ проводился в среде разработки R. Сравнение значений различных характеристик микробиоты и клинических показателей выполнялось с помощью критерия Краскела — Уоллиса. В случае, если различия между группами были статистически значимы (p<0,05), проводилось post-hoc попарное сравнение групп с помощью критерия Манна — Уитни. Для каждого найденного микроба проверялась ипотеза о том, что доля участников с ним во всех группах одинакова (с помощью критерия Фишера с поправкой на множественное сравнение Бенджамини — Хохберга). Далее для микробов, у которых были выявлены достоверные различия (p.adj<0,05), было проведено post-hoc попарное сравнение (критерий Фишера). Данные представлены в виде медианы и 25-го и 75-го процентилей (Ме (P25; P75)).
Результаты исследования
Общее описание микробного сообщества в исследуемых группах
Всего выявлено 485 видов бактерий в образцах кала у всех лиц, которые приняли участие в исследовании (рис. 1).
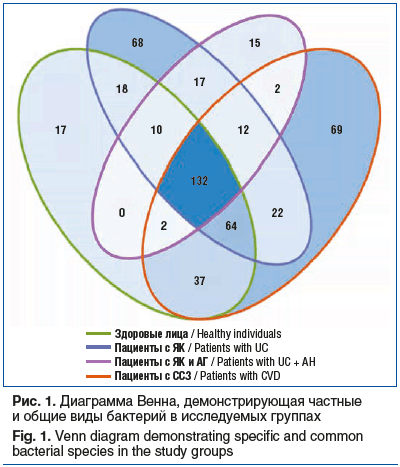
Для общего описания микробного сообщества кишечного содержимого проведено сравнение групп по общепринятым характеристикам микробиоты: α-разнообразию и средней длине генома микробов в образце.
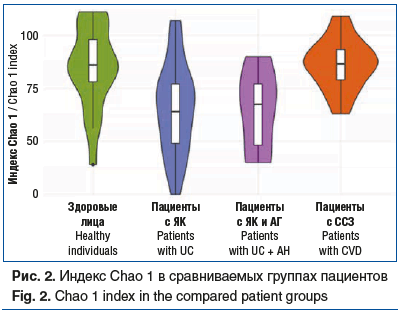
Установили, что Me (P25; P75) индекса Chao 1 у пациентов с ЯК без АГ составила 64 (49; 77), у пациентов с ЯК и АГ — 11,72 (7,14; 55,73), у пациентов с ССЗ — 86,5 (79,0; 93,25), в группе здоровых лиц — 86,0 (78; 98). Ме (P25, P75) индекса Shannon у пациентов с ЯК без АГ составила 3,24 (2,99; 3,53), у пациентов с ЯК и АГ — 3,13 (2,86; 3,32), у пациентов с ССЗ — 3,50 (3,33; 3,65), в группе здоровых лиц — 3,61 (3,07; 3,80).
Распределение индекса Chao 1 в 4 группах представлено на рисунке 2. Выявлены значимые различия в сравниваемых группах (H=12,0, df=3, p=0,00731): между группой здоровых участников и группой больных ЯК (U=477, p=0,002); группой больных ЯК и группой пациентов с ССЗ (U=132,5, p=0,0003); группой больных ЯК и АГ и группой пациентов с ССЗ (U=22, p=0,022), во всех остальных случаях значимых различий не установлено. Таким образом, наименьшее количество различных микроорганизмов в представленных для исследования образцах кала отмечено у пациентов с сочетанием ЯК с АГ.
Распределение индекса Shannon в группах представлено на рисунке 3. Выявлены значимые различия в сравниваемых группах (H=10,5, df=3, p=0,0145): между группой больных ЯК и группой лиц с ССЗ (U=182, p=0,006), пациентов с сочетанием ЯК с АГ и группой больных ССЗ без ЯК (U=19, p=0,011), во всех остальных случаях значимых различий не установлено. Таким образом, показатели α-разнообразия в соответствии со значением индекса Shannon у пациентов с ЯК и АГ также значимо ниже, чем в группах сравнения.
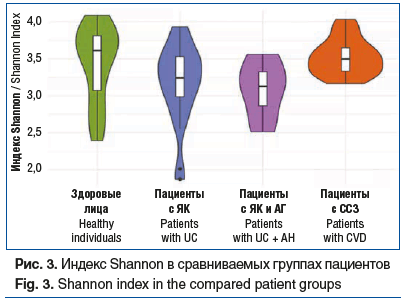
Согласно полученным данным у коморбидных пациентов с сочетанием ЯК с АГ отмечаются более низкие значения показателей α-разнообразия.
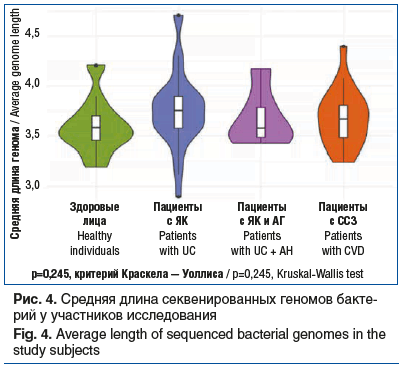
Средняя длина секвенированных геномов значимо не отличалась в группах сравнения (H=4,2, df=3, p=0,245), что показано на рисунке 4.
Соотношение филумов
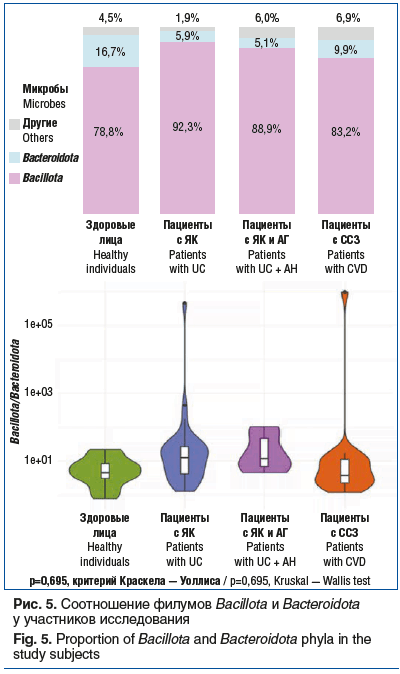
В феврале 2021 г. Международным комитетом по систематике прокариот была пересмотрена классификация и наименование филумов бактерий [10]. На основании молекулярного анализа методом секвенирования 16S рРНК установлено, что микрофлора толстой кишки в основном представлена 6 филумами (типами): до 90% состава микробиоты кишечника составляют Bacillota (ранее Firmicutes) и Bacteroidota (ранее Bacteroidetes), далее в порядке убывания располагаются Actinomycetota, Verrucomicrobiota, Alphaproteobacteriota (ранее Proteobacteria) и Methanobacteriota (ранее Euryarchaeota) [11].
Соотношение двух наиболее представленных филумов — Bacillota и Bacteroidota — часто используют для оценки состояния микробиоты. Согласно данным литературы повышенный индекс Bacillota/Bacteroidota характерен для ВЗК [12, 13]. В нашем исследовании Ме (P25; P75) индекса Bacillota/Bacteroidota у здоровых участников исследования составила 4,47 (3,09; 8,39), у пациентов с ИБС и АГ — 3,72 (2,25; 11,03), в то время как у пациентов с ЯК без АГ показатель составил 12,44 (4,48; 27,53), а у коморбидных пациентов с ЯК и АГ — 11,72 (7,14; 55,73), что выше, чем у участников исследования без ЯК. Однако данное различие статистически незначимо (p=0,695). Соотношение филумов Bacillota и Bacteroidota в группах сравнения представлено на рисунке 5.
Установлены значимые различия в содержании филума Verrucomicrobiota — содержание представителей данного филума было достоверно ниже у пациентов с ССЗ, включая пациентов как с ЯК, так и без ЯК (p<0,001). Наиболее изученным представителем филума Verrucomicrobiota является Akkermansia muciniphila — бактерия, участвующая в поддержании целостности кишечного барьера и модуляции воспаления [14]. В нашем исследовании данная бактерия была одним из наименее представленных таксонов в образцах кала пациентов с ЯК (р<0,001).
Установлено различие в содержании в кале представленности архей Methanobacteriota (р=0,002): их значимо меньшая доля в кале пациентов с сочетанием ЯК и АГ, а также у пациентов с ССЗ без ЯК.
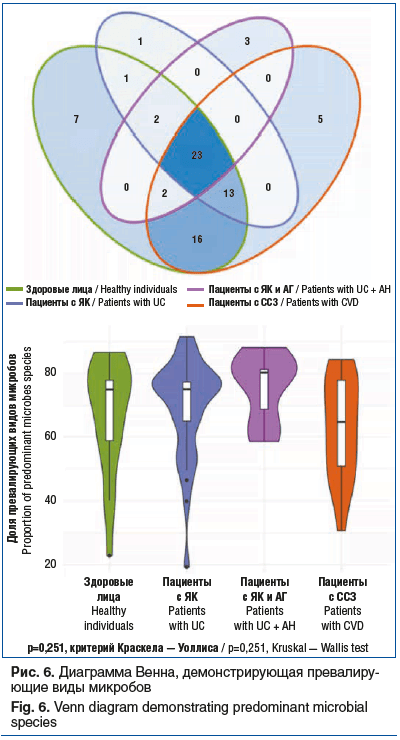
Превалирующие микроорганизмы (встречаются в ≥50% образцов группы): общие и различные
На диаграмме Венна (рис. 6) показано количество превалирующих видов микроорганизмов в группах, различие незначимо (р=0,251).
На рисунке 7 показана визуализация β-разнообразия методом PCoA: образцы участников исследования демонстрируют пространственную близость.
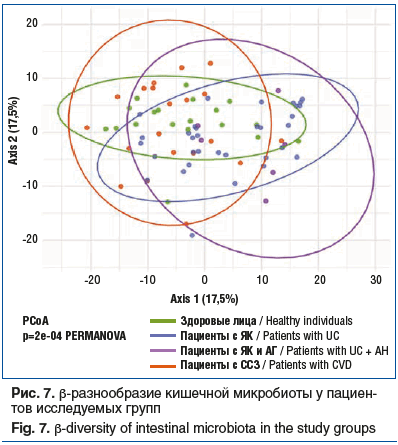
Сравнение с использованием post-hoc теста для PERMANOVA показало, что группа здоровых участников исследования и группа пациентов с ССЗ были схожи по β-разнообразию; группа больных ЯК и группа пациентов с ЯК и АГ также не отличались друг от друга по β-разнообразию. Таким образом, установленное различие было связано только с наличием ЯК у участников исследования (p=0,0002).
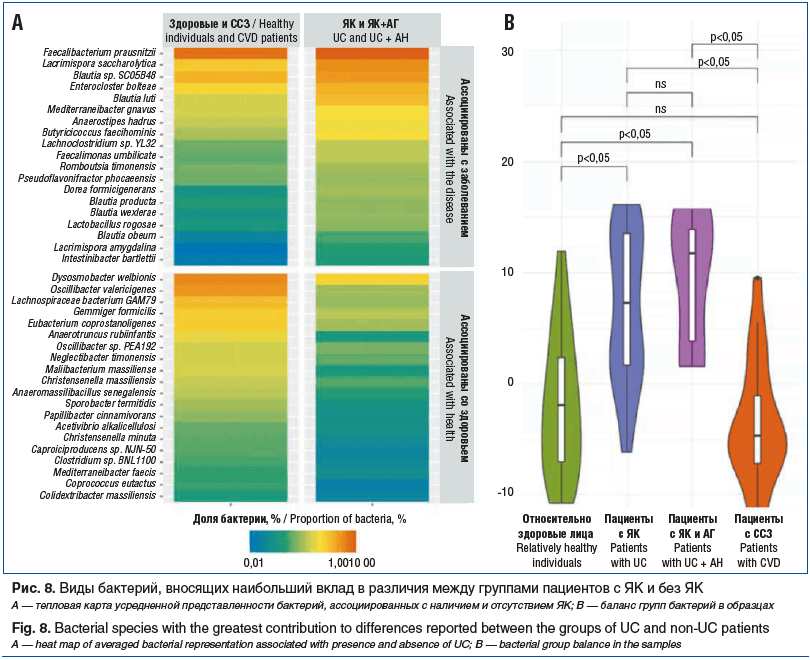
Для идентификации бактериальных таксонов, вносящих максимальный вклад в различия между группами, был применен композиционный анализ методом ближайшего баланса — это метод, учитывающий композиционную природу данных микробиома, где относительные доли таксонов взаимозависимы. Данный подход позволяет выделить две группы микроорганизмов, соотношение которых наиболее значимо различается между сравниваемыми выборками. Тепловая карта (рис. 8А) позволяет визуализировать усредненные пропорции таксонов, классифицированных как «ассоциированные с заболеванием» (потенциально «провоспалительные») и «ассоциированные со здоровьем» (потенциально «противовоспалительные»).
Установлена статистически значимая ассоциация баланса с наличием ЯК (p<0,05): у пациентов с ЯК значения баланса достоверно выше, что отражает смещение микробного состава в сторону условно «провоспалительных» таксонов (рис. 8В).
У больных ЯК с сочетанием с АГ установлены значимые различия при сравнении со здоровыми участниками исследования и пациентами с ССЗ по следующим видам бактерий:
Anaerotruncus rubiinfantis: доля у пациентов с ЯК составила 39,39%, с ЯК и АГ — 16,67%, с ССЗ — 85%, у здоровых участников — 89,47% (р<0,001);
Caproiciproducens sp. NJN-50: доля у пациентов с ЯК — 12,12%, с ЯК и АГ — 16,67%, с ССЗ — 55%, у здоровых участников — 73,68% (р<0,001);
Coprococcus eutactus: доля у пациентов с ЯК — 39,39%, с ЯК и АГ — 16,67%, с ССЗ — 45%, у здоровых участников — 63,16% (р<0,001);
Maliibacterium massiliense: доля у пациентов с ЯК — 33,33%, с ЯК и АГ — 16,67%, с ССЗ — 75%, у здоровых участников — 84,21% (р<0,001);
Sporobacter termitidis: доля у пациентов с ЯК — 33,33%, с ЯК и АГ — 0%, с ССЗ — 70%, у здоровых участников — 78,95% (р=0,003);
Oscillibacter valericigenes: доля у пациентов с ЯК — 57,58%, с ЯК и АГ — 33,33%, с ССЗ — 95%, у здоровых участников — 94,74% (р=0,004);
Papillibacter cinnamivorans: доля у пациентов с ЯК — 30,3%, с ЯК и АГ — 0%, с ССЗ — 70%, у здоровых участников — 73,68% (р=0,004);
Eubacterium coprostanoligenes: доля у пациентов с ЯК — 54,55%, с ЯК и АГ — 50%, с ССЗ — 45%, у здоровых участников — 94,74% (р=0,004);
Flintibacter sp. KGMB00164: доля у пациентов с ЯК — 66,67%, с ЯК и АГ — 66,67%, с ССЗ — 100%, у здоровых участников — 100% (р=0,004);
Lachnospiraceae bacterium: GAM79 доля у пациентов с ЯК — 57,58%, с ЯК и АГ — 33,33%, с ССЗ — 95%, у здоровых участников — 89,47% (р=0,027);
Mediterraneibacter faecis: доля у пациентов с ЯК — 18,18%, с ЯК и АГ — 33,33%, с ССЗ — 40%, у здоровых участников — 73,68% (р<0,001);
Colidextribacter massiliensis: доля у пациентов с ЯК — 15,15%, с ЯК и АГ — 0%, с ССЗ— 55%, у здоровых участников — 52,63% (р=0,009);
Christensenella minuta: доля у пациентов с ЯК — 24,24%, с ЯК и АГ — 0%, с ССЗ — 60%, у здоровых участников — 63,16% (р=0,008);
Anaeromassilibacillus senegalensis: доля у пациентов с ЯК — 36,36%, с ЯК и АГ — 50%, с ССЗ — 85%, у здоровых участников — 73,68% (р=0,020).
Обсуждение
У пациентов с ЯК состав КМ имеет уникальные отличия в видовой структуре по сравнению со здоровыми людьми. Ключевой вывод исследования заключается в том, что у пациентов с ИБС видовой состав микробиоты кишечника по своему составу ближе к таковому у здоровых участников, чем у больных ЯК. Это подтверждается анализом β-разнообразия — показателя, отражающего степень сходства или различия микробных сообществ между образцами. Близость микробного профиля пациентов с ИБС к здоровым участникам, в отличие от выраженного дисбиоза при ЯК, позволяет предположить, что изменения микробиоты при ССЗ носят менее выраженный характер. В исследовании H. Liu et al. [15] показано, что у пациентов с ИБС выявлены специфические изменения в виде снижения доли ряда таксонов, но общее α-разнообразие и β-разнообразие в подгруппе пациентов с ИБС без метаболического синдрома не отличались существенно от таковых у здоровых лиц.
Показатели α-разнообразия, включая видовое богатство и разнообразие КМ, оказались статистически значимо сниженными у пациентов с коморбидной патологией — сочетанием ЯК и АГ. Это свидетельствует о том, что при одновременном наличии ЯК и АГ микробное сообщество кишечника становится менее насыщенным. Снижение показателей α-разнообразия КМ как одной из характерных особенностей ЯК отмечается в большинстве исследований, посвященных изучению микробного профиля при данном заболевании [16, 17]. Согласно метаанализу A. Tsiavos et al. [18] у пациентов с АГ α-разнообразие КМ, как правило, остается стабильным, однако в некоторых случаях чаще наблюдается снижение индекса Shannon, чем индекса Chao1. В исследовании A.F. Ahmad et al. [19] показано, что у пациентов со стабильной стенокардией и острым коронарным синдромом α-разнообразие не отличалось от такового у группы контроля. Однако в метаанализе М. Choroszy et al. [20] показаны противоположные данные.
Средняя длина секвенированных геномов значимо не отличалась в группах сравнения. Стоит отметить, что данный показатель отражает среднее количество генов на микроорганизм, что определяет стабильность микробного сообщества под воздействием различных внешних факторов, включая диету [21]. Отсутствие значимых различий по сравнению со здоровыми лицами в указанных группах имеет принципиальное практическое значение и указывает на потенциальную эффективность диетической коррекции в качестве вспомогательного метода ведения пациентов как с ЯК, так и с ССЗ.
У пациентов с ИБС и АГ, включая лиц с ЯК и без ЯК, обнаружено статистически значимое снижение доли метаногенных бактерий Methanobacteriota (р=0,002) и филума Verrucomicrobiota (p<0,001). Последний включает представителя — A. muciniphila, который играет важную роль в поддержании целостности слизистого барьера кишечника и регуляции воспалительных процессов. Эти изменения могут отражать нарушение баланса микробиоты, ассоциированного с сердечно-сосудистой и коморбидной патологией [14].
Установлены особенности видового состава КМ у пациентов с ЯК — значимое уменьшение содержания анаэробных бактерий филума Bacillota: A. rubiinfantis, C. eutactus, M. massiliense, O. valericigenes, P. cinnamivorans, E. coprostanoligenes, M. faecis, которые в норме присутствуют в составе КМ человека. Функциональная значимость этих таксонов изучена недостаточно из-за сложностей культивирования (строгие анаэробы). Известно, что филум Bacillota, один из доминирующих типов бактерий в кишечной микробиоте человека, играет ключевую роль в синтезе короткоцепочечных жирных кислот (КЦЖК), различные таксоны участвуют в метаболизме сложных углеводов, синтезе витаминов, ограничивают избыточный рост условно-патогенных бактерий [22].
Экспериментальное исследование in vivo на модели мышей с ЯК продемонстрировало аналогичное снижение представительства A. rubiinfantis [23]. В этой работе показано, что у пациентов с сочетанием ЯК и АГ содержание A. rubiinfantis в образцах кала ниже, чем у пациентов с ЯК без АГ, что позволяет предположить, что коморбидность (ЯК и АГ) усугубляет дисбиотические изменения в КМ. Снижение содержания в образцах кала A. rubiinfantis может быть ассоциировано не только с воспалительным процессом в кишечнике, но, вероятно, и с АГ.
Coprococcus eutactus является важнейшим продуцентом бутирата и ацетата [24]. В ранее проведенных исследованиях показана связь Coprococcus с синтезом нейроактивных метаболитов, что указывает на потенциальную роль данной бактерии в балансе оси «кишечник — мозг» [25, 26]. C. eutactus способствуют улучшению трофики благодаря продукции КЦЖК и восстановлению экспрессии белков плотных контактов, таких как клаудин-1, окклюдин и ZO-1, и нормализации синтеза муцинов [27], снижение доли данного представителя в КМ коррелирует с увеличением активности воспалительного процесса при ВЗК [28].
Maliibacterium massiliense — недавно описанный таксон, выделенный из образцов фекалий человека [29]. Его открытие расширило представления о таксономическом разнообразии микробного сообщества кишечника, однако функциональная роль и вклад в поддержание гомеостаза остаются практически неизученными. В нашем исследовании продемонстрировано его значимое снижение в образцах кала у пациентов с ЯК, у пациентов с сочетанием ЯК и АГ, а также у пациентов с ИБС.
Название O. valericigenes связано со способностью данного вида продуцировать валериановую кислоту. Данные исследований показывают связь O. valericigenes с метаболическим синдромом. Так, в эксперименте на мышах in vivo показано, что фекальная трансплантация O. valericigenes индуцировала экспрессию сигнатурных генов, приводящих не только к ожирению, но и к другим проявлениям метаболического синдрома [30]. Авторы исследования отнесли таксон к «провоспалительным» представителям. Участие O. valericigenes в патогенезе ЯК не изучено. Согласно нашим данным доля этого микроорганизма значимо ниже у пациентов с ЯК по сравнению со здоровыми участниками исследования.
В образцах кала пациентов с ЯК обнаружено значимое снижение представительства вида P. cinnamivorans, известного своей способностью метаболизировать коричную кислоту циннамат (cinnamivorans — «поедающий циннамат»), содержащуюся, например, в корице. Несмотря на редкость и низкую представленность в микробиоме, этот таксон привлекает внимание из-за потенциальной роли в ферментации растительных полифенолов и поддержании кишечного гомеостаза. При ожирении и сахарном диабете 2 типа отмечается уменьшение доли этого вида, что указывает на его возможную роль в регуляции липидного и углеводного обмена [31]. В то же время исследований, изучающих связь ВЗК с P. сinnamivorans, в литературе не представлено. Согласно нашим данным у пациентов с сочетанием ЯК и АГ данный вид в представленных образцах обнаружен не был, однако у пациентов с ИБС его доля составила 70%, а у здоровых участников — 73,68%.
Eubacterium coprostanoligenes играет ключевую роль в метаболизме холестерина, согласно данным литературы [32]. Низкая численность этого представителя типа Bacillota ассоциирована с гиперхолестеринемией и повышенным риском атеросклероза. В исследовании Y. Liu et al. [33] показано, что у пациентов с ИБС его доля в микробиоте снижена на 30–40%. В нашем исследовании представленность E. coprostanoligenes в образцах кала у пациентов с ЯК, пациентов с сочетанием ЯК и АГ, а также больных ИБС значимо ниже, чем у практически здоровых участников исследования, что заслуживает особого внимания с позиции потенциальной роли в развитии коморбидных состояний.
Представленность Mediterraneibacter (базионим Ruminococcus) faecis у пациентов всех групп также ниже, чем у практически здоровых участников, согласно нашим данным. В исследовании, проведенном в Саудовской Аравии, было показано, что основные различия между пациентами с ВЗК и здоровыми участниками заключаются по многим таксонам, один из которых — M. faecis [34]. Примечательно, что в нашем исследовании у пациентов с АГ и ИБС их содержание значимо меньше, чем у здоровых участников исследования.
В общей сложности представленный анализ показал, что снижение содержания 14 бактериальных таксонов, представителей филума Bacillota, ассоциировано с ЯК, что углубляет представления о роли КМ в патогенезе данного заболевания и расширяет перечень потенциальных микробных биомаркеров.
Заключение
У пациентов с ЯК выявлены значимые отличия в видовом составе КМ по сравнению со здоровыми лицами. Наблюдается снижение представительства филума Bacillota, включая A. rubiinfantis, C. eutactus, E. coprostanoligenes и других таксонов, участвующих в синтезе КЦЖК и поддержании кишечного барьера, что подтверждает центральную роль дисбиоза в патогенезе ЯК. Микробный профиль пациентов с ИБС демонстрирует структурное сходство с нормой, что подтверждается анализом β-разнообразия. В представленном исследовании выявлены специфические изменения для пациентов с кардиоваскулярной патологией: снижение доли Methanobacteriota и Verrucomicrobiota (включая A. muciniphila), а также уменьшение доли E. coprostanoligenes, что, вероятно, связано с риском атеросклероза. Предполагаем, что указанная альтерация может носить вторичный характер на фоне системных метаболических нарушений либо развиваться первично в результате особенностей питания пациентов с ИБС и АГ, что предрасполагает к появлению данной патологии. Сочетание ЯК с АГ, вероятно, усугубляет дисбиоз: у таких пациентов наблюдается наиболее выраженное снижение α-разнообразия (видовое богатство и равномерность) и критическое уменьшение ключевых бутират-продуцентов (Coprococcus eutactus, A. rubiinfantis). M. massiliense и P. cinnamivorans — малоизученные маркеры дисбиоза при ЯК, требующие дальнейшего анализа. O. valericigenes (продуцент валериановой кислоты) ассоциирован с метаболическим синдромом, а его снижение при ЯК может отражать активацию противовоспалительных механизмов.
Клиническая значимость полученных данных заключается в установленном снижении в образцах доли E. coprostanoligenes и M. faecis — потенциальных биомаркеров риска коморбидных состояний (ЯК + АГ, ИБС). Стабильность средней длины геномов микробиоты у пациентов с ИБС и ЯК предполагает возможность коррекции дисбиоза посредством сбалансированной диеты. Перспективными направлениями являются изучение функциональной роли редких таксонов (Maliibacterium, Papillibacter) в синтезе метаболитов и модуляции иммунитета, а также разработка персонализированных подходов, направленных на восстановление бутират-продуцирующих бактерий при коморбидной патологии.
Результаты исследования расширяют понимание роли микробиоты в развитии ЯК и ССЗ, подчеркивают важность комплексного подхода к коррекции дисбиоза при коморбидных состояниях.
Сведения об авторах:
Бикбавова Галия Равильевна — к.м.н., доцент, доцент кафедры госпитальной терапии, эндокринологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0001-9252-9152
Ливзан Мария Анатольевна — д.м.н., член-корр. РАН, профессор, ректор, заведующая кафедрой факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0001-6581-7017
Блох Алексей Игоревич — к.м.н., доцент кафедры общественного здоровья и здравоохранения ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; заместитель директора по научной работе ФБУН «Омский НИИ природно-очаговых инфекций» Роспотребнадзора; 644080, Россия, г. Омск, пр-т Мира, д. 7; ORCID iD 0000-0002-0756-2271
Лисютенко Наталья Сергеевна — к.м.н., доцент кафедры госпитальной терапии, эндокринологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0003-4088-240X
Запоренко Маргарита Юрьевна — заведующая отделением кардиологии БУЗОО «ОКБ»; 644111, Россия, г. Омск, ул. Березовая, д. 3.
Романюк Алиса Евгеньевна — студентка 6-го курса лечебного факультета ФГБОУ ВО ОмГМУ; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0001-6308-4377
Машнин Михаил Юрьевич — студент 6-го курса лечебного факультета ФГБОУ ВО ОмГМУ; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0009-0007-8493-3690
Контактная информация: Бикбавова Галия Равильевна, e-mail: galiya1976@mail.ru
Источник финансирования: исследование выполнено за счет гранта Российского научного фонда (проект № 23-25-10035).
Конфликт интересов отсутствует.
Статья поступила 28.03.2025.
Поступила после рецензирования 23.04.2025.
Принята в печать 22.05.2023.
About the authors:
Galiya R. Bikbavova — C. Sc. (Med.), Assistant Professor, Assistant Professor of the Department of Hospital Therapy and Endocrinology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0001-9252-9152
Mariya A. Livzan — Dr. Sc. (Med.), Corresponding Member of the RAS, Professor, Rector, Head of the Department of Faculty Therapy and Gastroenterology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0001-6581-7017
Alexey I. Blokh — C. Sc. (Med.), Assistant Professor of the Department of Public Health and Healthcare, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; Deputy Director for Scientific Work, Omsk Research Institute of Natural Focal Infections; 7, Mira ave., Omsk, 644080, Russian Federation; ORCID iD 0000-0002-0756-2271
Natalia S. Lisyutenko — C. Sc. (Med.), Assistant Professor of the Department of Hospital Therapy and Endocrinology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0003-4088-240X
Margarita Yu. Zaporenko — Head of the Department of Cardiology, Regional Clinical Hospital; 3, Berezovaya str., Omsk, 644111, Russian Federation.
Alisa E. Romanyuk — 6th-year Student, Faculty of General Medicine, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0001-6308-4377
Mikhail Yu. Mashnin — 6th-year Student, Faculty of General Medicine, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0009-0007-8493-3690
Contact information: Galiya R. Bikbavova, e-mail: galiya1976@mail.ru
Financial Disclosure: the study was funded by a grant of the Russian Science Foundation (project No. 23-25-10035).
There is no conflict of interest.
Received 28.03.2025.
Revised 23.04.2025.
Accepted 22.05.2025.
[1] Артериальная гипертензия у взрослых. Клинические рекомендации. 2020. Одобрено Научно-практическим советом Минздрава России. (Электронный ресурс.) URL: https://scardio.ru/content/Guidelines/Clinic_rek_AG_2020.pdf (дата обращения: 19.05.2024).
[2] Стабильная ишемическая болезнь сердца. Клинические рекомендации. 2020. Одобрено Научно-практическим советом Минздрава России. (Электронный ресурс.) URL: https://scardio.ru/content/Guidelines/2020/Clinic_rekom_IBS- unlocked.pdf (дата обращения: 19.05.2024).
Информация с rmj.ru





