Введение
Инфаркт миокарда (ИМ) без обструкции коронарных артерий (ИМБОКА) — доказанный некроз миокарда ишемического генеза при стенозе менее 50% эпикардиальной коронарной артерии или его отсутствие, выявленное при коронарографии [1]. Термин ИМБОКА (MINOCA, myocardial infarction with non-obstructive coronary arteries) был впервые предложен в 2013 г. J.F. Beltrame [2] для замены существовавшего ранее термина MINCA (myocardial infarction with normal coronaries). Официальная аббревиатура MINOCA (ИМБОКА) впервые была использована в 2017 г. в рекомендациях Европейского общества кардиологов.
Содержание статьи
Эпидемиология, этиология, патогенез, факторы риска ИМБОКА
Частота встречаемости ИМБОКА составляет среди всех пациентов с ИМ от 6 до 14%, а у молодых пациентов — 10–20% [2–4]. Чаще выявляется у женщин, латиноамериканцев, представителей африканской расы. При сравнении пациенты с ИМБОКА моложе, нежели пациенты с ИМ с обструкцией коронарных артерий (ИМОКА), реже имеют классические факторы, а чаще — специфические факторы риска ИМ. У них часто отсутствует анамнез ишемической болезни сердца (ИБС) [5].
Существуют различные этиологические и патогенетические механизмы ИМБОКА, определяющие клиническую картину, тактику лечения и прогноз. К основным патогенетическим механизмам развития ИМБОКА относят: разрыв/эрозию атеросклеротической бляшки с обструкцией просвета менее 50%, спазм эпикардиальных коронарных артерий, микрососудистую дисфункцию, тромбоз и эмболию коронарных артерий, миокардиальные мышечные мостики, спонтанную диссекцию коронарной артерии. Разрыв/эрозия коронарных атеросклеротических бляшек выявляется в 25–40% случаев ИМБОКА [6, 7]. Данный механизм развивается на фоне уязвимой нестабильной атеросклеротической бляшки, обтурирующей просвет коронарной артерии менее 50%, которая обычно имеет большое рыхлое липидное ядро и тонкую покрышку. Механизм некроза миокарда при разрыве или эрозии атеросклеротической бляшки опосредован тромбозом, тромбоэмболией совместно со спазмом коронарных сосудов или комбинацией данных механизмов.
Спазм коронарной артерии, микрососудистая дисфункция, коронарный тромбоз in situ, спонтанная диссекция коронарной артерии обнаруживаются у 10–11% молодых мужчин и до 30% молодых женщин с ИМБОКА [8].
Спазм коронарных артерий как причина развития ИМБОКА наблюдается в среднем у 16–28% пациентов. Основными триггерами коронарного вазоспазма считаются: курение, злоупотребление алкоголем, употребление наркотических токсических веществ. Одним из механизмов спазма является атероматозное поражение интимы коронарной артерии, которое сопровождается воспалением и повышением чувствительности этого участка к спастическим влияниям. Доказана генетическая и этническая предрасположенность к коронарному вазоспазму. Так, полиморфизм гена рецептора ангиотензина 2 ассоциируется с повышенной склонностью к спазму атеросклеротически неизмененных коронарных артерий и характерен для азиатской популяции, где коронарный вазоспазм неизмененных коронарных артерий наблюдается чаще [9–12]. Основными механизмами микрососудистой дисфункции являются нарушение функции эндотелия, спазмы и ремоделирование микрососудов, экстрамуральная компрессия [13]. Изменения в микрососудистом русле при микрососудистой дисфункции приводят к повышению микроциркуляторного сопротивления и снижению коронарного резерва.
К факторам риска тромбоза и эмболии коронарных артерий относятся гиперкоагуляционные состояния, инфекции, врожденные и приобретенные тромбофилии, фибрилляция предсердий, внутрисердечные опухоли и имплантация внутрисердечных устройств.
Тромбофилиями обусловлено от 14 до 19% ИМБОКА [14, 15]. К наиболее значимым врожденным тромбофилиям относятся мутации в гене фактора V (FV Leiden), полиморфизм тромбоцитарных рецепторов GPIIb/IIIa, ТТ-генотип гена метилентетрагидрофолатредуктазы, варианты полиморфизма фибриногена (Fibrinogen G/A-455), полиморфизм ингибитора активатора плазминогена I типа. По данным исследования, проведенного в Греции, около 36% пациентов с ИМ с неизмененными коронарными артериями имели по крайней мере один положительный фактор наследственной тромбофилии по сравнению с пациентами без ИМ, у которых факторы наследственной тромбофилии выявлялись в 3,6% случаев. Мутация G20210A в гене протромбина была одним из основных генетических протромботических факторов риска, связанных с возникновением ИМ в молодом возрасте [16, 17]. Частота приобретенных тромбофилий в структуре факторов риска ИМ у молодых пациентов составляет от 3 до 5% [3, 18]. Триггерами приобретенных тромбофилий являются курение, ожирение, гиподинамия, применение оральных контрацептивов женщинами. Основными факторами риска приобретенных тромбофилий считаются женский пол, наличие онкологических, аутоиммунных, воспалительных заболеваний в анамнезе [19].
Эмболия коронарной артерии — один из наиболее редких механизмов ИМБОКА. Распространенность коронарной эмболии составляет 3% всех случаев острого коронарного синдрома (ОКС) [20]. Эмболия коронарной артерии может возникать вследствие разрыва атеросклеротической бляшки с образованием тромбов или отрыва вегетаций клапана при инфекционном эндокардите.
Миокардиальный мышечный мостик — аномалия развития коронарной артерии, анатомически проходящей через миокард. Миокардиальный мышечный мостик считается редкой причиной ИМ в целом, однако его распространенность у молодых пациентов с ИМ относительно высока. Частота встречаемости гемодинамически значимых миокардиальных мышечных мостиков составляет 0,5–4,9% [21].
Спонтанная диссекция коронарной артерии — спонтанное расслоение стенки коронарной артерии, не связанное с травмой или атеросклерозом. Обструкция просвета коронарной артерии возникает вследствие образования интрамуральной гематомы. К факторам риска развития спонтанной диссекции коронарной артерии относят фибромышечную дисплазию, многоплодную беременность, ранний послеродовый период, системные воспалительные заболевания. Частота спонтанной диссекции коронарных артерий составляет 1–4% случаев ОКС в целом, 15–20% случаев ОКС во время беременности, до 35% случаев ОКС у женщин моложе 60 лет. До 90% пациентов со спонтанной диссекцией коронарной артерии — женщины в возрасте от 40 до 60 лет [22]. Триггерами спонтанной диссекции коронарной артерии считаются стресс, интенсивные физические нагрузки, роды, употребление наркотических веществ, гормональных препаратов. При спонтанной диссекции коронарной артерии более чем в 50% случаев поражается передняя нисходящая артерия (ПНА), далее по частоте поражения следуют огибающая и правая коронарная артерии, ствол левой коронарной артерии. Обычно поражаются средние и дистальные сегменты коронарной артерии [23, 24].
Для пациентов с ИМБОКА, как правило, характерна классическая болевая форма ИМ. В то же время, по данным ряда исследований, у молодых пациентов с ИМБОКА болевой синдром может быть не выражен, иметь нетипичную локализацию в виде абдоминальных болей, болей в шее и спине. ИМ могут предшествовать различные продромальные явления в виде синкопальных состояний, головокружения, выраженной слабости, тревожности. Также клиническая картины ИМБОКА может иметь свои особенности в зависимости от патогенеза ИМ, что затрудняет диагностику [25].
Данные относительно прогноза пациентов с ИМБОКА носят противоречивый характер. Изначально многие авторы считали ИМБОКА относительно доброкачественным заболеванием с благоприятным прогнозом по сравнению с ИМОКА. Однако данные последних исследований не подтвердили это предположение. Так, уровень смертности от всех причин при поступлении и в течение 1 года у пациентов с ИМБОКА варьирует от 0,1 до 2,2% и от 2,2 до 4,7% соответственно [26]. Смертность от всех причин в течение 1 года после ИМ у пациентов с ИМБОКА и ИМОКА отличалась незначительно и составляла 4,7 и 6,7% соответственно [3].
Приводим описание клинических наблюдений ИМБОКА у молодых пациентов. Согласие пациентов на публикацию клинических наблюдений получено.
Клинические наблюдения
Клиническое наблюдение 1
Пациент А., 41 год, азиатской расы. Доставлен в стационар 22.05.2023 в 12:22 с жалобами на тошноту, однократный эпизод рвоты, давящие боли за грудиной без иррадиации.
Анамнез заболевания: 21.05.2023 пациент выпил 3 л пива. 22.05.2023 утром еще полбутылки пива и в 10:00 впервые в жизни отметил давящие боли за грудиной средней интенсивности. В 10:20 появилась тошнота, однократная рвота. Пациент терпел боли в течение 2 ч, затем вызвал скорую медицинскую помощь (СМП). Был госпитализирован. На догоспитальном этапе терапия аспирином 250 мг. Болевой синдром был полностью купирован на этапе коронароангиографии. Общая длительность болевого синдрома составила 3 ч.
Анамнез жизни: наследственность по сердечно-сосудистым заболеваниям (ССЗ) не отягощена, индекс курильщика 22 пачка/лет, алкоголь употребляет в течение 10 лет 2–3 раза в неделю по 3 л пива. Образование среднее, работает строителем.
Данные физикального обследования при поступлении. Состояние тяжелое, сознание ясное, кожные покровы обычной окраски. Частота дыхательных движений (ЧДД) 18 в 1 мин. При аускультации дыхание везикулярное, хрипов нет. Границы сердца не расширены, тоны сердца приглушены, ритмичные, шумов нет. Артериальное давление (АД) 130/75 мм рт. ст., частота сердечных сокращений (ЧСС) 65 в 1 мин. Живот при пальпации мягкий, безболезненный, печень не увеличена. Мочеиспускание свободное. Электрокардиограммы (ЭКГ) при поступлении и в динамике представлены на рисунке 1.
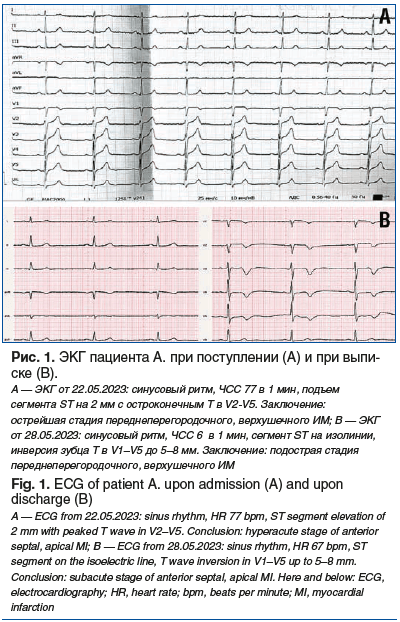
Тропонин I от 22.05.2023: 7,210 нг/мл (норма: 0,00–0,35).
По данным ЭхоКГ от 22.05.2023: фракция выброса (ФВ) 38% (N>50% по Simpson). Выявлены зоны гипо- и акинезии в средних переднем и переднеперегородочном, верхушечных переднем и переднеперегородочном сегментах.
Коронароангиография (КАГ) 13:05 22.05.2023. Ствол левой коронарной артерии (ЛКА) обычно развит, с неровными контурами, без гемодинамически значимых сужений. Левая ПНА (ЛПНА): в проксимальном сегменте сужение просвета до 50–55%, далее без гемодинамически значимых стенозов. Проведена проба с введением раствора нитроглицерина интракоронарно: уменьшение степени сужения просвета в проксимальном сегменте ЛПНА до 25–30%. Остальные артерии — без гемодинамически значимых стенозов. Тип кровоснабжения сердца — правый (рис. 2).
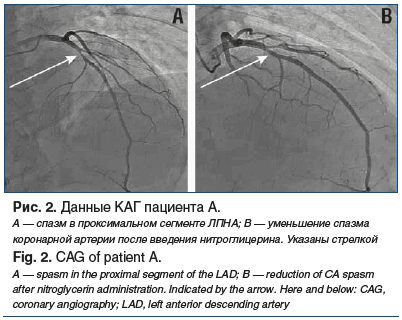
Консилиумом с учетом выполненной КАГ с положительной пробой с нитроглицерином было принято решение чрескожное коронарное вмешательство (ЧКВ) не выполнять.
Холтеровское мониторирование от 25.05.2023: зарегистрировано 4 эпизода ишемической депрессии сегмента ST по II каналу до 1,5–2 мм общей длительностью 17 мин, которые совпадали с эпизодами давящих болей за грудиной.
По данным электрокардиографии высокого разрешения (ЭКГВР), зарегистрированы поздние потенциалы желудочков (ППЖ) на 1-е и 7-е сутки. Вариабельность сердечного ритма (ВСР) была снижена на 1-е и 7-е сутки. На 7-е сутки отмечалось повышение ВСР с преобладанием симпатического компонента. При анализе турбулентности сердечного ритма (ТСР) один из параметров, начало турбулентности ТО (turbulence onset), выходил за пределы нормальных значений.
Учитывая данные клинической картины: давящие боли за грудиной средней интенсивности без иррадиации длительностью 3 ч, повышение уровня тропонина I, формирование отрицательного зубца Т в V1–V4 на ЭКГ, зоны гипо- и акинезии в передней, переднеперегородочной и верхушечной области левого желудочка (ЛЖ), стеноз в проксимальном сегменте ЛПНА до 55% на фоне спазма с положительной пробой с нитроглицерином, пациенту был выставлен клинический диагноз.
Основное заболевание: ИБС. Крупноочаговый переднеперегородочный, верхушечный ИМ ЛЖ без обструкции коронарных артерий от 22.05.2023. Вазоспазм проксимального сегмента ЛПНА. Вазоспастическая стенокардия.
Фоновое заболевание: хроническая алкогольная интоксикация.
Осложнения основного заболевания: не было.
Сопутствующие заболевания: хронический бронхит курильщика.
Медикаментозная терапия с 22.05.2023 по 28.05.2023: ацетилсалициловая кислота 100 мг 1 р/сут, клопидогрел 75 мг 1 р/сут, торасемид 5 мг 1 р/сут.
Клиническое наблюдение 2
Пациент П., 34 года. Доставлен в стационар 11.03.2024 в 12:00 с жалобами на интенсивные жгучие боли за грудиной с иррадиацией в левую руку, спину.
Анамнез заболевания: 11.03.2024 в 11:00 впервые в жизни отметил нестерпимые боли за грудиной жгучего характера, которые пациент терпел в течение 20 мин, затем вызвал СМП.
До приезда СМП по настоянию матери принял 2–3 дозы нитроглицерина (спрей), без эффекта. После принятия нитроглицерина отмечалась однократная рвота. Бригадой СМП снята ЭКГ, на которой был выявлен подъем сегмента ST в V1–V6. На догоспитальном этапе терапия морфином 10 мг внутривенно, аспирин 250 мг. После введения морфина боли купировались не полностью. С направительным диагнозом «острый коронарный синдром» с подъемом сегмента ST был госпитализирован. Болевой синдром был полностью купирован на этапе ЧКВ. Общая длительность болевого синдрома составила 2 ч.
Анамнез жизни: наследственность по ССЗ отягощена по мужской линии. ИМ у отца в 40 лет, у дедушки в 35 лет. Употребление алкоголя, курение отрицает. Употребляет энергетические напитки 1–2 раза в месяц, по 1 банке — 250 мл. Образование высшее, работает IT- специалистом.
Данные физикального обследования при поступлении. Состояние тяжелое, кожные покровов бледные. ЧДД 20 в 1 мин. При аускультации легких дыхание везикулярное, хрипов нет. Границы сердца не расширены, тоны ритмичные, приглушены. АД 90/60 мм рт. ст., ЧСС 65 в 1 мин. Живот при пальпации мягкий, безболезненный, печень не увеличена. Мочеиспускание свободное.
Электрокардиограммы пациента П. при поступлении и в динамике представлены на рисунке 3.
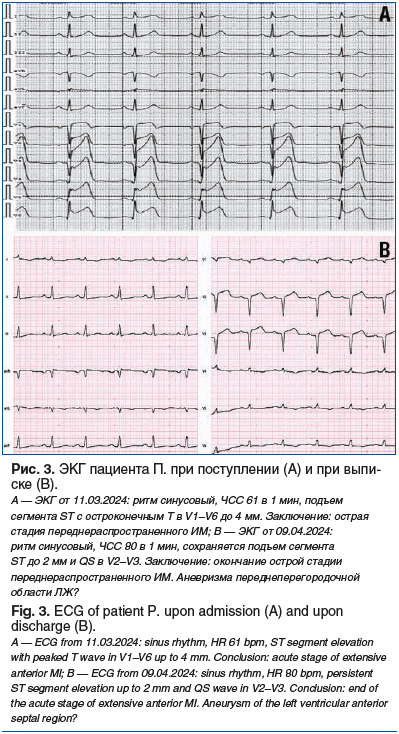
На серии ЭКГ от 13.03.2024, 14.03.2024, 15.03.2024, 18.03.2024, 19.03.2024, 20.03.2024, 21.03.2024, 25.03.2024, 26.03.2024, 27.03.2024, 28.03.2024, 29.03.2024, 01.04.2024, 02.04.2024, 04.04.2024, 08.04.2024: ритм синусовый, ЧСС 78–106 в 1 мин, отмечается снижение сегмента ST до 1–2 мм, с формированием патологического QS в V1–V5. Заключение: окончание острой стадии переднераспространенного ИМ, замедленная динамика переднераспространенного ИМ.
По данным ЭхоКГ от 11.03.2024: гипокинез средних переднеперегородочного, переднего сегментов; верхушечных переднего, переднеперегородочного, бокового, нижнего сегментов ЛЖ, ФВ 28%. На ЭхоКГ от 12.03.2025, 13.03.2025, 14.03.2025, 15.03.2025, 17.03.2025, 21.03.2025, 22.03.2025, 28.03.2025 отмечается увеличение ФВ ЛЖ до 44%, сохранение гипокинеза средних переднеперегородочного, переднего сегментов; верхушечных переднего, переднеперегородочного, бокового, нижнего сегментов ЛЖ.
Тропонин I от 11.03.2024: >50,000 нг/мг.
11.03.2024 в 12:35 пациент был экстренно направлен на КАГ (рис. 4). По данным КАГ: окклюзия ПНА в проксимальном сегменте 100%, кровоток TIMI 0. Проведена тромбэкстракция и стентирование ПНА.
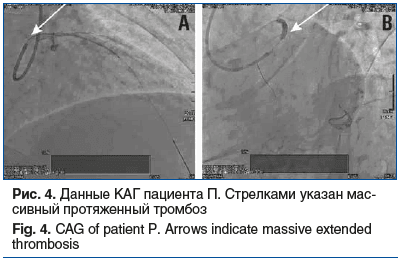
11.03.2024 в 14:30 после перевода в отделение реанимации у пациента сильная слабость, головная боль, отмечалось нарушение речи.
В 15:00 развилась острая сердечная недостаточность, классифицированная как Киллип III. В 15:20 зарегистрирована брадикардия с выраженной гипотензией и потерей сознания. Развилась асистолия, клиническая смерть. Проведены реанимационные мероприятия.
В 15:35 пациенту повторно проведена КАГ, по данным которой обнаружен тромбоз ранее установленного стента на всем протяжении с распространением тромботических масс в устье и проксимальный сегмент ОА, кровоток по ПНА TIMI 0, кровоток в ОА TIMI 2. Проведена тромбэкстракция в несколько пассажей.
Компьютерная томография (КТ) головного мозга от 11.03.2024: в правой лобной, левой теменной области, в обеих гемисферах мозжечка отмечаются гиподенсные зоны ишемических изменений. Заключение: КТ-признаки мультифокальных ишемических изменений в обеих полушариях головного мозга и мозжечка.
11.03.2024 пациент был переведен на экстракорпоральную мембранную оксигенацию (ЭКМО), 11.03.2024 подключен к аппарату искусственной вентиляции легких (ИВЛ).
12.03.2024: на прикроватном ЭКГ-мониторе пароксизмы неустойчивой желудочковой тахикардии (ЖТ).
На основании характерной клинической картины ИМ: интенсивные жгучие боли за грудиной с иррадиацией в левую руку, спину длительностью 2 ч; данных ЭКГ: подъем сегмента ST в V1–V6, повышение уровня кардиоспецифических ферментов (тропонина I >50,000 нг/мг), выявленный при ЭхоКГ гипокинез передней, перегородочной, боковой и верхушечной области ЛЖ; данных КАГ: окклюзия ПНА 100%; данных КГ головного мозга: КТ-признаки ишемии в лобной доле справа, пациенту был выставлен клинический диагноз.
Конкурирующие заболевания: 1. ИБС. Крупноочаговый переднераспространенный ИМ ЛЖ без обструкции коронарных артерий от 11.03.2024. Тромбэкстракция и стентирование ПНА от 11.03.2024. Тромбоз стента ПНА и повторная тромбэкстракция от 11.03.2024.
2. Мультифокальный инфаркт головного мозга в бассейнах левой и правой средних мозговых артерий, вертебробазиллярном бассейне.
Фоновое заболевание: наследственная тромбофилия?
Осложнения основного заболевания: ОСН Киллип класс III. Клиническая смерть от 11.03.2024. Успешные реанимационные мероприятия от 11.03.2024. Имплантация VA ЭКМО от 11.03.2024. ИВЛ от 11.03.2024. Пароксизмы неустойчивой ЖТ от 12.03.2024.
Сопутствующие заболевания: не было.
15.04.2024 пациент был проконсультирован гематологом, сдан генетический тест для верификации факторов наследственной тромбофилии, по результатам которого был выявлен клинически значимый генотип 4G4G по генетическому маркеру SERPINE1, полиморфизм 5G(-675)4G, связанный с повышенным риском развития тромбоза и ИМ.
По данным ЭКГВР, проведенной на 3-и сутки ИМ, отмечалось снижение общей ВСР с преобладанием симпатической активности. На 20-е сутки ИМ отмечалось дальнейшее снижение показателей общей ВСР с преобладанием очень низкочастотного компонента. ППЖ сохранялись на 3-и и 20-е сутки ИМ. При оценке ТСР оба параметра турбулентности сердечного ритма, начало турбулентности ТО (turbulence onset) и наклон кривой турбулентности (TS turbulence slope) выходили за пределы нормальных значений.
Клиническое наблюдение 3
Пациент И., 31 год. Доставлен в стационар 03.06.2024 в 19:15 с жалобами на сильные боли за грудиной давящего характера без иррадиации длительностью 2 ч.
Анамнез заболевания: в связи с увольнением с работы в январе 2023 г. находился в состоянии постоянного психоэмоционального стресса. С этого времени стал отмечать эпизоды повышения АД до 190/110 мм рт. ст. при привычных цифрах АД 130/70 мм рт. ст. Постоянную антигипертензивную терапию не принимал. 03.06.2024 в 17:00 на фоне сильного стресса отметил повышение АД до 180/100 мм рт. ст. и появление сильных давящих болей за грудиной. Самостоятельно принял кардиомагнил, каптоприл, без эффекта. В 18:30 вследствие продолжающихся болей вызвал СМП. Введен морфин 10 мг, болевой синдром купирован не полностью. Доставлен в стационар с направительным диагнозом ОКС с подъемом сегмента ST. Общая длительность болевого синдрома составила 3 ч.
Анамнез жизни: наследственность по ССЗ отягощена, ИМ у матери. Употребление алкоголя отрицает. Курит, индекс курильщика 10 пачка/лет. Эпизодически употребляет энергетические напитки, по 1–2 банки — 250 мл «Редбулл» в день, ежедневно употребляет до 5 чашек кофе. Образование высшее, не работает. Уровень стресса по тесту Л. Ридера: высокий.
Данные физикального обследования при поступлении: состояние тяжелое, сознание ясное. Кожные покровы обычного цвета. Дыхание ровное, ритмичное, ЧДД 18 в 1 мин. При аускультации дыхание везикулярное, усиленное, хрипов нет. Границы сердца не расширены. Тоны сердца приглушены, ритмичны. Сердечные шумы не выслушиваются. АД 180/100 мм рт. ст., ЧСС 80 в 1 мин. Живот при пальпации мягкий, безболезненный, печень не увеличена. Мочеиспускание свободное.
Тропонин I от 03.06.2024: 3,190 нг/мл (норма <0,5).
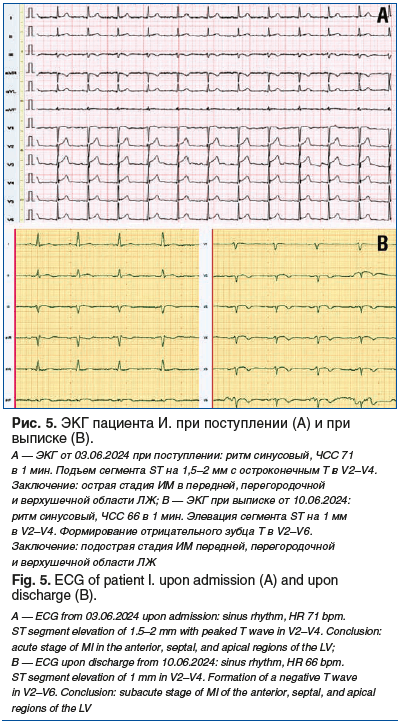
На серии ЭКГ с 04.06.2024 по 07.06.2024: динамика под-острой стадии ИМ передней, перегородочной и верхушечной области ЛЖ.
ЭхоКГ от 03.06.2024: ФВ 58%, гипокинез верхушечных переднего и перегородочного сегментов, верхушки ЛЖ. межжелудочковая перегородка 1,4 мм, задняя стенка ЛЖ 1,2 мм, гипертрофия миокарда ЛЖ.
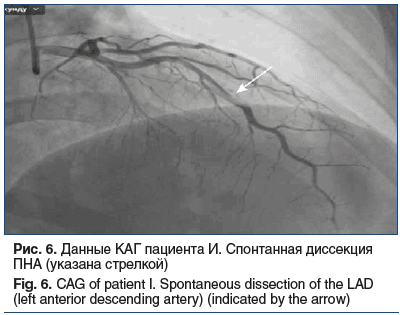
По данным КАГ от 03.06.2024: спонтанная диссекция ПНА (рис. 6) в среднем сегменте (тип Е), окклюзия в дистальном сегменте. Диагональная ветвь, интермедиальная артерия, огибающая артерия, ветви тупого края, правая коронарная артерия, задняя межжелудочковая ветвь не изменены на всем протяжении. Учитывая стабильное клиническое состояние пациента, отсутствие неровностей контуров и стенозирующих изменений в артериях других бассейнов, от ЧКВ было решено воздержаться по следующим причинам: возможное распространение интрамуральной гематомы проксимально в сторону ствола ЛКА с его компрессированием и компрессированием устья ОВ.
На основании характерной клинической картины ИМ: сильные давящие боли за грудиной без иррадиации длительностью 2 ч; повышение уровня кардиоспецифических ферментов (тропонин I 3,190 нг/мл); выявленный по данным ЭхоКГ гипокинез верхушечных переднего и перегородочного сегментов, верхушки ЛЖ; данных КАГ: спонтанная диссекция ПНА в среднем сегменте (тип Е), окклюзия в дистальном сегменте — пациенту был выставлен клинический диагноз:
Основное заболевание: ИБС. Крупноочаговый циркулярный ИМ верхушки ЛЖ без обструкции коронарных артерий от 03.06.2024. Спонтанная диссекция среднего сегмента ПНА (тип Е). Гипертоническая болезнь 2 стадии, 2 степени, риск 3.
Фоновое заболевание: высокий уровень стресса по тесту Л. Ридера. Избыточное потребление кофеинсодержащих напитков.
Осложнения основного заболевания: не было.
Сопутствующие заболевания: не было.
Медикаментозное лечение с 03.06.2024 по 10.06.2024: ацетилсалициловая кислота 100 мг 1 р/сут, эналаприл 5 мг 2 р/сут, тикагрелор 90 мг 2 р/сут.
По данным ЭКГВР ППЖ сохранялись на 7-е сутки. Также на 7-е сутки сохранялась низкая ВРС с преобладанием симпатической активности. При оценке ТСР один из параметров турбулентности сердечного ритма, начало турбулентности ТО (turbulence onset), выходил за пределы нормальных значений.
Обсуждение
В представленных клинических наблюдениях у молодых пациентов развился ИМ по типу ИМБОКА при отсутствии классических факторов риска и атеросклеротического поражения коронарных артерий, но со специфическими факторами риска ИМ и интактными коронарными артериями.
В первом клиническом наблюдении фактором риска ИМ были злоупотребление алкоголем и курение, которые являются факторами, вызывающими как атеросклероз, так и вазоспазм коронарных артерий. Пациент был представителем азиатской расы, для которых характерна генетическая предрасположенность к развитию вазоспазма интактных эпикардиальных коронарных артерий. Данные КАГ и эпизоды ишемической депрессии сегмента ST, выявленные при холтеровском мониторировании, подтверждают вазоспастический генез ИМ у пациента. Длительный стаж злоупотребления алкоголем мог стать дополнительным фактором появления предикторов внезапной сосудистой смерти (ВСС).
Во втором клиническом наблюдении у пациента отсутствовали факторы риска ИБС, кроме отягощенной наследственности по линии отца — ИМ в молодом возрасте у отца и дедушки. Как было выявлено, причиной ИМ в этом случае была гиперкоагуляция вследствие наследственной тромбофилии, связанной с гомозиготной мутацией 4G/4G в гене SERPINE1. Ген SERPINE1 негативно воздействует на фибринолиз, повышая риск развития тромбозов и тромбоэмболий. Генотип 4G считается неблагоприятным, приводящим к ослаблению фибринолитической активности крови. Для пациентов с этой патологией характерно развитие повторных ИМ с массивными тромбозами на интактных коронарных артериях [27]. В нашем случае ИМ также протекал тяжело, с повторным тромбозом стента, большим очагом поражения миокарда ЛЖ, острой сердечной недостаточностью, клинической смертью и развитием острого нарушения мозгового кровообращения. За время нахождения в стационаре у пациента отмечалось прогрессирующее снижение общей ВСР с преобладанием очень низкочастотного гуморального компонента, сохранялись ППЖ, также оба параметра ТСР имели патологические значения. С учетом пароксизмов неустойчивой ЖТ, перенесенной клинической смерти и значимого количества предикторов пациент был наиболее угрожаем по ВСС.
В третьем клиническом наблюдении основными факторами риска ИМ вследствие спонтанной диссекции коронарной артерии были сильный стресс, избыточное употребление кофеинсодержащих напитков. Согласно рекомендациям Европейского общества кардиологов таким пациентам предпочтительно консервативное лечение ИМ и лишь в отдельных случаях, при сохранении постоянной симптоматики ИМ с подъемом сегмента ST, рекомендуется проведение ЧКВ [28]. Существуют разногласия относительно оптимальной терапии пациентов со спонтанной диссекцией коронарной артерии. Использование антитромбоцитарной терапии является дискуссионным моментом. Имеются данные, что двойная антитромбоцитарная терапия может увеличивать интрамуральную гематому и способствовать еще большей обструкции просвета коронарной артерии. В приведенном клиническом наблюдении пациенту не выполнили ЧКВ, что согласуется с основными принципами ведения таких пациентов. Однако назначение тикагрелора с ацетилсалициловой кислотой является спорным и могло ухудшить течение заболевания. На фоне лечения у пациента сохранялся болевой синдром, что, вероятно, связано с неполным рассасыванием интрамуральной гематомы и сохраняющейся обструкцией просвета коронарной артерии. Это сопровождалось снижением ВСР и регистрацией ППЖ у пациента на 7-е сутки ИМ.
У всех трех пациентов после перенесенного ИМБОКА выявлялись предикторы ВСС: ППЖ, снижение ВСР, замедленное восстановление ТСР. Пациенты 1 и 3 входили в категорию 1, пациент 2 — в категорию 2 по наличию патологических параметров ТСР. Наиболее неблагоприятный прогноз был у второго пациента.
Заключение
Приведенные клинические наблюдения показывают, что у молодых пациентов причиной развития ИМБОКА могут быть различные специфические факторы риска и разные патогенетические механизмы ИМ. Клиническая картина ИМ у пациентов характеризовалась отсутствием анамнеза ИБС, поздним обращением за медицинской помощью, длительным болевым синдромом, тяжелыми осложнениями. В связи с неразработанностью патогенетического лечения данного типа ИМ у пациентов было невозможно в полной мере устранить причины, вызвавшие ИМБОКА. В связи с чем у них отмечалось тяжелое течение ИМ, сохранялись боли за грудиной и значимое количество предикторов ВСС. Таким пациентам требуется персонифицированный подход в лечении ИМ: устранение специфических модифицируемых факторов риска, снижение уровня стресса, отказ от злоупотребления алкоголем, избыточного потребления кофеинсодержащих напитков. При подозрении на наследственную тромбофилию необходимо проводить генетическое тестирование. Молодых пациентов с ИМБОКА без патогенетического лечения ИМ следует относить к группе с повышенным риском ВСС, необходимо диспансерное наблюдение у кардиолога и проведение оценки вероятности развития жизнеугрожающих аритмий. Требуется дальнейшая разработка патогенетического лечения пациентов с ИМБОКА.
Сведения об авторах:
Мартынов Алексей Юрьевич — к.м.н., доцент кафедры госпитальной терапии Российского университета дружбы народов; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 8; ORCID iD 0000-0002-2438-2862
Иркабаева Малика Мансуровна — ассистент кафедры госпитальной терапии Российского университета дружбы народов; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 8; ORCID iD 0000-0003-0346-8920
Политидис Рита Романовна — к.м.н., доцент кафедры госпитальной терапии Российского университета дружбы народов; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 8; ORCID iD 0000-0002-8627-2845
Контактная информация: Мартынов Алексей Юрьевич, e-mail: martynov-ayu@rudn.ru
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 23.04.2025.
Поступила после рецензирования 22.05.2025.
Принята в печать 18.06.2025.
About the authors:
Alexey Yu. Martynov — C. Sc. (Med.), Associate Professor, Department of Hospital Therapy, RUDN University; 8, Miklukho-Maklaya str., Moscow, 117198, Russian Federation; ORCID iD 0000-0002-2438-2862
Malika M. Irkabaeva — Assistant Professor of the Department of Hospital Therapy, RUDN University; 8, Miklukho-Maklaya str., Moscow, 117198, Russian Federation; ORCID iD 0000-0003-0346-8920
Rita R. Politidis — C. Sc. (Med.), Associate Professor of the Department of Hospital Therapy, RUDN University; 8, Miklukho-Maklaya str., Moscow, 117198, Russian Federation; ORCID iD 0000-0002-8627-2845
Contact information: Alexey Yu. Martynov, e-mail: martynov-ayu@rudn.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 23.04.2025.
Revised 22.05.2025.
Accepted 18.06.2025.
Информация с rmj.ru






