Введение. Историческая справка
«Удушье матки по причине жажды материнства» — это цитата из древнеегипетского папируса, датируемого 1855 годом до н. э., первое упоминание об эндометриозе — новой загадочной и неизвестной женской болезни [1]. Прошли тысячелетия с тех пор, когда были представлены клинические наблюдения, демонстрирующие совокупность симптомов, характерных для патологического процесса, который в медицине ХХI века мы называем эндометриозом [2, 3]. В IV–V веках до н. э. Гиппократ, наблюдая за бесплодием неясного генеза у замужних женщин, дал описание симптомов эндометриоза, которое вошло в Корпус Гиппократа (The Hippocratic Corpus) [4]. Его теория заключалась в том, что, если женщина не выполняет свою репродуктивную роль, то органы малого таза, матка теряют свои изначальные функции, возникает сбой в их физиологии и отсюда берут свое начало различные болезни. Концепция его теории состояла в том, что эндометриоз не только причина бесплодия, но и следствие отсутствия беременностей, что само по себе дает старт развитию эндометриоза.
Про «истерию матки» писал в своих трактатах византийский врач Аэций Амидийский в VI веке [1]. Он описывал это патологическое состояние матки как ее болезненные сокращения во время менструации. Хорошо известно, что альгодисменорея часто связана с наличием эндометриоза.
На протяжении веков «истерию матки» считали мистическим расстройством, но изучение этого патологического состояния под разным углом зрения, с учетом широкого спектра критериев, позволило выдвинуть неопровержимые доказательства того, что в большей части клинических наблюдений причиной болезни был эндометриоз. Таким образом, стало понятно, что ранее существовавшие теории были заблуждениями, которые приводили к массовым диагностическим ошибкам.
К концу XVII века врачи перестали связывать страдания женщин с их психическим состоянием. Свое внимание врачи переключили на изучение анатомических изменений при патологии матки. D. Shron в 1690 г. изложил в своей диссертационной работе Disputatio Inauguralis Medica de Ulceribus Ulceri клиническую картину заболевания [1, 5], схожую с современными представлениями об эндометриозе. Впервые он указал на признаки пораженных органов, смог дать характеристику тканям матки и достаточно точно описал ее анатомию. Свои открытия D. Shron сделал до изобретения микроскопа (с помощью приборов — предшественников микроскопов), что стало особенно ценным. В своей научной работе он описал заполненные гемолизированной кровью образования в малом тазу, за пределами матки, и указал, что застойная менструальная кровь является причиной поражения матки, придатков и тазовой брюшины. Им также упоминается наследственная предрасположенность к выявленным изменениям.
С 1826 г. начинается век микроскопии после внедрения Джозефом Джексоном Листером микроскопа. В XIX веке Рудольф Вирхов описал патологические изменения, похожие на менструальные гематоцисты, и назвал их кистозной аденомиомой — мягкой миксоматозной или мягкой апоматозной кистой.
Карл фон Рокитанский (Karl von Rokitansky) в 1860 г. стал первым, кто описал микроскопические изменения при эндометриозе: наличие желез эндометрия и стромы в патологических образованиях женских репродуктивных органов [6–9].
Исследования Томаса Каллена (Thomas Cullen), гинеколога из Канады, который занимался эндометриозом, стали фундаментальными. Впервые он выделил заболевание и применил термин «аденомиома» (adenomyoma) [10–12]. Но революционный прорыв в 1927 г. совершил доктор Джон Семпсон (John Sampson) в своей работе по теории развития эндометриоза, и с этого времени термин «эндометриоз» (endometriosis) — «болезнь внутри матки» — устойчиво закрепился в медицине и используется до настоящего времени для описания данной патологии [13].
На фоне исторических фактов об изучении эндометриоза и выделения этой патологии в отдельную нозологию особого внимания, по нашему мнению, заслуживает научный труд профессора Камрана Нежата (Camran Nezhat) из Калифорнии, опубликованный в 2011 г. [14]. Его фундаментальная работа «Эндометриоз: древняя болезнь, древнее лечение» базируется на архивных исторических данных. Целями данного исследования были оценка исторических данных об эндометриозе, тазовых болях (клинические и анатомические признаки болезни) и сопоставление их с современными концепциями эндометриоза.
Таким образом, история эндометриоза как отдельной нозологии, поражающей преимущественно женщин репродуктивного возраста, насчитывает около ста лет. Тем не менее в настоящее время эндометриоз остается одной из наименее изученных болезней, и обычно его характеризуют как многофакторное заболевание, болезнь гипотез и теорий.
Содержание статьи
- 1 Теории этиологии и патогенеза эндометриоза
- 2 Индукционная теория
- 3 Эпигенетическая (генетическая) концепция
- 4 Теория стволовых клеток в генезе эндометриоза
- 5 Теория перитонеального иммунного окружения
- 6 Теория о влиянии микро-РНК и экзосом
- 7 Перспективы изучения этиологии и патогенеза эндометриоза
- 8 Эндометриоз: КР Минздрава России (2020)
- 9 Тактика ведения пациенток с эндометриозом
- 10 Возможности гормональной терапии эндометриоза
- 11 Хирургическое лечение эндометриоза
- 12 Другие методы лечения
- 13 Заключение
Теории этиологии и патогенеза эндометриоза
Несмотря на огромное количество публикаций, посвященных этиологии и патогенезу эндометриоза, вопрос о доминирующих причинах и превалирующих теориях остается открытым для дискуссий в медицинском сообществе среди специалистов репродуктивной медицины. На данный момент этиология эндометриоза все еще плохо изучена, в современных научных источниках содержится противоречивая информация, а к известным теориям патогенеза эндометриоза (ретроградная, имплантационная, метапластическая, иммунологическая, генетическая) добавляются новые.
Теория аутоиммунных реакций
При эндометриозе гистологически всегда определяется воспалительный процесс, что предполагает вовлечение иммунной системы. Существует мнение, что дефектный ответ иммунной системы способствует повреждению преимущественно тазовой брюшины и образованию эндометриоидных гетеротопий. Как предположили V.H. Eisenberg et al. [15], лизис эндометриоидных очагов в брюшине нарушается. Иммунную реакцию при эндометриозе можно охарактеризовать как активацию поликлональных B-лимфоцитов, нарушение функций T- и B-лимфоцитов, повреждение тканей и вовлечение в процесс нескольких органов и систем. Совокупность данных процессов наблюдается при любом аутоиммунном заболевании [16]. С эндометриозом зачастую связаны аутоиммунные состояния — аллергические реакции, гипотиреоидизм, воспалительные заболевания желудочно-кишечного тракта и фибромиалгии [17]. Однако при наличии в организме аутоиммунных состояний нельзя с уверенностью сказать, являются ли они провоцирующими факторами для развития эндометриоза или следствием его наличия. Аутоиммунная теория эндометриоза [18] основывается на наличии циркулирующих антител к яичниковым и эндометриальным антигенам, которые, возможно, участвуют в патогенезе этого заболевания, а также могут играть свою роль в случаях репродуктивных потерь. Аутоиммунные патогенетические механизмы нуждаются в оценке и изучении.
Индукционная теория
Индукционная теория включает в себя 2 известные концепции: имплантационную и концепцию целомической метаплазии. Еще одна точка зрения, основанная на имплантационной теории и теории целомической метаплазии, предполагает, что существуют субстанции, образующиеся в результате дегенеративных процессов в эндометрии при его десквамации. Данный процесс способствует образованию эндометриоидных очагов [19]. С течением времени процесс эндометриоза прогрессирует от малых форм до формирования тяжелых опухолевидных инфильтратов.
Постепенное развитие эндометриоза можно объяснить наличием клеточных модификаций в связи с эпигенетическими и генетическими изменениями, которые освещены в теории эндометриоидной болезни [20].
Эпигенетическая (генетическая) концепция
P.R. Koninckx et al. [21] установили, что эндометриоидные кисты яичников являются моноклональными по своему происхождению и что в некоторых эндометриоидных клетках, способных к инвазивному росту в условиях in vitro, не наблюдалась экспрессия эпителиального кадгерина, что свойственно для патофизиологии опухолевого процесса [22]. N. Rahmioglu et al. [23] изучали вопросы наследственной предрасположенности к эндометриозу. Молекулярно-генетические методы показали наличие генетических мутаций и повреждение ДНК последовательностей в гистологических препаратах эндометриоидных очагов. Обнаруженные дефекты генов находились в локусах, отвечающих за функции клеток: пролиферацию и апоптоз — работу клеточного цикла, регуляцию транскрипции и клеточную адгезию [24]. В пользу этой теории можно сказать, что эндометриоз ассоциирован с генетическими мутациями [25]: разнообразные гены взаимодействуют друг с другом под действием факторов внешней среды, что и способствует вариабельности клинических проявлений эндометриоза у каждой конкретной пациентки.
Теория стволовых клеток в генезе эндометриоза
J. Yang et al. [26] предположили, что эндометриоидные гетеротопии имеют свойство быстро регенерировать и по характеру эндометриоидные клетки схожи со стволовыми. P.G. Figueira [27] показал, что эндометриоз ассоци-ирован со стволовыми клетками: редкую популяцию клеток с колонизационными свойствами он обнаружил в пластах эндометрия и стромальных клетках, которые сравнимы с мезенхимальными стволовыми клетками по мультилинейному потенциалу дифференцировки [28]. Ряд других исследователей эти предположения подтвердили [29–32]. Описана морфология мезенхимальных стволовых клеток, начало которым, возможно, дали клетки менструальной крови, и по своим свойствам эти клетки схожи с мезенхимальными стволовыми, которые были получены из костного мозга, печени, селезенки в эксперименте. Такие данные способствовали появлению идеи о мультипотентности мезенхимальных стволовых клеток, исходящих из менструальной крови. Так, теория стволовых клеток предполагает, что менструальная кровь, идущая ретроградным путем в полость малого таза, может содержать мультипотентные клетки, дающие начало эндометриоидным гетеротопиям при определенных условиях.
Теория перитонеального иммунного окружения
Прогрессированию эндометриоза, безусловно, способствуют иммунные факторы перитонеальной жидкости и брюшины, это объясняется изменениями в работе клеток иммунной системы, наличием местного воспалительного процесса в полости малого таза, остановкой процесса реабсорбции ретроградной менструальной крови по ряду причин [33–35]. Блокировка апоптоза эндометриоидных клеток, расположенных по брюшине и на органах малого таза при наружном эндометриозе, происходит вследствие нарушенного иммунного ответа [36]. Большое разнообразие иммунных факторов в перитонеальной жидкости, существование которых доказано [37], влияет на рост и дифференцировку эктопического эндометрия посредством изменения экспрессии генов (эпигенетические изменения микро-РНК, метилирование ДНК и др.) [38, 39].
Теория о влиянии микро-РНК и экзосом
Срез данных литературы, накопленных за последние годы, показал интерес к изучению роли микро-РНК в развитии эндометриоза. Опубликованы результаты экспериментальных исследований патогенетических механизмов развития эндометриоза с участием микро-РНК на посттранскрипционном уровне [40]. E.M. Teague et al. [41] выделили 22 разновидности микро-РНК, которые образуются в клетках в эндометриоидных очагах при прогрессировании эндометриоза. Оценивая микро-РНК клеток гетеротопий брюшины, связанных с эндометриозом, исследователи выявили специфические микро-РНК в эндометриоидных эпителиальных клетках и в плазме крови женщин, у которых был диагностирован эндометриоз. При этом в периферических тканях, не пораженных эндометриозом, такие микро-РНК не были обнаружены [42, 43]. То есть значимость микро-РНК в этиологии эндометриоза высока. Ряд исследователей считают оценку микро-РНК перспективным компонентом в диагностическом алгоритме эндометриоза [44].
После публикации данных о клетках, выделяющих в межклеточное пространство экстрацеллюлярные везикулы (экзосомы), исследователи начали изучать их роль в модуляции иммунного ответа при эндометриозе. Экзосомы способствуют межклеточным коммуникациям, они содержат микро-РНК, активно участвуют в модуляции иммунного ответа [45, 46]. R.J. Lobb et al. [47] изучали экзосомы, выделяемые клетками из эндометриоидных гетеротопий, и показали, что каскад иммунологических реакций способствует образованию локальных зон на брюшине, куда легко прикрепляются клетки ретроградной менструальной крови. В данном механизме экзосомы модулируют клетки и ткани посредством межклеточной коммуникации: снижают активность иммунных реакций, способствуют прогрессированию пролиферации клеток, их инвазии с развитием ангиогенеза в будущих эндометриоидных очагах [48, 49]. Из этого следует, что ретроградный эндометрий стремится к таким зонам и именно в них образуются малые формы эндометриоза с дальнейшей прогрессией [50].
Перспективы изучения этиологии и патогенеза эндометриоза
Таким образом, в научном сообществе на сегодняшний день продолжается обсуждение теорий патогенеза эндометриоза. Перспективным является дальнейшее углубленное изучение молекулярных и клеточных механизмов заболевания с учетом генетической предрасположенности, ассоциированной с мультипотентными клетками.
Клиницисты, занимающиеся лечением пациенток с эндометриозом, пристально следят за прогрессом научных изысканий в этой области. Практикующие специалисты заинтересованы в появлении новых лекарственных средств, разработанных с учетом изученных патогенетических механизмов, которые позволят добиться значительного регресса эндометриоза и, возможно, полного выздоровления пациенток.
На текущий момент практикующие специалисты в Российской Федерации применяют клинические рекомендации (КР), основанные на последних научных данных и регламентирующие методы терапии с учетом высокой степени доказательности их эффективности, полученной в клинических исследованиях.
Эндометриоз: КР Минздрава России (2020)
В опубликованных и действующих КР[1] под эндометриозом подразумевается патологический процесс, при котором вне полости матки определяется наличие ткани, по морфологическим и функциональным свойствам подобной эндометрию [51–53]. Этиология, патогенетические аспекты и эпидемиология заболевания обозначены в клиническом протоколе и в дополнительных комментариях не нуждаются. Специалистам, работающим в системе обязательного медицинского страхования, четко нужно знать коды заболевания по Международной классификации болезней, что важно для работы врачей страховых компаний и проведения оплаты услуг по страховым случаям по максимально выгодным для государственных учреждений здравоохранения ценам. Вопросы классификации эндометриоза четко обозначены в протоколе. Описаны локализации наружного и внутреннего (аденомиоз) эндометриоза и подробно обозначено стадирование патологического процесса, что важно для планирования терапии, объема хирургического вмешательства и оценки эффективности проводимых методов лечения.
Клиническая картина эндометриоза представлена кратко с учетом наиболее часто встречающихся клинических проявлений заболевания. Предполагая наличие эндометриоза, практикующие специалисты всегда должны обращать внимание на хроническую тазовую боль, дисменорею, диспареунию, дисхезию [54, 55], бесплодие [56], нарушения менструального цикла [57], аномальные маточные кровотечения [58], а также наличие опухолевидных образований (эндометриоидные кисты) в малом тазу [59]. Все перечисленные клинические проявления могут быть ассоциированы с развитием эндометриоза. Также при наличии гастроинтестинальных симптомов и симптомов, указывающих на патологию мочевого пузыря (боль при мочеиспускании, появление крови в моче), необходимо подумать об эндометриозе.
Симптомы эндометриоза и факторы риска — те самые «красные флаги», на которые необходимо обращать внимание при подозрении на эндометриоз, назовем их1:
обильные менструальные кровотечения, посткоитальные кровотечения;
дисменорея и/или диспареуния, симптомы которых не исчезают или слабо купируются при приеме комбинированных оральных контрацептивов (КОК) и нестероидных противовоспалительных препаратов (НПВП);
дисменорея и/или диспареуния, которые могут стать причиной нетрудоспособности;
неоднократные обращения в неотложном порядке по поводу дисменореи;
наличие эндометриоза у матери или сестры пациентки;
субфертильность при регулярной овуляции, проходимости фаллопиевых труб и нормальной спермограмме у партнера;
диарея, запор, тошнота, боли при дефекации, спазмы в кишечнике, вздутие живота и раннее насыщение;
предменструальные и постменструальные скудные кровянистые выделения в виде мазни в течение двух дней и более;
аллергия на цветение трав, аллергический ринит и повышенная чувствительность к пищевым продуктам. У пациенток с эндометриозом аллергические заболевания в анамнезе встречались чаще по сравнению с женщинами без эндометриоза (отношение шансов составляло 4,28, 95% доверительный интервал (ДИ) от 2,93 до 6,27) [60];
депрессия, тревожность, синдром хронической усталости, поскольку при данных состояниях у женщин эндометриоз встречается существенно чаще [61–63]1;
мигрень. Установлено, что частота мигрени среди больных эндометриозом в перименструальном периоде составляла 38,3% (95% ДИ от 30,1 до 47,2%), в то время как у здоровых женщин — 15% (95% ДИ от 10 до 21,4%, p<0,001) [62, 64, 65];
частые императивные мочеиспускания с болью или без нее, поскольку показано, что пациентки с эндометриозом значительно чаще страдают интерстициальным циститом [66]1.
Разобравшись с разнообразием клинических проявлений, обратимся к диагностике эндометриоза, описанной в клинических рекомендациях. Изучив подробно жалобы и анамнез, переходим к физикальному обследованию (визуальный осмотр наружных половых органов, осмотр шейки матки в зеркалах, бимануальное влагалищное и ректовагинальное исследование), которое проводится всем пациенткам независимо от последующей врачебной тактики.
Признаки эндометриоза, выявляющиеся при бимануальном исследовании [67]:
латеральное смещение шейки матки;
фиксированная и резко смещенная матка;
объемные образования придатков;
наличие узлов в маточно-крестцовой области, утолщение, напряжение и/или образования в крестцово-маточной связке;
укорочение и напряжение сводов влагалища;
выраженный стеноз шейки матки;
наличие мелкобугристого образования в ректовагинальной области;
болезненность и ограничение подвижности слизистой кишечника (при ректовагинальном исследовании).
Важно помнить, что специфических лабораторных маркеров эндометриоза нет [68]. Оценка уровней маркеров эпителиальных опухолей (СА-125, СА-19,9, РЭА, НЕ-4) не рекомендована для рутинной диагностики [69, 70]. Повышение уровня СА-125 возможно на фоне течения эндометриоза [71], однако значения, не выходящие за рамки референтных (менее 35 МЕ/мл) [72], также не показатель для того, чтобы снять диагноз при явных клинических проявлениях эндометриоза.
«Золотым стандартом» первичной инструментальной диагностики эндометриоза является ультразвуковое исследование органов малого таза (УЗИ ОМТ) трансвагинальным доступом [73–75]. Трансабдоминальный и/или трансректальный доступы применяются также для диагностики глубоких инфильтративных форм эндометриоза с вовлечением петель кишечника, развитием ректосигмоидного эндометриоза и поражением ректовагинальной перегородки, мочевого пузыря, мочеточников.
Выполнение магнитно-резонансной томографии (МРТ) ОМТ для рутинной диагностики эндометриоза неприемлемо [72]. МРТ показана при подозрении на глубокий инфильтративный эндометриоз с вовлечением кишечника, мочевого пузыря или мочеточников [76–78], а также при наличии аденомиоза с целью выбора оптимальной хирургической тактики для определения доступа и объема оперативного лечения [79].
При отсутствии патологии по данным УЗИ или МРТ ОМТ показано проведение диагностической лапароскопии [80] с целью диагностического поиска при наличии клинических проявлений эндометриоза, верификации диагноза, оценки степени распространения, установки клинической формы заболевания, выявления инфильтративного эндометриоза.
C. Tomassetti et al. [82] рекомендуют у пациенток с эндометриоз-ассоциированным бесплодием проводить интраоперационную оценку индекса фертильности с учетом данных анамнеза и хирургического вмешательства (Endometriosis Fertility Index).
Ряду пациенток рекомендовано проведение гистероскопии с целью исключения внутриматочной патологии, а также при аномальных маточных кровотечениях, бесплодии неясного генеза [72, 80, 81], для исключения синехий в полости матки и возможных пороков развития матки.
Выполнение гистологического исследования операционного материала обязательно к выполнению с целью верификации диагноза [72]. Важно помнить, что отсутствие данных за патологический процесс в гистологических препаратах не исключает наличия заболевания [14, 80].
Всем пациенткам с подозрением на эндометриоз и наличием синдрома хронической тазовой боли (СХТБ) необходимо проводить оценку боли с использованием визуальной аналоговой шкалы, нумерологической оценочной шкалы, Рейтинговой шкалы оценки боли по изображению лица (шкала Вонга — Бейкера) [68, 83].
Тактика ведения пациенток с эндометриозом
В настоящее время эксперты говорят о персонализированном подходе к лечению эндометриоза, который направлен на повышение качества жизни женщин в целом, борьбу с СХТБ, терапию бесплодия, минимизацию хирургических вмешательств [51, 56, 69, 70, 72, 80, 84].
Лечение эндометриоза включает медикаментозные и хирургические методы. Пациентки с клиническими проявлениями эндометриоза чаще обращаются к гинекологам амбулаторно. На первом этапе эмпирически назначаются НПВП курсом не более 3 мес. [85, 86]. Далее проводится первичная диагностика и подбор гормонального лечения либо планируется хирургическое вмешательство с последующей гормональной терапией [84, 87, 88]. Тактика по ведению пациентки с эндометриозом представлена на рисунке.
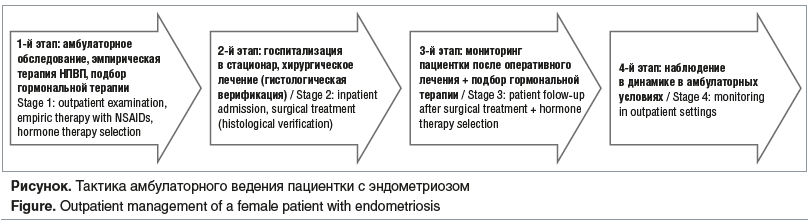
Врачу на амбулаторном приеме важно донести до пациентки информацию о ее состоянии, возможном диагнозе, если эндометриоз не верифицирован. В случае установления диагноза такая беседа необходима для повышения эффективности терапии и снижения риска рецидива заболевания. В разговоре с пациенткой при подозрении/наличии диагноза «эндометриоз» врачу следует:
объяснить, что такое эндометриоз. Донести информацию о том, что заболевание хроническое, протекает до менопаузы и требует постоянной гормональной терапии с перерывами в случае планирования беременности и лактации;
информировать о том, что хирургическое лечение возможно по показаниям (неэффективность гормональной терапии, осложнения заболевания);
отметить, что операция по поводу эндометриоза не ставит точку в заболевании. Важно динамическое наблюдение в послеоперационном периоде на фоне постоянного приема гормональной терапии;
обсудить материальный аспект гормональной терапии, совместно с пациенткой выбрать конкретный препарат для лечения и обсудить возможные побочные эффекты лечения.
Возможности гормональной терапии эндометриоза
Спектр гормональных препаратов для терапии эндометриоза широк. На данный момент с целью лечения эндометриоза и СХТБ могут быть назначены: гестагены, КОК, агонисты или антагонисты гонадотропин‑рилизинг‑гормона (Гн‑Рг) (антагонисты не зарегистрированы в РФ) [51, 80]. Данный спектр препаратов в 2022 г. был рекомендован рабочей группой Европейского общества репродукции человека и эмбриологии (European Society of Human Reproduction and Embryology, ESHRE) по эндометриозу. Применение даназола в настоящее время ограничено из-за значимой частоты побочных эффектов [80]. При недостаточной эффективности гормональной терапии возможно применение ингибиторов ароматазы в комплексе с пероральными контрацептивами, гестагенами, агонистами Гн-Рг [51, 80]. Отечественные исследователи не согласны с назначением КОК, учитывая, что большие дозы эстрогенов, которые они содержат, могут потенцировать обратный эффект — развитие эндометриоза [51, 87]. В отношении гестагенов (дидрогестерон, диеногест, нор-этистерон) в качестве первой линии терапии эндометриоза и СХТБ позиции наших экспертов и экспертов ESHRE схожи [51, 80]. Монотерапия прогестагенами проводится в непрерывном режиме или в циклическом, если пациентка находится на этапе прегравидарной подготовки [88, 89]. Рекомендации по приему КОК с профилактической целью и агонистов Гн-Рг в случаях инфильтративных форм эндометриоза также опубликованы в литературе [51, 72, 90–94]. Важно упомянуть, что назначение агонистов курсом более 6 мес. требует назначения add-back-терапии при возможных симптомах гипоэстрогении.
Использование левоноргестрела в форме внутриматочной терапевтической системы у пациенток с эндометриозом и аномальными маточными кровотечениями, не планирующих беременность, также регламентировано клиническим протоколом [51, 95].
Важно отметить, что медикаментозная терапия эндометриоза должна строиться на принципах персонализации [96] и совместного принятия решений (shared deсision making); назначая лечение, врач обязательно должен обсуждать все моменты совместно с пациенткой, что безусловно повысит комплаентность и результативность лечения.
Хирургическое лечение эндометриоза
Рано или поздно у пациенток репродуктивного возраста с жалобами на тазовую боль, дисменорею и диспареунию, с диагностированным бесплодием встает вопрос о хирургическом лечении. Решение о выходе на оперативное лечение должно быть взвешенным и обоснованным. Экспертами рекомендовано применение лапароскопического доступа с гистологической верификацией [69, 70–72, 80, 84, 88, 97] при недостаточном эффекте гормональной терапии или его отсутствии (срок оценки эффективности составляет 3 мес.), а также на этапе планирования беременности в случае бесплодия.
Наружный эндометриоз с формированием эндометриоидных кист необходимо оперировать эндоскопически с проведением бережной и щадящей энуклеации капсулы кисты, цель которой — максимальное сохранение овариального резерва, в особенности у пациенток репродуктивного возраста, не реализовавших свою репродуктивную функцию [51, 80, 98, 99]. Эвакуацию капсулы эндометриоидной кисты рекомендовано проводить с использованием контейнера (endobag), так же как и аспирацию брюшной полости и малого таза рекомендовано проводить до полного удаления патологического процесса для снижения частоты рецидива. Данные манипуляции повысят вероятность наступления долгожданной беременности [100, 101].
В случаях распространения эндометриоза на смежные органы бригаду хирургов необходимо усилить соответствующими профильными специалистами. Пациенткам с эндометриозом 3–4-й степени распространения и выраженным спаечным процессом оперативное лечение необходимо проводить в стационарах 3-го уровня (стационары, оказывающие специализированную, в том числе высокотехнологичную, медицинскую помощь женщинам, разрабатывающие новые методы диагностики и лечения гинекологической патологии).
При диагностированных узловых формах аденомиоза на фоне аномальных маточных кровотечений оптимальным методом выбора терапии также будет оперативное лечение [71, 72, 80, 83, 102]. Учитывая скромный процент наступления беременности (10–15%) после удаления аденоматозных узлов III–IV стадии аденомиоза, тотальная гистерэктомия будет максимально эффективной методикой у таких пациенток [51, 72, 79, 103, 104]. Безусловно, выполнение реконструктивно-пластических операций у молодых женщин с аденомиозом возможно, но эффективность таких вмешательств будет невысока и не повысит вероятность наступления беременности.
Другие методы лечения
На сегодняшний день КР Минздрава России и рекомендации ESHRE категорически не рекомендуют к назначению витамины, пищевые и минеральные добавки пациенткам с эндометриозом любых локализаций [51, 72, 80]1. Специальная диетотерапия также не показана.
Заключение
На сегодняшний день многие аспекты этиологии и патогенеза эндометриоза изучены недостаточно, проводится активная исследовательская работа. Разрабатываются и совершенствуются методы хирургического и консервативного лечения. Практикующие врачи, понимая невозможность полного излечения заболевания, сконцентрировали свои усилия на разработке новых методом медикаментозной терапии и усовершенствовании методов хирургического лечения. Таким образом, по разным направлениям исследователями и врачами ведется интенсивная работа, результаты которой позволят улучшить качество оказания медицинской помощи пациенткам с эндометриозом.
СВЕДЕНИЯ ОБ АВТОРАХ:
Доброхотова Юлия Эдуардовна — д.м.н., профессор, заведующая кафедрой акушерства и гинекологии лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117513, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-7830-2290.
Маркова Элеонора Александровна — к.м.н., ассистент кафедры акушерства и гинекологии лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117513, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-9491-9303.
Хлынова Светлана Анатольевна — к.м.н., доцент кафедры акушерства и гинекологии лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117513, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0003-1554-3633.
Нариманова Метанат Рафиговна — к.м.н., доцент кафедры акушерства и гинекологии лечебного факультета РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0003-0677-2952.
Контактная информация: Маркова Элеонора Александровна, e-mail: markova.eleonora@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 01.02.2024.
Поступила после рецензирования 27.02.2024.
Принята в печать 25.03.2024.
ABOUT THE AUTHORS:
Yulia E. Dobrokhotova — Dr. Sc. (Med.), Professor, Head of the Department of Obstetrics and Gynecology of the Medical Faculty, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-7830-2290.
Eleonora A. Markova — C. Sc. (Med.), Associate Professor of the Department of Obstetrics and Gynecology of the Medical Faculty, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-9491-9303.
Svetlana A. Khlynova — C. Sc. (Med.), Associate Professor of the Department of Obstetrics and Gynecology of the Medical Faculty, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0003-1554-3633.
Metanat R. Narimanova — C. Sc. (Med.), Associate Professor of the Department of Obstetrics and Gynecology of the Medical Faculty, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117997, Russian Federation; ORCID iD 0000-0003-0677-2952.
Contact information: Eleonora A. Markova, e-mail: markova.eleonora@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 01.02.2024.
Revised 27.02.2024.
Accepted 25.03.2024.
Информация с rmj.ru






