Содержание статьи
Введение
Распространенность артериальной гипертензии (АГ) среди взрослого населения составляет 30–45% и увеличивается с возрастом, достигая 60% и выше у лиц старше 60 лет [1]. К 2025 г. число пациентов с АГ увеличится на 15–20% и достигнет почти 1,5 млрд [2].
Повышенный уровень артериального давления (АД) является основным фактором риска преждевременной смерти и причиной почти 10 млн смертей в мире (по данным на 2015 г.) [3, 4]. Уровень систолического АД (САД) ≥140 мм рт. ст. ассоциируется с повышением риска смертности и инвалидности в 70% случаев, при этом наибольшее число смертей в течение года, связанных с уровнем САД, возникает вследствие ишемической болезни сердца (ИБС), ишемических и геморрагических инсультов [4].
Между уровнем АД и риском сердечно-сосудистых заболеваний (ССЗ) существует прямая связь, которая прослеживается с относительно низких значений АД — 110–115 мм рт. ст. для САД и 70–75 мм рт. ст. для диастолического АД (ДАД) [5]. Прямая связь между повышенным уровнем АД и риском сердечно-сосудис-тых событий (ССС) продемонстрирована для всех возрастных [6] и этнических групп [7]. У пациентов старше 50 лет САД является более сильным предиктором событий, чем ДАД [6]. Поэтому важен контроль, а у пациентов очень высокого риска — достижение целевых уровней АД как одно из ключевых мероприятий вторичной профилактики ССС.
Основой антигипертензивной терапии для снижения АД и уменьшения числа ССС являются 5 классов антигипертензивных препаратов: ингибиторы ангиотензинпревращающего фермента (иАПФ), блокаторы рецепторов ангиотензина II (БРА), β-адреноблокаторы (ББ), блокаторы медленных кальциевых каналов — антагонисты кальция (АК) и диуретики.
Антагонисты кальция метаболически нейтральны и не оказывают отрицательного действия на углеводный, липидный и пуриновый обмен. Помимо антигипертензивного, они оказывают антиангинальное и органопротективное действие и входят в рекомендации по лечению АГ в сочетании с симптомами стенокардии (с классом доказательности I А) [8]. Следует отметить, что гипотензивная эффективность АК не всегда обеспечивает приверженность больных терапии препаратами данной группы в связи с частым развитием нежелательных явлений (НЯ), основными из которых являются периферические отеки. По данным исследования VALUE, частота их развития у пациентов, принимающих амлодипин, достигает 32,9%. По данным исследования ASCOT, у каждого четвертого больного АГ, принимавшего комбинированную терапию амлодипином и иАПФ, отмечались периферические отеки, в частности отеки лодыжек и голеней [7].
Особенностью лерканидипина является почти полное отсутствие характерных для класса дигидропиридинов НЯ, таких как отеки нижних конечностей, а также покраснение лица, тахикардия. Лерканидипин характеризуется высокой аффинностью к кальциевым каналам L-типа, высокой липофильностью и способностью формировать длительно сохраняющееся депо. Медленное высвобождение лерканидипина из депо приводит за счет периферической вазодилатации к постепенному снижению АД, при этом не наблюдается повышения симпатической активности [9].
Концентрация лерканидипина именно в сосудистой стенке, а не в плазме крови обусловливает фармакологическую активность лерканидипина, в том числе длительность антигипертензивного действия в течение суток.
Лерканидипин — высокоселективный вазодилататор. Воздействуя на периферические сосуды, он вызывает снижение АД и постнагрузку на сердце. При этом лерканидипин не оказывает прямого и клинически значимого влияния на сократимость, автоматизм и проводимость миокарда и может применяться при нарушениях атриовентрикулярной проводимости и брадикардии [10, 11]. Лерканидипин, проявляя вазодилатирующее действие на уровне артериол, редко вызывает такой побочный эффект, как отеки в области лодыжек 12].
Антиангинальный эффект и ослабление реперфузионного повреждения миокарда под влиянием лерканидипина обусловлены увеличением доставки крови к миокарду вследствие дилатации коронарных артерий и уменьшения потребности миокарда в кровоснабжении за счет снижения АД и постнагрузки.
Антиангинальный эффект лерканидипина изучался у пациентов со стабильной стенокардией, в т. ч вазоспастической, что вызывает интерес в оценке эффективности и переносимости у пациентов с АГ после перенесенного острого коронарного синдрома (ОКС) и/или реваскуляризации.
Одним из плейотропных эффектов лерканидипина являются ангиопротективные свойства, которые заключаются в снижении центрального АД в аорте, что связано с изменением жесткости/эластичности сосудистой стенки и скорости пульсовой волны, что в свою очередь может оказывать влияние на возникновение ССС [13].
Эластичность сосудистой стенки может оцениваться путем измерения в динамике сердечно-лодыжечного сосудистого индекса (Cardio-Ankle Vascular Index, CAVI) — индикатора эластичности артериального русла [14–19]. Методика расчета CAVI описана в ряде пособий, измерение проводится согласно уравнению Bramwell — Hill на основании параметра жесткости β [14, 15]. Была показана взаимосвязь между степенью тяжести поражения коронарных артерий и величиной CAVI у пациентов, подвергнутых коронароангиографии [20]. Исследователями сделаны выводы, что динамика этого индекса позволяет выявить изменения эластических свойств сосудов на фоне длительной терапии у больных обоих полов с хронической ИБС [21]. Кроме того, по данным недавних исследований, наличие атеросклероза в сочетании с повышенной жесткостью сосудистой стенки у больных стабильной стенокардией в молодом возрасте может рассматриваться в качестве маркера синдрома раннего сосудистого старения и позволяет предположить дальнейшее более тяжелое течение ИБС и атеросклероза в данной группе пациентов [22]. Таким образом, динамика индекса CAVI может служить возможным критерием вазопротекторного эффекта терапии.
Цель исследования: изучить эффективность, безопасность и переносимость лерканидипина при лечении пациентов с АГ после ОКС и/или реваскуляризации миокарда.
Материал и методы
В период с 01.06.2021 по 01.12.2021 на базе БУЗОО «ККД» (Омск) было проведено открытое наблюдательное проспективное клиническое исследование, одобренное локальным этическим комитетом. В исследование включили пациентов, перенесших ОКС и/или стентирование инфаркт-зависимой коронарной артерии. Пациенты были взяты на диспансерное наблюдение врачами-кардиологами в первые 3 дня после выписки из сосудистых отделений стационаров г. Омска.
Пациентам назначалась медикаментозная терапия, включающая двойную антиагрегантную терапию, высокодозовую терапию аторвастатином, β-адреноблокаторы, антагонисты ренин-ангиотензин-альдостероновой системы, АК (воспроизведенный препарат амлодипина), антикоагулянты с учетом показаний. В рамках диспансерного наблюдения через 1 мес. оценивались параметры эффективности лечения, при недостижении уровня АД 120–130/80 мм рт. ст., наличии ангинозных приступов определялось соответствие пациентов критериям включения в исследование. В соответствии с этим в исследование были включены 80 пациентов.
Критериями включения являлись: реваскуляризация по поводу ОКС, отсутствие достижения целевого уровня АД на фоне комбинированной лекарственной терапии, наличие типичных жалоб при стенокардии II–III функционального класса (ФК) и нежелательных явлений (НЯ) на фоне терапии амлодипином, подписанное добровольное информированное согласие.
Критерии исключения: хроническая сердечная недостаточность (ХСН) в стадии декомпенсации, обструкция выносящего тракта левого желудочка, тяжелая печеночная недостаточность, тяжелая почечная недостаточность (скорость клубочковой фильтрации <30 мл/мин), включая пациентов, проходящих диализ, прием ингибиторов CYP3A4, циклоспорина, синдром слабости синусового узла (без электрокардиостимулятора).
Изучаемые параметры: уровень САД и ДАД, частота приступов стенокардии, ФК стенокардии, НЯ (отеки голеней и стоп, рефрактерная тахикардия, гиперемия лица), индекс CAVI.
В исследование включены 80 пациентов, средний возраст которых составил 59,4±9,6 года, мужчин было 59 (73,7%). ИМ перенесли 65 (81,3%), нестабильную стенокардию имели 15 (18,7%). В анамнезе у 80 (100%) пациентов отмечена АГ, у 16 (20%) — ХСН, из них у 4 (25%) — со сниженной фракцией выброса (ФВ), у 8 (50%) — с промежуточной ФВ, у 4 (25%) — с сохраненной ФВ, у 12 (15%) — постинфарктная стенокардия, связанная с наличием гемодинамически значимого стеноза коронарных артерий малого диаметра (менее 2 мм), а также с коронарным многососудистым стенозирующим атеросклерозом у пациентов, воздерживающихся от проведения аортокоронарного шунтирования, у 4 (5%) — сахарный диабет 2 типа, у 5% — фибрилляция предсердий. Пациентам, включенным в исследование, была проведена замена амлодипина на лерканидипин 10 или 20 мг (оригинальный лерканидипин Занидип®-Рекордати, Recordati Ireland, Ltd., Ирландия). Замена терапии пациентам осуществлялась по причине недостижения целевого уровня АД и развития НЯ, таких как отеки лодыжек у 56 (70%) пациентов, покраснение лица и тахикардия у 20 (25%) и 4 (5%) пациентов соответственно. На старте и в ходе терапии доза лерканидипина назначалась/титровалась врачом по собственному усмотрению.
При опросе пациентов выявлялись жалобы, отвечающие критериям стенокардии, согласно клиническим рекомендациям [23], проводился подсчет количества приступов стенокардии в течение последней перед визитом недели согласно дневникам пациентов. Кроме того, оценивалась интенсивность боли посредством визуально-аналоговой шкалы (ВАШ).
В исследовании определены три визита:
визит 1 (визит включения): определение соответствия пациента критериям включения в исследование; получение добровольного информированного согласия; оценка данных самоконтроля АД (СКАД), офисного АД, суточного мониторирования АД (СМАД), оценка количества приступов стенокардии, определение индекса CAVI, оценка интенсивности приступов стенокардии по ВАШ, назначение лерканидипина;
визит 2: через 1 мес. от начала лечения проводилась оценка данных СКАД, офисного АД, СМАД, переносимости терапии, наличия приступов стенокардии, индекса CAVI; оценка интенсивности приступов стенокардии по ВАШ; оценка НЯ;
визит 3: через 3 мес. от начала лечения проводилась оценка данных СКАД, офисного АД, СМАД, переносимости терапии, наличия приступов стенокардии, индекса CAVI; оценка интенсивности приступов стенокардии по ВАШ; оценка НЯ.
Методика анализа СКАД и СМАД соответствовала критериям, подробно изложенным авторами в предыдущей работе [24].
В ходе исследования изучали также безопасность и переносимость лерканидипина, проводили регистрацию НЯ и оценку причинно-следственной связи с приемом исследуемого препарата.
Статистический анализ осуществлялся с использованием пакетов Excel, Statistica 10. Проверка нормальности распределения проводилась с использованием метода Шапиро — Уилка. Средние выборочные значения количественных признаков приведены в тексте в виде медианы, 25‑го процентиля и 75‑го процентиля. Для проверки статистических гипотез применяли непараметрические методы: Т‑критерий ранговых знаков Вилкоксона, критерий χ2 Пирсона. В исследовании применялись методы однофакторного дисперсионного анализа, анализа таблиц сопряженности. При анализе таблиц сопряженности использовали χ2 Пирсона. Во всех процедурах статистического анализа за критический уровень р‑значения принималась величина <0,05.
Результаты исследования
Динамика уровней САД, ДАД и ЧСС представлена в таблице 1.
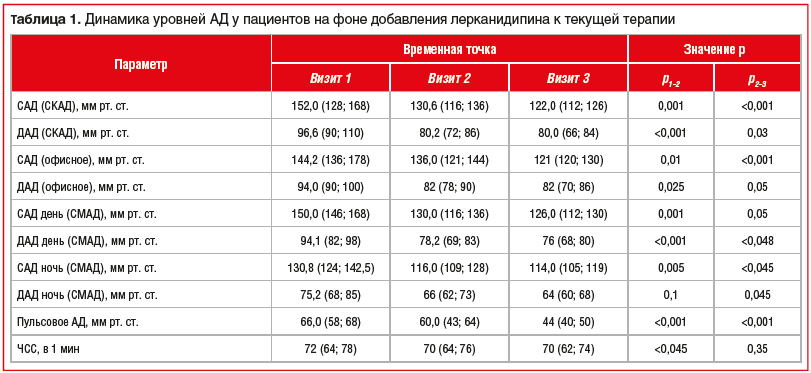
На визите 1 лерканидипин (Занидип®-Рекордати) в дозе 10 мг был назначен 60 (75%) пациентам, в дозе 20 мг — 20 (25%) пациентам. На визите 2 коррекция дозы потребовалась 4 (5%) пациентам, таким образом, к визиту 3 препарат в дозе 10 мг получали 56 (70%) пациентов, в дозе 20 мг — 24 (30%).
Через 1 мес. терапии лерканидипином отмечена значимая динамика снижения уровня АД по отношению к исходным значениям: целевых уровней АД достигли 74 (92,4%) пациента, через 3 мес. на фоне коррекции дозировок достижение целевых показателей АД отмечено у всех пациентов.
На визите 2 нормализация вариабельности САД зарегистрирована у 42 (52,5%), ДАД — у 58 (72,5%) пациентов. Через 3 мес. терапии нормализация вариабельности САД отмечена у 80 (100%) и ДАД у 78 (97,5%) пациентов (по отношению к исходным значениям для САД и ДАД p<0,001).
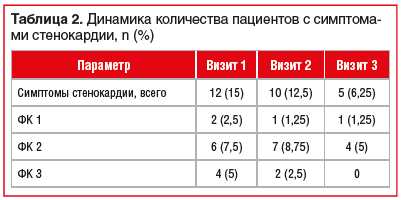
На визите 1 симптомы стенокардии наблюдались у 12 (15%) пациентов с частотой 3,8±2,2 в неделю, к визитам 2 и 3 доли пациентов с симптомами стенокардии снизились (табл. 2). На визите 2 частота приступов стенокардии составила 3,1±2,1 в неделю, на визите 3 отмечено значимое уменьшение числа приступов стенокардии до 0,5±0,3 в неделю (р<0,001). Согласно ВАШ отмечалось уменьшение выраженности приступов, снижение оценки с 7 до 4 баллов, с 4 до 2 баллов через 1 и 3 мес. приема лерканидипина соответственно.
В течение 10–14 дней после начала применения лерканидипина у всех пациентов произошло разрешение НЯ: регрессировали отеки, тахикардия, не наблюдалось случаев гиперемии лица, и в дальнейшем ни у одного пациента данные симптомы не отмечались.
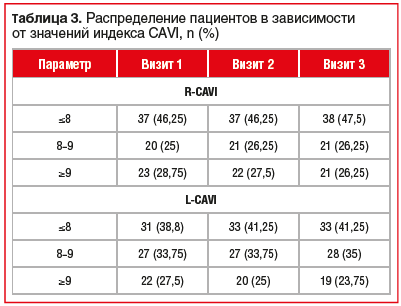
В отношении индекса CAVI через 1 и 3 мес. наблюдения существенной динамики показателя не выявили (табл. 3).
Прием исследуемого препарата хорошо переносился пациентами. Ни один пациент не выбыл из исследования из-за развития НЯ. В ходе исследования НЯ, связанные с приемом лерканидипина, отсутствовали.
Обсуждение
Достижение целевого уровня АД является одним из ключевых мероприятий вторичной профилактики ССЗ у пациентов после ОКС и/или реваскуляризации. Антигипертензивная эффективность лерканидипина была установлена во многих клинических исследованиях, одно из которых показало достижение целевого уровня АД лерканидипином в дозе 10–20 мг/сут около 68% [25]. В другом исследовании на фоне терапии лерканидипином ДАД снизилось с 96±4 до 83±6 мм рт. ст. (p<0,0001), снижение САД составило 18 мм рт. ст. [26]. Кроме того, назначение лерканидипина как в монотерапии, так и в комбинированной терапии с иАПФ достоверно снижало центральное САД и ДАД и способствовало улучшению структуры сосудистой стенки [27]. В настоящем исследовании на фоне комбинированной гипотензивной терапии, включающей лерканидипин (Занидип®-Рекордати), у 100% пациентов произошло достижение целевого уровня САД и 97,5% — ДАД, уменьшилась частота и выраженность ангинозных приступов у пациентов с постинфарктной стенокардией, связанной с наличием гемодинамически значимого стеноза коронарных артерий малого диаметра (менее 2 мм), а также у пациентов с коронарным многососудистым стенозирующим атеросклерозом, воздерживающихся от проведения аортокоронарного шунтирования.
Стоит отметить, что у 56 (70%) пациентов достижение целевого уровня АД произошло на терапевтической дозе препарата Занидип®-Рекордати 10 мг, у 24 (30%) пациентов применялась доза 20 мг, что говорит об эффективности терапии лерканидипином.
Отсутствие в ходе исследования НЯ, связанных с приемом лерканидипина, обусловлено механизмом действия данного препарата и определяет высокую приверженность лечению. По данным литературы, у пациентов с кардиоваскулярной коморбидностью НЯ в течение 6-недельной терапии лерканидипином в дозе 10 мг/сут встречались редко: покраснение лица у 0,3% пациентов, периферические отеки — у 0,14%, сердцебиение — у 0,06% [28]. В ходе настоящего исследования НЯ, связанные с приемом лерканидипина, не зарегистрированы.
В отношении индекса CAVI не отмечено значимой динамики показателя у пациентов, что обусловлено краткосрочностью наблюдения и требует дальнейшего изучения.
Заключение
Достижение целевого уровня АД исключительно важно в профилактике ССЗ у пациентов, перенесших ОКС и/или реваскуляризации. Оригинальный лерканидипин (Занидип®-Рекордати, Recordati Ireland, Ltd., Ирландия) в дозе 10 и 20 мг/сут позволяет эффективно достигать и поддерживать целевые уровни САД, ДАД, уменьшать частоту и интенсивность приступов стенокардии, обеспечивает стабильное сохранение эффекта терапии у пациентов с АГ после перенесенного ОКС и реваскуляризации миокарда. Отсутствие НЯ, характерных для всей группы АК в целом и амлодипина в частности, делает лерканидипин препаратом выбора в группе АК. Для выявления значимой динамики индекса CAVI необходимо дальнейшее длительное наблюдение пациентов.
Информация с rmj.ru





