Введение
Россия демонстрирует значительный прогресс в борьбе с туберкулезом, однако формы с множественной и широкой лекарственной устойчивостью (МЛУ/ШЛУ-ТБ) по‑прежнему представляют серьезную проблему[1] [1, 2]. Низкая эффективность их лечения приводит к формированию деструктивных форм заболевания, нередко требующих хирургического вмешательства [3]. Послеоперационные респираторные осложнения и неблагоприятные исходы во многом определяются исходным функциональным резервом кардиореспираторной системы пациента. Стандарты предоперационной оценки риска при резекциях легкого в основном разработаны для пациентов с раком легкого (РЛ) [4–6], у которых хирургическое лечение также остается важным компонентом комплексной терапии, и в клинической практике нередко экстраполируются на больных туберкулезом легких (ТЛ).
Общеизвестные алгоритмы оценки операционного риска основаны на показателях функции внешнего дыхания (ФВД), прежде всего объеме форсированного выдоха за первую секунду (ОФВ1), отражающем выраженность вентиляционных нарушений, а также диффузионной способности легких (ДСЛ) и расчете предсказанных послеоперационных значений [4–6]. Несмотря на широкое использование спирометрии, ОФВ1 и даже ДСЛ, измеренные в покое, не всегда позволяют точно предсказать, возникнут ли у пациента проблемы после операции [7], не могут адекватно отразить реальный функциональный резерв и возможности пациента в условиях повышенного кислородного запроса. Кардиопульмональное нагрузочное тестирование (КПНТ) с определением пикового потребления кислорода (VO2peak) и субмаксимальных показателей рассматривается как один из наиболее информативных методов стратификации функционального риска у пациентов с респираторной патологией, в том числе перед оперативными вмешательствами на легких [8, 9].
У больных ТЛ, особенно при деструктивных формах и посттуберкулезных изменениях, формируются выраженные морфофункциональные нарушения (фиброз, деформация бронхиального дерева, плевральные наслоения, сложные нарушения механики дыхания). Клинически это нередко сопровождается значительным снижением толерантности к физической нагрузке при относительно сохранных показателях ОФВ1 и ДСЛ в покое [10]. В отличие от пациентов с РЛ, у которых поражение часто носит локализованный характер, функциональные последствия туберкулезного процесса могут быть более диффузными и затрагивать как механические свойства дыхательной системы, так и системные компоненты (снижение массы тела и мышечной функции, последствия длительного воспаления).
В доступной литературе представлены данные о прогностической значимости VO2peak у кандидатов на резекцию по поводу РЛ. В клинической практике при предоперационной оценке риска обычно предполагается, что у больных ТЛ и РЛ при одинаковой степени снижения ОФВ1 и сходных значениях ДСЛ функциональные резервы и прогноз сопоставимы. Однако это допущение не подтверждено прямым сравнением данных КПНТ, и неизвестно, могут ли традиционные показатели ФВД и ДСЛ служить достаточной основой для предоперационной оценки риска у больных ТЛ.
Учитывая различия в характере поражения легких и системных последствиях заболевания, целью настоящего исследования мы определили проведение сравнительной оценки ДСЛ и показателей кардиопульмонального нагрузочного тестирования, включая пиковое потребление кислорода и субмаксимальные показатели, у больных с деструктивными (хирургическими) формами ТЛ и больных РЛ при сопоставимой степени снижения ОФВ1.
Содержание статьи
Материал и методы
Проведено ретроспективно-проспективное одноцентровое исследование на базе Центра торакальной хирургии ФГБУ «СПб НИИФ» Минздрава России с набором материала с 2015 по 2025 г.
Ретроспективно были изучены результаты исследований пациентов с ТЛ, для сравнения проспективно была обследована группа пациентов с РЛ. Все больные подписали информированное согласие на участие в исследовании и публикацию результатов в обезличенной форме. Исследование проведено в соответствии с этическими стандартами, изложенными в Хельсинкской декларации; одобрено локальным этическим комитетом ФГБУ «СПб НИИФ» Минздрава России (протокол № 101 от 20.12.2023).
Критерии включения: возраст 18–75 лет; верифицированный диагноз ТЛ (этиологическими и/или гистологическими методами) или РЛ; наличие показаний к резекции легких; проведенное КПНТ; подписанное информированное согласие. Критерии невключения: наличие противопоказаний к выполнению нагрузочных тестов; сочетание РЛ и ТЛ.
В исследование было включено 377 пациентов с хирургическими формами ТЛ и 169 больных РЛ. Среди больных ТЛ 263 (69,761%) пациента с фиброзно-кавернозным туберкулезом, 66 (17,507%) — с кавернозным туберкулезом, 47 (12,467%) — с туберкулемами и 1 (0,265%) пациент с цирротическим туберкулезом. Бактериовыделение микобактерий туберкулеза (МБТ) выявлено у 226 (59,95%) пациентов. Лекарственная чувствительность МБТ сохранялась у 108 (28,65%) пациентов, у 121 (32,09%) выявлена МЛУ у 123 (32,63%) — ШЛУ, у 25 (6,63%) — другие виды ЛУ. Длительность заболевания до 1 года — у 104 (27,59%) пациентов, от 1 года до 5 лет — у 145 (38,46%), более 5 лет — у 128 (33,95%). Распространенность поражения в пределах 1–2 сегментов была у 38 (10,1%) пациентов, в пределах одной доли — у 121 (32,1%), все легкое было поражено у 98 (26,0%), оба легких — у 120 (31,8%).
Среди пациентов с РЛ у 118 (69,8%) выявлен периферический процесс, у 48 (28,4%) — центральный, у 3 (1,8%) — их сочетание. Гистологический тип определялся на основе классификации эпителиальных опухолей Всемирной организации здравоохранения (2021): аденокарцинома была выявлена у 68 (40,2%) пациентов, плоскоклеточный рак — у 64 (37,9%), немелкоклеточный рак неуточненный — у 19 (11,2%), типичный карциноид — у 9 (5,3%), крупноклеточный рак — у 4 (2,4%), эпителиально-миоэпителиальный рак — у 1 (0,6%), мелкоклеточный — у 3 (1,8%), низкодифференцированный рак — у 1 (0,6%).
Исследование ФВД выполнено на комплексной установке MasterScreen Body Diffusion (VIASYS Healthcare, Германия) с использованием референтных величин, предложенных Европейским сообществом угля и стали (European Coal and Steel Community, 1993) [11], и в соответствии с техническими стандартами, изложенными в международных и российских рекомендациях [12–15]. Анализировали ОФВ1, форсированную жизненную емкость легких (ФЖЕЛ), тест Тиффно (ОФВ1/ЖЕЛ). Варианты вентиляционных нарушений определяли, опираясь на данные спирометрии и бодиплетизмографии. Исследование ДСЛ проведено методом одиночного вдоха по монооксиду углерода. Оценивали величину ДСЛ, скорректированную по уровню гемоглобина (DLCOHb). Интерпретацию данных ФВД проводили, опираясь на рекомендации АТО/ЕРО [16].
Кардиопульмональное нагрузочное тестирование с одновременным измерением газообмена, вентиляции, постоянным мониторированием 12-канальной ЭКГ, артериального давления и насыщения крови кислородом проводили на приборе OxyconPro с велоэргометром (VIASYS Healthcare, Германия) согласно рекомендациям по проведению и интерпретации КПНТ ЕРО и Американской кардиологической ассоциации [17, 18]. Для возможности не только измерить показатели на пиковой нагрузке, но и рассчитать анаэробный порог использовали протокол со ступенчато возрастающей нагрузкой с длительностью ступени 1 мин. Мощность прироста нагрузки рассчитывали индивидуально, исходя из должной (Д) максимальной величины с учетом тяжести состояния. Пациенты выполняли педалирование с частотой 60±10 оборотов в минуту до достижения предельных возможностей испытуемого или появления патологических критериев прекращения теста. Анализировали потребление кислорода на пиковой нагрузке (VO2peak) в мл/мин/кг и процентах (%) от должной величины максимального потребления кислорода (VO2max) и на анаэробном пороге (VO2-AT) в мл/мин/кг и %Д VO2max. Вентиляционный коэффициент по диоксиду углерода (VE/VCO2) оценивали на уровне анаэробного порога.
Статистический анализ выполняли с использованием пакета Statistica (версия 10 StatSoft Inc., США). В качестве описательных статистик использовали медиану и квартили (Ме [Q1–Q3]). Для оценки различий между группами применяли U-критерий Манна — Уитни, χ2 Пирсона. Различия считали статистически значимыми при p<0,05, при p≥0,05–0,1 они рассматривались как тенденция. Для оценки влияния нозологической формы (ТЛ или РЛ) на показатели ДСЛ и кардиореспираторных резервов при учете степени снижения функции внешнего дыхания применяли анализ ковариации (ANCOVA) в модуле General Linear Models. В качестве факторной переменной включали нозологическую принадлежность (ТЛ/РЛ), в качестве ковариаты — ОФВ1, выраженный в %Д. В расширенных моделях дополнительно учитывали возраст, индекс массы тела (ИМТ) и стаж курения (пачка-лет). Различия между группами интерпретировали по скорректированным средним значениям с 95% доверительными интервалами. Нормальность распределения остатков и гомогенность дисперсий проверяли с использованием визуальных методов (Q–Q графики) и теста Левена.
Результаты и обсуждение
Для стратификации пациентов по уровню ОФВ1 был выбран порог в 60%Д как клинически значимый, отражающий переход к выраженному снижению бронхиальной проходимости и неблагоприятному функциональному профилю. Сравнительная характеристика пациентов с хирургическими формами ТЛ и РЛ в подгруппах с ОФВ1 ≥60%Д и <60%Д представлена в таблице 1.
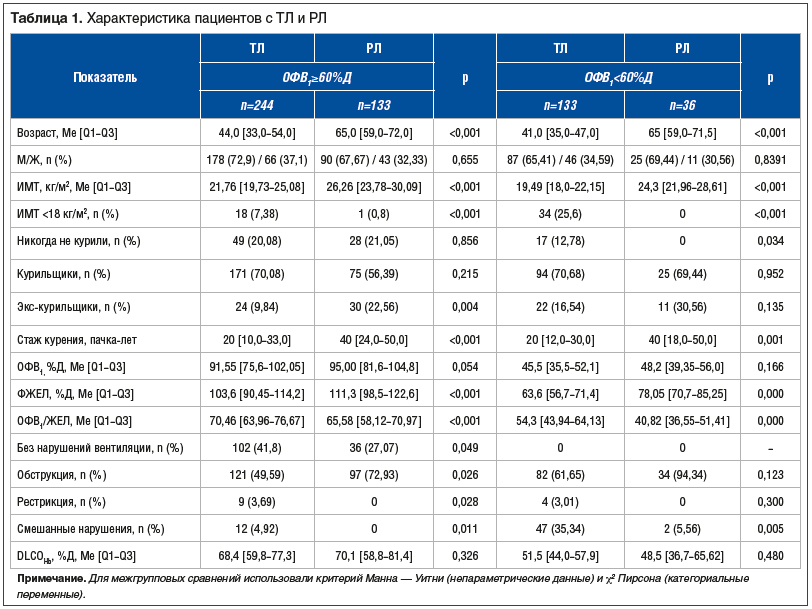
При стратификации по ОФВ1 ≥60%Д и <60%Д группы пациентов с РЛ и ТЛ оказались не одинаковы по ряду фоновых признаков: пациенты с ТЛ существенно моложе пациентов с РЛ (около 44 лет против 65 лет), имели более низкий ИМТ, в том числе у них чаще регистрировали ИМТ<18 кг/м2.
В группе с ТЛ отмечалась заметная доля никогда не куривших, тогда как в группе с РЛ при ОФВ1<60%Д таких пациентов не было. Кроме того, для больных РЛ был характерен больший стаж курения и бόльшая доля экс-курильщиков. Несмотря на сопоставимые категории ОФВ1, характер вентиляционных нарушений различался: у пациентов с ТЛ и при ОФВ1≥60%Д, и при ОФВ1<60%Д были выявлены рестриктивные нарушения, среди пациентов с РЛ таких нарушений не выявлено; смешанные нарушения при ОФВ1≥60%Д выявлены только у больных ТЛ, при ОФВ1<60%Д этот вариант вентиляционных нарушений выявлен только у 2 больных РЛ, значительно чаще он встречался у пациентов с ТЛ; у пациентов с РЛ преобладал обструктивный вариант вентиляционных нарушений в обеих подгруппах. Соответственно в обеих подгруппах ФЖЕЛ была больше в группе пациентов с РЛ, тест Тиффно — в группе пациентов с ТЛ. Статистически значимых различий по ДСЛ не оказалось.
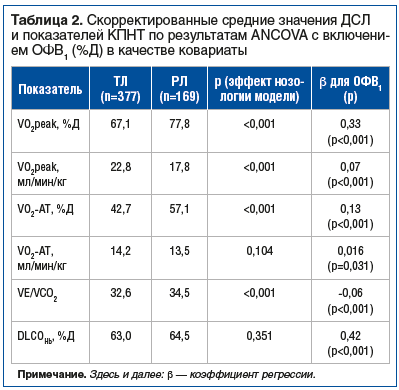
Для анализа различий между результатами ДСЛ и КПНТ у больных РЛ и ТЛ первоначально данные были скорректированы по ОФВ1 (табл. 2). По данным базовой модели ANCOVA, где фактором был заявлен диагноз, а ковариатой ОФВ1 (%Д), между скорректированными средними значениями DLCOHb у больных ТЛ и РЛ статистически значимых различий также не было (63,0%Д против 64,5%Д, p>0,05). Скорректированные средние потребления кислорода на пике нагрузки и на анаэробном пороге в процентах от должных значений (VO2peak и VO2-AT) у больных ТЛ были ниже, чем у больных РЛ (67,1% против 77,8%, 42,7% против 57,1% соответственно, р<0,001), однако в абсолютных значениях на 1 кг массы тела VO2peak оказался выше у пациентов с ТЛ (22,8 мл/мин/кг против 17,8 мл/мин/кг, p<0,001). Скорректированные по ОФВ1 средние значения потребления кислорода на анаэробном пороге у пациентов с ТЛ и РЛ не отличались (14,2 против 13,5, p>0,05).
В связи с выявленными межгрупповыми различиями по возрасту, ИМТ и статусу курения при оценке влияния нозологической формы на показатели ДСЛ и показатели КПНТ дополнительно строили расширенные модели ANCOVA, в которые, помимо ОФВ1 (%Д), в качестве ковариат включали возраст, ИМТ и стаж курения (пачка-лет). Сравнение результатов базовой модели (с коррекцией только по ОФВ1) и расширенной модели использовали для оценки устойчивости ассоциации между нозологической формой и функциональными показателями (табл. 3).
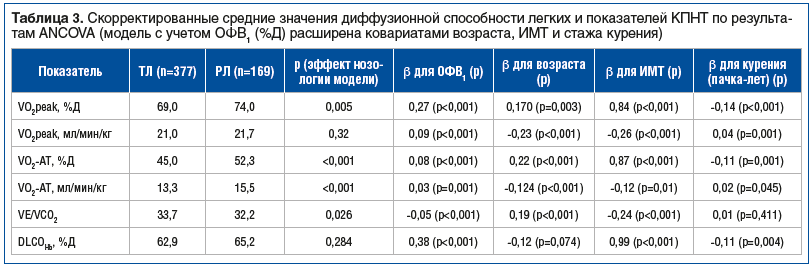
В расширенной модели множественной линейной регрессии потребление кислорода на пиковой нагрузке (VO2peak, %Д) и на анаэробном пороге (VO2-AT, %Д и мл/мин/кг) было статистически значимо ниже у пациентов с ТЛ. Важно отметить, что в базовой модели VO2peak (мл/мин/кг) был выше у больных ТЛ, что, вероятно, связано с их более молодым возрастом и меньшей массой тела. Однако после корректировки на возраст, ИМТ и стаж курения влияние этих факторов нивелировалось, и нозология (ТЛ) ассоциировалась уже с более низкими абсолютными значениями VO2peak по сравнению с РЛ при одинаковом уровне ОФВ1. Вентиляционный эквивалент на анаэробном пороге (VE/VCO2) у пациентов с ТЛ был выше, чем у пациентов с РЛ. Скорректированные средние значения ДСЛ в расширенной модели между пациентами с ТЛ и РЛ также не различались.
С учетом значимого влияния ОФВ1 на потребление кислорода и вентиляционный эквивалент VE/VCO2 пациенты были стратифицированы по уровню ОФВ1: ≥60%Д и <60%Д. Скорректированные средние значения показателей КПНТ и ДСЛ у больных ТЛ и РЛ в расширенной модели ANCOVA с учетом ОФВ1, возраста, ИМТ и стажа курения в группе пациентов с ОФВ1 ≥60%Д представлены в таблице 4.
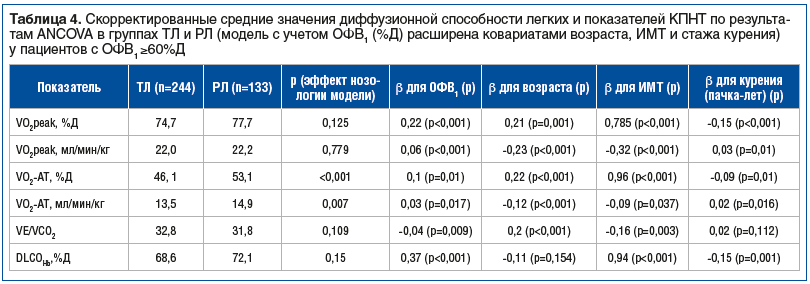
У пациентов с ТЛ и РЛ без значительных нарушений вентиляции различия по VO2peak оказались несущественными, однако на анаэробном пороге потребление кислорода было значительно ниже как в процентах от должной величины VO2max, так и в единицах на 1 кг массы тела.
Скорректированные средние значения показателей КПНТ и ДСЛ по результатам в группах ТЛ и РЛ у пациентов со значительными вентиляционными нарушениями (ОФВ1 <60%Д) представлены в таблице 5.
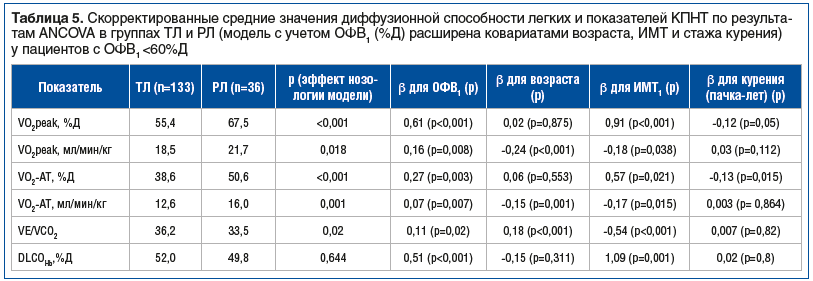
При значительных вентиляционных нарушениях у пациентов с ТЛ потребление кислорода было статистически значимо ниже по сравнению с пациентами с РЛ как при пиковой нагрузке (VO2peak), так и на анаэробном пороге. Это различие сохранялось и в процентах от должной величины, и на 1 кг массы тела. Вентиляционный эквивалент был значимо выше у пациентов с ТЛ. ДСЛ у пациентов с ТЛ по сравнению с пациентами с РЛ не различалась как при ОФВ1≥60%Д, так и при ОФВ1<60%Д.
Результаты проведенного исследования демонстрируют, что при сопоставимой степени вентиляционных нарушений, оцениваемой по ОФВ1, у пациентов с деструктивным ТЛ и РЛ наблюдаются существенные различия в толерантности к физической нагрузке, оцениваемой методом кардиопульмонального нагрузочного тестирования. Непереносимость физической нагрузки — сложный синдром, определяемый неадекватным энергетическим потребностям организма уровнем потребления кислорода [19]. Непереносимость физической нагрузки у пациентов с заболеваниями легких не может быть надежно предсказана по физиологическим показателям, определяемым в покое, таким как ОФВ1 и ДСЛ. Длительное время спирометрия рассматривалась как основной стандарт функциональной оценки, однако многочисленные исследования показали, что нарушения респираторной функции и связанные с ними неблагоприятные исходы могут возникать, несмотря на нормальные показатели спирометрии [20]. В покое нарушения функции внешнего дыхания не всегда выявляются благодаря компенсаторным механизмам, но они становятся очевидными при КПНТ, когда дозированная физическая нагрузка сопровождается регистрациейпоказателей вентиляции, газообмена, работы сердечно-сосудистой системы [10, 21, 22]. Нарушение толерантности к физической нагрузке влияет не только на качество жизни, но и на клинический исход и ассоциировано с увеличением смертности [23–25].
Главным и наиболее клинически важным выводом является статистически значимо более низкое потребление кислорода у пациентов с ТЛ как на пике нагрузки (VO2peak), так и на уровне анаэробного порога (VO2-AT). Эти различия сохранялись и усиливались в подгруппе пациентов с выраженными вентиляционными нарушениями (ОФВ1<60%Д), где показатели VO2peak и VO2-AT у больных ТЛ были достоверно ниже, чем у пациентов с РЛ. Более низкие показатели не только пикового потребления кислорода, но и уровня анаэробного порога свидетельствуют о более низкой толерантности к нагрузке у пациентов с ТЛ по сравнению с больными РЛ при одинаковом снижении ОФВ1.
Данный факт свидетельствует о более существенном снижении функциональных резервов кардиореспираторной системы у пациентов с хирургическими формами туберкулеза, которое не улавливается стандартным измерением ОФВ1, и ДСЛ в покое. Примечательно, что в абсолютных значениях на 1 кг массы тела VO2peak у пациентов с ТЛ был выше, что, вероятно, связано со значимо более низким ИМТ в этой группе. После поправки на ИМТ в расширенной модели у пациентов различия по абсолютным значениям VO2peak нивелировались, а по относительным сохранялись.
Отсутствие статистически значимых различий в скорректированных показателях ДСЛ между группами ТЛ и РЛ подчеркивает важный клинический тезис: у пациентов с деструктивным туберкулезом снижение толерантности к нагрузке в большей степени обусловлено не альвеолярно-капиллярным блоком, а другими факторами. Более диффузный и гетерогенный характер поражения легочной ткани при ТЛ по сравнению с часто локальным процессом при РЛ, сложные нарушения механики дыхания вследствие фиброза, плевральных наслоений и деформации бронхиального дерева приводят к повышенной работе дыхания и неэффективной вентиляции. На это указывает более высокий вентиляционный эквивалент по CO2 (VE/VCO2) у пациентов с ТЛ, особенно в группе с ОФВ1<60%Д, что также может влиять на соотношение вентиляции к кровотоку и недостаточную эффективность газообмена при нагрузке. Нельзя исключить влияние системных эффектов хронического воспаления: кахексии, снижения мышечной массы и дисфункции периферических мышц, которые не отражаются в показателях ФВД, но критически влияют на способность к физической работе.
Проведенный анализ с коррекцией на ключевые конфаундеры (возраст, ИМТ, стаж курения) подтвердил устойчивость выявленной ассоциации между нозологической формой (ТЛ) и сниженными показателями нагрузочного тестирования. Это позволяет утверждать, что обнаруженные различия не являются артефактом разницы в демографических характеристиках групп.
Полученные данные ставят под сомнение правомерность прямой экстраполяции общепринятых алгоритмов предоперационного риска, разработанных преимущественно для онкологических пациентов, на больных с деструктивным ТЛ. Ориентация только на ОФВ1 в покое может привести к недооценке функционального риска у этой категории больных. Наши результаты подтверждают, что КПНТ, и в частности определение VO2 на анаэробном пороге, обладает более высокой дискриминативной способностью для выявления скрытого снижения резервов у пациентов с ТЛ.
Ограничения исследования включают его наблюдательный дизайн (ретроспективно-проспективный), что не исключает влияния неучтенных факторов. Группы пациентов с ТЛ и РЛ существенно различались по возрасту, ИМТ, стажу курения, однако применение методов многомерного анализа (ANCOVA) позволило скорректировать эти различия. Для подтверждения выводов и установления конкретных пороговых значений показателей КПНТ, ассоциированных с послеоперационными исходами у больных ТЛ, необходимы дальнейшие проспективные исследования.
Выводы
У пациентов с хирургическими формами ТЛ при сопоставимой степени снижения ОФВ1 толерантность к физической нагрузке ниже, чем у больных РЛ. Это проявляется снижением пикового потребления кислорода и потребления кислорода на уровне анаэробного порога.
Выявленные различия в показателях кардиопульмонального нагрузочного тестирования не объясняются возрастом, ИМТ, стажем курения и ДСЛ. При учете этих факторов нозологическая форма (ТЛ против РЛ) остается независимым предиктором менее благоприятного функционального статуса.
Использование только показателя ОФВ1 может приводить к недооценке функционального риска у пациентов с деструктивным ТЛ. Для нозологически ориентированной оценки операбельности в этой группе следует включать исследование диффузионной способности легких и кардиопульмональное нагрузочное тестирование в стандарт предоперационного функционального обследования.
Полный список литературы Вы можете найти на сайте http://www.rmj.ru
[1] Global tuberculosis report 2025. Geneva: World Health Organization; 2025. (Electronic resource.) URL: https://www.who.int/teams/global-programme-on-tuberculosis-and-lung-health/tb-reports/global-tubercu… (access date: 25.02.2026).
Информация с rmj.ru


