Ацетил-L-карнитин в лечении периферической нейропатической боли: систематический обзор и метаанализ рандомизированных контролируемых исследований (реферат)
Содержание статьи
Введение
Периферическая нейропатическая боль обусловлена поражением периферических нервов, которое может быть результатом осложнений сахарного диабета, побочного действия лекарственных препаратов или иных состояний. Периферическая нейропатическая боль, хотя и не угрожает жизни, существенно влияет на ее качество. Она ассоциирована с большой распространенностью депрессии [1] и других психических расстройств, которые могут усугублять основное заболевание.
В настоящее время основную стратегию лечения периферической нейропатической боли составляет симптоматическая терапия [2]. Однако, несмотря на высокую стоимость медикаментов и их потенциальное побочное действие, во многих случаях подобное лечение оказывается малоэффективным [3]. Поэтому поиск новых препаратов для купирования периферической нейропатической боли весьма актуален.
Ацетил-L-карнитин играет фундаментальную роль в метаболизме жирных кислот в митохондриях и модулирует действие факторов роста нервов и нейротрансмиттеров в нервной системе [4]. Хотя в последние годы неоднократно предпринимались попытки использовать ацетил-L-карнитин для лечения диабетической и недиабетической периферической нейропатии, его эффекты остаются противоречивыми. Учитывая вышеизложенное, мы провели систематический обзор рандомизированных контролируемых испытаний (РКИ) с целью определить эффективность и безопасность ацетил-L-карнитина по сравнению с плацебо или другими активными препаратами у пациентов с диабетической и недиабетической периферической нейропатией.
Материал и методы
Методология настоящего исследования соответствует положениям инструкции «Предпочтительные параметры отчетности для систематических обзоров и метаанализа» (PRISMA).
Поиск по базам данных
Выполнен поиск релевантных статей по базам данных MEDLINE (1996–2014), EMBase (1974–2014) и CENTRAL (May 2014) вплоть до 27 июня 2014 г. с использованием комбинаций следующих ключевых слов: «карнитин», «нейро», «нейропатическая боль» и «нейропатия». Кроме того, осуществлялся поиск вручную по списку литературы с целью обнаружения дополнительных потенциально значимых исследований. Публикации проверяли на дублирование. Также определяли наличие перекрывающихся публикаций. Популяции пациентов считали перекрывающимися, если они имели одинаковые критерии: больница, автор, период наблюдения и разновидность вмешательства. В случае дублированных или перекрывающихся популяций пациентов мы включали в метаанализ более информативные или более поздние публикации.
Критерии включения и исключения
Подходящие исследования должны были удовлетворять следующим критериям: 1) относились к РКИ; 2) включались пациенты с диабетом и без диабета с периферической нейропатической болью, диагностированной по клинической картине и/или нейрофизиологическим изменениям конечностей; 3) назначался ацетил-L-карнитин (любой способ введения); 4) в качестве контроля использовались плацебо или другие положительные контрольные препараты; 5) для оценки первичной конечной точки применялась визуально-аналоговая шкала (ВАШ), в качестве вторичных конечных точек выступали побочные эффекты.
В метаанализ включали только публикации на английском языке. Мы исключали: тезисы конференций, не содержащие оригинальных данных; исследования без адекватного анализа конечных точек; дублированные и перекрывающиеся публикации.
Извлечение данных
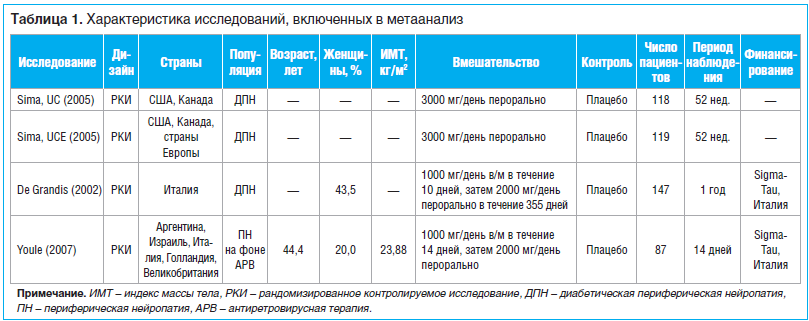
Два независимых исследователя (S.L. и Q.L.) просматривали все публикации, обнаруженные в ходе поиска. Разногласия устранялись путем консультации с третьим экспертом (H.T.). Данные из выделенных исследований отбирались независимым образом с использованием специальной формы. Регистрировались следующие характеристики исследований: первый автор, год публикации, название, дизайн, источник финансирования, страна, по пациентам — пол, средний возраст, индекс массы тела (ИМТ), вмешательство, численность в основной и контрольной группах, продолжительность периода наблюдения, критерии диагноза нейропатии, количество баллов по ВАШ и число побочных эффектов в каждой группе.
Оценка риска смещения исследований
Два исследователя (S.L. и Q.L.) независимо оценивали риск смещения каждого из включенных исследований с помощью инструмента «оценка смещения» из рекомендаций Кохрейновского сотрудничества [5], который включает 7 доменов (генерация рандомизационных последовательностей, сокрытие распределения испытуемых в группы вмешательства, ослепление испытуемых и медицинских работников, ослепление экспертов, предоставление сведений о неполных исходах, предоставление сведений о селективных исходах и «другое»). Инструмент снабжен понятными и четкими инструкциями, которые помогают оценить риск смещения как «высокий», «низкий» или «неопределенный». Разногласия в оценке устранялись путем обсуждения.
Статистический анализ
Статистический анализ осуществляли с помощью программного обеспечения Review Manager 5.2.7 (Копенгаген, Северный Кохрейновский центр, Кохрейновское сотрудничество, 2012). Для характеристики непрерывных данных для каждого исследования вычислялось среднее отклонение (MD) и 95% доверительный интервал (ДИ). Гетерогенность исследований изначально оценивалась графически путем анализа форест-графиков, а затем с использованием критерия однородности хи-квадрат (χ2) и индекса несовместимости (I2) [6]. Исследования считались статистически достоверно гетерогенными при Р50%. Исследования объединялись в пул с помощью модели со случайными эффектами [7] при наличии статистической или иной гетерогенности или с помощью модели с фиксированными эффектами во всех иных случаях [8]. Анализ по подгруппам проводили в зависимости от причины нейропатии (сахарный диабет или иное) и способа введения ацетил-L-карнитина. Для оценки стабильности результатов анализировалась чувствительность путем исключения одного исследования за раз.
Результаты исследования
На рисунке 1 представлены результаты отбора статей. После скрининга 717 статей подходящими были признаны 3 статьи [9–11], в которых сообщалось о 4 РКИ с участием 523 пациентов. В 3 исследованиях участвовали пациенты с диабетической периферической нейропатией [9, 10], а в одном — пациенты с периферической нейропатией, вызванной действием противовирусных препаратов [11]. Только в 1 исследовании [11] были представлены данные о возрасте испытуемых (в среднем 44,4 года) и ИМТ (в среднем 23,88 кг/м2, табл. 1). Во всех исследованиях эффекты ацетил-L-карнитина сравнивались с эффектами плацебо. В ходе 2 исследований [9] ацетил-L-карнитин вводился перорально, в ходе других 2 исследований [10, 11] — последовательно внутримышечно и перорально. Продолжительность периода наблюдения варьировала от 14 дней до одного года.
Результаты оценки качества представлены на рисунке 1 и в таблице 2. Только 1 исследование [10] оказалось лишено всех вариантов смещения за исключением того смещения, о котором в нем сообщалось. Что касается других исследований [9, 11], то по ним остались вопросы относительно смещения отбора, смещения оценки, смещения обнаружения и селективного смещения.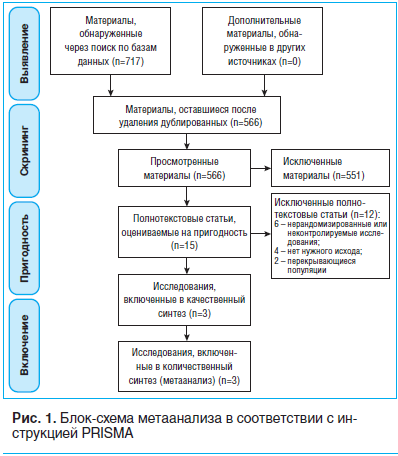
Влияние ацетил-L-карнитина на болевой синдром
Во всех 4 исследованиях [9–11] влияние ацетил-L-карнитина на болевой синдром оценивали по ВАШ. Несмотря на отсутствие статистически достоверной гетерогенности исследований, для анализа была использована модель со случайными эффектами, поскольку популяции испытуемых были разными. Совокупные результаты свидетельствуют о том, что ацетил-L-карнитин уменьшает болевой синдром по сравнению с плацебо, причем разница статистически достоверна (MD по ВАШ 1,20; 95% ДИ 0,68–1,72; P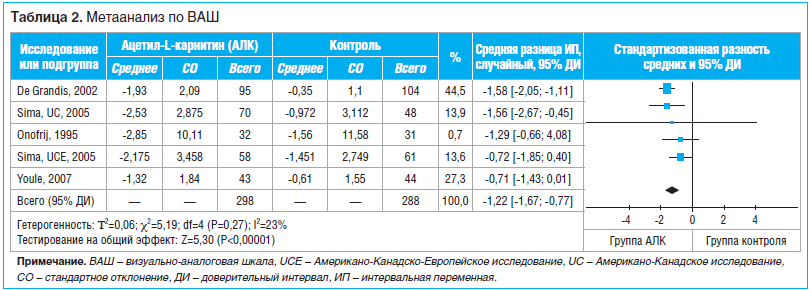
Анализ по подгруппам осуществляли путем РКИ в зависимости от генеза периферической нейропатии (диабетическая или недиабетическая). В 3 исследованиях [9, 10] участвовали пациенты с диабетической периферической нейропатией, в 1 исследовании [11] — пациенты с недиабетической периферической нейропатией. В подгруппе с диабетом не обнаружено достоверной гетерогенности исследований (I2=0%, P=0,38), в связи с чем была выбрана модель с фиксированными эффектами. Результаты анализа (табл. 3) свидетельствуют о том, что у пациентов с диабетом, получавших ацетил-L-карнитин, сумма баллов по ВАШ достоверно уменьшилась по сравнению с суммой баллов у пациентов из группы плацебо (MD -1,47; 95% ДИ -1,87; 1,06, P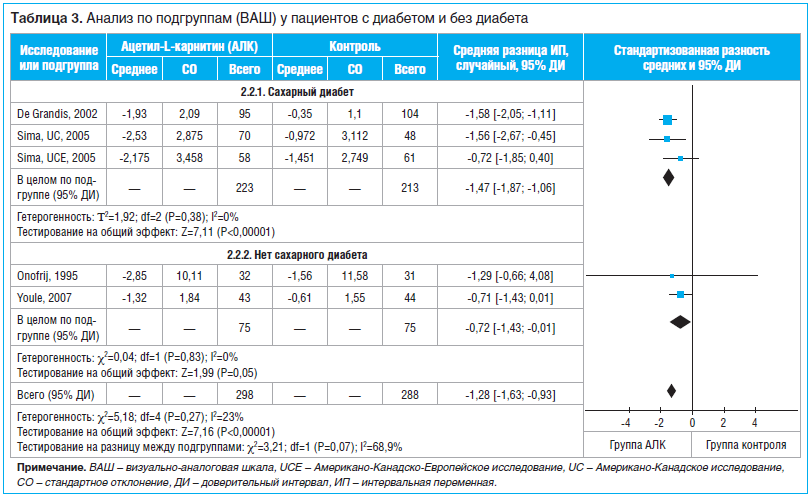
Также был проведен анализ по подгруппам в зависимости от способа введения ацетил-L-карнитина. В ходе 2 РКИ [10, 11] ацетил-L-карнитин вводили последовательно внутримышечно и перорально, в ходе 2 других [9] — только перорально. Влияние способа введения на сумму баллов по ВАШ оказалось одинаковым (MD 1,19; 95% ДИ 0,34–2,04; P=0,006 и MD 1,15; 95% ДИ 0,33–1,96; P=0,006).
Побочные явления
Между группами лечения не было выявлено статистически достоверной разницы по частоте встречаемости побочных эффектов (табл. 4).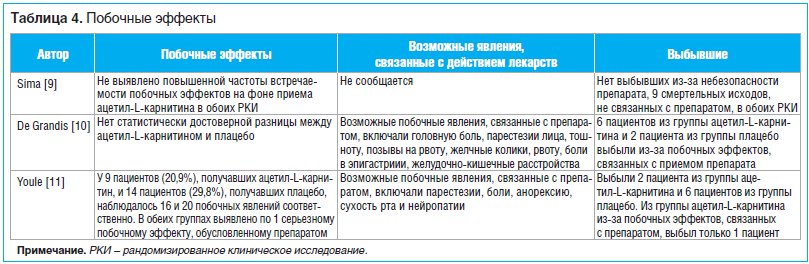
Обсуждение результатов
Периферической нейропатической боли придается особое значение в силу того, что она доставляет пациентам страдания, оказывая существенное влияние на качество жизни [12]. Одной из основных причин этого болевого синдрома является сахарный диабет. Примерно треть пациентов с сахарным диабетом испытывают нейропатические боли [13]. Хотя ацетил-L-карнитин часто назначают при периферической нейропатической боли, этот препарат не упоминается в большинстве современных руководств по лечению болевого синдрома на фоне диабетической нейропатии [14]. Мы не встречали среди научных публикаций ни одного систематического обзора, в котором рассматривалось бы влияние ацетил-L-карнитина на периферическую нейропатическую боль. Учитывая это, мы отобрали и проанализировали все значимые РКИ и выяснили, что ацетил-L-карнитин эффективно и безопасно облегчает болевой синдром при периферической нейропатии.
Ацетил-L-карнитин необходим для метаболизма жирных кислот в митохондриях. Он способен повышать болевой порог за счет активации холинергических влияний [15], что, как считают, связано с экспрессией гена GRM2 [16]. Дефицит карнитина приводит к подавлению выработки энергии вследствие нарушения деградации жирных кислот [17] и, по сообщениям, ассоциирован с развитием сахарного диабета и его осложнений [18]. У пациентов с диабетической ретинопатией, диабетической нейропатией и сахарным диабетом в сочетании с гиперлипидемией существенно снижен уровень общего и свободного карнитина по сравнению с пациентами с диабетом без осложнений или сопутствующих заболеваний. Результаты ряда обсервационных исследованай свидетельствуют о явном облегчении симтоматики после назначения ацетил-L-карнитина пациентам с периферической нейропатической болью [19–21].
Как было продемонстрировано в ходе нашего метаанализа, ацетил-L-карнитин статистически достоверно уменьшает сумму баллов по ВАШ. И хотя подсчет суммы баллов по этой шкале субъективен, доказано, что ВАШ — это новый достоверный способ оценки симптоматики при периферической нейропатической боли, т. е. таким больным можно помочь путем назначения ацетил-L-карнитина. Результаты другого исследования [21], в котором использовали модифицированную краткую форму опросника боли Макгилла, свидетельствуют о значительном уменьшении болевого синдрома через 3 нед. после начала лечения ацетил-L-карнитином по сравнению с исходным уровнем. В ходе ряда других исследований [10, 21–23] в группах получавших ацетил-L-карнитин и плацебо сравнивали данные электромиографии — стандартного исследования при периферической нейропатической боли [14]. Данные электромиографии позволяют говорить о существенном повышении скорости проведения возбуждения по чувствительным и двигательным нервам на фоне лечения ацетил-L-карнитином. Абстрагируясь от периферической нейропатической боли, упомянем, что корешковую боль можно облегчить с помощью ацетил-L-карнитина [24, 25].
Согласно результатам анализа по подгруппам, пациенты с периферической нейропатической болью на фоне сахарного диабета, по-видимому, лучше реагируют на ацетил-L-карнитин, чем пациенты с болевым синдромом иного генеза, что соотносится с выводами последних систематических обзоров [26, 27]. Так, результаты одного из обзоров по диабетической нейропатии [26], который включал 2 РКИ [10, 28], свидетельствуют о том, что ацетил-L-карнитин облегчает болевой синдром при нейропатии. Впрочем, результаты другого обзора, по ВИЧ-ассоциированной нейропатии, который включал 1 РКИ [11], не демонстрируют превосходства ацетил-L-карнитина перед плацебо. Эту разницу можно объяснить восстановлением уровня карнитина у пациентов с периферической нейропатической болью диабетического генеза. Поскольку в обзоре ВИЧ-ассоциированной нейропатии [11] речь шла только об 1 РКИ, неэффективность ацетил-L-карнитина также может быть связана с ограничениями самого исследования, такими как низкая доза препарата и короткий период наблюдения. Как бы то ни было, выводы неоднозначны из-за ограниченного объема данных. Результаты другого анализа по подгруппам указывают на то, что пероральный прием ацетил-L-карнитина оказывает тот же эффект, что и последовательное применение (внутримышечное и пероральное), но пероральный прием удобнее.
Вопрос об эффективной дозе ацетил-L-карнитина пока остается открытым. Однако результаты исследований, включенных нами в метаобзор, демонстрируют больший эффект от дозировки более 2000 мг/день [9, 10], в то время как при дозе менее 1500 мг/день суммы баллов по шкале ВАШ (величина Р неизвестна) уменьшается не столь выраженно [9]. Необходимы новые исследования для подбора дозы ацетил-L-карнитина.
Поскольку химическая структура ацетил-L-карнитина идентична незаменимым компонентам организма, его введение не должно причинять вреда. Полученные нами результаты свидетельствуют о том, что ацетил-L-карнитин безопасен и не вызывает никаких побочных эффектов.
Приведенный метаанализ имеет некоторые ограничения, в частности непродолжительный период наблюдения.
Выводы
Таким образом, современные данные позволяют предполагать, что ацетил-L-карнитин является эффективным и безопасным средством лечения периферической нейропатической боли, особенно на фоне сахарного диабета. Рекомендован пероральный прием ацетил-L-карнитина, поскольку при сопоставимой эффекивности он более удобный. Впрочем, необходимы новые исследования с бóльшим объемом выборок, разнообразием популяций испытуемых и более продолжительным периодом наблюдения.
Реферат подготовлен редакцией «РМЖ» по материалам статьи: Li S., Li Q., Li Y. et al. Acetyl-L-Carnitine in the Treatment of Peripheral Neuropathic Pain: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. PLoS One. 2015;10(3):e0119479. DOI: 10.1371/journal.pone.0119479.
Информация с rmj.ru