Введение
Стромальный герпетический кератит (ГК) — одна из наиболее тяжелых форм герпетического поражения глаз. Включение стромального ГК в разряд сложных заболеваний связано в большинстве случаев с вовлечением в воспаление сосудистой оболочки глаза, риском развития рецидивирующего течения и, наконец, с формированием стойких помутнений роговицы, что приводит к снижению качества жизни пациента. Вовлечение в патологический процесс стромы роговицы связано с выходом вирусной инфекции из-под контроля иммунной системы и активацией аутоиммунного воспаления, сохраняющегося даже после инактивации вируса [1–4]. Кроме того, репликация герпесвируса приводит к повреждению нервов и потере чувствительности роговицы, вызывая нейротрофическую кератопатию [1, 2].
Медикаментозное лечение ГК на сегодняшний день включает химиотерапию (применение аналогов нуклеозидов), иммунную терапию (использование интерферонов, интерфероногенов, препаратов, активирующих клеточное звено иммунитета и пр.), специфическую терапию (герпетическая вакцина, противогерпетический иммуноглобулин) [5, 6]. Кроме того, в ведении пациентов с данной патологией можно выделить два этапа: первый — непосредственное лечение активной вирусной инфекции и воспаления тканей глаза, о чем было сказано выше; второй — лечение осложнений перенесенного заболевания (помутнений роговицы, поствоспалительного синдрома «сухого глаза», неоваскуляризации роговицы). Длительное противовирусное лечение с применением пероральных аналогов нуклеозидов используется в качестве терапии первой линии для лечения первичной и рецидивирующей герпетической инфекции уже более четырех десятилетий [2]. Данная стратегия лечения эффективно подавляет литическую репликацию вируса, а для предотвращения реактивации нередко требуется длительное лечение малыми дозами аналогов нуклеозидов. Здесь следует отметить, что основным недостатком перорального приема аналогов нуклеозидов является их ограниченная биодоступность (10–20%) и короткий период полувыведения из крови, что требует высоких суточных доз в течение длительного времени для достижения терапевтической концентрации в роговичной ткани [7]. Однако длительное применение противовирусных препаратов, особенно в случаях рецидивирующего кератита, когда требуется увеличение суточной дозы препарата, может вызывать токсическое повреждение печени и почек, а также способствует росту числа устойчивых к аналогам нуклеозидов штаммов герпесвирусов [8]. Кроме того, при использовании противовирусных препаратов в лечении ГК происходит лишь подавление репликации вируса, но данные препараты малоэффективны в контроле аутоиммунного воспаления стромы. В качестве сопутствующей терапии с целью более быстрого подавления как инфекционного, так и аутоиммунного воспаления следует использовать иммунные препараты (топические, системные) и местные противовоспалительные препараты (нестероидные противовоспалительные препараты (НПВП), «мягкие» глюкокортикостероиды) [9–13]. Таким образом, терапия тяжелых стромальных ГК представляет собой комплекс мер по активному подавлению репликации герпетических вирусов, купированию симптомов воспаления, восстановлению нормальной работы как локального, так и системного иммунитета, лечению осложнений и профилактике рецидивов.
Цель исследования: сравнительный анализ клинического течения стромального ГК при различных схемах лекарственной терапии.
Материал и методы
Под нашим наблюдением в период с 2023 по 2025 г. находилось 36 пациентов (36 глаз) — 14 (38,9%) мужчин, 22 (69,1%) женщины — со стромальным ГК. Средний возраст составил 38,6±13,3 года (минимальный — 18 лет, максимальный — 61 год).
Критерии включения в исследование:
-
подписанная форма информированного согласия, подтверждающая согласие пациента на участие в исследовании;
-
возраст старше 18 лет;
-
стромальный ГК с изъязвлением и без изъязвления;
-
отрицательные результаты анализов крови на ВИЧ, сифилис, гепатиты В и С;
-
возможность амбулаторного наблюдения пациента.
Критерии невключения в исследование:
-
невозможность или нежелание пациента дать информированное согласие на участие в исследовании или на выполнение требований исследования;
-
поверхностные формы ГК;
-
сахарный диабет 1 или 2 типа; тяжелая легочная, почечная, печеночная, сердечно-сосудистая патология; онкологические, аллергические системные заболевания и другие заболевания, которые, по мнению исследователя, не позволили бы пациенту участвовать в исследовании.
В зависимости от проводимой терапии пациенты были разделены на 3 группы (табл. 1). В качестве топической иммунной терапии пациентам группы I назначали интерферон α-2b с кратностью инстилляций в конъюнктивальную полость 6–8 р/сут (согласно инструкции к применению препарата). Пациенты групп II и III получали препарат суммы полисахаридов побегов Solanum tuberosum Панавир® (лекарственная форма — глазные капли) с кратностью инстилляций в конъюнктивальную полость 4 р/сут (согласно инструкции к применению препарата). Местную противовоспалительную терапию назначали с первого дня наблюдения за пациентом: на первом этапе (4–5 дней) использовали НПВП бромфенак, с последующим введением в схему топической терапии «мягкого» глюкокортикостероида с контролем внутриглазного давления и состояния роговицы. Кроме того, пациентам всех трех групп назначали топическую терапию антисептиком пиклоксидин с кратностью инстилляций 4 р/сут (согласно инструкции к применению препарата). Пациентам группы III дополнительно к системной терапии пероральными аналогами нуклеозидов и топической терапии назначали внутривенное введение препарата Панавир® (см. табл. 1). Суточные дозы и продолжительность применения аналогов нуклеозидов были основаны на накопленном совместном с инфекционистами-иммунологами опыте лечения пациентов с тяжелыми формами офтальмогерпеса [14–16]. Системность герпетической инфекции служит веским и однозначным обоснованием для назначения интенсивной системной противовирусной терапии в повышенных дозировках. ГК нередко характеризуются упорным, затяжным течением, в связи с чем мы (совместно с инфекционистами-иммунологами) рекомендуем длительный прием аналогов нуклеозидов — не менее 10–20 дней. Кроме того, на этапе реконвалесценции продолжительность приема этих препаратов целесообразно увеличить, поскольку в этот период сохраняется высокий риск рецидива заболевания.

Осмотр пациентов проводили еженедельно до полного купирования симптомов активного воспаления. Сравнительный анализ интенсивности симптомов воспаления в группах проводили, используя данные, полученные во время первого визита пациента, и на 20-й день терапии (после завершения перорального приема высоких доз (1000 мг/сут) аналогов нуклеозидов).
В качестве критериев оценки интенсивности воспаления были выбраны:
-
жалобы пациентов на чувство дискомфорта, сухости, боли в глазу;
-
степень интенсивности гиперемии конъюнктивы (отсутствует, умеренная гиперемия, выраженная гиперемия);
-
степень выраженности роговичного синдрома, которую оценивали при помощи схемы, предложенной Е.В. Яни и соавт. [13]: 1 балл — роговичный синдром отсутствует при направлении света щелевой лампы; 2 балла — роговичный синдром не проявляется при дневном свете, но проявляется при направлении света щелевой лампы; 3 балла — роговичный синдром проявляется при дневном свете; 4 балла — роговичный синдром проявляется при комнатном освещении;
-
окрашивание роговицы витальным красителем (флюоресцеином);
-
тактильная чувствительность роговицы оценивалась как «нормальная», «сниженная», «отсутствует» при помощи ватного фитилька в пяти точках: центр и 4 точки (назальная, темпоральная, верхняя, нижняя) по периферии роговицы.
Лабораторная диагностика включала проведение следующих тестов: общеклинический анализ крови и молекулярные методы подтверждения активности герпетических вирусов. Лабораторное подтверждение репликации герпесвирусов проводили при помощи метода полимеразной цепной реакции (ПЦР). Наличие ДНК вируса простого герпеса (ВПГ), вируса варицелла-зостер (ВВЗ), вируса Эпштейна — Барр (ВЭБ), цитомегаловируса (ЦМВ), герпесвирусов человека (ГВЧ) 6-го и 7-го типов определяли в четырех биологических жидкостях (слезе, слюне, моче, крови).
Статистическую обработку результатов исследования проводили с помощью программы SPSS 26‑й версии. Для проведения сравнительного анализа выраженности дискомфорта, гиперемии конъюнктивы, роговичного синдрома, подавления репликации вируса (переменную обозначали как 1 — вирус обнаружен, 0 — вирус не обнаружен) использовали непараметрический аналог однофакторного дисперсионного анализа — тест Краскела — Уоллиса. Для анализа парных категориальных данных использовали точный тест Макнемара. Уровень статистической значимости был установлен на значении p<0,05.
Результаты и обсуждение
Стромальный ГК в представленной когорте пациентов чаще всего носил черты хронического вялотекущего воспаления (80,6%), реже — рецидивирующего (19,4%). Согласно полученным анамнестическим данным продолжительность заболевания составила 3,5±2,3 мес.: максимальная продолжительность — 12 мес. (1 случай), минимальная — 1 мес. Более длительные сроки сохранения симптомов воспаления переднего отдела глаза регистрировали у пациентов, перенесших опоясывающий герпес (n=6) с поражением первой ветви тройничного нерва (Herpes zoster ophthalmicus — HZO) – от 4 до 12 мес.
Анализ анамнестических данных пациентов, перенесших HZO, выявил характерные недостатки в тактике ведения: системная терапия аналогами нуклеозидов часто инициировалась с опозданием, проводилась в недостаточных дозировках. В ряде случаев обращение пациента к инфекционисту было запоздалым. По-видимому, раннее начало (с первого дня постановки диагноза) противогерпетической терапии высокими дозами аналогов нуклеозидов играет ведущую роль не только в длительности течения глазных воспалительных осложнений HZO, но и в развитии офтальмогерпеса как такового.
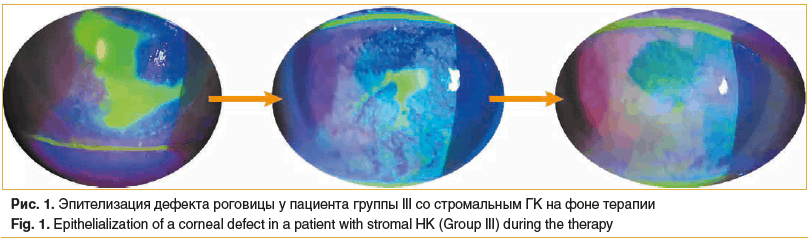
Все пациенты (100%) обозначенных групп предъявляли жалобы на дискомфорт, сухость, болевые (колющие) ощущения в пораженном глазу: у 22 (88,9%) пациентов интенсивность жалобы субъективно оценивалась как выраженная, у 4 (11,1%) — как умеренно выраженная. Степень интенсивности гиперемии была выраженной и умеренно выраженной у 69,4 и 30,6% пациентов соответственно. Низкую чувствительность роговицы определяли у 22 (61,1%) пациентов со стромальным ГК, анестезию — у 14 (38,9%). Роговичный синдром интенсивностью в 4 балла выявлен в 12 (36,1%) наблюдениях, 3 балла — в 19 (52,8%), 2 балла — в 4 (11,1%). Точечное прокрашивание роговицы витальным красителем (флуоресцеин) наблюдали у всех пациентов. В 1 случае (у пациента группы III) стромальный ГК протекал с изъязвлением. Полная эпителизация дефекта роговицы в указанном случае наступила на 3-й неделе проводимой терапии (рис. 1).
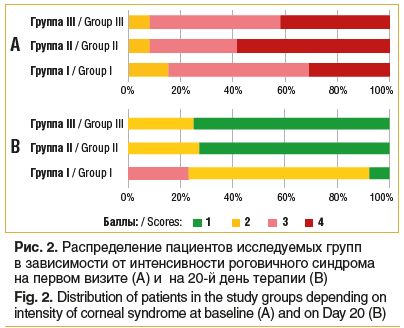
Сравнительный анализ выраженности дискомфорта, гиперемии конъюнктивы, роговичного синдрома (рис. 2, А) у пациентов групп исследования до начала терапии не выявил статистически значимых межгрупповых различий (p>0,05). Попарный анализ с поправкой на множественные сравнения выявил статистически значимую разницу в интенсивности гиперемии конъюнктивы к 20-му дню терапии между группой I и группами II и III (p=0,027 и p=0,019 соответственно). Статистически значимых различий между группами II и III не обнаружено (p=1,000). Следует отметить, что чувство сухости глаз (жалоба, входящая в критерий «дискомфорт») на фоне терапии в группах II и III было полностью купировано к 20-му дню терапии. Возможно, данное обстоятельство связано с применением топической формы препарата Панавир®, который не входил в схему местного лечения у пациентов группы I.
Выраженность роговичного синдрома на 20-й день терапии в группе I была выше в сравнении с таковой в группах II и III (p=0,002 и p=0,004 соответственно). Статистически значимой разницы между показателями выраженности роговичного синдрома в группах II и III не было (p=0,993) (рис. 2, В).
Динамика показателей тактильной чувствительности роговицы представлена в таблице 2. При первичном осмотре (1-й день) ни в одной из групп не было зафиксировано пациентов с нормальной чувствительностью роговицы. Исходно у большинства пациентов во всех группах регистрировалось снижение чувствительности роговицы (69,2% в группе I, 64,6% в группе II, 50,0% в группе III), отсутствие чувствительности (анестезия) отмечалось в 30,8, 36,4 и 50,0% случаев соответственно (см. табл. 2).
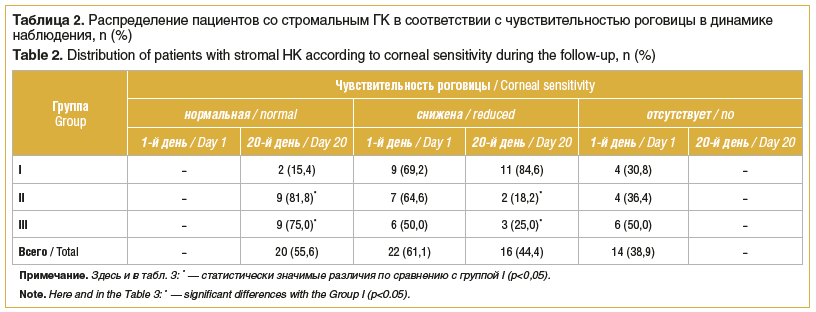
К 20-му дню наблюдения картина существенно изменилась. В группах II и III доля пациентов с нормальной чувствительностью роговицы статистически значимо выросла, составив 81,8% (p<0,05) и 75,0% (p<0,05) соответственно; значительно уменьшилась частота выявления сниженной чувствительности (до 18,2 и 25,0% соответственно). В группе I, напротив, к 20-му дню восстановление нормальной чувствительности роговицы отмечено лишь у 15,4% пациентов. Важно отметить, что во всех группах к 20-му дню не осталось пациентов с полным отсутствием роговичной чувствительности (см. табл. 2).
К 20-му дню терапии во всех группах наблюдали снижение частоты положительной флуоресцеиновой пробы (точечного прокрашивания роговицы), однако в группе I доля пациентов с положительным симптомом оставалась высокой (61,5%). В группах II и III во время визита на 20-й день терапии симптом регистрировали достоверно реже: у 2 (18,2%) и у 1 (8,1%) пациента соответственно, что указывает на почти полную эпителизацию роговицы у пациентов этих групп (табл. 3).
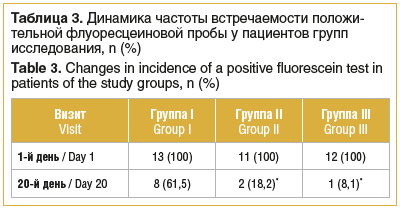
Результаты парных сравнений однозначно свидетельствуют об эффективности медикаментозной терапии с применением препарата Панавир® (в виде глазных капель — группа II; в виде глазных капель и парентерального введения — группа III). На фоне терапии, применяемой в группах II и III, доля пациентов с положительным результатом флуоресцеиновой пробы значимо снизилась (p=0,049 и p=0,018 соответственно) в сравнении с результатами, полученными у пациентов группы I (см. табл. 3).
Между группами II и III не было обнаружено статистически значимых различий в динамике как частоты положительной флуоресцеиновой пробы (точечного прокрашивания роговицы), так и показателей ее тактильной чувствительности (p>0,05).
Результаты оценки динамики флуоресцеиновой пробы, выраженности роговичного синдрома являются объективным индикатором скорости эпителизации роговицы. Тот факт, что изначально у всех пациентов наблюдали положительный результат флуоресцеиновой пробы, подтверждает однородность и тяжесть исходного состояния. К 20-му дню отчетливо видна градация эффективности применявшихся терапевтических подходов в исследуемых группах.
Результаты неспецифической лабораторной диагностики показали изменение уровня нейтрофилов, лимфоцитов и моноцитов в общеклиническом анализе крови. Одновременно лимфоцитоз и нейтропению наблюдали в 30 (83,3%) случаях, что является показателями так называемой «вирусной крови». В 6 (20%) случаях из 30 наряду с лимфоцитозом и нейтропенией выявляли повышение уровня моноцитов в периферической крови. Следует отметить, что изменение хотя бы одного из трех показателей (лимфоцитов, нейтрофилов, моноцитов) в общеклиническом анализе крови определяли у всех пациентов (100%). Эти результаты дополнительно свидетельствуют об активности вирусной инфекции и реакции иммунокомпетентных клеток на патоген. Лимфоцитоз является показателем активации и пролиферации T- и B-лимфоцитов, специфичных в отношении вируса. Развитие нейтропении, по-видимому, связано с вирусопосредованной деструкцией нейтрофилов. Повышение уровня моноцитов (лейкоцитов из системы мононуклеарных макрофагов) связано, прежде всего, с тем, что данные клетки являются основными антигенпрезентирующими элементами и эффекторами фагоцитоза. Изменение вышеперечисленных показателей в периферической крови у пациентов с клинической картиной стромального ГК указывает на системный (генерализованный) характер инфекции с клинической картиной локального воспаления — офтальмогерпес.
Результаты специфической лабораторной диагностики, проведенной в первый день обращения пациента, выявили активную герпесвирусную инфекцию в стадии репликации вируса у 88,9% (n=32) обследованных. ВЭБ являлся наиболее часто выявляемым герпетическим вирусом (n=22; 68,7%) (рис. 3). В остальных случаях диагноз устанавливали на основании клинической картины и последующей положительной динамики в течении заболевания на фоне проводимой специфической терапии. Следует отметить, что в 23 (71,9%) случаях определяли ДНК двух и более типов герпесвирусов в биологических жидкостях пациентов; наиболее часто встречаемыми ассоциациями вирусов были: ВЭБ + ГВЧ6 (n=11; 47,8%) и ВВЗ + ВЭБ (n=8; 34,8%). Микст-инфекция несколькими типами вирусов, возможно, является определяющим фактором более тяжелого течения герпетической инфекции и развития глубокого, стромального дефекта роговицы. На фоне проводимой терапии к 20-му дню генетический материал вирусов определяли в 16 (44,4%) случаях.
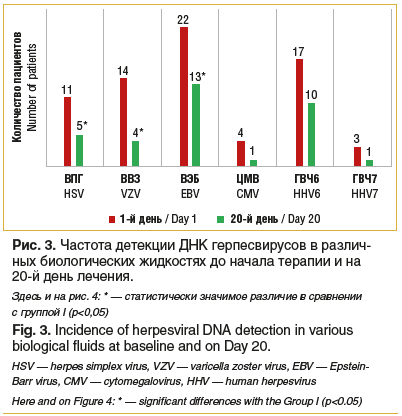
Результаты анализа данных детекции ДНК герпетических вирусов показали статистически значимое снижение содержания генетического материала ВПГ, ВВЗ и ВЭБ в биологических жидкостях и тенденцию к снижению уровня остальных вирусов, что свидетельствует об эффективности примененного терапевтического подхода в отношении инактивации вируса (рис. 4).
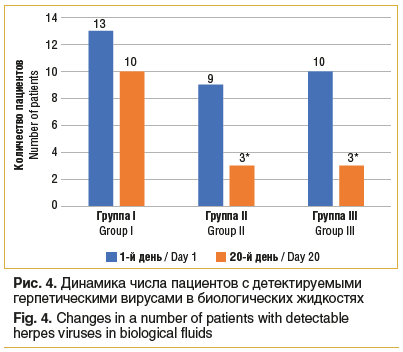
Результаты исследования показывают, что комплексная терапия пациентов группы III с применением препарата суммы полисахаридов побегов Solanum tuberosum (глазная форма и парентеральное введение) оказалась наиболее эффективной в подавлении репликации герпетических вирусов в сравнении с группой I (p=0,031). Различие в эффективности терапии между группами I и II статистически незначимо, однако демонстрирует тенденцию к отличию (p=0,059). Следует отметить, что сравнение эффективности двух схем лечения с использованием только глазной формы (группа II) и глазной формы совместно с парентеральным введением (группа III) препарата суммы полисахаридов побегов Solanum tuberosum не выявило достоверных различий (p=0,886); однако в сравнении с группой I группа III продемонстрировала статистически значимые отличия, нежели группа II. Данное обстоятельство позволяет отметить наибольшую эффективность в подавлении репликации вируса комплекса препаратов: системный аналог нуклеозида + системный препарат суммы полисахаридов побегов Solanum tuberosum.
Здесь следует отметить, что лекарственные формы препарата Панавир®, применяемые в комплексном лечении пациентов II и III групп, обладают противовирусным, иммуномодулирующим и противовоспалительным свойствами. Препарат демонстрирует двойную активность: цитопротективную и противовирусную. Защищая клетки от вирусной агрессии, он одновременно подавляет ключевые этапы репликации вируса — синтез белков и сборку вирионов. В результате инфекционная активность патогена существенно снижается, а жизнеспособность инфицированной клеточной культуры возрастает [17].
Ограничения исследования. Исследование включало относительно небольшое число пациентов (n=36), распределенных на три примерно равные группы. Малый размер выборки ограничивает статистическую мощность исследования и возможность выявления более тонких различий в эффективности схем лечения.
Оценка эффективности лечения проводилась на 20-й день терапии, что является адекватным для анализа купирования острой фазы воспаления. Однако отсутствуют данные о результатах лечения в отдаленном периоде (3, 6, 12 мес.), что позволило бы определить эффективность терапии в отношении рецидивов заболевания.
С целью оценки симптомов заболевания (дискомфорт, боль) использовалась субъективная оценка пациентов без применения валидированных опросников или шкал (например, визуально-аналоговой шкалы), что может снижать воспроизводимость результатов.
В исследовании не анализировалось потенциальное влияние сопутствующих заболеваний, иммунного статуса пациентов и предшествующей противовирусной терапии на результат лечения в разных группах, что могло выступать в качестве неучтенных смещающих факторов.
Выводы
-
Лабораторные данные (лимфоцитоз, нейтропения, моноцитоз) и высокая частота обнаружения ДНК вирусов в крови и других биологических жидкостях подтверждают, что стромальный ГК является симптомом системной герпесвирусной инфекции, что обосновывает необходимость комплексного подхода к диагностике и лечению пациентов с офтальмогерпесом.
-
Комплексная терапия пациентов со стромальным ГК с включением препарата суммы полисахаридов побегов Solanum tuberosum (как в виде топических глазных капель, так и в сочетании с парентеральным введением) статистически значимо превосходит схему лечения «пероральные аналоги нуклеозидов + интерферон α-2b» по ряду клинических критериев: скорости купирования воспаления, регенерации и восстановлению чувствительной иннервации роговицы.
-
Комплексная системная терапия (аналог нуклеозида + препарат суммы полисахаридов побегов Solanum tuberosum) стромального ГК продемонстрировала наибольшую эффективность в подавлении репликации герпесвирусов, подтвержденную снижением вирусной нагрузки по данным ПЦР.
-
Результаты нашего исследования показывают, что терапия тяжелых стромальных форм ГК должна включать: местное использование глазных форм иммунных препаратов (препарат суммы полисахаридов побегов Solanum tuberosum) и «мягких» глюкокортикостероидов; системное назначение высоких суточных доз аналогов нуклеозидов и препаратов, модулирующих иммунный ответ (препарат суммы полисахаридов побегов Solanum tuberosum, форма для внутривенного введения).
Сведения об авторах:
Клещева Елена Александровна — к.м.н., доцент, доцент кафедры офтальмологии ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1; врач-офтальмолог Московского городского офтальмологического центра ММНКЦ Боткинская больница; 125284, Россия, г. Москва, 2-й Боткинский пр-д, влад. 5; врач-офтальмолог ООО «Герпетический центр»; 117036, Россия, г. Москва, ул. Гримау, д. 10А, стр. 2; ORCID iD 0000-0002-1392-3432
Чернакова Галина Мэлсовна — к.м.н., доцент, заведующая поликлиническим отделением № 2 Московского городского офтальмологического центра ММНКЦ Боткинская больница; 125284, Россия, г. Москва, 2-й Боткинский пр-д, влад. 5; врач-офтальмолог ООО «Герпетический центр»; 117036, Россия, г. Москва, ул. Гримау, д. 10А, стр. 2; ORCID iD 0000-0002-9630
Мельникова Наталья Владимировна — к.м.н., доцент, доцент кафедры офтальмологии ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1; врач-офтальмолог Московского городского офтальмологического центра ММНКЦ Боткинская больница; 125284, Россия, г. Москва, 2-й Боткинский пр-д, влад. 5; ORCID iD 0000-0003-3917-0691
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 17.12.2025.
Поступила после рецензирования 12.01.2026.
Принята в печать 30.01.2026.
материал rmj.ru
