Введение
Роль термографии в медицине довольно значима и хорошо известна. Этот метод часто используется в ревматологии для диагностики и последующего наблюдения за течением артрита, в онкологии — для выявления рака груди, в дерматологии — для выявления различных кожных заболеваний, даже для диагностики импотенции [1–4]. В офтальмологии измерение температуры глазной поверхности (ТГП) ранее не получило широкого распространения вследствие того, что термографы старого образца предполагали контактную методику измерения [5]. Существенным недостатком этих приборов была необходимость прямого контакта с роговицей, что провоцировало повышенное слезоотделение и тем самым снижало точность измерений. Такие устройства, как термистор и термопара измеряли температуру, можно сказать, между воздухом и роговицей, кроме того, сам контактный зонд обладал охлаждающим эффектом [6]. Радиометрические устройства, такие как болометр, основанные на изменении электрического сопротивления термочувствительного элемента при его нагревании вследствие поглощения измеряемого потока излучения, хотя и являлись технически бесконтактными, но в момент измерения должны были находиться очень близко к поверхности роговицы, вызывая негативную реакцию у пациента [7]. В 1968 г. R. Mapstone провел исследование на 53 больных с острым передним увеитом с использованием болометра [8] и выявил повышение температуры роговицы и кожных покровов периорбитальной области у всех пациентов. Более того, он выявил связь увеита с системным заболеванием у пациентов, у которых относительное повышение температуры поверхности роговицы составляло более 1 °C. Позже R. Mapstone описал термографические паттерны в норме и при различных патологических состояниях глаза с помощью инфракрасной камеры [9], продемонстрировал снижение температуры правого глаза, а также в области лба справа при стенозе правой внутренней сонной артерии.
По мере технического совершенствования аппаратуры [10, 11] когда стало возможным использование бесконтактных приборов для проведения термографии в офтальмологии, стали появляться исследования, демонстрирующие важную роль этого метода при таких патологиях, как синдром «сухого глаза», передний увеит и другие заболевания, обусловленные изменениями глазной поверхности [11–13]. Установлено, что при синдроме «сухого глаза» ТГП может снижаться [11]. При кератитах, связанных с дисфункцией мейбомиевых желез, также фиксировалась более низкая температура роговицы [13]. Возможным объяснением этих наблюдений может быть усиление испарения слезной пленки, приводящее к охлаждению поверхности глаза.
Различные воспалительные заболевания глаз могут быть выявлены при рутинном осмотре с помощью щелевой лампы, но в случае скрытого воспаления, например при заднем склерите (ЗС), необходимо применение дополнительных методов. В некоторых случаях диагноз может оставаться неясным даже после клинического обследования и В-сканирования (УЗИ глаза), поскольку объем данных, полученных при их применении, недостаточен. Использование в таких случаях термографии для выявления повышенной ТГП может дать дополнительную информацию, позволяющую диагностировать воспалительные процессы.
Эта методика может быть полезной и при наблюдении за динамикой состояния глаза пациента, а также в случае самоизоляции при пандемии COVID-19, когда пациенты не могут посетить врача-специалиста. Это простое портативное бесконтактное устройство может помочь врачам оценить воспаление при проведении телеконсультации, а также задокументировать полученные данные.
Цель нашего исследования — изучить возможности использования термографической камеры для выявления повышенной ТГП у пациентов с подтвержденным ЗС и для оценки вариабельности ТГП после начала лечения в рамках динамического наблюдения.
Материал и методы
Проспективное наблюдательное исследование «случай — контроль» было проведено с мая 2017 г. по май 2019 г. Исследование было одобрено внутренним наблюдательным советом и соответствовало принципам Хельсинкской декларации.
В исследуемую группу были включены пациенты с клиникой увеита и ЗС на одном глазу (n=6). Диагноз ЗС устанавливался в соответствии с общепринятыми клиническими и ультразвуковыми критериями [14, 15]: была проведена термография с последующим B-сканированием для измерения задней толщины склеры и подтверждения диагноза. Пациенты получали терапию пероральными нестероидными противовоспалительными препаратами (НПВП) (эторикоксиб 60 мг 1 р./сут или индометацин 75 мг 2 р./сут в течение 1–2 нед.) и/или пероральными (преднизолон 1 мг/кг с постепенным снижением дозы) и местными стероидами (преднизолон 6 р./сут с постепенным снижением дозы), а также, по показаниям, иммуномодулирующую терапию (метотрексат 15–20 мг/нед. у трех пациентов). В исследование не включались пациенты, уже получавшие лечение на момент обращения, имеющие двусторонний ЗС, глазные или системные заболевания (помимо с ЗС в исследуемой группе), которые могли бы повлиять на ТГП: синдром «сухого глаза», воспалительные заболевания (особенно области орбиты и придаточного аппарата), глазной ишемический синдром, недавний синусит или лихорадку в анамнезе.
Динамическое наблюдение и оценка состояния процесса с применением термографии у пациентов с ЗС осуществлялись как минимум на 4 последовательных визитах, в группе контроля — каждые 5 дней в течение 3 нед. (суммарно также 4 визита). Единый протокол обследования соблюдался для всех пациентов в исследуемой и контрольной группах при каждом визите. Все пациенты обследовались одним врачом в одном и том же помещении глазного госпиталя с использованием одного и того же оборудования.
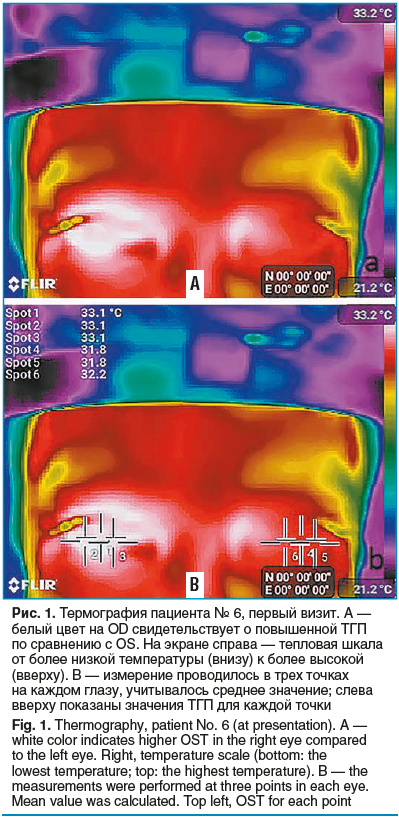
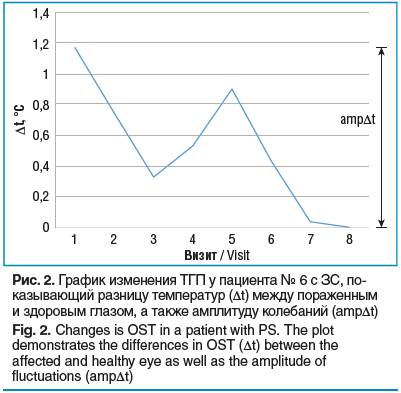
Проводилась биомикроскопия, непрямая офтальмоскопия (без контакта с поверхностью глаза) после медикаментозного мидриаза (тропикамид 0,8% и фенилэфрин 5%). Термография выполнялась спустя 5 мин после вышеперечисленных процедур, использовалась тепловизионная камера FLIR™, встроенная в мобильный телефон Cat S 60™ (тепловое разрешение 80×60, 9 Гц, чувствительность 0,15 °C). Камеру размещали таким образом, чтобы на экране термографа отображалось лицо пациента: глаза — в центре, виски — близко к краям экрана, лоб и нос должны быть видимыми (рис. 1). Непосредственно перед снимком пациента просили 1 раз моргнуть. Термография проводилась при отсутствии контактных линз, туши для ресниц и других косметических средств.Термограммы оценивались одним исследователем. Разница ТГП между пораженным и здоровым глазом (Δt) вычислялась с помощью встроенного мобильного приложения FLIR Tools. В контрольной группе Δt рассчитывалась как разница ТГП между глазами с более высоким и более низким средним значением этого показателя. Для каждого пациента была рассчитана амплитуда колебаний температуры (ampΔt): из максимального значения Δt (ΔtMax) (чаще всего — на первом визите) вычитали минимальное значение (ΔtMin) (чаще всего — в конце лечения) (рис. 2).
Результаты исследования
Исследуемую группу составили 6 пациентов с ЗС (мужчин — 3, женщин — 3), средний возраст — 45,33 года (диапазон 22–59 лет), в контрольную группу вошли 10 человек (мужчин — 2, женщин — 8), средний возраст — 45 лет (диапазон 23–58 лет).
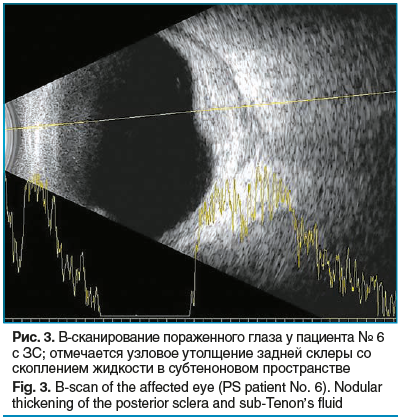
Все пациенты предъявляли жалобы на боль в пора-женном глазу, 4 из них отмечали снижение зрения. У 4 пациентов отмечалась гиперемия в верхнеконъюнктивальном своде, других патологических изменений в переднем отрезке глаза выявлено не было. При офтальмоскопии отмечалось наличие хориоидальных складок (n=4), складок внутренней пограничной мембраны (n=2), субретинальной жидкости (n=3) и отечности диска зрительного нерва (n=2). B-сканирование показало утолщение задних отделов склеры от легкой степени до тяжелой во всех случаях (диапазон 2,1–3,94 мм). В 3 случаях был выявлен узловой ЗС (рис. 3).
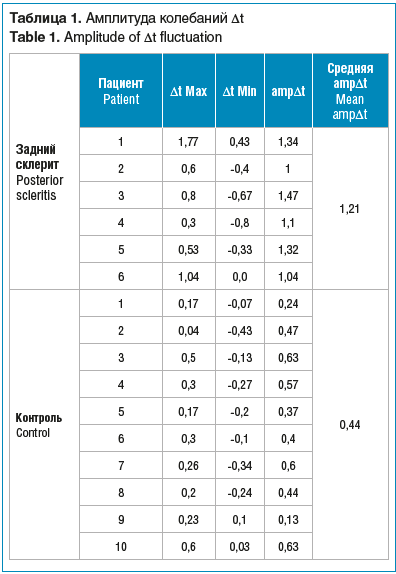
У пациента № 1 в фазе активного воспаления ΔtMax составляла 1,77 °C, а при разрешении процесса ΔtMin — 0,43 °C, следовательно, ampΔt достигала 1,34 °C. Аналогичным образом ampΔt рассчитывали из значений ΔtMax и ΔtMin во всех случаях (табл. 1). AmpΔt в контрольной группе оказалась ниже по сравнению с этим показателем в группе ЗС: среднее значение ampΔt в группе ЗС составило 1,21 °C (диапазон 1,47–1,04 °C), в контрольной группе — 0,44 °C (диапазон 0,13–0,63 °C). В 3 случаях (пациенты № 3, 4, 6) при ЗС были рецидивы после снижения дозы стероидов, что отразилось в увеличении ТГП (и Δt) по сравнению с показателями, полученными на визитах до рецидива.
Обсуждение
Об увеличении ТГП на фоне глазных воспалительных процессов, за исключением ЗС, ранее сообщалось в различных исследованиях [13, 16]. Сложности в диагностике ЗС могут возникнуть вследствие недостаточного опыта, субклинического течения воспаления или атипичности симптомов. При В-сканировании можно выявить утолщение задних отделов склеры, которое иногда бывает обусловлено другими заболеваниями невоспалительного характера. Интенсивность боли, которая является частым симптомом при ЗС, может варьировать у разных пациентов, иногда боль и вовсе отсутствует. Измерение ТГП может помочь врачу-офтальмологу заподозрить воспалительное заболевание.
Выполненное нами исследование показало, что амплитуда колебаний ТГП больше в глазах с ЗС в сравнении со здоровыми глазами, т. е. ТГП повышается во время активного воспаления при ЗС и возвращается к исходному уровню после разрешения воспаления. Нами также показано, что в норме температура глаза вариабельна, но эти колебания незначительны по сравнению с таковыми при воспалительном процессе.
Менявшаяся от визиту к визиту ТГП серьезно влияла на точность ее измерения. Для минимизации такого влияния нами проводилось измерение разницы температуры правого и левого глаза с использованием одного и того же термографа в одном и том же помещении. Оценка разницы температур (Δt) позволяет значительно уменьшить погрешности измерений, вызванные внешними факторами (температура окружающей среды, влажность), а также ежедневными колебаниями температуры тела пациента, изменениями глазного кровотока, кроме того, колебаниями ТГП в рамках одной серии измерений. В контрольной группе пациентов абсолютные показатели ТГП имели довольно широкий разброс от визита к визиту, однако вариабельность Δt, показывающая разницу между OD и OS, была значительно ниже, чем у пациентов с ЗС. Это позволило получить относительно стабильный температурный параметр для динамической оценки ТГП на разных визитах.
У здоровых пациентов отмечается небольшая разница температур между двумя глазами, обычно не превышающая 0,62 °C [17]. В исследуемой нами небольшой контрольной группе показатели ΔtMax также не превышали 0,6 °C. Таким образом, можно заподозрить одностороннюю патологию, когда разница температур между двумя глазами больше 0,6 °C. Но все же могут быть исключения: например, в группе ЗС у пациента № 4 ΔtMax составляла всего 0,3 °C в период активного воспаления. Когда воспаление разрешилось, Δt упала до -0,8 °C, что доказывает: пораженный глаз данного пациента обычно (базальная температура) имел более низкую температуру, чем здоровый глаз. Мы считаем ampΔt надежным индикатором для мониторинга ТГП при одностороннем воспалительном процессе в глазу. По аналогии с колебанием уровня внутриглазного давления в здоровых глазах, выявляемом при бесконтактной тонометрии, знание своей индивидуальной ampΔt ТГП, выявленной методом термографии, позволит заподозрить воспалительный процесс в глазу при выходе значений за пределы индивидуальной нормы. Среднее значение ampΔt в контрольной группе составляло 0,44 °C (диапазон 0,13–0,63 °C), что было значительно ниже, чем в исследуемой группе (1,2 °C, диапазон 1,04–1,47 °C). Таким образом, нами показано, что термография может обнаружить увеличение ТГП в клинически диагностированных случаях ЗС и использоваться для оценки динамики воспалительного процесса. При ЗС не всегда могут присутствовать такие характерные признаки, как боль, наличие хориоидальных складок или субретинальной жидкости, а также выявляемые при В-сканировании жидкость в субтеноновом пространстве или локальное утолщение склеры, которое может встречаться и при некоторых невоспалительных заболеваниях. В таких случаях термография поможет дифференцировать воспалительную патологию от невоспалительной. Мы предполагаем, что даже различия в локализации воспалительного процесса будут по-разному влиять на показатели ТГП. Так, например, при сравнении хориоидальной гранулемы и узлового ЗС температура будет выше при ЗС из-за особенностей теплопроводности тканей склеры. Термографию можно рассматривать как важный диагностический метод в условиях самоизоляции при пандемии COVID-19, так как она дает возможность пациентам самостоятельно провести объективное исследование органа зрения и отправить результаты врачу в рамках телемедицинской консультации, что очень актуально для динамического наблюдения пациентов с ЗС. Зная индивидуальную ampΔt у конкретного пациента, на основании присланных им данных термографии врач может заподозрить рецидив воспалительного процесса.
Бесконтактная термография может найти свое применение в качестве скринингового метода для выявления скрытых воспалительных процессов у лежачих больных или детей.
Ограничениями данного исследования следует считать малую численность групп, включение только пациентов с односторонним ЗС, использование тепловизионной камеры с низким разрешением и проведение работы одним исследователем.
Заключение
В настоящее время в условиях пандемии COVID-19 интерес к термографии стремительно растет как у офтальмологов, так и у врачей многих других специальностей.
В данном исследовании доказан факт увеличения ТГП при активном скрытом воспалительном процессе на примере пациентов с ЗС. Также показана важность измерения Δt и ampΔt. Исходя из анализа литературных источниковпредставленные нами результаты — первый описанный опыт измерения ТПГ при динамическом наблюдении пациентов с ЗС. Рекомендуется дальнейшее проведение более крупных исследований с использованием специализированной глазной термографической камеры с высоким разрешением для подтверждения полученных в данной работе результатов и изучения возможностей термографии при других скрытых воспалительных заболеваниях глаза.
Сведения об авторах:
Анкуш А. Кавали — MD, DNB, врач-консультант отделения увеитов и иммуноопосредованных заболеваний глаз, ORCID iD 0000-0002-5536-8051;
Сринивасан Санджай — MBBS, DNB, врач-консультант отделения увеитов и иммуноопосредованных заболеваний глаз, ORCID iD 0000-0001-9756-1207;
Падмамалини Махендрадас — MBBS, DNB, руководитель отделения увеитов и иммуноопосредованных заболеваний глаз, ORCID iD 0000-0002-6137-8870;
Рохит Шетти — DNB, FRCS, PhD, руководитель отделения хирургии роговицы и рефракционной хирургии, ORCID iD 0000-0002-4556-1587.
Глазная больница Нараяна Нетралая. 121/C, Корд-Роуд, Бангалор, 560010, Индия.
Контактная информация: Анкуш А. Кавали, e-mail: akawali332@gmail.com. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 23.05.2020.
About the authors:
Ankush A. Kawali — MD, DNB, Consultant in Uveitis and Ocular Immunology Department, ORCID iD 0000-0002-5536-8051;
Srinivasan Sanjay — MBBS, DNB, Consultant in Uveitis and Ocular Immunology Department, ORCID iD 0000-0001-9756-1207;
Padmamalini Mahendradas — MBBS, DNB, Head of Uveitis and Ocular Immunology Department, ORCID iD 0000-0002-6137-8870;
Rohit Shetty — Head of Cornea and Refractive Surgery Department, ORCID iD 0000-0002-4556-1587.
Narayana Nethralaya Eye Hospital. 121/C, Chord Rd, Rajajinagar, Bengaluru, Karnataka, 560010, India.
Contact information: Ankush A. Kawali, e-mail: akawali332@gmail.com. Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 23.05.2020.
.
материал rmj.ru
