Клиническая эффективность препаратов бензидамина в терапии обострений хронического тонзиллофарингита
Содержание статьи
Введение
В общей структуре заболеваемости удельный вес тонзиллофарингитов достигает от 2,8 до 3%; среди пациентов до 75% составляют лица до 30 лет [1]. В настоящее время дифференциальная диагностика хронического тонзиллита (ХТ) и хронического фарингита вызывает большие трудности. Посредством кластерного и корреляционного анализа доказана общность этиологии, патогенеза, а также клинической симптоматики этих двух самостоятельных нозологий [2]. В ходе воспалительного процесса, нарушения иммунологической и нервно-рефлекторной регуляции происходит дисбаланс местного биоценоза ротоглотки с травматизацией и повреждением слизистой оболочки глотки и небных миндалин [2, 3].
По информации Центра по контролю и профилактике заболеваний, этиологическими агентами, вызывающими фарингит, в подавляющем большинстве случаев (85%) являются вирусы (риновирусы, аденовирусы, коронавирусы, вирусы гриппа, парагриппа и респираторно-синцитиальные вирусы) [4, 5]. Ведущую роль в развитии ХТ играют ассоциации β-гемолитических стрептококков (в частности,
β-гемолитического стрептококка группы А (БГСА)) и золотистого стафилококка [6], причем при хроническом процессе присутствие S. haemolyticus возрастает до 28,5% [7, 8]. Также в возникновении ХТ значительную роль играют вирусные агенты. Наиболее часто встречаются цитомегаловирус, аденовирус, вирусы парагриппа, герпес-вирусы, вирус Эпштейна — Барр [4, 6].
Используемые в лечении тонзиллофарингитов препараты можно подразделить на следующие группы: этиотропные (антибиотики, антисептики), патогенетические (противовоспалительные препараты) и симптоматическая терапия (анальгетики, местные анестетики) [9, 10].
На современном этапе назначение системной антибиотикотерапии целесообразно только при доказанном стрептококковом (БГСА) генезе воспаления, что обусловлено риском развития острой ревматической лихорадки или гломерулонефрита, а также других осложнений [10]. В связи с этим весьма важным является определение этиологии заболевания у каждого конкретного пациента. На сегодняшний день системная противомикробная терапия необходима лишь 20–30% детей и 5–15% взрослых с острым тонзиллофарингитом или обострением хронического процесса, а фактически антибиотики назначают гораздо чаще, причем в 65% случаев — необоснованно [9, 10].
При отсутствии данных о бактериальном инфицировании на первое место выходит назначение местной терапии, главными целями которой являются купирование воспалительных явлений в глотке, уменьшение выраженности болевого синдрома и предотвращение дальнейшего распространения воспалительного процесса по дыхательным путям [11].
Одной из групп лекарственных препаратов, действие которых направлено на подавление воспалительной реакции в глотке, являются нестероидные противовоспалительные препараты (НПВП), действующие на ключевое звено поддержания этой реакции [5]. Местные НПВП могут как входить в состав комплексных средств, так и применяться в виде монопрепаратов. Среди них наиболее часто используется бензидамина гидрохлорид, обладающий выраженным противовоспалительным, местноанестезирующим и противоотечным действием [5, 9, 10].
Целью данного исследования было оценить эффективность, переносимость и безопасность действия препаратов бензидамина в форме спрея для местного применения дозированного на длительность течения и тяжесть обострения хронического тонзиллофарингита (ХТФ).
Материал и методы
В клиническое исследование были включены 30 пациентов, среди них 8 (26,7%) мужчин и 22 (73,3%) женщины в возрасте от 18 до 68 лет. Компенсированная форма ХТФ была диагностирована у 8 (26,7%) пациентов, декомпенсированная — у 22 (73,3%).
Включенные в исследование пациенты были рандомизированы на 2 группы по 15 человек: 1-я группа (опытная) —
пациенты с обострением ХТФ, для их лечения применялась стандартная терапия, в составе которой в качестве местного противовоспалительного средства был использован препарат Ангидак®, спрей для местного применения дозированный, согласно инструкции по применению препарата; 2-я группа (контрольная) — пациенты с обострением ХТФ, в лечении которых применялась стандартная терапия, в ее составе в качестве местного НПВП был использован препарат Тантум® Верде, спрей для местного применения дозированный, согласно инструкции по применению препарата.
В качестве стандартной терапии назначалась симптоматическая системная терапия для купирования лихорадки и/или болевого синдрома (при наличии) в виде использования НПВП в стандартных рекомендованных дозах; терапия местными средствами для лечения острого тонзиллофарингита с целью быстрого уменьшения выраженности болевого синдрома, воспалительных явлений, а также для профилактики вторичного инфицирования поврежденной слизистой оболочки. В качестве препарата для местного лечения применялся местный НПВП бензидамин, спрей для местного применения дозированный.
Исследуемые группы пациентов статистически значимо не различались по возрастному, гендерному составу и частоте встречаемости декомпенсированных форм ХТФ (табл. 1). 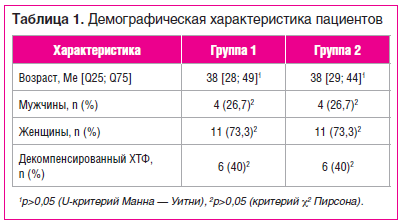
Включенные в исследование пациенты совершали 3 визита к ЛОР-врачу. 1-й визит: включение в исследование, сбор анамнестических данных, рандомизация, ЛОР-обследование, взятие материала для бактериологического исследования, назначение лечения; 2-й визит (5–7-е сут терапии): клиническая оценка состояния больного, оценка жалоб, локального статуса, переносимости препарата, наличия побочных эффектов; 3-й визит (10–14-е сут терапии): клиническая оценка состояния больного, его жалоб, оценка локального статуса, повторное взятие материала для бактериологического исследования, оценка переносимости препарата, наличия побочных эффектов.
Оценка жалоб самим пациентом, степени выраженности симптомов заболевания в сравнении с желаемым (асимптомным) состоянием проводилась по модифицированной 10-балльной визуально-аналоговой шкале (ВАШ. 0 — очень хорошо, 10 — очень плохо): оценка слабости, недомогания, выраженности першения, саднения, сухости в горле, затруднения глотания, степени выраженности болей в горле, степени нарушения качества жизни.
Оценка тяжести клинического состояния пациентов с ХТФ при визите к врачу проводилась по балльной системе от 0 до 3 баллов с учетом:
степени гипертрофии небных миндалин: 0 — нет гипертрофии (за дужками), 1 — 1-я степень, 2 — 2-я степень, 3 — 3-я степень;
состояния слизистой глотки: 0 — розовая, 1 — отечная, 2 — сухая, 3 — атрофичная;
характера содержимого лакун: 0 — нет содержимого, 1 — казеозные массы, 2 — гной, 3 — гной и казеозные массы;
цвета слизистой глотки: 0 — бледно-розовый, 1 — инъекция сосудистая, 2 — умеренная гиперемия, 3 — яркая гиперемия;
результатов термометрии тела: 0 — нормальная температура тела, 1 — субфебрильная температура тела, 2 — повышение температуры тела не выше 38 °C, 3 — повышение температуры тела выше 38 °C;
симптомов общей интоксикации: 0 — отсутствие симптомов, 1 — незначительные симптомы, 2 — симптомы умеренной выраженности, 3 — выраженные симптомы.
В ходе визитов 1 и 3 выполнялось бактериологическое исследование мазков из глотки с определением чувствительности к антибиотикам. На визитах 1 и 3 стерильным тампоном проводился забор биоматериала с поверхности небных миндалин для исследования на бактериальную флору и грибы. Категориями бактериологического ответа на антимикробную терапию являлись:
эрадикация — отсутствие первоначального возбудителя при посеве адекватного материала из места первичной локализации инфекционного процесса;
предполагаемая эрадикация — предположение, что возбудитель элиминировался, если нет подходящего для посева материала из места первичной локализации инфекции;
персистирование — сохранение первичного возбудителя к концу лечения при наличии или отсутствии признаков воспаления.
Эффективность исследуемого бензидамина, спрея для местного применения дозированного, оценивалась на основании сравнения клинических и лабораторных показателей в 2 группах пациентов.
Оценка безопасности бензидамина, спрея для местного применения дозированного, была основана на регистрации нежелательных явлений в ходе исследования.
В течение 7 сут лечения каждый пациент заполнял дневник, который отражал субъективную оценку статуса в динамике, индексированную в баллах (от 0 до 10). Оценивались: температура тела, выраженность слабости, недомогания, интенсивность головных болей, выраженность стекания слизи по задней стенке глотки, жалобы на затруднение глотания, выраженность першения, саднения в горле, выраженность болей в горле, кашля, запаха изо рта, количество выделений пробок из миндалин, степень нарушения качества жизни.
С целью повышения объективности и комплексности оценки жалоб пациентов, клинических проявлений заболевания, объективного статуса ЛОР-органов при визите к врачу, а также удобства последующей статистической обработки и интерпретации полученных данных баллы (дневник пациента и клиническое наблюдение) были суммированы относительно визитов пациента к врачу или сроков от начала лечения (1–7-й дни).
Статистический анализ. В исследовании были использованы методы описательной и аналитической статистики. Рассматривались как категориальные (наличие или отсутствие изучаемого фактора, пол), так и количественные данные (суммы баллов из дневников пациента и клинического наблюдения). Анализируемые параметры категориальных данных представлены в виде долей и частот от общего числа исследуемых (%). Параметры количественных данных в исследовании представлены в виде медианы (Me) и 25%, 75% квартилей [Q25; Q75], поскольку все они не соответствовали закону нормального распределения согласно критерию Шапиро — Уилка.
Оценка эффекта лечения при повторных измерениях проводилась путем сравнительной статистической оценки сумм баллов из дневников пациентов и протоколов клинического наблюдения. Выявление различий в субъективном и объективном статусах пациентов на фоне терапии проводилось с использованием непараметрического критерия χ2 Фридмана с критическим уровнем значимости 0,05. С целью уточнения скорости наступления лечебного эффекта проводились апостериорные множественные попарные сравнения балльных и термометрических показателей каждого из дневников между собой (post hoc-анализ) с использованием непараметрического Z-критерия Уилкоксона с поправкой Бонферрони для критического уровня значимости: р/m, m — количество возможных гипотез (сравнений). Таким образом, для 3 групп сравнения динамики баллов из протоколов клинического наблюдения за статусом пациента во время 3 визитов к врачу критический уровень с учетом поправки Бонферрони составлял 0,017. Для 7 же повторных наблюдений из дневников пациентов, обусловливающих 14 возможных сравнений, за критический уровень значимости принималось значение 0,0036.
При обработке данных использовался программный пакет IBM SPSS Statistics 22 (США).
Результаты исследования
Все пациенты прошли лечение в соответствии с установленным протоколом. При этом была достигнута удовлетворительная комплаентность. Все пациенты отметили хорошую переносимость всех применяемых в лечении препаратов, в т. ч. бензидамина. В ходе наблюдения за пациентами нежелательных явлений при приеме бензидамина зарегистрировано не было.
Результаты динамики клинического статуса пациентов
В процессе лечения ХТФ продемонстрировано достижение статистически значимой положительной динамики жалоб и показателей клинического статуса пациентов обеих групп при повторных осмотрах (табл. 2).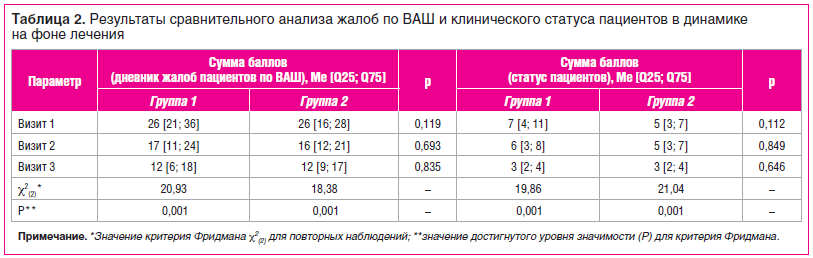
Апостериорные попарные сравнения данных балльных показателей (повторная оценка жалоб и клинического статуса пациентов) относительно номера визита к врачу выявили их отчетливую равномерную положительную динамику со 2-го визита в обеих группах пациентов.
Оценка результатов лечения пациентов с обострением ХТФ на основании динамического сравнения суммированных балльных показателей из их дневников (субъективный статус) выявила достижение статистически значимого уменьшения степени выраженности клинических проявлений основного заболевания на фоне проводимого лечения в обеих группах (табл. 3).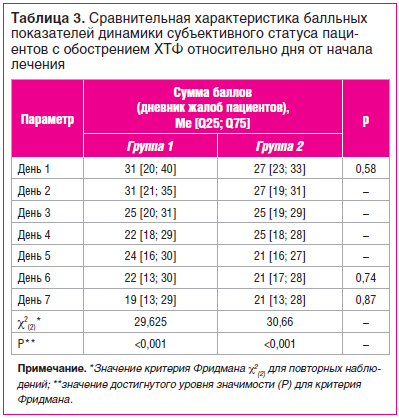
Статистически значимых различий при групповом попарном сравнении балльных показателей субъективного статуса пациентов и данных термометрии относительно дня от начала лечения обострения ХТФ выявлено не было.
Результаты бактериологических исследований
Рост бактериальной флоры констатирован при всех заборах как до, так и после проведенного лечения (60 культуральных исследований на бактериальную флору). Роста грибковой флоры не выявлено при обследовании всех 30 включенных в исследование пациентов (60 исследований на грибковую флору), страдающих ХТФ.
Характеристика выделенной бактериальной микрофлоры. Во всех первичных образцах биоматериала была выделена полифлора: 2 микроорганизма — в 10 (33,3%) образцах; 3 микроорганизма — в 20 (66,7%) образцах.
Бактерии рода Streptococcus были выделены при всех культуральных исследованиях мазков с поверхности небных миндалин; Str. anhaemoliticus (негемолитический стрептококк) — в 15 (50,0%) образцах, БГСА — в 15 (50,0%); Staphylococcus aureus — в 21 (70,0%). Условно-патогенная флора: Neisseria spp. выявлены у 28 (93,3%) пациентов, Klebsiella spp. — у 2 (6,7%).
Антибактериальная эффективность местного лечения бензидамином, спреем для местного применения дозированным.
Получены следующие результаты бактериологических исследований у 15 (100%) пациентов — носителей БГСА: отсутствие роста патогена (эрадикация) и снижение обсемененности биоматериала (предполагаемая эрадикация) — у 11 (73,3%) больных; персистирование возбудителя — у 4 (26,7%) (табл. 4).
При местном лечении бензидамином 21 пациента с обострением ХТФ (носители S. aureus) получены следующие результаты: отсутствие роста патогена (эрадикация) и снижение обсемененности биоматериала (предполагаемая эрадикация) — у 12 (76,1%) больных; персистирование возбудителя — у 9 (23,9%) пациентов (табл. 4).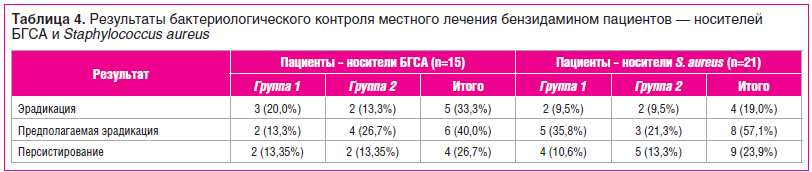
Заключение
Бензидамин, спрей для местного применения дозированный, включенный в стандартную терапию обострений ХТФ, показал свою клиническую эффективность, которая подтверждена клиническими специализированными оториноларингологическими исследованиями, а также анкетами-опросниками по оценке субъективных ощущений пациентов. Эффективность местной противовоспалительной терапии сохранялась на протяжении всего периода наблюдения.
Эффективность противовоспалительного, обезболивающего действия доказана с использованием современных методов медицинской статистики. При этом различия клинических и цифровых показателей группы 1 (стандартная терапии + Ангидак®, спрей для местного применения дозированный) и группы 2 (стандартная терапия + Тантум® Верде, спрей для местного применения дозированный) не были статистически значимы. Это свидетельствует о сходной эффективности препаратов Ангидак® и Тантум® Верде, спрей для местного применения дозированный, содержащих бензидамин.
Побочных и нежелательных эффектов терапии у обследованных 30 пациентов не зафиксировано.
Бактериологические исследования мазков с поверхности небных миндалин, выполненные до и после проведенного лечения, продемонстрировали выраженный антимикробный эффект бензидамина в отношении основных клинически значимых патогенов ХТ, проявляющийся в виде эрадикаци и снижения обсемененности биоматериала: в 73,3% случаев для БГСА, в 76,1% — для Staphylococcus aureus.
Таким образом, препарат бензидамин, спрей для местного применения дозированный, является безопасным и эффективным средством в составе комплексного лечения пациентов с обострением ХТФ и может применяться в любой фазе развития заболевания.
материал rmj.ru
