Введение
Аутологичная трансплантация гемопоэтических стволовых клеток (аутоТПГСК) является стандартным методом лечения ряда злокачественных заболеваний, таких как множественная миелома, высокоагрессивные лимфомы и некоторые виды лейкозов [1]. В отличие от аллогенной трансплантации, при аутоТПГСК пациент получает собственные заранее заготовленные стволовые клетки. Это позволяет избежать риска реакции «трансплантат против хозяина», однако не отменяет других серьезных осложнений, связанных с высокодозной химиотерапией. Одной из наиболее значимых и частых проблем в раннем посттрансплантационном периоде является поражение желудочно-кишечного тракта (ЖКТ) [2].
Главным механизмом повреждения ЖКТ является токсическое действие лекарственных препаратов на быстро делящиеся клетки слизистых оболочек организма. Существует прямое цитотоксическое действие: кондиционирующие режимы (например, на основе мелфалана, кармустина, этопозида, циклофосфамида) вызывают апоптоз эпителиоцитов крипт тонкой и толстой кишки, что приводит к нарушению регенерации слизистой, ее истончению, изъязвлению и потере барьерной функции. Повреждение слизистого барьера позволяет бактериям, их эндотоксинам и другим продуктам жизнедеятельности проникать в системный кровоток. Это является одним из основных триггеров системной воспалительной реакции и бактериемий, а также стимулирует выброс провоспалительных цитокинов (фактора некроза опухоли α, интерлейкинов 1 и 6), которые усугубляют повреждение и замедляют регенерацию [3]. Чаще всего посттрансплантационный период осложняют оральный мукозит (75–100% случаев) и тяжелая энтеропатия (50–90% случаев). Степень тяжести мукозита оценивается по шкале ВОЗ или СTСАЕ [3].
В нашей клинике используются предтрансплантационные курсы химиотерапи, такие как высокодозный мелфалан (в 70–90% случаев приводит к оральному мукозиту 3–4-й степени и в 30–50% случаев — к тяжелой энтеропатии), миелоаблативый курс СEAM (в 50–80% случаев приводит к развитию мукозита ротовой полости и в 60–90% — к тяжелому течению энтеропатий).
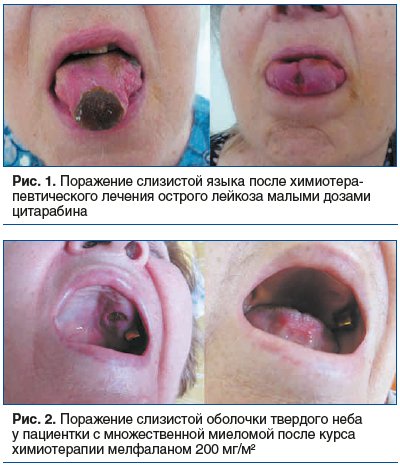
Поражение ЖКТ после аутоТПГСК представляет собой спектр синдромов, которые часто наслаиваются друг на друга. Мукозит слизистой затрагивает ЖКТ на всем его протяжении [4]. Воспаление и изъязвление слизистой оболочки выявляется от полости рта до прямой кишки. В клинике преобладают болевой синдром, дисфагия, одинофагия (боль при глотании), тошнота, рвота, водянистая диарея, боль в животе. Оральный мукозит встречается практически у всех пациентов, перенесших высокодозную химиотерапию, и является одним из самых субъективно тяжелых осложнений [3]. Кишечный мукозит выступает ведущей причиной диареи и может приводить к грозным инфекционным и электролитным осложнениям. Поражение ротовой полости (рис. 1, 2) и верхних отделов ЖКТ приводит к выраженному болевому синдрому, необходимости в парентеральном питании и опиоидной анальгезии, повышает риск обезвоживания и инфекционных осложнений [3, 4].
Диарейный синдром — основное проявление поражения слизистой кишечника. Пораженный ЖКТ быстро заселяется патогенной микрофлорой, такой как Clostridioides difficile, которая часто возникает на фоне антибиотикотерапии. Реже присоединяются энтеропатогенные инфекции (вирусы, бактерии, грибы) [4, 5].
Тошнота и рвота на фоне химиотерапевтического лечения и длительной антибиотикотерапии также усиливают поражение стенки кишки. Они обусловлены как прямым действием химиопрепаратов на хеморецепторную триггерную зону в головном мозге, так и прямым повреждением слизистой ЖКТ, снижают качество жизни и приводят к нарушению нутритивного статуса [4].
Диагностика состояния преимущественно основывается на клинической картине. Клиническая оценка предусматривает ведение дневника диареи, оценку боли по шкалам, мониторинг баланса жидкости. Лабораторные исследования: общий анализ крови (контроль нейтропении, тромбоцитопении), биохимические показатели (электролиты, альбумин), микробиологические исследования на C. difficile и другие патогены, кальпротектин в кале (маркер воспаления в кишечнике). Эндоскопические исследования (гастроскопия, колоноскопия) проводятся редко, в основном при подозрении на тяжелое кровотечение или для дифференциальной диагностики. Визуализация (компьютерная томография брюшной полости) может потребоваться при подозрении на токсический мегаколон или другие осложнения [5].
Лечение поражения слизистых оболочек носит комбинированный характер: коррекция диеты, зачастую требуется обезболивающая терапия с использованием опиоидных анальгетиков, проведение длительного антибактериального, противогрибкового и противовирусного лечения, коррекция электролитных и белковых нарушений [5–8]. Воспаление слизистых может вызывать септические состояния и приводить к летальному исходу. Кроме проблем клинических, поражение оболочек при аутологичной трансплантации зачастую приводит к удлинению сроков госпитализации и удорожанию лечения. В связи с вышесказанным очень актуальна проблема профилактики данного поражения [5].
Учитывая механизмы повреждения слизистых оболочек, было принято решение включить в схему лечения этой группы пациентов медицинское изделие фиксированной комбинации гиалуроновой кислоты и хондроитина сульфата и биоадгезивного вещества полоксамер 407 — Альфазокс. Основные клинические показания к использованию — создание механического барьера от агрессивной среды, которая приводит к эрозивным поражениям ЖКТ. Изделие ускоряет регенерацию, обладает противовоспалительным действием, уменьшает проницаемость слизистой оболочки для патогенной флоры [9].
Первый опыт использования препарата в нашем стационаре был предпринят у пациента Б. 33 лет с лимфомой серой зоны с обширным дефектом слизистой пищевода, с пищеводно-плевральным свищом в 2022 г. (рис. 3). В рамках комплексной терапии пациент получал иммунохимиотерапию, параллельно был установлен стент пищевода, наложена гастростома, кроме того, использовалось медицинское изделие Альфазокс 4 р/сут, начиная со 2-го месяца лечения, когда было разрешено потребление жидкости через рот. В результате продолжительного (4 мес.) многокомпонентного лечения дефект полностью эпителизировался.
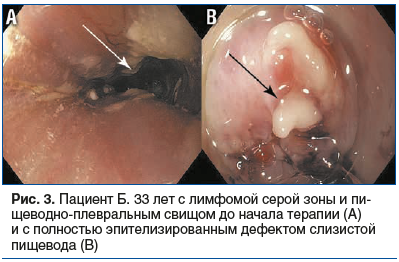
В связи с хорошим регенераторным эффектом было принято решение включить это медицинское изделие в схему ведения пациентов на высокодозной химиотерапии при аутоТПГСК. Представляем первый собственный опыт.
Собственный опыт
В 2025 г. в течение 7 мес. провели исследование, в которое было включено 10 пациентов (группа наблюдения, средний возраст 56,4 года), получивших Альфазокс во время предтрансплантационной подготовки, трансплантации и в посттрансплантационном периоде (7 пациентов с множественной миеломой, получавших лечение мелфаланом 200 мг/м2, 3 пациента c высокоагрессивными лимфомами, получавших курс CEAM). Группа сравнения (ретроспективная) — 10 пациентов (средний возраст 53 года) с такими же нозологическими формами. Слизистая ротовой полости, зубы и кишечник на догоспитальном этапе у всех пациентов были санированы. Пациенты в обеих группах на момент госпитализации в общем анализе крови имели нормальный уровень лейкоцитов и нейтрофилов, но у всех отмечалось снижение уровня IgG сыворотки крови ниже 5 г/л.
Сравнивали длительность госпитализации, степень тяжести мукозита ротовой полости, пищевода и энтеропатии.
Пациенты в группе наблюдения с 1-го дня госпитализации до выписки из стационара (17–21-й день) получали Альфазокс по 1 саше 4 р/сут, использовался охлажденный раствор. Пациенты 2 мин держали препарат во рту перед проглатыванием с целью большей адгезии препарата к слизистой ротовой полости.
Гематологическая токсичность развивалась у всех пациентов, перенесших высокодозную химиотерапию и получивших аутоТПГСК.
В группах сравнения с 5-го дня (после аутологичной трансплантации) у пациентов, получивших курс терапии CEAM, и с 8-го дня у пациентов, получивших мелфалан 200 мг/м2, развивался агранулоцитоз.
Среднее время развития тромбоцитопении 3–4-й степени во всех группах приходилось на 11-й день после трансплантации, у 3 пациентов в группе сравнения отмечался геморрагический синдром по слизистой ротовой полости. В группе наблюдения геморрагий на слизистой рта выявлено не было.
Пациенты обеих групп с момента развития фебрильной нейтропении получали карбапенемы (имипенем 0,5 г 4 р/сут или меропенем по 1 г 3 р/сут) и противогрибковые препараты парентерально (флуконазол 400 мг) [7]. Cреднее время начала противомикробной терапии у всех пациентов — 5-й день после трансплантации. У 8 пациентов группы сравнения отмечался оральный мукозит средней и тяжелой степени (по клинической выраженности симптомов мальабсорбции) и у 4 пациентов — энтеропатия средней степени тяжести. Требовалась комплексная терапия, включающая нестероидные противовоспалительные препараты (НПВП) и опиоидные анальгетики (2 пациента), коррекция электролитных нарушений и парентерального питания. У пациентов группы наблюдения отмечался оральный мукозит легкой степени в 5 случаях и средней степени тяжести в 1 случае. С целью обезболивания они получали НПВП. Энтеропатия легкой степени отмечалась у 6 пациентов, парентеральное питание не назначалось.
При разрешении агранулоциоза (в среднем на 16-й день после трансплантации) на фоне комплексной терапии воспалительные изменения слизистых регрессировали, клинические признаки орального мукозита и энтеропатии были купированы, обезболивание не требовалось. Отмечалась стойкая нормотермия в обеих группах. На длительность госпитализации использование препарата существенно не повлияло, среднее время пребывания в стационаре в обеих группах — 22 дня.
Таким образом, использование медицинского изделия фиксированной комбинации гиалуроновой кислоты и хондроитина сульфата и биоадгезивного вещества полоксамер 407 улучшает переносимость лечения. В группе наблюдения клинически отмечалось уменьшение выраженности явлений орального мукозита, поражения слизистой ЖКТ, реже возникала потребность в применении обезболивающих препаратов и не назначались опиодные анальгетики. Кроме этого, препарат работает пристеночно и не всасывается в кровяное русло, что может минимизировать лекарственные взаимодействия при проведении интенсивной цитостатической терапии.
Заключение
Поражение ЖКТ остается одним из наиболее частых и клинически значимых осложнений аутоТПГСК. Несмотря на отсутствие риска кишечной реакции «трансплантат против хозяина», токсичность миелоаблативных курсов терапии приводит к развитию тяжелого мукозита, диареи и связанных с ними метаболических и инфекционных осложнений, которые определяют течение раннего посттрансплантационного периода.
Современные подходы к лечению гемобластозов становятся все более агрессивными и требуют комплексной интенсивной сопроводительной терапии, адекватного обезболивания и профилактики инфекционных осложнений. Дальнейшие исследования в области цитопротективных агентов открывают новые перспективы для снижения гастроинтестинальной токсичности и улучшения исходов у пациентов, переносящих аутоТПГСК.
Список литературы Вы можете найти на сайте http://www.rmj.ru
Информация с rmj.ru


