Введение
Жировая болезнь печени (ЖБП) различной этиологии, включающая неалкогольную (НАЖБП) и алкогольную жировую болезнь печени (АЖБП), — актуальная проблема здравоохранения в связи с высокой распространенностью и потенциальным прогрессированием в цирроз печени и гепатоцеллюлярную карциному [1, 2]. Прогрессирование ассоциировано со стеатогепатитом, представляющим сложный спектр патологических изменений в печени, включая, кроме стеатоза, воспаление, апоптоз, некроз и фиброз [3, 4]. Именно поэтому разграничение стеатоза и стеатогепатита при ЖБП столь важная, но не простая задача.
«Золотой стандарт» диагностики ЖБП, включая стеатогепатит, — биопсия печени, поскольку ни один из доступных неинвазивных тестов не обладает приемлемой точностью [5]. Гистологическое исследование биоптата позволяет оценить степень стеатоза, некротических изменений, фиброза, определить активность и стадию болезни. Однако в реальной практике использование биопсии ограничено целым рядом факторов, таких как инвазивность и вероятность осложнений, оценка очень малой части органа, что при мозаичном поражении печени снижает точность диагностики, и т. д. [6]. Именно поэтому большое значение приобретают неинвазивные способы оценки функции и структуры печени.
Среди визуализирующих методов в качестве первоочередного инструмента для диагностики стеатоза рекомендуется ультразвуковое исследование (УЗИ) печени, однако этот метод не позволяет разграничить стеатоз и стеатогепатит [6]. Возможность количественной оценки стеатоза печени путем измерения ультразвукового ослабления эховолны, именуемого контролируемым параметром затухания, — CAP-функция была реализована на устройстве FibroScan [7]. Еще более точный метод диагностики и оценки степени выраженности стеатоза — магнитно-резонансная спектроскопия [8]. Однако оба подхода не позволяют оценить наличие активного воспаления в печени.
Для диагностики стеатоза было предложено несколько лабораторных методов: применение SteatoTestTM, определение индекса ожирения печени (FLI), индекса стеатоза печени (HSI), индекса накопления липидов, индексов NASH и ASH, а также показателя содержания жира в печени при НАЖБП (NAFLD-LFS) [9]. Однако диагностические характеристики данных тестов трудносопоставимы в случае определения стеатоза, а при установлении выраженности стеатогепатита необходима информация о его этиологии (неалкогольная или алкогольная), которая не всегда очевидна.
Для неинвазивной диагностики неалкогольного стеатогепатита было предложено несколько маркеров или показателей, таких как фрагменты цитокератина 18, комбинация клинических показателей, комбинация клинических показателей с мутацией I148M в гене PNPLA3, оценки на основе метаболомики или липидомики, а также методы визуализации. Однако противоречивые результаты, отсутствие валидационных исследований и ряда параметров, включенных во многие шкалы оценки, ограничивают рекомендации относительно применения предлагаемых инструментов в клинической практике [8, 10]. Именно поэтому продолжается поиск новых малоинвазивных и доступных маркеров, позволяющих дифференцировать стеатоз от стеатогепатита.
В проведенных нами ранее исследованиях показаны особенности электрических и вязкоупругих параметров эритроцитов у пациентов с диффузной патологией печени различного генеза [11], при разных стадиях заболевания [12], степени фиброза [13], применение их для различения пациентов с ЖБП алкогольного и неалкогольного генеза [14].
Цель исследования: изучение возможностей использования электрических и вязкоупругих параметров эритроцитов для дифференцирования стеатогепатита от стеатоза печени.
Материал и методы
Проведено сравнительное нерандомизированное открытое исследование серии случаев. Обследованы 84 мужчины (средний возраст 48,9±2,5 года) с ЖПБ по данным УЗИ органов брюшной полости. Степень выраженности фиброза печени устанавливали методом непрямой эластометрии на аппарате FibroScan® 502 (Echosens, Франция) с разграничением стадии фиброза по шкале METAVIR от F0 до F4. У всех обследованных она не превышала 1-ю степень, что было подтверждено алгоритмом FibroTest в составе FibroTest-ActiTest (BioPredictive, Франция) [5]. Степень некровоспалительной активности в печени определяли с помощью алгоритма ActiTest в составе FibroTest-ActiTest, предполагающего определение 6 биохимических параметров: α2-макроглобулина, гаптоглобина, аполипопротеина А1, общего билирубина, гамма-глютамилтранспептидазы (ГГТП), аланинаминотрансферазы (АЛТ).
Пациентов распределили в 2 группы в зависимости от степени активности некровоспалительного процесса. В 1-ю группу (n=44) включили пациентов со стеатозом, у которых определялась минимальная гистологическая активность (А0–1); во 2-ю группу (n=40) вошли пациенты со стеатогепатитом с показателями выраженной некровоспалительной активности (А2–3). Пациенты со стеатозом и стеатогепатитом были сопоставимы по возрасту, этиологии ЖБП, показателям липидного профиля и пуринового обмена.
Отсутствие серологических маркеров, определяемых методом иммуноферментного анализа (ИФА), и/или ДНК и РНК вирусов, определяемых методом полимеразной цепной реакции, исключали вирусную этиологию заболевания. Алкогольный генез стеатоза устанавливали по данным о потреблении алкоголя в настоящее время и в анамнезе с использованием стандартного опроса о стиле потребления алкоголя, в том числе с помощью опросников CAGE, AUDIT. НАЖБП диагностирована в соответствии с критериями клинических рекомендаций [15]. В случае регулярного потребления пациентами алкоголя и проявлений у них метаболического синдрома этиологию ЖБП считали смешанной (метаболическая + алкогольная) и диагностировали ее согласно рекомендациям экспертов Всероссийского научного общества кардиологов.
Пациентам проведено комплексное клинико-инструментальное обследование, включающее изучение показателей красной крови и биохимическое исследование.
Наличие или отсутствие инсулинорезистентности оценивали на основании расчетного индекса Caro [16]: Индекс Caro = глюкоза (ммоль/л) натощак инсулин (мкЕд/мл) натощак
Значения индекса <0,33 свидетельствовали о наличии инсулинорезистентности.
Также рассчитывали NAFLD-LFS по формуле [17]: NAFLD-LFS = -2,89 + 1,18 × (МС: да — 1, нет — 0) + 0,45 × (СД2: да — 2, нет — 0) + 0,15 × инсулин (мкЕд/мл) + 0,04 × АСТ (Ед/л) — 0,94 × (АСТ (Ед/л)) (АЛТ (Ед/л)) ,
где МС — метаболический синдром, СД2 — сахарный диа-бет 2 типа, АЛТ— активность аланинаминотрансферазы, АСТ — активность аспартатаминотрансферазы.
У всех обследованных изучены параметры электрических и вязкоупругих характеристик эритроцитов методом диэлектрофореза в неоднородном переменном электрическом поле с помощью электрооптической системы детекции клеток [11]. Оценивали средний диаметр эритроцитов (мкм), относительное количество дискоцитов (%), сфероцитов (%), деформированных клеток (%), поляризуемость клеток на разных частотах диапазона (м3), относительную поляризуемость (соотношение величины показателя на частоте 1 МГц к величине на частоте 0,1 МГц), обобщенные показатели жесткости (Н/м), вязкости (Па×с), электропроводность мембран (См/м), индексы деструкции (на разных частотах диапазона) (%) и агрегации (усл. ед.), амплитуду деформации эритроцитов на частоте 1 МГц (м), степень деформации клеток на частоте 0,5 МГц (%), емкость мембран эритроцитов (Ф), скорость движения клеток к электродам (мкм/c), положение равновесной частоты (Гц), величину дипольного момента (Кл×м). Для распознавания образа клеток и компьютерной обработки данных использовали пакет оригинальных программ CELLFIND (Россия). Ошибка воспроизводимости метода составила 7–12%.
Статистическая обработка данных выполнена с использованием программы IBM SPSS Statistics 26.0 (IBM, США). Определяли характер распределения количественных признаков методом Колмогорова — Смирнова. В случае нормального распределения вычисляли среднее значение (М) и стандартную ошибку средней арифметической (m) (M±m). При сравнении двух выборок с нормальным распределением использовали t-тест Стьюдента. При отсутствии нормального распределения вычисляли медиану (Me), верхний и нижний квартиль (Me [Q1; Q3]) достоверность различия показателей оценивали с помощью непараметрических критериев (U-критерий Манна — Уитни, Краскела —Уоллиса, χ2 критерий Пирсона). Для оценки статистической значимости различий относительных показателей использован χ2 критерий Пирсона. Связи между признаками для интервальных и порядковых переменных оценивали ранговым коэффициентом корреляции Спирмена. Для определения параметров эритроцитов, которые могут служить потенциальными маркерами для дифференцирования стеатогепатита и стеатоза печени, проводили процедуру нормализации показателей с последующим использованием метода Volcano plot (непарная статистика). Диагностическую точность показателей эритроцитов в качестве биомаркеров стадии заболевания оценивали с помощью ROC-анализа. Во всех процедурах статистического анализа критический уровень значимости нулевой гипотезы (p) принимали равным 0,05.
Исследование одобрено этическим комитетом НИИТПМ — филиалом ИЦиГ СО РАН (протокол заседания № 122 от 29.11.2016). Все обследуемые дали информированное согласие на участие в исследовании.
Результаты и обсуждение
В 1-й группе у 11 (25%) пациентов диагностировали АЖБП, у 10 (22,7%) — НАЖБП, у 23 (52,3%) этиология ЖБП оказалась смешанной (метаболическая + алкогольная). Во 2-й группе у 12 (30%) пациентов стеатогепатит был алкогольного генеза, у 10 (25%) — неалкогольного, у 18 (45%) — смешанного. В группе пациентов со стеатогепатитом статистически значимо выше были показатели синдрома цитолиза (активность трансаминаз, уровни билирубина, сывороточного железа) (p<0,05) и маркеры воспаления (фибриноген, С-реактивный белок (СРБ), ферритин) (p<0,05). Индекс Caro свидетельствовал о наличии инсулинорезистентности у большей части пациентов обеих групп. Индекс NAFLD-LFS не различался в обеих группах, поскольку в них преобладали пациенты с метаболическим синдромом.
Клинико-биохимические показатели пациентов исследуемых групп представлены в таблице 1.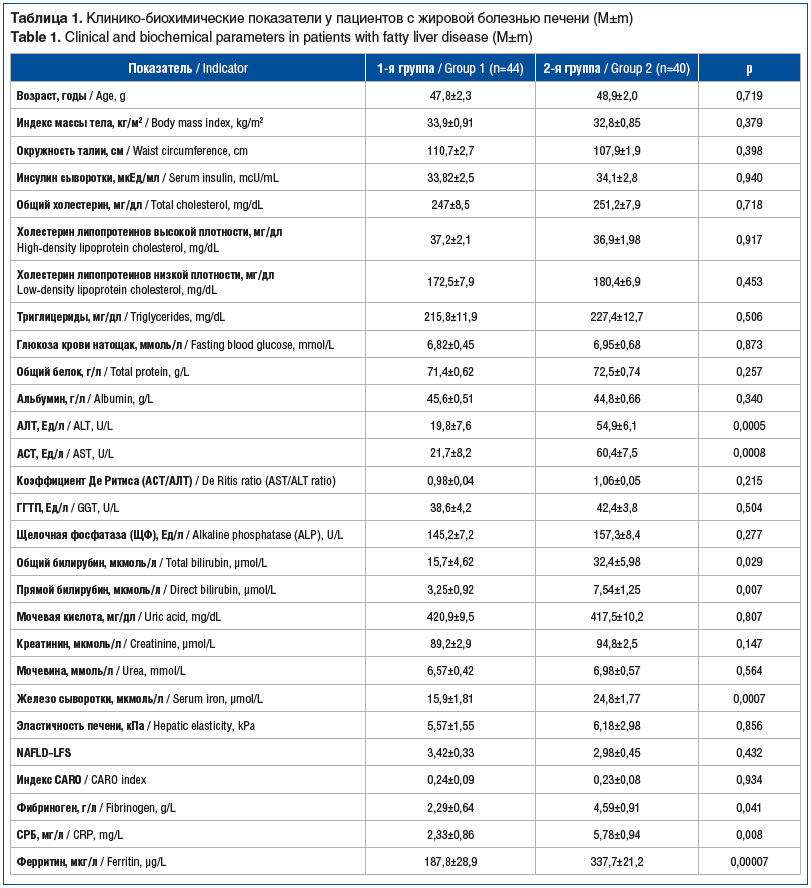
У пациентов обеих групп исследованы электрические и вязкоупругие параметры эритроцитов методом диэлектрофореза.
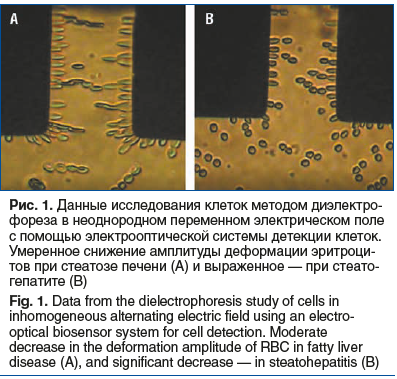
Размер эритроцитов у пациентов со стеатогепатитом и стеатозом не различался, однако среди пациентов со стеа-тогепатитом количество сфероцитов (p=0,024) и деформированных клеток (p=0,005) оказалось значимо больше (табл. 2). Снижение количества дискоцитов (p=0,03) ассоциировано с внутриклеточным энергодефицитом [18]. У пациентов со стеатогепатитом была снижена амплитуда деформации на высоких частотах электрического поля (p<0,001 и p=0,002 на 1 МГц и 0,5 МГц соответственно) с увеличением обобщенных показателей жесткости (p=0,004) и вязкости (p=0,006) по сравнению с пациентами со стеатозом (рис. 1). Уменьшение способности эритроцитов к деформации приводит к снижению высвобождения кислорода и внутриэритроцитарного оксида азота в тканях [19], в том числе в печени, способствуя нарастанию ишемии и гипоксии — факторов повреждения гепатоцитов и триггеров фиброгенеза [20]. При продукции активных форм кислорода (АФК) нарушается деформируемость эритроцитов с одновременной деградацией мембранных белков, индукцией перекисного окисления фосфолипидов эритроцитарной мембраны, набуханием эритроцитов, образованием метгемоглобина, окислительным гемолизом [21]. Внеклеточные АФК, по-видимому, индуцируют перекисное окисление липидов эритроцитов, в то время как внутриклеточная генерация АФК сшивает мембранные белки, включая гемоглобин-мембранные поперечные связи [20].
![Таблица 2. Электрические и вязкоупругие показатели эритроцитов у пациентов со стеатозом и стеатогепатитом (Me [Q1; Q3]) Table 2. Electrical and viscoelastic parameters of erythrocytes in patients with steatosis and steatohepatitis (Me [Q1; Q3]) Таблица 2. Электрические и вязкоупругие показатели эритроцитов у пациентов со стеатозом и стеатогепатитом (Me [Q1; Q3]) Table 2. Electrical and viscoelastic parameters of erythrocytes in patients with steatosis and steatohepatitis (Me [Q1; Q3])](https://medblog.su/wp-content/uploads/2023/07/1689066957_866_Vozmozhnosti-ispolzovaniya-elektricheskih-i-vyazkouprugih-parametrov-eritrotsitov-dlya-diagnostiki-steatogepatita.png)
Равновесная частота (отражающая токсическое воздействие на эритроциты циркулирующих свободных жирных кислот, цитокинов с измененными профилями и хемокинов [12]) у пациентов со стеатогепатитом оказалась сдвинутой в высокочастотный диапазон по сравнению с лицами со стеатозом (p=0,049). В группе со стеатогепатитом обнаружены косвенные признаки модификации структуры мембран эритроцитов: статистически значимое снижение показателей дипольного момента (p<0,001) и скорости движения клеток к электродам (p=0,02), ассоциированные с уменьшением поверхностного отрицательного заряда эритроцитов [22]. Одна из возможных причин наблюдаемых изменений — адсорбция на поверхности клеток крупномолекулярных белков, в том числе маркеров воспаления [23]. Действительно, корреляционный анализ позволил выявить связь между величинами дипольного момента, скоростью движения эритроцитов к электродам и уровнями фибриногена (r=-0,675, p<0,0001 для дипольного момента, r=-0,428, p=0,042 для скорости), СРБ (r=-0,507, p=0,004 для дипольного момента, r=-0,534, p=0,004 для скорости), ферритина (r=-0,417, p=0,032 для дипольного момента, r=-0,411, p=0,007 для скорости).
Повышенный показатель электропроводности (p=0,004) и сниженный — емкости мембран клеток (p<0,001) у пациентов со стеатогепатитом свидетельствуют об утолщении мембран с повышением способности проводить электрический ток [12]. Подобные сдвиги могут быть обусловлены изменением соотношения в мембранах эритроцитов холестерина и фосфолипидов, уменьшением фракций легкоокисляемых фосфолипидов, изменением профиля жирных кислот (повышение уровней насыщенных, мононенасыщенных, линолевой, омега-6 полиненасыщенных жирных кислот (ПНЖК) и снижение — омега-3 ПНЖК, увеличение активности элонгазы (белка ELOVL6), показателя липогенеза de novo — C16:0/C18:2n-6 и снижение активности стеароил-КоА-десатуразы 1) [24] и связанной с этим нарушением активности вискозитропных трансмембранных ферментов [18].
Метод диэлектрофореза позволяет исследовать показатели поляризуемости и гемолиза эритроцитов на разных частотах электрического поля, которые служат моделью воздействия стресса различной интенсивности [12]. Поляризуемость клеток отражает уровень их биологической активности, жизнеспособности. Клетки в предгемолитическом состоянии продемонстрировали низкие уровни поляризуемости [25]. У пациентов со стеатогепатитом были статистически значимо снижены уровни поляризуемости на высоких частотах электрического поля — 1 МГц (p<0,001) и 0,5 МГц (p=0,002), а также относительной поляризуемости (p=0,015), ассоциированной с адаптационными возможностями клеток [12]. Индекс деструкции также оказался значимо выше на высоких частотах при наличии воспаления по сравнению со стеатозом (p<0,0001). Выявленные изменения свидетельствуют о том, что функциональные различия между клетками пациентов со стеатогепатитом и стеатозом проявляются при воздействии на клетки выраженного стресса. В случае стресса низкой интенсивности поведение клеток в переменном электрическом поле не различалось (табл. 3).
![Таблица 3. Индексы деструкции эритроцитов и показатели поляризуемости у пациентов со стеатогепатитом и стеатозом (Me [Q1; Q3]) Table 3. RBC destruction and polarizability indices in patients with steatohepatitis and steatosis (Me [Q1; Q3]) Таблица 3. Индексы деструкции эритроцитов и показатели поляризуемости у пациентов со стеатогепатитом и стеатозом (Me [Q1; Q3]) Table 3. RBC destruction and polarizability indices in patients with steatohepatitis and steatosis (Me [Q1; Q3])](https://medblog.su/wp-content/uploads/2023/07/1689066957_215_Vozmozhnosti-ispolzovaniya-elektricheskih-i-vyazkouprugih-parametrov-eritrotsitov-dlya-diagnostiki-steatogepatita.png)
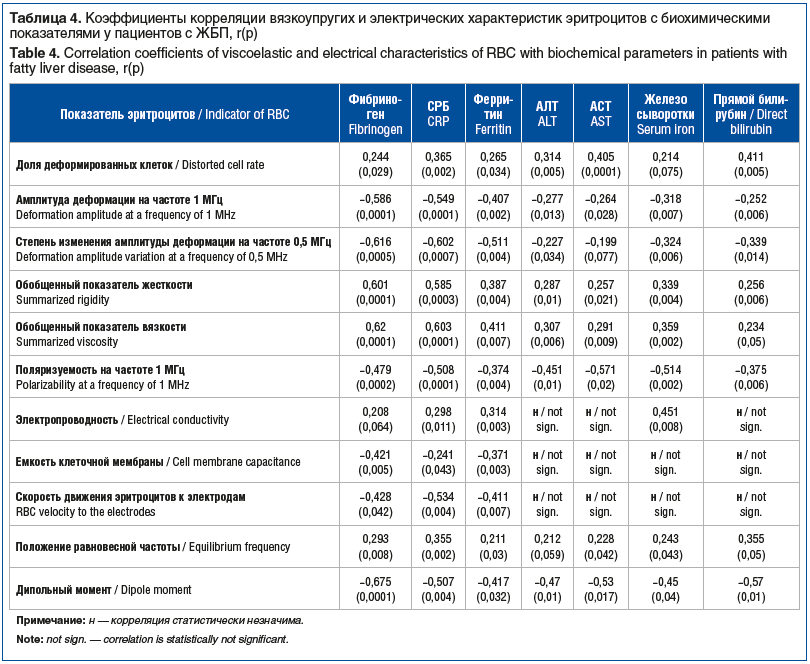
Исследование корреляций между электрическими, вязкоупругими параметрами эритроцитов и биохимическими показателями выявило обратную связь с амплитудой деформации эритроцитов, поляризуемостью на частоте 1 МГц, скоростью движения к электродам, величиной дипольного момента, емкостью мембран и показателями синдрома цитолиза, а также маркерами воспаления. Корреляции доли деформированных клеток, обобщенных показателей вязкости, жесткости, электропроводности и положения равновесной частоты с теми же биохимическими параметрами оказались прямыми (табл. 4).
В клинической практике повышение активности АЛТ, АСТ расценивают как проявление стеатогепатита при наличии ЖБП, хотя референтные уровни аминотрансфераз не исключают наличие воспаления в ткани печени [25]. Повышение активности трансаминаз — проявление синдрома цитолиза, обусловленного нарушением проницаемости мембран гепатоцитов и их органелл, что приводит к выделению составных частей клеток в межклеточное пространство и кровь [26]. Повышенная активность трансаминаз в настоящем исследовании ассоциировалась с более значимыми изменениями эритроцитов: большей долей деформированных клеток с меньшей амплитудой деформации, а также со сниженным поверхностным зарядом.
Для выявления параметров эритроцитов, наиболее значимых для различения стеатогепатита и стеатоза (потенциальных биомаркеров стеатогепатита), значения показателей были нормализованы с последующим использованием метода Volcano plot (табл. 5).
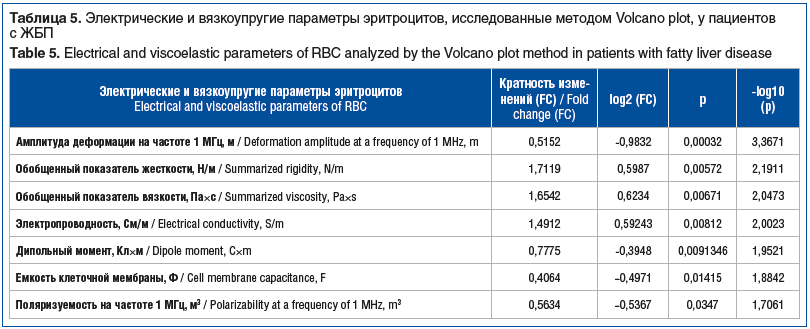
Наиболее значимы для различения стеатогепатита и стеа-тоза оказались показатели вязкоупругих свойств эритроцитов — амплитуда деформации на частоте 1 МГц, обобщенные показатели вязкости, жесткости, параметры, отражающие состояние мембран клеток, — дипольный момент, электропроводность, емкость и поляризуемость клеток на частоте 1 МГц, отражающая резистентность эритроцитов.
Данные параметры были объединены в одну диагностическую панель и при проведении ROC-анализа для различения стеатогепатита и стеатоза продемонстрировали чувствительность 0,9, специфичность 0,83 (рис. 2).
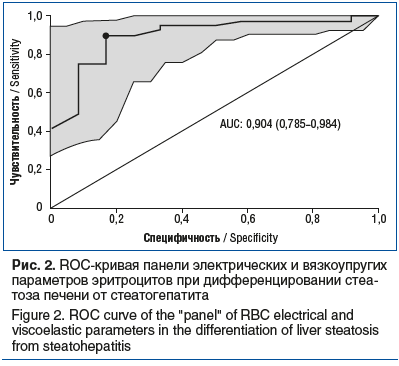
Представленная модель показала высокую диагностическую точность при дифференцировании стеатогепатита от стеатоза, что, вероятно, обусловлено тесными ассоциациями электрических и вязкоупругих параметров эритроцитов с показателями синдрома цитолиза, маркерами воспаления. Предложенный подход к диагностике стеатогепатита следует считать перспективным, поскольку традиционно используемые показатели для оценки наличия стеатогепатита могут оставаться в пределах референтных значений. Низкие время- и трудозатратность метода диэлектрофореза позволяют в короткие сроки выявлять пациентов со стеатогепатитом, нуждающихся в углубленном обследовании. Использование данного подхода в процессе лечения даст возможность объективизировать его эффективность.
Ограничения настоящего исследования: небольшой объем обследованных, анализ корреляций параметров эритроцитов с ограниченным перечнем показателей, отсутствие определения параметров эритроцитов, ассоциированных со стеатогепатитом при различном генезе ЖБП. В последующем предполагается валидизация предложенной диагностической модели на популяционном уровне.
Выводы
Исследование электрических и вязкоупругих параметров эритроцитов у пациентов с ЖБП позволило выявить ряд особенностей, ассоциированных с наличием стеатогепатита в отличие от стеатоза печени: снижение амплитуды деформации (p=0,0003), дипольного момента (p=0,009), емкости (p=0,014) и поляризуемости клеток на частоте 1 МГц (p=0,03), а также более высокие уровни обобщенных показателей вязкости (p=0,006), жесткости (p=0,005), электропроводности (p=0,008) (метод Volcano plot).
Диагностическая панель, включающая совокупность электрических и вязкоупругих параметров эритроцитов, для дифференцирования стеатогепатита от стеатоза продемонстрировала AUC 0,904, чувствительность 0,9, специфичность 0,83.
Установлены корреляции параметров эритроцитов с показателями синдрома цитолиза (активность трансаминаз, уровни сывороточного железа, прямого билирубина) и сывороточными маркерами воспаления (фибриноген, СРБ, ферритин).
Электрические и вязкоупругие параметры эритроцитов, исследованные с помощью метода диэлектрофореза, следует рассматривать как новый перспективный подход в определении степени тяжести ЖБП.
Сведения об авторах:
Кручинина Маргарита Витальевна — д.м.н., доцент, ведущий научный сотрудник, заведующая лабораторией гастроэнтерологии НИИТПМ — филиала ИЦиГ СО РАН; 630089, Россия, г. Новосибирск, ул. Бориса Богаткова, д. 175/1; профессор кафедры пропедевтики внутренних болезней ФГБОУ ВО НГМУ Минздрава России; 630091, Россия, г. Новосибирск, Красный пр-т, д. 52; ORCID iD 0000-0003-0077-3823.
Паруликова Марина Владимировна — врач-гастроэнтеролог, старший преподаватель отдела образования НИИТПМ — филиала ИЦиГ СО РАН; 630089, Россия, г. Новосибирск, ул. Бориса Богаткова, д. 175/1.
Белковец Анна Владимировна — д.м.н., доцент, старший научный сотрудник лаборатории гастроэнтерологии, заведующая клиникой НИИТПМ — филиала ИЦиГ СО РАН; 630089, Россия, г. Новосибирск, ул. Бориса Богаткова, д. 175/1; профессор кафедры пропедевтики внутренних болезней ФГБОУ ВО НГМУ Минздрава России; 630091, Россия, г. Новосибирск, Красный пр-т, д. 52; ORCID iD 0000-0002-2610-1323.
Громов Андрей Александрович — к.м.н., старший научный сотрудник лаборатории клинических биохимических и гормональных исследований терапевтических заболеваний, руководитель центра профилактики тромбозов НИИТПМ — филиала ИЦиГ СО РАН; 630089, Россия,
г. Новосибирск, ул. Бориса Богаткова, д. 175/1; ORCID iD 0000-0001-9254-4192.
Контактная информация: Кручинина Маргарита Витальевна, e-mail: kruchmargo@yandex.ru.
Прозрачность финансовой деятельности: работа выполнена по Государственному заданию в рамках бюджетных тем FWNR-2022-0024, FWNR-2023-0003. Никто из авторов не имеет финансовой заинтересованности в представленных материалах и методах.
Конфликт интересов отсутствует.
Статья поступила 10.04.2023.
Поступила после рецензирования 04.05.2023.
Принята в печать 31.05.2023.
About the authors:
Margarita V. Kruchinina — Dr. Sc. (Med.), Associate Professor, Leading Researcher, Head of the Laboratory of Gastroenterology, Research Institute of Therapy and Preventive Medicine — Branch of Federal Research Center Institute of Cytology and Genetics of the Siberian Branch of the RAS; 175/1, Boris Bogatkov str., Novosibirsk, 630089, Russian Federation; Professor of the Department of Propaedeutics of Internal Medicine, Novosibirsk State Medical University; 52, Krasny Ave, Novosibirsk, 630091, Russian Federation; ORCID iD 0000-0003-0077-3823.
Marina V. Parulikova — gastroenterologist, Senior Lecturer of the Department of Education, Research Institute of Therapy and Preventive Medicine — Branch of Federal Research Center Institute of Cytology and Genetics of the Siberian Branch of the RAS; 175/1, Boris Bogatkov str., Novosibirsk, 630089, Russian Federation.
Anna V. Belkovets — Dr. Sc. (Med.), Associate Professor, Leading Researcher of the Laboratory of Gastroenterology, Head of the Research Institute of Therapy and Preventive Medicine — Branch of Federal Research Center Institute of Cytology and Genetics of the Siberian Branch of the RAS; 175/1, Boris Bogatkov str., Novosibirsk, 630089, Russian Federation; Professor of the Department of Propaedeutics of Internal Medicine, Novosibirsk State Medical University; 52, Krasny Ave, Novosibirsk, 630091, Russian Federation; ORCID iD 0000-0002-2610-1323.
Andrey A. Gromov — C. Sc. (Med.), Senior Researcher at the Laboratory of Clinical Biochemical and Hormonal Studies of Therapeutic Diseases, Head of the Center for Thrombosis Prevention of Research Institute of Therapy and Preventive Medicine — Branch of Federal Research Center Institute of Cytology and Genetics of the Siberian Branch of the RAS; 175/1, Boris Bogatkov str., Novosibirsk, 630089, Russian Federation; ORCID iD 0000-0001-9254-4192.
Contact information: Margarita V. Kruchinina, e-mail: kruchmargo@yandex.ru.
Financial Disclosure: the research was carried out within the state assignment (them No. FWNR-2022-0024, FWNR-2023-0003). No authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 10.04.2023.
Revised 04.05.2023.
Accepted 31.05.2023.
Информация с rmj.ru