Содержание статьи
Влияние асфиксии на фибринолиз недоношенного новорожденного
А. В. Катюхина
ГБУЗ ГКБ № 24 ДЗМ, Москва
Асфиксия новорожденного (лат. asphyxia) — удушье, патологический
процесс, возникающий в связи с нарушением газового обмена новорожденного,
сопровождающийся недостатком кислорода в крови и тканях и накоплением
углекислоты в организме.
Асфиксия является следствием многих видов акушерской патологии и различных
заболеваний материнского организма и плода [1].
Асфиксии новорожденных делят по происхождению на первичные, или
внутриутробные, и вторичные, или внеутробные (приобретенные), и по степени
тяжести (легкая, среднетяжелая и тяжелая). После рождения оценивается состояние
ребенка на 1-й и 5-й минуте по шкале Апгар (1–9 баллов). Асфиксией легкой
степени считают 7–8-9 баллов, среднетяжелой — 4–6 балла и тяжелой — 1–3 балла.
Причинами первичной асфиксии являются острая и хроническая внутриутробная
гипоксия плода, внутричерепная травма, иммунологическая несовместимость крови
матери и плода, внутриутробная инфекция, полная или частичная закупорка
дыхательных путей плода или новорожденного слизью, околоплодными водами
(аспирационная асфиксия), пороки развития плода. Возникновению асфиксии
способствуют экстрагенитальные заболевания беременной (сердечно-сосудистые,
особенно в стадии декомпенсации, тяжелые заболевания легких, выраженная анемия,
сахарный диабет, тиреотоксикоз, инфекционные болезни и др.), поздние токсикозы
беременных, преждевременная отслойка плаценты, патология пуповины, плодных
оболочек и плаценты, осложнения в родах (несвоевременное излитие околоплодных
вод, аномалии родовой деятельности, несоответствие размеров таза роженицы и
головки плода, неправильные вставления головки плода и др.).
Наиболее частой причиной вторичных асфиксий у новорожденных первых дней жизни
являются так называемые пневмопатии (полисегментарные и рассеянные ателектазы,
гиалиновые мембраны, отечно-геморрагический синдром, массивные кровоизлияния в
легкие и др.), которые формируются во внутриутробном периоде или во время родов
и сопровождаются развитием синдрома дыхательных расстройств (СДР). Кроме
пневмопатий, СДР может быть обусловлен внутричерепными кровоизлияниями,
внутри—утробной инфекцией и др. [2].
Под асфиксией новорожденного понимают такое состояние, когда после его
рождения дыхание не появляется или выражается в отдельных, нерегулярных, чаще
всего судорожных или поверхностных дыхательных движениях при наличии сердечной
деятельности. Асфиксия является одной из ведущих причин мертворождаемости.
Кратковременная или умеренная гипоксия и гипоксемия вызывают включение
компенсаторных адаптационных механизмов плода с активацией симпатико-адреналовой
системы гормонами коры надпочечников и цитокинами. При этом увеличивается число
циркулирующих эритроцитов, учащается сердечный ритм, возможно некоторое
повышение систолического артериального давления без увеличения сердечного
выброса.
Продолжающаяся гипоксия, гипоксемия, сопровождается снижением рО2
ниже 40 мм рт. ст. и способствует включению энергетически невыгодного пути
обмена углеводов — анаэробного гликолиза. Накапливаются продукты нарушенного
метаболизма, оказывая повреждающее действие на органы и ткани.
Сердечно-сосудистая система отвечает на данное состояние перераспределением
циркулирующей крови с преимущественным кровоснабжением жизненно важных органов
(мозг, сердце, надпочечники, диафрагма), что приводит к кислородному голоданию
кожи, легких, кишечника, мышечной ткани, почек и других органов. Сохранение
фетального состояния легких является причиной шунтирования крови справа налево,
которое приводит к перегрузке правых отделов сердца давлением, а левых —
объемом, что способствует развитию сердечной недостаточности, усилению
дыхательной и циркуляторной гипоксии. Централизация кровообращения, активация
анаэробного гликолиза с накоплением лактата способствует развитию
метаболического ацидоза.
В случае тяжелой и (или) продолжающейся гипоксии возникает срыв механизмов
компенсации: гемодинамики, функции коры надпочечников, что, наряду с
брадикардией и снижением минутного кровообращения, приводит к артериальной
гипотензии вплоть до шока. Нарастание метаболического ацидоза способствует
активации плазменных протеаз, провоспалительных факторов, что ведет к
повреждению клеточных мембран, развитию дисэлектролитемии.
Повышение проницаемости сосудистой стенки приводит к сладжированию
(склеиванию) эритроцитов, образованию внутрисосудистых тромбов и кровоизлияниям.
Выход жидкой части крови из сосудистого русла способствует развитию отека
головного мозга и гиповолемии. Повреждение клеточных мембран усугубляет
поражение центральной нервной системы (ЦНС), сердечно-сосудистой системы, почек,
надпочечников с развитием полиорганной недостаточности. Указанные факторы
приводят к изменению коагуляционного и тромбоцитарного звена гемостаза.
В основе гипоксически-ишемического поражения головного мозга лежат
цереброваскулярные расстройства и нарушения механизма ауторегуляции мозгового
кровообращения, наступающие при дефиците кислорода.
Основные патогенетические механизмы формирования клинических проявлений
гипоксии новорожденных, родившихся в асфиксии, со стороны системы гемостаза и
эритропоэза — тромбоцитопения, витамин-К-дефицит, синдром диссеминированного
внутрисосудистого свертывания.
Асфиксия на фоне хронической антенатальной гипоксии развивается на фоне
антенатальной патологии: пневмопатии, энцефалопатии, незрелости ферментативных
систем печени, низких резервов надпочечников и щитовидной железы, а также
патологического ацидоза и вторичного иммунодефицитного состояния. Основным
метаболическим компонентом такой гипоксии является сочетание гипоксемии,
гиперкапнии и метаболического ацидоза с момента рождения. Ацидоз рано вызывает
повреждение клеточных мембран с развитием гемодинамических, гемостатических
нарушений и транскапиллярного обмена, что определяет механизмы развития
дыхательной недостаточности (ДН), правожелудочковой сердечной недостаточности,
коллапса с падением артериального давления (АД), гиповолемии на фоне
недостаточности симпато-адреналовой системы, ишемии миокарда и фазовых
расстройств гемостаза, что еще больше ухудшает микроциркуляцию. Важнейшая роль
нарушений гемостаза в общей патологии человека определяется не только частотой,
разнообразием геморрагических и тромбоэмболических заболеваний и синдромов, но и
является существенным звеном патогенеза других заболеваний —
инфекционно-септических, иммунных [3] и т. д. Целью данной работы было изучение
показателей фибринолиза у недоношенных новорожденных детей с разной оценкой по
шкале Апгар и разработать методы профилактики развития геморрагического
синдрома.
Материалы и методы исследования
На базе педиатрического отделения для недоношенных детей ГБУЗ ГКБ № 24 ДЗМ
(Москва) проводилось изучение показателей фибринолиза у новорожденных детей с
различной оценкой по шкале Апгар. В исследовании приняли участие 60
новорожденных детей различного срока гестации, веса и половой принадлежности в
возрасте до одного месяца жизни. Гестационный возраст детей был представлен
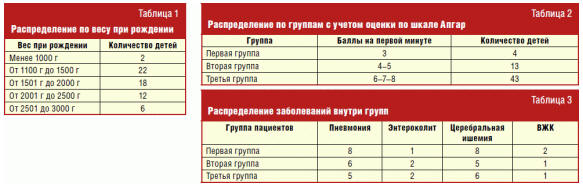
27–36 неделями. Вес обследуемых детей колебался в пределах 990–3000 г (табл. 1).
Все дети были разделены на три группы по интервалу оценки по шкале Апгар без
учета веса и срока гестации (табл. 2).
При первичном осмотре изучался анамнез матерей, течения беременности и родов.
Клинический осмотр новорожденных проводился на 1-й, 2-й, 3-й и 4-й неделе жизни.
Оценивалось физическое развитие новорожденных по центильным таблицам. Особенное
внимание уделялось выявлению признаков геморрагического синдрома и тромбоза.
Основными диагнозами, с которыми наблюдались дети, были: внутриутробная
пневмония, энтероколит, церебральная ишемия, внутрижелудочковое кровоизлияние.
Лабораторное изучение показателей фибринолиза проводилось без учета
заболеваний и получаемого лечения. Взятие крови для исследования производился на
1-й, 2-й, 3-й и 4-й неделе жизни. Исследование препаратов крови проводилось в
лаборатории ГБУЗ ГКБ № 24 ДЗМ и лаборатории Научного центра сердечно-сосудистой
хирургии им. А. Н. Бакулева РАМН г. Москвы на аппарате АСL-9000 с использованием
хромогенного субстрата стрептокиназы [4, 5].
Результаты и обсуждение
Изучив материнский анамнез, было выявлено, что 70% женщин имели отягощенный
соматический и акушерско-гинекологический анамнез, часть из них имели обострения
хронических болезней в период беременности. Большинство детей рождены от первой
или второй беременности и первых родов. Оценивая физическое развитие детей при
рождении, выявлено, что 12% новорожденных имеют задержку внутриутробного
развития. В ходе клинического осмотра оценивалось состояние детей — наличие
признаков геморрагического синдрома или тромбоза, выраженность ДН, уровень
мышечного тонуса и рефлексов, менингеальные симптомы. В первой группе признаки
геморрагического синдрома в виде желудочно-кишечного кровотечения отмечались у
одного ребенка на 2-й неделе жизни, во второй группе у двух детей на 1-й неделе
жизни и в третьей группе также у двух детей на 2-й неделе жизни. При
рентгенографическом исследовании выявлены признаки энтероколита. Признаков
тромбоза выявлено не было ни у одного ребенка. Проявления пневмонии отмечались у
8 детей первой группы в течение всего периода обследования, во второй группе у 6
детей до 3-й и 4-й недели жизни и в третьей группе у 5 новорожденных до 2-й и
3-й недели жизни в виде ДН различной степени выраженности и рентгенологической
картины пневмонии. При нейросонографическом исследовании детей первой группы
выявлены изменения ишемического характера у 8 детей и геморрагического (внутрижелудочковое
кровоизлияние (ВЖК)) у 2 детей. Во второй группе ишемические изменения отмечены
у 5 детей, ВЖК у 1 ребенка, а в третьей группе у 6 и 1 ребенка соответственно.
Распределение заболеваний по группам приведено в табл. 3.
Взятие крови для лабораторного анализа показателей фибринолиза проводился
4-кратно, на 1-й, 2-й, 3-й и 4-й неделе жизни.
Диапазон полученных данных с учетом оценки по шкале Апгар представлен в табл.
4.
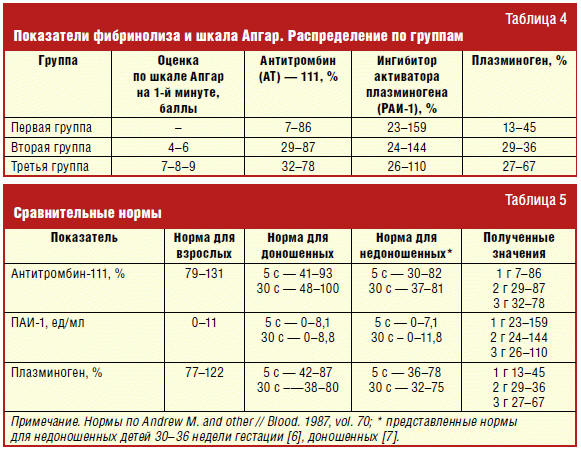
В данной таблице приведены результаты показателей фибринолиза, от
минимального до максимального, полученные в ходе исследования. Сравнив средние
показатели АТ-111, видим, что практически одинаковые значения представлены во
второй и третьей группе, низкие в первой группе. Что касается плазминогена, то
наибольшие значения в третьей группе, минимальные во второй группе. Максимальный
уровень РАИ-1 наблюдается в первой группе, а вторая и третья группы имеют почти
одинаковые значения.
Чтобы оценить полученные данные относительно известных норм, обратимся к
табл. 5.
При сравнении полученных данных с нормами для недоношенных детей видим, что
уровень АТ-111 у обследуемых детей соответствует таковому во второй и третьей
группе по данным Andrew. У недоношенных детей отмечается депрессия
физиологических антикоагулянтов, особенно выраженная в первые сутки жизни [8].
Значения РАИ-1 имеют достаточно большой диапазон значений по сравнению с нормами
у недоношенных. В каждой группе получены значения как меньше нормы, так и
больше. Что касается плазминогена, то имеется тенденция к его снижению. Согласно
данной таблице, приведены нормы для недоношенных детей 30–36 недели гестации, в
то время как в исследовании участвовали дети с 27-й по 36,5-ю недели гестации.
Из методов параметрической статистики применялся критерий t Стьюдента для оценки
количественных непрерывных величин при нормальном распределении. Значение р
считалось достоверным при α ≤ 0,05. Для оценки корреляционной взаимосвязи
применяли метод Спирмена [9].
Выводы
Сравнивая результаты показателей фибринолиза у детей трех групп, можем
выделить особенности данных показателей при асфиксии и оценить влияние асфиксии
на фибринолитическую систему недоношенного новорожденного.
- Низкие значения РАИ-1 и АТ-111 наблюдаются у детей с геморрагическим
синдромом (желудочно-кишечное кровотечение и ВЖК) как проявление
гипокоагуляции. Данные изменения больше характерны для недоношенных из первой
группы, то есть рожденных в асфиксии тяжелой степени. - Имея данные о депрессии фибринолитической системы у недоношенных
новорожденных относительно доношенных, следует ожидать более частого
проявления геморрагического синдрома. Однако в ходе исследования данных,
подтверждающих это высказывание, не получено. Из всех обследованных детей (30
человек) только у 16,7% (5 человек) были проявления гипокоагуляции. - Относительно низкие значения плазминогена и встречающиеся в этот же
возрастной период высокие цифры РАИ-1 во всех группах свидетельствует о
периодах гиперкоагуляции, сменяющих гипокоагуляцию, но неподтвержденных
клинически. - У детей, родившихся в асфиксии тяжелой степени, получены более низкие
значения плазминогена и АТ-111, чем при среднетяжелой и легкой степени.
Фибринолиз идет быстрее, чем выше локальная концентрация плазминогена в
сгустках [10]. - Уровень РАИ-1 во всех группах имеет тенденцию к возрастанию от первой
недели к месяцу жизни.
Учитывая вышеизложенное, можно сделать заключение о более выраженном
ингибирующем влиянии асфиксии тяжелой степени, гипоксии на фибринолитическую
систему недоношенных новорожденных в отличие от доношенных детей. Однако только
имея данные особенности, касающиеся многих систем организма, недоношенный
ребенок имеет больше возможности приспособиться к изменяющимся условиям среды и
легче пережить период адаптации.
Литература
-
Рогалёва Т. Е. Состояние иммунитета и гемостаза при перинатальных
поражениях ЦНС у новорожденных детей от матерей с гестозами. Дис… к.м.н.
Чита, 2009. С. 11–16. -
Любименко В. А., Пальчик А. Б., Шабалов Н. П., Ярославский В. К.
Асфиксия новорожденных. 3-е изд-е. 2003. С. 9, 12, 15. -
Дементьева И. И., Чарная М. А., Морозов Ю. А. Патология системы
гемостаза. М.: ГЕОТАР- Медиа, 2011. С. 25, 27. -
Баркаган З. С. Диагностики и контролируемая терапия нарушений
гемостаза. М.: Ньюдиамед, 2008. С. 158–159, 277–278, 282. -
Баркаган З. С, Момот А. П. Диагностика и контролируемая терапия
нарушений гемостаза. М.: Ньюдиамед, 2011. С. 13. -
Румянцев А. Г., Самочатова Е. В., Коколина В. Ф. Практическое
руководство по детским болезням. Гематология/онкология детского возраста. М.:
Медпрактика-М, 2004. С. 312, 318. -
Доскин В. А., Келлер Х., Мураенко Н. М., Тонкова-Ямпольская Р. В.
Морфофункциональные константы детского организма. М.: Медицина, 1997. С 226. -
Володин Н. Н., Мухина Ю. Г., Чубарова А. И. Неонатология. Т. 1.
М.: Династия, 2011. С. 159. -
Гореева Н. М., Демидова Л. Н., Орехов С. А. Статистика. М.: Эксмо,
2010. -
Булатов В. П., Черезова И. П., Макарова Т. П., Шаммасов Р. З.
Гематология детского возраста. Ростов-на-Дону: Феникс. Казань: Казанский
государственный медицинский университет, 2006. С. 37–39.
Статья опубликована в журнале
Лечащий Врач
материал MedLinks.ru







