Содержание статьи
Введение
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) является одной из наиболее часто встречаемых патологий в практике терапевта и гастроэнтеролога. По разным данным, показатель распространенности заболевания в мире варьирует от 8,8% до 33,1% и продолжает расти [1, 2]. ГЭРБ определяется как хроническое рецидивирующее заболевание, обусловленное нарушением моторно-эвакуаторной функции органов гастроэзофагеальной зоны и характеризующееся регулярно повторяющимся забросом в пищевод желудочного и, в ряде случаев, дуоденального содержимого, что приводит к появлению клинических симптомов, ухудшающих качество жизни пациентов, к повреждению слизистой оболочки дистального отдела пищевода с развитием в нем дистрофических изменений неороговевающего многослойного плоского эпителия, катарального или эрозивно-язвенного эзофагита (рефлюкс-эзофагита), а у части больных — цилиндроклеточной метаплазии [3, 4]. Одним из актуальных вопросов представляется курация пациентов с ГЭРБ, имеющих внепищеводные (атипичные) симптомы заболевания: кардиальные, легочные, оториноларингологические и стоматологические [4]. Согласно Монреальской классификации симптомов ГЭРБ внепищеводные проявления ГЭРБ подразделяются на две группы: к первой группе относят симптомы, связь которых с ГЭРБ основана на убедительных клинических доказательствах (хронический кашель, связанный с рефлюксом, хронический ларингит, бронхиальная астма и эрозии эмали зубов), ко второй группе относят проявления, связь которых с ГЭРБ лишь предполагается (фарингит, синусит, легочный фиброз, средний отит) [4]. И если сегодня механизмы формирования и методы купирования пищеводных симптомов, к которым относят изжогу, отрыжку, срыгивание и одинофагию, широко известны и не вызывают особых затруднений у клиницистов, то поиск подходов к ведению пациентов с внепищеводными проявлениями ГЭРБ сохраняет свою актуальность [3, 4].
Настоящая публикация подготовлена с целью систематизации данных о распространенности и характере внепищеводных симптомов ГЭРБ, а также об эффективности и безопасности терапии эзофагопротектором больных ГЭРБ с внепищеводными проявлениями.
Внепищеводные проявления ГЭРБ: встречаемость, механизмы развития и клинические симптомы
Высокая распространенность атипичных симптомов ГЭРБ установлена в многоцентровом проспективном исследовании с участием 6215 больных ГЭРБ. Согласно полученным данным внепищеводные проявления встречаются у каждого третьего пациента с ГЭРБ и возникают чаще у лиц с эрозивным эзофагитом (34,9%), чем у больных неэрозивной рефлюксной болезнью (30,5%) [5]. Кроме того, наличие и выраженность внепищеводных симптомов ГЭРБ могут быть ассоциированы с длительностью течения заболевания [5]. Наиболее часто встречающимся атипичным проявлением является боль в груди, не связанная с заболеваниями сердечно-сосудистой системы (14–20% случаев). Распространенность ларингеальных симптомов достигает 10% случаев ГЭРБ [6, 7].
В норме нижний пищеводный сфинктер предотвращает поступление желудочного содержимого в полость пищевода, а верхний пищеводный сфинктер защищает от гастроэзофагофарингеального рефлюкса [8]. Основные защитные гликопротеины, муцины, поступают в пищевод со слюной и секретируются собственными железами пищевода, что позволяет нейтрализовать агрессивный желудочный рефлюктат в случае его поступления в просвет пищевода. Формирование атипичных симптомов ГЭРБ связывают с двумя основными механизмами. Во-первых, внепищеводные симптомы ГЭРБ, прежде всего ларингофарингеальные, возникают в связи с ларингофарингеальным рефлюксом (ЛФР) — аспирацией содержимого желудка и повреждением слизистой оболочки верхних дыхательных путей (гортань, горло, носоглотка, пазухи, среднее ухо). Респираторный эпителий менее устойчив к агрессивным молекулам желудочного рефлюктата, чем эпителий пищевода, и даже незначительный ЛФР может вызвать ларингеальный мукозит, сохраняющийся до нескольких недель. Аспирация желудочного рефлюктата наиболее часто происходит в ночное время, когда пищеводные сфинктеры расслаблены [9]. Таким образом, аспирация кислого или желчного желудочного содержимого способствует прямому повреждению эпителия гортани, трахеи, бронхов и легочной ткани, что создает условия для формирования хронического воспаления и раздражения нервных окончаний в зоне повреждения рефлюктатом [10]. Во-вторых, формирование внепищеводных симптомов может быть связано с общей иннервацией пищевода, органов дыхательной и сердечно-сосудистой системы вагусом с участием вагусной рефлекторной дуги [10]. Воздействие соляной кислоты и, при дуоденогастральном рефлюксе, желчных солей стимулирует выброс эпителиоцитами провоспалительных цитокинов: интерлейкинов-1, -6, -8, -10 и фактора некроза опухолей α, привлекая Т-клетки и нейтрофилы в поврежденную ткань. Провоспалительные цитокины усугубляют повреждение эпителиоцитов и стимулируют выработку мезенхимальными и эндотелиальными клетками еще большего количества медиаторов воспаления с формированием порочного круга [11, 12]. Кроме того, деструкция комплексов апикального соединения, снижение продукции белков плотных контактов наряду с расширением межклеточных промежутков у пациентов с ГЭРБ становятся дополнительными факторами, усиливающими раздражение присутствующих в стенке пищевода афферентных нервных волокон [11, 13].
Поступление кислого желудочного содержимого в ротовую полость приводит к снижению pH слюны, создавая условия для очаговой деминерализации эмали зубов с образованием кариеса, эрозий эмали и дентина, а также к нарушению состава оральной микробиоты [9, 10]. Наиболее распространенными стоматологическими поражениями при ГЭРБ являются поражения мягких тканей (афтозный стоматит, изменение формы и чувствительности сосочков языка, чувство жжения языка), некариозные поражения твердых тканей зубов (эрозии эмали) и кариес [14].
Симптоматика поражения органов дыхания при ГЭРБ может включать утреннее нарушение голоса, кашель после еды и по утрам, усиливающийся при смене положения тела, сухость в горле, ощущение инородного тела или кома в горле, ощущение стекания выделений по задней стенке горла, боль в горле, неприятный запах изо рта, удушье, одышку с ночными обострениями [15]. Заболевание часто осложняется воспалением верхних и нижних дыхательных путей (фарингит, ларингит, синусит, бронхит, идиопатический легочный фиброз, аспирационная пневмония), экссудативным отитом, астматическими симптомами, возникающими преимущественно в ночное время [6]. У каждого десятого больного может быть выявлена охрип-лость и/или першение в горле [5, 7].
По нашим наблюдениям, такое состояние вызвано изменениями в области верхнего отдела гортани — от входа до вестибулярных складок, наличием вязкой, практически неотхаркиваемой слизи в грушевидных карманах и межчерпаловидном пространстве, а также «налипанием» вязкого субстрата на голосовых складках, связанным с ЛФР, что вызывает у пациентов постоянное желание «прочистить горло».
Коррекция внепищеводных проявлений ГЭРБ: что известно и что нового
С целью купирования внепищеводных симптомов ГЭРБ, помимо модификации образа жизни, включая поднятие головного конца кровати, отказ от курения и коррекцию рациона питания (уменьшение потребления жиров, шоколада, алкоголя, цитрусовых, томатов, кофе и чая, избегание больших порций и прием пищи не позднее чем за 3 ч до сна), больным рекомендуется прием препаратов первого выбора — ингибиторов протонной помпы (ИПП) [16]. Известно, что эффективность контроля изжоги и других пищеводных симптомов ГЭРБ и скорость заживляющего действия на слизистую оболочку пищевода у ИПП выше, чем у иных групп препаратов [17, 18]. В то же время лишь 80% больных ГЭРБ, получающих монотерапию ИПП, отмечают снижение выраженности клинических симптомов заболевания, в 10–40% случаев наблюдается неполный ответ на прием стандартной дозы ИПП [19].
Эффективность применения монотерапии ИПП в лечении внепищеводных проявлений ГЭРБ остается предметом дискуссий. В литературе представлены исследования, указывающие на невысокую эффективность применения монотерапии ИПП для лечения хронического кашля, ассоциированного с рефлюксом [20]. В рандомизированном контролируемом исследовании (РКИ) с участием 40 пациентов с хроническим кашлем, связанным с ГЭРБ, не установлено различий в улучшении качества жизни и купировании кашля между приемом плацебо и приемом 40 мг эзомепразола дважды в день в течение 12 нед. [21]. В исследовании с участием 30 таких пациентов установлено снижение выраженности симптомов астмы, улучшение пиковой скорости выдоха после 3-месячной непрерывной кислотосупрессивной терапии омепразолом [22]. С другой стороны, в систематическом обзоре рандомизированных плацебо-контролируемых исследований, включившем 6 исследований с применением ИПП у пациентов с рефлюкс-ассоциированной астмой, не обнаружено значимого влияния на функции внешнего дыхания и контроль симптомов астмы [23]. В метаанализе исследований с участием больных рефлюкс-ассоциированной астмой показано статистически значимое повышение пиковой скорости выдоха на фоне приема ИПП, однако существенного уменьшения выраженности симптомов астмы не установлено [24]. Метаанализ 13 РКИ с участием 831 пациента, страдающего ЛФР, продемонстрировал более выраженное клиническое улучшение в ответ на терапию ИПП дважды в день в течение 3–6 мес. по сравнению с плацебо, однако частота ответа на лечение при этом существенно не различалась [25]. Еще один метаанализ 8 контролируемых исследований, включивший 344 пациента с ЛФР, продемонстрировал отсутствие значимых клинических улучшений у больных при назначении терапии ИПП в сравнении с плацебо [26].
Терапия стоматологических поражений при ГЭРБ может включать в себя прием антацидов сразу после появления изжоги или ощущения кислотного рефлюкса в ротоглотке, полоскание рта ополаскивателем с нейтральным рН, отказ от чистки зубов сразу после эпизодов рефлюкса, применение фторсодержащего геля сразу после рефлюкса, стимуляцию слюноотделения с помощью жевательной резинки без сахара [27]. Исследования, посвященные влиянию кислотосупрессивной терапии на стоматологические поражения, ассоциированные с ГЭРБ, в настоящее время отсутствуют.
Пациентам с внепищеводными симптомами ГЭРБ, которые не отвечают на длительную терапию ИПП, может быть рекомендовано хирургическое вмешательство, в том числе лапароскопическая фундопликация по Ниссену [3, 28]. В мировой литературе представлены исследования, демонстрирующие лишь ограниченную эффективность оперативных вмешательств с целью купирования внепищеводных симптомов ГЭРБ. Так, хирургическое лечение ГЭРБ может быть эффективным лишь у отдельных пациентов, преимущественно со слабощелочным рефлюксом [29]. Ретроспективное когортное исследование с участием 115 больных, результаты которого были опубликованы в 2017 г., продемонстрировало меньшую эффективность хирургических вмешательств у пациентов с внепищеводными симптомами ГЭРБ, чем у больных с типичными симптомами. Кроме того, эффективность контроля симптомов после хирургического вмешательства коррелировала с выраженностью ответа на терапию ИПП [30]. В другом исследовании авторы заявили об отсутствии выраженного эффекта в отношении симптомов ЛФР после проведения хирургической фундопликации по Ниссену [31]. В то же время отдельные публикации демонстрируют положительное влияние хирургического вмешательства на внепищеводные симптомы. Так, в исследовании с участием 299 человек, страдающих хроническим кашлем, ассоциированным с ГЭРБ, описано положительное влияние оперативного лечения на внепищеводные проявления заболевания, особенно у лиц с тяжелыми симптомами [32]. В другом исследовании после оперативного вмешательства установлено улучшение течения бронхиальной астмы, связанной с ГЭРБ: снизились частота и тяжесть приступов, уменьшилась потребность в препаратах [23]. Таким образом, эффективность оперативного вмешательства с целью купирования стойких внепищеводных симптомов ГЭРБ остается дискутабельной.
Причинами рефрактерности к монотерапии ИПП могут быть повышение частоты спонтанных релаксаций нижнего пищеводного сфинктера, наличие грыжи пищеводного отверстия диафрагмы, недостаточная приверженность приему ИПП, наличие дуоденогастрального рефлюкса, а также снижение резистентности слизистой оболочки пищевода [33]. Кроме того, соляная кислота обладает не самым высоким повреждающим потенциалом. Более выраженное деструктивное действие на эпителий пищевода оказывает желудочный рефлюктат с неконъюгированными желчными кислотами при кислом рН. Отмечено, что симптомы у больных с ЛФР в большей степени обусловлены персистенцией слабокислых и слабощелочных, нежели кислых, высоких рефлюксов [34, 35]. Таким образом, наличие сопутствующего дуоденогастрального рефлюкса значимо повышает риск развития не только пищевода Барретта, дисплазии и неоплазии эпителия пищевода, но и внепищеводных симптомов ГЭРБ [36, 37].
Более быстрое достижение клинической ремиссии внепищеводных симптомов ГЭРБ может быть получено при назначении дополнительных препаратов к терапии ИПП [38, 39]. Так, альгинаты позволяют нейтрализовать «кислотный карман» при грыже пищеводного отверстия диафрагмы, а прокинетики помогают восстановить моторику верхних отделов пищеварительного тракта [39–41].
К прорывам в лечении рефлюкс-эзофагита следует отнести и появление нового класса средств терапии ГЭРБ [33]. Группа эзофагопротекторов относится к принципиально новому классу препаратов, доступному клиницистам в лечении ГЭРБ, и сегодня представлена медицинским изделием Альфазокс [33]. Оно состоит из смеси низкомолекулярной гиалуроновой кислоты и низкомолекулярного хондроитина сульфата, растворенных в биоадгезивном носителе (полоксамер 407). Вместе компоненты образуют макромолекулярный комплекс, который способствует более быстрому восстановлению слизистой оболочки пищевода, выступая в роли механического барьера, равномерно обволакивая стенку пищевода и препятствуя контакту с повреждающими молекулами рефлюктата [33, 42, 43]. Первый компонент, низкомолекулярная гиалуроновая кислота, является многофункциональным высокомолекулярным гликозаминогликаном, который присутствует в большинстве внеклеточных матриксов. Гидрофильные и гидродинамические свойства гиалуроновой кислоты обусловливают ее участие в репарации, регенерации, морфогенезе и ряде иных физиологических молекулярно-клеточных процессов, протекающих в слизистой оболочке. Кроме того, гиалуроновая кислота стимулирует рост кровеносных сосудов за счет увеличения скорости пролиферации и миграции клеток эндотелия [44, 45]. Описана способность гиалуроновой кислоты стимулировать продукцию белков плотных контактов и, следовательно, восстанавливать барьерную функцию эпителия слизистой оболочки пищевода [46]. Второй компонент Альфазокса, хондроитина сульфат, является естественным гликозаминогликаном, который входит в состав внеклеточного матрикса тканей хряща, кожи, кровеносных сосудов, связок и сухожилий [47]. Хондроитина сульфат участвует в процессах пролиферации, дифференциации и миграции клеток, морфогенезе тканей, органогенезе [48]. Описаны иммуномодулирующие, противовоспалительные, антиоксидантные свойства хондроитина сульфата, а также его способность избирательно связываться с биоактивными молекулами, например пепсином, и снижать его пептическую активность [47, 49]. Третий компонент, биоадгезивный носитель Полоксамер 407, играет роль носителя, который используется для фиксации активных веществ на слизистой оболочке пищевода. Полоксамер 407 обеспечивает пролонгированное действие компонентов медицинского изделия [50].
Клиническая эффективность эзофагопротектора в лечении ГЭРБ была изучена в серии клинических проспективных плацебо-контролируемых исследований [51–53]. Показана его высокая эффективность в снижении выраженности «классических» симптомов ГЭРБ, в том числе неэрозивной формы, и повышении интенсивности восстановления слизистой оболочки пищевода.
Ранее авторами настоящей публикации выполнено открытое рандомизированное проспективное исследование с участием 60 пациентов, страдающих эрозивным эзофагитом (степени С, D по Лос-Анджелесской классификации) [54, 55]. Было продемонстрировано более эффективное купирование симптомов ГЭРБ, а также определена тенденция к более выраженному улучшению качества жизни пациентов при применении комбинированной терапии ИПП и эзофагопротектором в сравнении с монотерапией ИПП. Через 4 нед. от начала лечения у больных, получавших комбинированную терапию, была отмечена более выраженная редукция макроскопических признаков эрозивного эзофагита. В основной группе у 3 (10%) пациентов была достигнута эндоскопическая ремиссия, а у 27 (90%) зафиксировано уменьшение тяжести рефлюкс-эзофагита до степени А–В. В то же время в группе больных, принимавших ИПП, случаев эндоскопической ремиссии не зафиксировано, а уменьшение тяжести рефлюкс-эзофагита до степени А–В описано у 24 (80%) человек. Согласно данным гистологического и иммуногистохимического исследования биоптатов назначение комбинированной терапии позволило достичь более выраженной редукции гистологических изменений эзофагита, существенно повысить экспрессию белков плотных контактов (клаудина-1, -4) слизистой оболочки пищевода и снизить экспрессию маркера клеточной пролиферации Ki-67 [54, 55]. Выраженность экспрессии клаудина-1 после лечения представлена на рисунке.
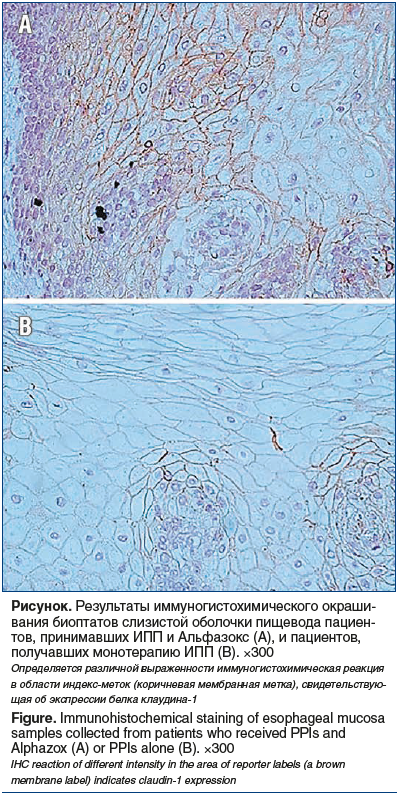
Эффективность применения гиалуроновой кислоты в комплексе с хондроитина сульфатом, растворенных в биополимерном носителе, в лечении больных с внепищеводными симптомами ГЭРБ продемонстрирована J. Chmielecka-Rutkowska et al. из Лодзинского медицинского университета в исследовании с участием пациентов с установленным ЛФР. Прием эзофагопротектора в течение 14 дней позволил значимо снизить выраженность симптомов ЛФР, способствовал существенному уменьшению или устранению морфологических изменений в гортани [56]. Эффективность применения эзофагопротектора с целью купирования ларингофарингеальных симптомов и редукции морфологических изменений слизистой оболочки пищевода и гортани у пациентов с ГЭРБ также была продемонстрирована в серии клинических наблюдений [6].
В целом использование эзофагопротектора в сочетании с ИПП позволяет достигать клинической, эндоскопической и гистологической ремиссии у пациентов с ГЭРБ чаще и в более краткие сроки, а также эффективно купирует внепищеводные симптомы ГЭРБ у пациентов с ЛФР. Действие Альфазокса реализуется благодаря его способности обволакивать и защищать область ротоглотки и пищевода от повреждающего действия кислого или желчного рефлюкса, гидратации слизистой оболочки и прямому заживляющему действию, что обеспечивает более быстрое и полное восстановление структуры эпителия пищевода и гортани [54–56].
Заключение
Таким образом, сегодня в вопросах курации больных ГЭРБ с внепищеводными симптомами предметом обсуждения остаются не только трудности диагностики, но и вопросы подбора эффективной терапии, позволяющей в наиболее короткие сроки купировать внепищеводные симптомы ГЭРБ и достигать стойкой ремиссии. Применение эзофагопротектора у таких больных может обеспечить механическую защиту слизистой оболочки гортани и пищевода за счет повышения интенсивности восстановления ее молекулярно-клеточной структуры и нормализации барьерной функции, что также будет способствовать купированию симптомов и повышению качества жизни больных с внепищеводными проявлениями ГЭРБ.
Сведения об авторах:
Лаптева Ирина Вячеславовна — к.м.н., заведующая терапевтическим отделением № 1, руководитель гастроэнтерологического центра БУЗОО «ГБ № 3»; 644029, Россия, г. Омск, ул. Энергетиков, д. 19.
Федорин Максим Михайлович — ординатор кафедры факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-0238-4664.
Нестерова Климентина Ивановна — д.м.н., доцент, профессор кафедры оториноларингологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-9793-7179.
Ливзан Мария Анатольевна — д.м.н., профессор, член-корреспондент РАН, заведующая кафедрой факультетской терапии и гастроэнтерологии, ректор ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-6581-7017.
Мозговой Сергей Игоревич — д.м.н., доцент, профессор кафедры патологической анатомии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-6733-5572.
Контактная информация: Федорин Максим Михайлович, e-mail: mail.maxim.f@gmail.com.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 22.03.2022.
Поступила после рецензирования 14.04.2022.
Принята в печать 13.05.2022.
About the authors:
Irina V. Lapteva — C. Sc. (Med.), Head of the Therapeutic Department No. 1, Head of the Gastroenterological Center, City Hospital No. 3; 19, Energetikov str., Omsk, 644029, Russian Federation.
Maksim M. Fedorin — resident of the Department of Faculty Therapy and Gastroenterology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-0238-4664.
Klimentina I. Nesterova — Dr. Sc. (Med.), Associate Professor, professor of the Department of Otorhinolaryngology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-9793-7179.
Maria A. Livzan — Dr. Sc. (Med.), Professor, Corresponding Member of the RAS, Head of the Department of Faculty Therapy and Gastroenterology, Chancellor Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-6581-7017.
Sergey I. Mozgovoy — Dr. Sc. (Med.), Associate Professor, professor of the Department of Pathological Anatomy, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-6733-5572.
Contact information: Maksim M. Fedorin, e-mail: mail.maxim.f@gmail.com.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 22.03.2022.
Revised 14.04.2022.
Accepted 13.05.2022.
.
Информация с rmj.ru