Содержание статьи
Введение
Остеоартрит (ОА) является самой распространенной формой поражения суставов и ведущей причиной инвалидизации пациентов [1]. Этиопатогенез данного заболевания до сих пор не установлен, однако все чаще оно рассматривается не как дегенеративное, а как системное воспалительное заболевание, при котором повышенные нагрузки на сустав считаются лишь одним из факторов риска [1, 2]. Данные современных исследований свидетельствуют о том, что аномальное ремоделирование тканей сустава определяется провоспалительными медиаторами, такими как интерлейкин (ИЛ) 1β, ИЛ-6, ИЛ-8, ИЛ-17, фактор некроза опухоли-α (ФНО-α), онкостатин, оксид азота (NO) [3]. Эти цитокины стимулируют деградацию матрикса хряща, продукцию хемокинов, что приводит к изменениям клеточного фенотипа и формированию персистирующего воспаления в тканях сустава [3, 4], а морфологические изменения синовии при ОА сопоставимы с картиной синовита при хроническом артрите. При этом каскад патофизиологических реакций с повышенной активностью катаболических ферментов (матриксной металлопротеиназы (MMП) 1, MMП-13 и др.) и одновременным снижением продукции коллагена II типа и аггрекана обусловливает аутофагию, ускоренное старение и апоптоз [5]. Это подтвержается данными исследований, в которых показана связь олигомерного матриксного белка хряща (cartilage oligomeric matrix protein, СОМР) с показателями воспаления при ОА: высокочувствительным С-реактивным белком (СРБ), наличием и выраженностью синовита [6, 7]. СОМР — это продукт распада хряща, его уровень увеличивается с тяжестью ОА коленного сустава, а содержание в сыворотке крови может быть индикатором ранней деградации хрящевой ткани [8].
В целом ОА сегодня рассматривают как системный процесс, имеющий общие патогенетические моменты с метаболическими и сосудистыми заболеваниями [9–13]. Так, инсулинорезистентность и гипергликемия способствуют прогрессированию ОА, поскольку продукты обмена глюкозы негативно влияют на сосудистую стенку, приводят к микро- и макроангиопатии, усугубляя ишемию. Это сопровождается увеличением синтеза MMП-13, MMП-1 и провоспалительных цитокинов (ФНО-α, ИЛ-1β, ИЛ-6, ИЛ-8,
ИЛ-18) [10–12]. Подобные изменения происходят и при артериальной гипертензии (АГ), которая способствует субхондральной ишемии с последующим апоптозом и резорбцией. Прорастание новых сосудов и выделение большого количества провоспалительных медиаторов усиливают диффузию кислорода в вышележащий хрящ, запуская в нем процессы оссификации [13]. При этом описана связь СОМР с нарушением функции эндотелия и атерогенезом [14].
Таким образом, терапия ОА требует системного подхода с учетом всех патогенетических предпосылок. В последние годы разработан ряд рекомендаций по ведению пациентов с ОА: Европейского общества по клиническим и экономическим аспектам остеопороза и остеоартроза (ESCEO), Международного научного общества по изучению остеоартроза (OARSI), экспертов Российской Федерации [9, 15–17]. Основная цель медикаментозной терапии состоит в уменьшении или купировании болевого синдрома, улучшении функции сустава и качества жизни пациента. Помимо быстродействующих анальгетических препаратов в арсенале врача имеются медленнодействующие симптоматические препараты (Symptomatic Slow Acting Drugs for Osteoarthritis, SYSАDOA), направленные на снижение болевого синдрома, торможение деструктивного процесса в хрящевой ткани и прогрессирования заболевания, рекомендованные для лечения ОА всеми экспертами [9, 15–18]. Среди таких препаратов — хондроитина сульфат (ХС) и глюкозамина сульфат, которые имеют наибольшую доказательную базу и чье противовоспалительное действие связано с подавлением экспрессии ядерного фактора транскрипции NF-κB, провоспалительных цитокинов, матриксных металлопротеиназ, NO и простагландинов [16–19]. Так, снижение содержания ХС коррелирует с тяжестью поражения сустава [3, 18]. Применение ХС снижает активность индуцированной липополисахаридами ММП-13 в хондроцитах, подавляет стимулированный ИЛ-1 синтез простагландина синовиальными фибробластами, активность аггреканазы, экспрессию ЦОГ-2 и простагландина Е [3, 18]. Показано, что применение ХС достоверно замедляет сужение суставной щели, а также что симптоматический эффект лечения не уступает с течением времени нестероидным противовоспалительным препаратам (НПВП), при этом по безопасности ХС не отличается от плацебо [16–19]. На сегодняшний день дискутабельным остается вопрос: какая форма введения ХС эффективнее? Так, внутримышечное введение увеличивает биодоступность ХС и, кроме того, уменьшает количество таблетированных препаратов у пациента с коморбидной патологией, прежде всего кардиоваскулярной, уменьшая возможности лекарственного взаимодействия [18, 19]. Одним из инъекционных препаратов ХС для внутримышечного введения является Мукосат®.
Цель исследования: оценить эффективность двухмесячной терапии инъекционным препаратом ХС у пациентов с ОА, потенциал препарата в плане структурно-модифицирующего действия.
Материал и методы
Проведено открытое проспективное исследование без группы контроля с участием 30 пациентов, из них 19 (63,3%) женщин, с установленным диагнозом: ОА, гонартроз (критерии R.D. Altman, 1995) II рентгенологической стадии по Kellgren — Lowrence. Возраст пациентов варьировал от 25 до 64 лет (медиана 55,5, среднее значение 52,5±11,7 года). У всех пациентов выраженность клинически манифестного болевого синдрома в коленном суставе превышала 50 баллов по визуально-аналоговой шкале (ВАШ), составив в среднем 54,4±3,4 балла. При этом локализованный ОА с поражением одного или двух коленных суставов имели 18 (60%) пациентов, у остальных 12 (40%) человек патологический процесс был генерализованным в анамнезе с вовлечением суставов кистей, позвоночника и др. У 23 (76,7%) пациентов на момент включения в исследование были диагностированы сопутствующие заболевания: АГ — у 13 (43,3%), ИБС — у 2 (6,7%), сахарный диабет 2 типа — у 3 (10%), хронический гастродуоденит — у 9 (30%), бронхиальная астма — у 5 (16,7%) пациентов. Большинство (70%) обследованных имели избыточную массу тела, в среднем индекс массы тела составил 26,1±2,7 кг/м2.
Критерии невключения в исследование: вторичный ОА и другая ревматологическая патология, соматические заболевания в стадии декомпенсации, прием антикоагулянтов, период беременности и лактации.
На момент включения в исследование пациенты не получали SYSADOA и любую внутрисуставную терапию (глюкокортикостероиды; препараты гиалуроновой кислоты; плазму, обогащенную тромбоцитами) как минимум в течение предшествующих 3 мес. Допускался прием НПВП в стандартной терапевтической дозе. Препарат ХС для внутримышечного введения (Мукосат®) назначали по схеме: 1 мл внутримышечно через день первые 3 дня, далее при хорошей переносимости — по 2 мл внутримышечно через день, курсом до 25–30 инъекций на период лечения 60 дней.
Перед началом лечения (визит 1), через 14 дней (визит 2) и 1 мес. (визит 3) терапии и через 2 мес. (визит 4), по окончании курса лечения, всем пациентам проводилось стандартное клиническое обследование с оценкой показателей суставного синдрома, выраженности боли по ВАШ, измерением окружности сустава, с применением опросников, индексов и шкал качества жизни и функции суставов: WOMAC (Western Ontario and McMaster Universities osteoarthritis Index), Леккена, KOOS (The Knee injury and Osteoarthritis Outcome Score), EQ-5D (EuroQol Group). В дополнение к рутинному лабораторному обследованию определяли содержание СОМР и высокочувствительного СРБ исходно и через 2 мес. лечения. УЗИ коленных суставов проводили до и после окончания курса лечения на аппарате экспертного класса GE Vivid 7Dimension из четырех стандартных доступов [20]. В ходе исследования оценивали толщину медиального и латерального хряща индексного коленного сустава и высчитывали среднюю величину.
Статистический анализ проводили с помощью пакета прикладных программ Statistica 9.0 (StatSoft, США). Описательные статистические данные представлены в виде M±SD, где M — среднее значение, SD — среднеквадратическое (стандартное) отклонение. Для сравнения двух групп по количественному и качественному признакам использовали непараметрические U-критерий Манна — Уитни и критерий χ2 Пирсона. Корреляционный анализ проводили по методу Спирмена. Различия показателей считали статистически значимыми при p<0,05.
Результаты исследования
На момент включения в исследование все пациенты имели выраженный суставной синдром с болезненностью и припухлостью коленных суставов, ограничением объема движений, снижением функции суставов и ухудшением качества жизни (табл. 1). Реактивный синовит коленных суставов клинически и по данным УЗИ выявлен в 16 (53,3%) случаях. При этом отмечена достоверная (p<0,05) сильная корреляционная связь между возрастом пациента и WOMAC (r=0,726), шкалой KOOS (r=0,715), умеренная связь — с наличием синовита суставов (r=0,547). Также с помощью непараметрического теста Манни — Уитни показано значимое негативное влияние наличия АГ на длительность утренней скованности (p=0,00), функциональную активность по шкале KOOS (p=0,00) и показатель качества жизни EQ-5D (p=0,04). Все пациенты испытывали потребность в приеме НПВП с целью уменьшения боли.
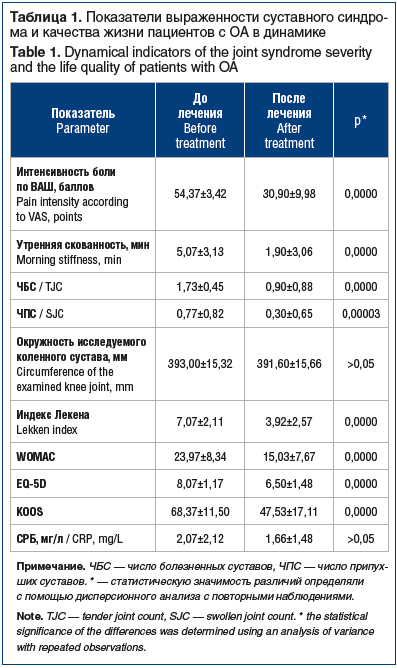
Первый клинический эффект от применения препарата Мукосат® был отмечен у всех пациентов уже через 2 нед. лечения. Через 1 мес. терапии имелась стойкая тенденция к улучшению основных клинических показателей суставного синдрома, потребность в постоянном приеме НПВП сохранялась у 40% пациентов. К концу курса лечения наблюдалось достоверное (p<0,05) уменьшение интенсивности боли в 1,8 раза, числа болезненных и припухших суставов в 2 и более раз, снижение утренней скованности, улучшение показателей функциональной активности и качества жизни пациентов (см. табл. 1). При этом исчезла сильная корреляционная связь между возрастом пациента и показателями WOMAC (r=0,525), шкалы KOOS (r=0,401). Потребность в регулярном приеме НПВП сохранялась только у 20% пациентов.
После курса терапии препаратом ХС хоть и имелась тенденция к снижению уровня СРБ, но она была недостоверной, что, вероятно, связано с малым количеством наблюдений (см. табл. 1).
При этом в результате лечения у большинства пациентов купировался синовит коленных суставов, по данным клинического обследования и УЗИ, он сохранялся только у 5 (17%) человек (p=0,003), что может свидетельствовать о снижении локальной воспалительной активности.
Средние показатели СОМР были в пределах референсных значений (менее 1500 нг/мл), однако в процессе лечения имела место тенденция (p=0,24) к их снижению — с 1048,33±423,42 нг/мл до 987,56±370,21 нг/мл, при этом до терапии препаратом Мукосат® выше нормы данный показатель был у 3 пациентов, а после лечения — только у одного.
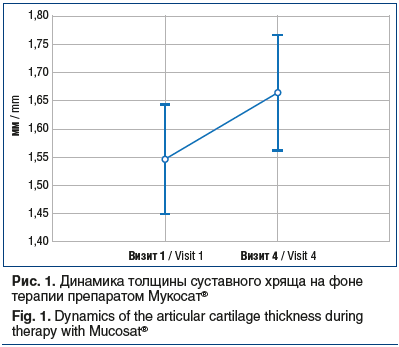
Согласно данным УЗИ коленных суставов отмечалось достоверное (р=0,0000) увеличение средней толщины суставного хряща с 1,55±0,26 мм первоначально до 1,67±0,27 мм после 2 мес. лечения (рис. 1).
Отдельно стоит выделить 13 (43,3%) пациентов с АГ, имевших первоначально достоверно (p≤0,01) более высокие показатели интенсивности боли, число болезненных и припухших суставов, длительность утренней скованности. К концу курса лечения наблюдалось более значимое снижение числа болезненных (p=0,04) и припухших суставов (p=0,03), интенсивности болевого синдрома по ВАШ (p=0,01), улучшение качества жизни EQ-5D (p=0,02) при отсутствии АГ в анамнезе. Пациенты с повышенным артериальным давлением (АД) также имели достоверную положительную динамику по всем показателям, но несколько меньшую по сравнению с пациентами с нормальным АД. Также с помощью дисперсионного анализа с повторными наблюдениями выявлено, что у пациентов без АГ увеличение толщины хряща, по данным УЗИ коленных суставов, к окончанию исследования более существенное, чем в группе пациентов с АГ (p=0,046). При этом уменьшение утренней скованности было значимым и происходило в равной степени в двух группах (p=0,75) независимо от повышения АД.
В целом на фоне 2 мес. терапии инъекционным препаратом ХС не было зарегистрировано ни одного нежелательного явления или ухудшения течения сопутствующей патологии. Все пациенты, включенные в исследование, полностью прошли курс терапии, ни один пациент не выбыл из исследования.
Обсуждение
Надо отметить, что в данном исследовании была достаточно неоднородная группа, включавшая как лиц молодого возраста с развитием ОА после травмы, так и возрастных пациентов с первичным патологическим процессом. Закономерным представляется ухудшение показателей функциональной активности у лиц старшего возраста. В то же время корреляция возраста и наличия выпота в полости сустава косвенно может свидетельствовать о значительной роли воспаления в генезе первичного ОА.
В целом результаты исследования показали, что применение препарата Мукосат® демонстрирует хороший симптоммодифицирующий эффект, статистически значимо положительно влияет на выраженность боли, показатели суставного сидрома, функции суставов и качество жизни, существенно снижает потребность в регулярном приеме НПВП. Ослабление корреляционной связи между возрастом пациента и индексом WOMAC и шкалой KOOS на фоне терапии подтверждает важность обезболивания, поскольку лица пожилого возраста тяжелее переносят боль и имеют тенденцию к быстрой ее хронизации.
При этом не было отмечено побочных явлений терапии, что очень важно при высокой коморбидности у этой категории пациентов.
Именно АГ как самая частая коморбидная патология [9] требует прицельного выявления. Хотя терапия инъекционным препаратом ХС была эффективна у всех пациентов, положительная динамика клинических показателей была несколько ниже при наличии АГ, прежде всего за счет медленного регресса боли и воспаления. Это согласуется с данными литературы о том, что АГ способствует субхондральной ишемии, поддержанию локального воспаления, усилению боли и прогрессированию ОА, которые в свою очередь способствуют повышению АД [13]. Соответственно, при обследовании пациентов с ОА необходимо не только прицельное выявление повышенного АД, но и своевременная его коррекция. Можно предположить, что таким пациентам нужна более длительная терапия (повторные курсы) препаратом ХС для контроля катаболических процессов в хрящевой ткани и профилактики обострения болевого синдрома.
Изменения содержания СРБ и СОМР в процессе лечения не были статистически значимыми, хотя и имелась тенденция к снижению показателей, что объясняется неоднородностью исследуемой группы и, возможно, малым числом наблюдений. В то же время о существенном противовоспалительном эффекте терапии Мукосатом может свидетельствовать купирование синовита коленных суставов не только по данным клинического обследования, но и по данным УЗИ. Учитывая, что показатель СОМР тесно связан с уровнем СРБ и наличием выпота в полости сустава [6, 7], тенденция к его снижению в данном исследовании вполне логична и позволяет обсуждать вероятность снижения деградации хряща на фоне терапии ХС. Это предположение подкрепляется и тем фактом, что на фоне двухмесячной терапии препаратом Мукосат® достоверно увеличивается толщина суставного хряща, по данным УЗИ суставов, определяя возможность структурно-модифицирующего действия конкретного препарата.
Заключение
Применение инъекционного препарата ХС (Мукосат®) у пациентов с гонартрозом эффективно в отношении таких клинических проявлений, как боль, локальное воспаление и функция суставов. Тенденция к снижению деградации хряща и увеличению его толщины позволяет предполагать положительное действие ХС в виде замедления прогрессирования заболевания в отдаленном периоде. Отсутствие нежелательных явлений и ухудшения течения коморбидной патологии на фоне лечения свидетельствует о хорошем профиле безопасности препарата и подтверждает возможность применения в клинической практике у разных групп пациентов с ОА.
Сведения об авторах:
Лапшина Светлана Анатольевна — к.м.н., доцент кафедры госпитальной терапии ФГБОУ ВО Казанский ГМУ Минздрава России; 420012, Россия, г. Казань, ул. Бутлерова, д. 49; ORCID iD 0000-0001-5474-8565.
Мингалеева Гульназ Фаритовна — ассистент кафедры внутренних болезней ФГБОУ ВО Казанский ГМУ
Минздрава России; 420012, Россия, г. Казань, ул. Бутлерова, д. 49; ORCID iD 0000-0002-3760-062X.
Контактная информация: Лапшина Светлана Анатольевна, e-mail: svetlanalapshina@mail.ru.
Источник финансирования: исследование проведено при поддержке ООО «ДИАМЕД-фарма».
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 11.06.2021.
Поступила после рецензирования 07.07.2021.
Принята в печать 30.07.2021.
About the authors:
Svetlana A. Lapshina — C. Sc. (Med.), Associate Professor of the Department of Hospital Therapy of the Kazan State Medical University; 49, Butlerov str., Kazan, 420012, Russian Federation; ORCID iD 0000-0001-5474-8565.
Gulnaz F. Mingaleeva — Assistant of the Department of Internal Diseases of the Kazan State Medical University; 49, Butlerov str., Kazan, 420012, Russian Federation; ORCID iD 0000-0002-3760-062X.
Contact information: Svetlana A. Lapshina, e-mail: svetlanalapshina@mail.ru.
Financial Disclosure: the study was conducted with the support of DIAMED-Pharma LLC. No authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 11.06.2021.
Received 07.07.2021.
Accepted 30.07.2021.
.
Информация с rmj.ru