Введение
Синдром Гудпасчера (СГ), или заболевание, ассоциированное с антителами к базальной мембране клубочков (анти-БМК антитела), согласно современной классификации, относится к редким иммунокомплексным органоспецифическим системным васкулитам [1]. Заболеваемость СГ максимальна в возрасте от 18 до 30 и от 50 до 65 лет. Мужчины заболевают приблизительно в 6–8 раз чаще [2].
Считается, что патогенез СГ связан с циркулирующими антителами преимущественно классов IgG1 и IgG3 к терминальному фрагменту α3-цепи, реже к α4— и α5-цепям, молекулы коллагена IV типа (α3(IV)NC1) базальной мембраны почечных клубочков (анти-БМК антитела) и альвеол [1, 3, 4]. Наличие этих антител вызывает быстропрогрессирующий гломерулонефрит и геморрагический альвеолит, при этом механизм выработки анти-БМК антител до конца не изучен.
У 80–90% пациентов проявлением СГ является развитие быстропрогрессирующей почечной недостаточности. К моменту установления диагноза до 50% пациентов нуждаются в проведении заместительной почечной терапии, а уровень смертности составляет примерно 25% через 1 год после постановки диагноза [5, 6]. У 40–60% пациентов поражение почек сочетается с патологией легких в виде диффузного альвеолярного кровотечения, которое может развиться внезапно и привести к смерти пациента в течение нескольких часов [7].
Синдром Гудпасчера в медицинской литературе описывают в виде отдельных клинических наблюдений [8, 9], а лечение данного заболевания, включающее плазмаферез и иммунодепрессанты, эффективно только на ранней стадии болезни, что определяет необходимость повышения осведомленности различных специалистов об этой редкой патологии.
Представлено собственное клиническое наблюдение СГ у молодой женщины — с развитием фульминантного гломерулонефрита и острой почечной недостаточности в дебюте болезни в сочетании с геморрагическим альвеолитом, быстропрогрессирующим течением и летальным исходом от наступивших осложнений.
Клиническое наблюдение
Пациентка, 23 года, 20.08.2021 поступила в ревматологическое отделение ГБУЗ ТО «ОКБ № 1» с жалобами на общую слабость, отеки лица и нижних конечностей, отсутствие мочи. Из анамнеза известно, что 04.08.2021 появились симптомы ОРВИ. Обратилась в поликлинику. При обследовании выявлен положительный результат ПЦР-теста на новую коронавирусную инфекцию COVID-19, однако клинические и инструментальные данные за пневмонию отсутствовали (рис. 1). До обращения в медучреждение хроническими заболеваниями не страдала.
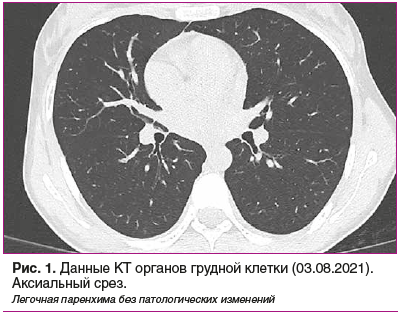
Лечилась амбулаторно: проводилась противовирусная и антибактериальная терапия, назначенная участковым терапевтом. Состояние было удовлетворительным. 11.08.2021 возникли выраженные боли в животе, тошнота, многократная рвота, субфебрилитет. Бригадой скорой помощи с подозрением на «острый живот» пациентка доставлена в многопрофильный стационар г. Тюмени. При поступлении исключена острая хирургическая патология, но выявлена выраженная азотемия (креатинин 2258 мкмоль/л, мочевина 51,3 ммоль/л, калий 6,05 ммоль/л). С предварительным диагнозом «Острая почечная недостаточность неуточненная (N17.9)» госпитализирована в реанимационное отделение, назначена заместительная терапия в виде гемодиафильтрации. При дополнительном обследовании выявлено: тромбоциты 720×109/л, лейкоциты 29×109/л, анемия тяжелой степени (эритроциты 2,8×1012/л, Hb 61 г/л), потребовавшая переливания эритроцитарной массы, С-реактивный белок (СРБ) 154 мг/л.
15.08.2021 на КТ органов грудной клетки выявлены двухсторонние инфильтративные изменения, сливные периваскулярные очаги, двухсторонний гидроторакс. Повторный ПЦР-тест отрицательный, в динамике антитела к SARS-CoV-2 отрицательные. Из областного ревматологического центра был приглашен врач-ревматолог, который по результатам обследования заподозрил системный васкулит и назначил дообследование на иммунологические маркеры, в результате которого обнаружены высокие титры специфических антител к БМК и отрицательные антитела к цитоплазме нейтрофилов.
17.08.2021 (через 2 нед. от дебюта болезни) на основании клинических, лабораторных и инструментальных критериев установлен клинический диагноз: «Синдром Гудпасчера. Быстропрогрессирующий гломерулонефрит с исходом в острую почечную недостаточность. Геморрагический альвеолит. Антитела к базальной мембране клубочков. Анемия тяжелой степени».
Пациентке была назначена интенсивная терапия с применением пульс-терапии метилпреднизолоном (1 г в/в 3 дня подряд). На фоне лечения отмечалось улучшение общего самочувствия и положительная динамика лабораторных показателей: эритроциты 3,26×1012/л, Нb 94 г/л, тромбоциты 170×109/л, лейкоциты 29,8×109/л, СРБ 24 г/л, мочевина 51,3 ммоль/л, креатинин 711 мкмоль/л, калий 4,4 ммоль/л.
Пациентку 20.08.2021 перевели в ревматологическое отделение ГБУЗ ТО «ОКБ № 1». 21.08.2021 был проведен очередной сеанс гемодиафильтрации. В ночь с 21 на 22 августа 2021 г. регистрировалось появление и нарастание одышки, сухого кашля, слабости, появление крепитирующих хрипов в нижних отделах легких, SpO2 до 89%, тахикардия 100 уд/мин, АД 90–85/60 мм рт. ст., повышение температуры до субфебрильных цифр и признаки легочного кровоизлияния по данным КТ легких (рис. 2).
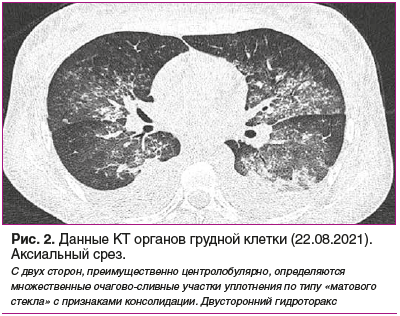
Данная ситуация была расценена как прогрессирование болезни, в связи с чем назначены повторные курсы интенсивной терапии: плазмаферез аппаратом MultiFiltrate (3 сеанса с интервалом в 2 дня) с восполнением объема свежезамороженной плазмой. После каждого сеанса плазмафереза вводился 1 г метилпреднизолона, иммуноглобулин человеческий 0,5 г/кг массы тела, а также 800 мг циклофосфамида после 2-й процедуры плазмафереза. На фоне лечения состояние стабилизировалось: SpO2 100%, АД 140/90 мм рт. ст., ЧСС 80 в минуту. Лечебная доза преднизолона — 60 мг/сут, запланировано повторное введение циклофосфамида.
На фоне проводимой терапии 03.09.2021 отмечено резкое ухудшение состояния с острой, нарастающей по интенсивности головной болью, рвотой, повышением АД до 185/120 мм рт. ст., психомоторным возбуждением и последующим развитием комы. Отмечена отрицательная динамика рентгенологических изменений в легких (рис. 3). По экстренным показаниям проведена КТ головного мозга, выявлен обширный геморрагический инсульт, множественные паренхиматозные кровоизлияния в обоих полушариях, отек и аксиальная дислокация головного мозга (рис. 4). Пациентка переведена в отделение анестезиологии и реанимации, где до 07.09.2021 продолжалось динамическое наблюдение профильными специалистами (ревматологом и неврологом), в/в введение метилпреднизолона и симптоматическое лечение.

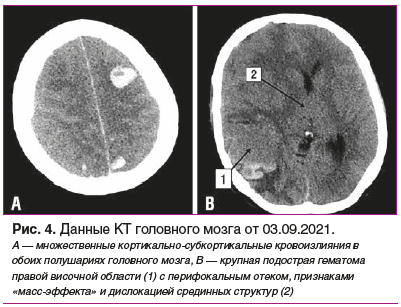
На 28-й день от первых проявлений болезни (07.09.2021) в 12:20 диагностированы клинические признаки смерти мозга, в 22:45 на фоне нарастающих явлений полиорганной недостаточности произошла остановка кровообращения, в 23:15 констатирована биологическая смерть.
Патологоанатомический диагноз: «Основное заболевание: синдром Гудпасчера — геморрагический пневморенальный синдром с некротическим васкулитом. Диффузные альвеолярные кровоизлияния, легочной капиллярит, геморрагический альвеолит; гломерулонефрит с формированием полулуний, субтотальный склероз почек.
Осложнения основного заболевания: состоявшееся легочное кровотечение. Почечная артериальная гипертензия. Внутримозговое кровоизлияние в правую височно-теменно-затылочную область (7×6×4 см), левую лобно-теменную область (3×1,5×1,5 см), ствол мозга (0,5×1×1 см) с перифокальным ишемическим размягчением вещества головного мозга. Мозговая кома (клинически). Двусторонний гидроторакс (по 1000 мл). Острое венозное полнокровие внутренних органов. Тяжелая белковая дистрофия эпителия проксимальных канальцев нефрона с переходом в нефронекроз».
Данные патогистологического исследования секционного материала представлены на рисунках 5, 6.
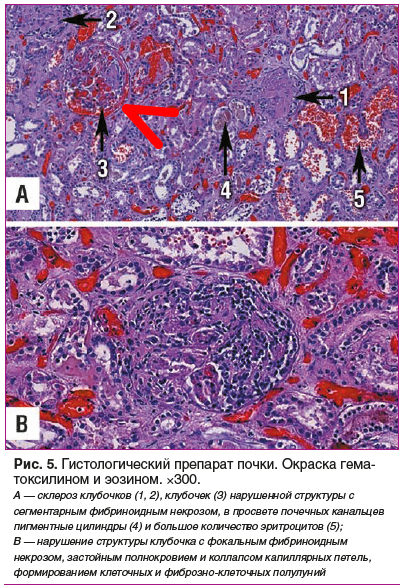

Обсуждение
Синдром Гудпасчера является редким аутоиммунным заболеванием, и, несмотря на яркую симптоматику, верификация диагноза представляет значительные трудности. В ревматологическом отделении ГБУЗ ТО «ОКБ № 1» настоящее наблюдение СГ является первым, подтвержденным иммунологическими и морфологическими методами обследования.
В настоящее время вместо СГ предлагается употреблять термин «болезнь, обусловленная антителами к базальной мембране клубочка (анти-БМК болезнь)», который зарегистрирован в онлайн-версии регистра наследственных болезней человека (Online Mendelian Inheritance in Man, OMIM) под номером 233450 [10] и в Международном регистре орфанных заболеваний под номером ORPHA375 [11]. Однако действующая Международная классификация болезней 10-го пересмотра (МКБ-10), являющаяся в настоящее время основополагающим документом для постановки клинического диагноза, кодом М31.0 определяет «синдром Гудпасчера», а термин «анти-БМК болезнь» в МКБ-10 отсутствует [12].
Причины развития СГ не установлены. Большинство авторов отмечают связь заболевания с перенесенной респираторной вирусной или бактериальной инфекцией, а также с контактом с углеводородами, такими как трихлорэтан, тетрахлорметан, пары клея, газообразный хлор, перхлорэтилен, толуол [13].
В дебюте заболевания у описываемой пациентки регистрировались явления ОРВИ, но утверждать, что дебют СГ был ассоциирован с определенной вирусной инфекцией, не представляется возможным.
Хотя классическая клиническая картина СГ включает сочетание поражения легких с быстропрогрессирующим гломерулонефритом (у 60–80% больных), до 40% пациентов имеют только признаки анти-БМК гломерулонефрита, у части из них почечная дисфункция прогрессирует исключительно медленно [14]. У 10% пациентов поражение легких носит изолированный характер [15].
Особенностями течения СГ в представленном клиническом наблюдении явились:
молниеносная (в течение суток) утрата функции почек, потребовавшая незамедлительного назначения заместительной терапии;
стертые клинические проявления патологии легких и подтверждение геморрагического альвеолита только с помощью инструментального обследования (КТ).
Основные этапы терапии СГ включают использование плазмафереза и применение глюкокортикостероидов (ГКС) и цитостатиков. В литературе встречаются единичные работы по успешному применению для лечения СГ ритуксимаба [16], однако это лекарственное средство назначается при данном заболевании off-label, отсутствует четкое понимание, на каком этапе развития болезни следует его назначать.
Стоит отметить, что национальные рекомендации по диагностике и лечению гломерулонефрита при СГ разработаны и утверждены Ассоциацией нефрологов России в 2014 г. [17], а представленный проект клинических рекомендаций от 2021 г. по диагностике и лечению гломерулонефрита, обусловленного анти-БМК антителами [18], в настоящее время пока не одобрен научно-практическим советом Минздрава РФ, следовательно, не может быть принят к исполнению в учреждениях здравоохранения. Информация о СГ для ревматологов очень ограничена и приводится в клинических рекомендациях от 2017 г. только в разделе «Классификация системных васкулитов» [19]. Междисциплинарные клинические рекомендации при этом отсутствуют. Таким образом, существующие коллизии нормативных документов затрудняют определение того, какой специалист должен вести пациента с СГ.
В качестве стартовой терапии были назначены пульсовые дозы ГКС в комбинации с циклофосфамидом. Плазмаферез был проведен только после перевода пациентки в специализированное ревматологическое отделение, так как при госпитализации в многопрофильное лечебное учреждение данная процедура отсутствовала.
Несмотря на применение синхронной комбинированной пульс-терапии, у пациентки не удалось достичь стабилизации состояния, течение СГ осложнилось легочным кровотечением, а в последующем возникло внутримозговое кровоизлияние на фоне гипертонического криза, с развитием мозговой комы и летального исхода.
Особенностями ведения пациентки с СГ в представленном клиническом наблюдении явились:
госпитализация в лечебное учреждение с отсутствием в штате врача-ревматолога, в связи с чем иммуносупрессивная терапия начата на 6-й день после поступления в стационар;
отсутствие технической возможности проведения плазмафереза в лечебном учреждении, куда была госпитализирована пациентка, на начальном этапе курации;
резистентность к синхронной интенсивной иммуносупрессивной терапии на этапе оказания специализированной медицинской помощи в ревматологическом отделении.
Заключение
Синдром Гудпасчера, или анти-БМК болезнь, относится к разряду редких нозологий, протекает с различными вариантами дебюта, развития и исходов, что может вызвать затруднение ее диагностики врачами различных специальностей, особенно при отсутствии достаточных знаний и опыта. Демонстрация как типичных, классических вариантов СГ, так и атипичных форм способствует более четким представлениям о данной нозологии. Представленное клиническое наблюдение свидетельствует о необходимости сохранения настороженности в отношении СГ во всех случаях быстропрогрессирующего гломерулонефрита. Кроме того, анализ ведения представленной пациентки выявил острую потребность в пересмотре и адаптации к рутинной клинической практике междисциплинарных алгоритмов ведения больных СГ, с устранением терминологических разногласий, определением порога вмешательства врача первичного звена и врача-специалиста (нефролога, пульмонолога, ревматолога).
Информация с rmj.ru
