Содержание статьи
Введение
Обширные проникающие корнеосклеральные и склеральные ранения (длиной более 6 мм) отличаются тяжелым течением раневого процесса и низкими функциональными исходами, в особенности когда речь идет о ранениях зоны III (часть склеры, находящаяся дальше 6–8 мм от лимба в сторону экватора). По данным разных исследователей, отсутствие предметного зрения после лечения таких травм наблюдается в 61–80% случаев, половина из которых заканчивается субатрофией [1–5].
В настоящий момент ввиду полиморфизма открытой травмы глаза нет единых подходов к оперативному лечению. Поэтапный, отложенный подход к проведению субтотальной витрэктомии у пациентов с обширными ранениями склеры с задействованной зоной III является ключевой причиной неблагоприятных исходов ввиду развития пролиферативной витреоретинопатии (ПВР). При данной тактике предполагается в рамках первичной микрохирургической обработки (ПМХО) ушивать проникающую рану склеры, проводить герметизацию и восстановление тонуса глазного яблока, а субтотальную витрэктомию проводить через 10–14 дней после достижения гемостаза, купирования острого воспалительного ответа на травму и формирования задней отслойки стекловидного тела [6–9]. Современная стратегия ведения пациентов с обширными ранениями склеры с задействованной зоной III предусматривает отсроченное выполнение субтотальной витрэктомии. Высокая частота неудовлетворительных исходов лечения диктует необходимость поиска новых подходов к обработке зоны повреждения с учетом анатомических особенностей.
При данном подходе не учитывается трехслойность обширного проникающего ранения (рис. 1).
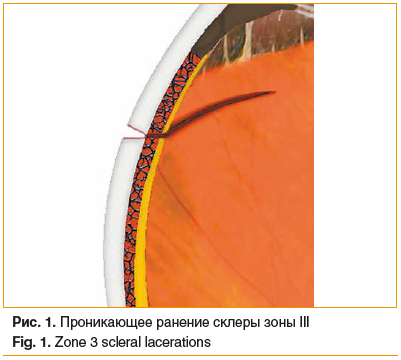
В результате в рамках ПМХО проводится ушивание одного слоя раны (склеры), в то время как остальные слои (сетчатка, хориоидея) остаются без внимания на протяжении 10–14 и более дней. Обширные хориоретинальные раны в подавляющем большинстве случаев приводят к развитию отслоек сетчатки, а также к запуску патологического пролиферативного процесса уже в первые дни [10–12].
Продукты распада тотальных и субтотальных гемофтальмов, сопровождающих обширные проникающие ранения склеры, токсически воздействуют на ткани сетчатки, инициируя бурное развитие ПВР [13, 14].
С учетом этих недостатков классического подхода в отношении обширных ран склеры, попадающих в зону III, нами был разработан подход к проведению ПМХО с использованием одномоментной витрэктомии и герметизацией хориоретинального дефекта [15]. Отличие данной методики состоит в учете трехслойности проникающего ранения и, соответственно, в одновременной обработке всех слоев раны (склера, сетчатка, хориоидея), а также в воздействии на разные звенья патогенеза ПВР и ее профилактике.
Цель исследования: оценить результаты лечения пациентов с обширными ранениями склеры с захватом зоны III с проведением одномоментной витрэктомии и обработкой хориоретинальной раны.
Материал и методы
Исследование проведено в 2022–2023 гг. на базе ГАУЗ СО «ЦГКБ № 23».
Под наблюдением находилось 14 пациентов (14 глаз), среди которых 12 мужчин и 2 женщины, с диагнозом «Обширное проникающее склеральное/корнеосклеральное ранение».
Критерии отбора пациентов в исследуемую группу:
обширная рана склеры с захватом зоны III (уходящая дальше 6–7 мм от лимба) (есть рана сетчатки);
наличие субтотального/тотального гемофтальма;
острота зрения при поступлении от pr. l. incerta до 0,02 (4-я и 5-я степень тяжести нарушения зрительных функций);
сроки поступления в стационар после травмы до 3 сут.
В исследование не включали пациентов с полным отсутствием светоощущения (острота зрения 0, амавроз), с ранениями без захвата зоны III (отсутствие раны сетчатки), с частичным гемофтальмом или без него (рана сетчатки визуализируется офтальмоскопически).
Для всех ранений был характерен полиморфизм внутриглазных повреждений. Колобомы радужки / частичные аниридии диагностированы в 5 (35,7%) наблюдениях, травматическая катаракта — в 8 (57,1%), ранение цилиарного тела — в 12 (85,7%), ранение сетчатки — в 14 (100%), отслойка сетчатки — в 5 (35,7%), субретинальное кровоизлияние — в 4 (28,6%), повреждение зоны макулы и диска зрительного нерва — в 2 (14,3%), эндофтальмит — в 1 (7,1%), наличие внутриглазных инородных тел — в 4 (28,6%).
При поступлении в стационар всем пациентам было выполнено комплексное обследование, которое включало визометрию, бесконтактную пневмотонометрию (тонометр Huvitz), периметрию, биомикроскопию, офтальмоскопию, ультразвуковое исследование (B-скан Compact Touch, Quantel Medical), при подозрении на внутриглазное инородное тело выполняли компьютерную томографию (томограф General Electric Optima CT520 Series).
Острота зрения при поступлении соответствовала 4-й и 5-й степени нарушения зрительных функций и распределялась следующим образом: pr. l. Incerta — 8 случаев; pr. l. Certa — 4 случая; 0,01 — 2 случая.
Всем пациентам проведена ПМХО согласно разработанной методике, которая состояла из трех основных этапов:
Этап 1. ПМХО раны «снаружи» (ушивание раны склеры и роговицы).
Этап 2. Субтотальная витрэктомия.
Этап 3. ПМХО раны «изнутри» (локализация хориоретинальной раны, очистка дна раневой поверхности, эндокоагуляция кровоточащих сосудов, выравнивание краев, эндолазеркоагуляция вокруг, заполнение хориоретинального дефекта чистой, обогащенной тромбоцитами плазмой (Pure platelet rich plasma — P-PRP), эндотампонада силиконовым маслом или газовоздушной смесью).
При необходимости после ПМХО раны склеры выполняли диализ передней камеры, экстракцию травматической катаракты для формирования визуального доступа к витреальной полости. Инородное тело при наличии удаляли цанговым магнитом или пинцетом через плоскую часть цилиарного тела или через дефект в задней капсуле хрусталика. Быстрому формированию ровного, гладкого хориоретинального рубца способствовала P-PRP. Регенеративные свойства обогащенной тромбоцитами плазмы широко применяются в лечении периферических и центральных разрывов сетчатки [16–22].
Основные этапы операции представлены на рисунке 2.
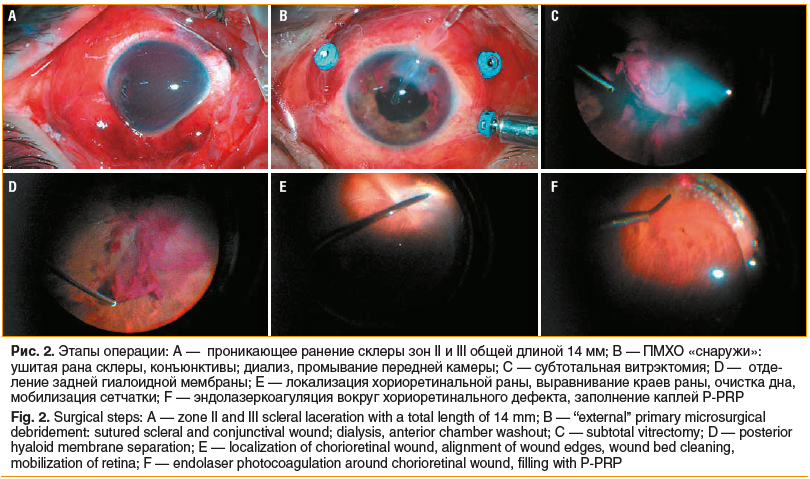
Тампонада силиконовым маслом была проведена в 9 случаях, газовоздушной смесью — в 5. Силиконовое масло удаляли через 3–5 мес., газ рассасывался в течение 1,5 мес.
Комплексное послеоперационное обследование включало визометрию, тонометрию, периметрию, биомикроскопию, офтальмоскопию, ультразвуковое исследование. Через 6 мес. всем пациентам проводили оптическую когерентную томографию макулярной области и зоны сформированного хориоретинального рубца на Optovue RTVue XR Avanti.
Срок наблюдения составил 6 мес.
Результаты исследования
Острота зрения через 6 мес. после получения травмы и последующего лечения составила в среднем 0,12±0,15. В 2 наблюдениях она соответствовала pr. l. inserta, в 4 — 0,02–0,04, в 3 — 0,05–0,09, в 5 — 0,1–0,5. Внутриглазное давление в среднем составляло 20,2±4,5 мм рт. ст.
У большинства (11 из 14; 78,6%) пациентов хориоретинальные рубцы характеризовались локальными неагрессивными пролиферациями без проминенции в витреальную полость, сглаженной поверхностью без грубых деформаций, без разрастания пролиферативной ткани за пределы сформированных рубцов. Пример сформированного хориоретинального рубца представлен на рисунке 3.
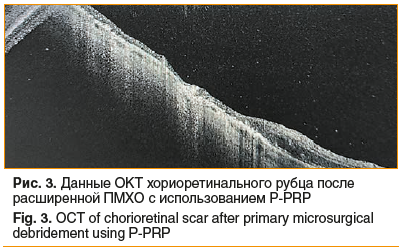
В течение 6 мес. не отмечено ни одного случая развития субатрофии глазного яблока. Один или несколько признаков развития и прогрессирования ПВР на фоне тампонады силиконовым маслом в виде образования интраретинальных сращений, субретинальных тяжей, распространяющихся на здоровые ткани сетчатки, отмечены у 3 (21,4%) пациентов. Им проведены соответствующие оперативные вмешательства с использованием техники ретинотомии и повторной тампонады силиконовым маслом.
Обсуждение
Обширные прободные ранения с повреждениями зоны III сочетают в себе комплекс факторов повышенного риска развития ПВР и характеризуются низкими функциональными результатами. Согласно представленным в литературе данным при использовании традиционного подхода к хирургическому лечению таких травм острота зрения менее 0,02, а также отсутствие предметного зрения в виде правильной или неправильной светопроекции, полное отсутствие светоощущения (острота зрения 0) отмечаются в 61,4–80,3% случаев. Исходы с остротой зрения от 0,04 до 0,1 получены у 16–24,4% больных, от 0,2 до 1,0 — у 11–18% [2, 5, 14, 23].
Более чем в 60% случаев ПВР служит основной причиной прогрессирующего снижения зрительных функций и требует проведения дополнительных оперативных вмешательств, при этом 17% рецидивирующих отслоек с картиной последних стадий ПВР признаются неоперабельными [1, 24].
Полученные нами клинико-функциональные показатели при использовании расширенного алгоритма ПМХО свидетельствуют о более высоких результатах. Неблагоприятные визуальные исходы в виде остроты зрения менее 0,02, в том числе неправильная светопроекция, получены в 35,7% случаев, а агрессивный патологический пролиферативный ответ — в 21,4%.
Для того чтобы сформулировать окончательные выводы об эффективности и применимости предложенной методики ПМХО, необходимы исследования на большей выборке пациентов, с более длительным периодом наблюдения, в сравнении с контрольной группой и детальным статистическим анализом.
Заключение
Использованный в настоящей работе подход к ПМХО при тяжелой травме глаза с проникающим ранением склеры позволяет улучшить результаты лечения этой категории пострадавших. В течение 6-месячного периода послеоперационного наблюдения не отмечено ни одного случая развития субатрофии глазного яблока, зафиксирован низкий уровень развития ПВР, что может говорить о высокой эффективности одномоментной витрэктомии в лечении тяжелых травм глаза. Сформированные деликатные хориоретинальные рубцы свидетельствуют о положительном влиянии P-PRP при такой патологии. Для полной оценки результатов хирургии обширных проникающих ранений склеры предлагаемым способом необходимы дальнейшие исследования.
Сведения об авторах:
Шамкин Сергей Сергеевич — врач-офтальмолог, заведующий отделением палат повышенной комфортности ГАУЗ СО «ЦГКБ № 23»; 620017, Россия, г. Екатеринбург, ул. Старых Большевиков, д. 9; ORCID iD 0000-0002-3504-8886.
Субботина Серафима Николаевна — врач-офтальмолог офтальмологического отделения ГАУЗ СО «ЦГКБ № 23»; 620017, Россия, г. Екатеринбург, ул. Старых Большевиков, д. 9; ORCID iD 0000-0001- 9284-6502.
Степанянц Армен Беникович — д.м.н., заведующий курсом усовершенствования врачей, профессор кафедры офтальмологии ФГБОУ ВО УГМУ Минздрава России; 620028, Россия, г. Екатеринбург, ул. Репина, д. 3.
Салов Дмитрий Викторович — студент лечебно-профилактического факультета ФГБОУ ВО УГМУ Минздрава России; 620028, Россия, г. Екатеринбург, ул. Репина, д. 3.
Контактная информация: Шамкин Сергей Сергеевич, e-mail: SergeyShamkin87@yandex.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 08.06.2023.
Поступила после рецензирования 04.07.2023.
Принята в печать 27.07.2023.
About the authors:
Sergey S. Shamkin — Head of the Department of Superior Comfort, ophthalmologist, Central City Clinical Hospital № 23; 9, Starykh Bolshevikov str., Yekaterinburg, 620017, Russian Federation; ORCID iD 0000-0002-3504-8886.
Serafima N. Subbotina — ophthalmologist, Department of Ophthalmology, Central City Clinical Hospital № 23; 9, Starykh Bolshevikov str., Yekaterinburg, 620017, Russian Federation; ORCID iD 0000-0001- 9284-6502.
Armen B. Stepanyants — Dr. Sc. (Med.), Professor of the Department of Ophthalmology, Head of the Advanced Medical Training Course, Ural State Medical University; 3, Repin str., Yekaterinburg, 620028, Russian Federation.
Dmitriy V. Salov — student of the Medical and Preventive Faculty, Ural State Medical University; 3, Repin str., Yekaterinburg, 620028, Russian Federation. Contact information: Sergey S. Shamkin, e-mail: SergeyShamkin87@yandex.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 08.06.2023.
Revised 04.07.2023.
Accepted 27.07.2023.
Информация с rmj.ru