Содержание статьи
Факторы выбора химиотерапии при метастатическом раке молочной железы (Е.В. Артамонова)
Основной целью терапии при метастатическом раке молочной железы (мРМЖ) является не только увеличение продолжительности жизни, но и сохранение или улучшение ее качества. В Российской Федерации первичный мРМЖ составляет 8% от всех диагностированных случаев РМЖ, а отдаленные метастазы в различные сроки после первичного лечения выявляются не менее чем у 40% пациенток. С точки зрения прогноза тройной негативный РМЖ имеет наиболее неблагоприятный вариант течения. В одном из исследований [1], где оценивался прогноз у пациенток с первичным мРМЖ или с прогрессированием РМЖ. Показано, что тройной негативный РМЖ имел самые низкие показатели общей выживаемости. Как известно, единого стандарта лечения мРМЖ не существует, на выбор лечебной тактики влияют различные факторы — прежде всего, молекулярно-генетический подтип РМЖ и клиническое течение болезни. Основным методом лечения мРМЖ является химио- и/или гормонотерапия, которая может дополняться по показаниям таргетной или иммунотерапией.
При выборе терапии мРМЖ основополагающей является молекулярно-генетическая классификация болезни. Основные используемые иммуногистохимические показатели:
РЭ (рецепторы эстрогенов);
РП (рецепторы прогестерона);
HER2 (рецепторы человеческого эпидермального фактора роста 2-го типа);
ki-67 (индекс пролиферации).
Дополнительные показатели:
мутации BRCA 1 и 2;
экспрессия PD-L1 при тройном негативном мРМЖ;
мутации PIK3CA при люминальном HER2- мРМЖ.
Химиотерапия (ХТ) является важной опцией лечения большого числа пациентов с мРМЖ. В одной из публикаций [2] ведущих европейских экспертов были представлены условия, при которых назначается ХТ при мРМЖ:
негативный статус гормональных рецепторов (ГР-статус);
неэффективность (исчерпанность) последовательной эндокринной терапии;
совместное применение с таргетной терапией;
быстрая прогрессия заболевания;
выраженные симптомы;
угрожающие жизни метастазы (висцеральный криз).
Концепция «ожидаемого висцерального криза» расширяет контингент пациентов, которые нуждаются в достижении объективного ответа и в лечении которых ХТ играет ведущую роль.
По мере развития и прогрессирования заболевания все пациенты с мРМЖ могут получить несколько линий ХТ. Предпочтительный выбор ХТ при мРМЖ — последовательное назначение монорежимов. Комбинации могут применяться при быстром прогрессировании РМЖ, висцеральном кризе, а также при необходимости быстрого контроля симптомов заболевания.
При отсутствии противопоказаний в качестве первой линии ХТ назначаются антрациклины и таксаны в монорежиме, если пациентки не получали их в неоадъювантном или адъювантном режиме. Также в качестве первой линии ХТ показано назначение капецитабина или винорелбина. В клинических рекомендациях говорится о необходимости проведения пролонгированной терапии первой линии, так как она достоверно коррелирует с увеличением общей выживаемости. Существуют определенные ограничения в проведении противоопухолевой химиотерапии. Целый ряд препаратов не может применяться в течение длительного времени: например, антрациклины имеют предельно допустимую дозу, при превышении которой развивается кардиотоксичность (доксорубицин 550 мг/м2, эпирубицин 900 мг/м2); таксаны также часто вызывают развитие осложнений (доцетаксел — риск кумулятивной задержки жидкости; паклитаксел — риск кумулятивной нейротоксичности). На фоне терапии капецитабином имеется высокий риск развития тяжелого ладонно-подошвенного синдрома, тяжелой диареи [3]. Поэтому зачастую на определенном этапе лечения возникает необходимость прекратить ХТ или перейти на поддерживающую терапию.
В связи с вышеизложенным особого внимания заслуживает винорелбин — антимикротрубочковый агент, нарушающий полимеризацию тубулина и препятствующий формированию митотического веретена. В результате происходит блокировка митоза клеток на стадии метафазы G2–M, что приводит к апоптотической гибели клетки.
Винорелбин действует преимущественно на митотические микротрубочки. Влияние на аксональные микротрубочки, с которым связана периферическая полинейропатия, у винорелбина отмечается в меньшей степени, в основном при применении его высоких доз. Поэтому винорелбин характеризуется низким риском развития нейротоксичности и является препаратом выбора в качестве комфортной для пациента терапии.
При выборе конкретного варианта ХТ также необходимо учитывать форму выпуска препарата. Большинство пациентов отдают предпочтение пероральной терапии по сравнению с внутривенными препаратами при условии одинаковой эффективности лечения. Пероральные лекарственные средства имеют преимущества за счет удобства приeма, исключения венопункции и связанных с ней осложнений. При применении пероральных форм в случае необходимости достаточно просто менять их дозировку. Кроме того, пациент имеет возможность проходить лечение в более комфортных домашних условиях, уменьшить число визитов в клинику и совмещать терапию с работой [4, 5]. Винорелбин капсулы по эффективности в первой линии ХТ мРМЖ сопоставим с таксанами [6], при этом обеспечивает все преимущества пероральной терапии. Винорелбин включен в российские [7] и зарубежные [8] клинические рекомендации.
Химиотерапия при люминальных подтипах HER2- мРМЖ (Ж. Фрейер)
В сравнительных исследованиях лечения пациентов с HR+/HER2- РМЖ было показано, что сочетание гормональных препаратов с ингибиторами CDK 4/6 имеет преимущество по продолжительности БРВ по сравнению со стандартным лечением. Применение ингибиторов CDK 4/6 повышает общую выживаемость пациентов с 45 мес. до более чем 50 мес.
В случае необходимости перехода с ингибиторов CDK 4/6 на другие препараты возможно применение следующих таргетных препаратов:
ингибитор PI3KCA — алпелисиб (исследование SOLAR 1);
ингибитор AKT — капивасертиб (исследование FAKTION);
ингибитор mTOR — эверолимус.
Данные препараты хуже переносятся и имеют ряд побочных эффектов, существенно снижающих качество жизни пациентов.
В настоящее время имеются новые лекарственные агенты — селективные супрессоры эстрогеновых рецепторов (SERD):
эласестрант (исследование EMERALD), продемонстрировавший эффективность в поздних линиях лечения гормонозависимого HER2-негативного РМЖ;
ингибиторы PARP при наличии мутации гена BRCA;
олапариб (исследование OLYMPIAD);
талазопариб (исследование EMBRACA).
Несмотря на появление новых классов препаратов, ХТ остается важным терапевтическим звеном помощи онкологическим больным, особенно при развитии резистентности к гормональной терапии.
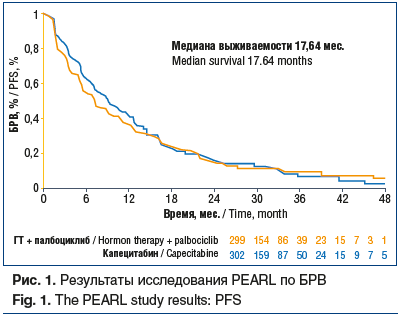
Вопросы своевременности применения ХТ изучались в рандомизированном исследовании III фазы PEARL [9]. В исследование были включены пациентки с мРМЖ HR+/HER2- (с резистентным и промежуточно чувствительным РМЖ), у которых имелись: рецидив на фоне адъювантной гормонотерапии ингибиторами ароматазы или через год после ее окончания; прогрессирование на фоне гормонотерапии ингибиторами ароматазы по поводу метастазирующей опухоли или через месяц после ее окончания; метастазирующие опухоли. Стратификация пациентов (n=300) осуществлялась по следующим параметрам: метастазы (внутренние органы / другая локализация); ранее выявленная гормонозависимость; предшествующая ХТ по поводу метастазирующей опухоли.
Пациентки были рандомизированы на 2 равные группы: 1-я группа получала фулвестрант 500 мг на 1-й и 15-й дни 1-го цикла, затем 1-й день каждого 28-дневного цикла + палбоциклиб 125 мг с 1-го по 21-й день каждого 28-дневного цикла; 2-я группа получала капецитабин 1250 мг/м2 (1000 мг/м2 получали пациентки старше 70 лет) 2 р/сут в течение 2 нед. каждого 3-недельного цикла. В данной работе не было продемонстрировано преимущества БРВ пациенток, получающих гормональную терапию или ХТ (рис. 1).
Результаты многофакторных анализов показали, что при люминальных подтипах мРМЖ есть определенные прогностические факторы. При анализе базы данных SEER (n=18 322) установлено, что наличие висцеральных метастазов в печень, легкие и головной мозг, а также наличие костных метастазов является крайне плохим прогностическим признаком. Многофакторный анализ продемонстрировал, что возраст, раса, семейное положение, степень злокачественности опухоли, подтип и размер опухоли, оперативное лечение первичной опухоли и лучевая терапия или ХТ в анамнезе являются независимыми прогностическими факторами [10, 11]. Также было продемонстрировано, что полихимиотерапия гораздо эффективнее монохимиотерапии, но при этом более токсична. Полихимиотерапия улучшает БРВ, не влияя при этом на общую выживаемость. Более длительная ХТ первой линии достоверно увеличивает ВБП и ОВ у больных мРМЖ. Важным моментом является необходимость оценки риска возникновения висцерального криза до его развития и применение монохимиотерапии.
Напомним, что висцеральный криз — это тяжелая полиорганная недостаточность, диагностируемая по клиническим признакам и симптомам, лабораторным данным и быстрому прогрессированию заболевания. Висцеральный криз проявляется не только метастатическим поражением внутренних органов, но и тяжелым нарушением их функций, что является клиническим показанием для назначения терапии, обеспечивающей более быстрое развитие эффекта (однако это не имеет доказательных данных), так как других вариантов лечения на фоне прогрессирования может не быть (уровень доказанности: экспертное мнение).
Пероральные химиопрепараты в терапии первой линии рекомендовано применять, основываясь: на характеристике опухоли: HR+, гормонорезистентность, отсутствие признаков висцерального криза или костных метастазов; на предпочтении пациента: амбулаторное лечение, снижение риска развития алопеции; на уровне токсичности: хорошая переносимость; на предпочтении врача: одобрение длительной поддерживающей терапии.
В настоящее время научное сообщество обладает большим объемом данных по применению пероральных препаратов винорелбин, капецитабин и их комбинации.
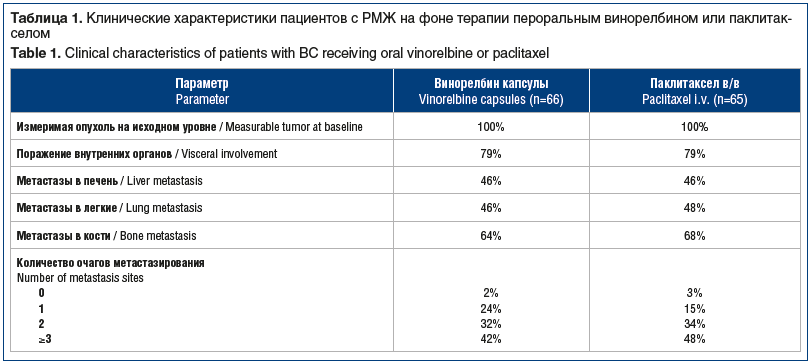
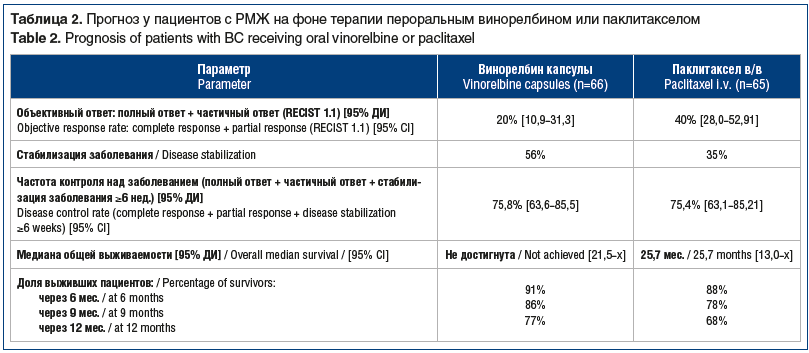
Преимущество перорального применения винорелбина было продемонстрировано в ряде исследований. В рандомизированном исследовании NorBREAST-231 II фазы участвовали 2 группы пациентов: группа A (n=66) получала винорелбин капсулы еженедельно 60 мг/м2 в 1, 8 и 15-й дни 1-го цикла, затем с повышением дозы до 80 мг/м2 в 1, 8 и 15-й дни следующих циклов (при отсутствии токсических реакций 3–4-й степени); группа B (n=65) получала паклитаксел еженедельно 80 мг/м2 в 1, 8 и 15-й дни [6]. Первичной конечной точкой был уровень контроля над заболеванием.
Существенной разницы (табл. 1, 2) с точки зрения контроля над заболеванием не выявлено, однако на фоне терапии винорелбином отмечался лучший ответ. С точки зрения БРВ и медианы выживаемости результаты в группах были схожими. Таким образом, винорелбин является хорошим кандидатом для применения в качестве ХТ первой линии.
Клиническое наблюдение пациента женского пола (С.Н. Чернядьева)
Пациентка М., 58 лет. Рост 159 см, масса тела 65 кг.
Диагноз: рак правой молочной железы T1N2M0 IIA стадия. Дата установления диагноза — октябрь 2017 г. По данным УЗИ молочной железы, выполненного по месту жительства в сентябре 2017 г., выявлен узел размером 1 см в правой молочной железе. При маммографии в октябре 2017 г.в верхнем квадранте правой молочной железы определялось 1 узловое образование неправильной формы размером 10×15 мм с тяжистым контуром; BAIRADS справа 4, слева 0.
Общеклиническое обследование: без особенностей.
Гистология: инвазивный рак правой молочной железы IIIА стадии злокачественности с метастазами в 7 подмышечных лимфоузлов.
Иммуногистохимия: РЭ — 8, РП — 6; негативный статус по онкогену — HER2neu, ki-67 — 44%.
Сопутствующие заболевания: гипертоническая болезнь II стадии, 2-й степени, риск 3, хроническая сердечная недостаточность 1-й степени, гипертрофия левого желудочка.
По данным трепанобиопсии: инвазивный рак правой молочной железы 3-й степени злокачественности.
Комплексное лечение. В октябре 2017 г. пациентке была выполнена радикальная мастэктомия по Маддену справа. В октябре 2017 г. — январе 2018 г. проведена стандартная адъювантная ХТ: 4 курса AC + 4 курса доцетаксела. Данные компьютерной томографии (КТ) органов грудной клетки, головного мозга в январе 2018 г.: без особенностей.
Далее в октябре 2017 г. — сентябре 2019 г. выполнена лучевая терапия и назначена адъювантная гормонотерапия первой линии: тамоксифен 20 мг в течение 3 лет. В сентябре 2019 г. у пациентки появились признаки дыхательной недостаточности, одышка при незначительной физической нагрузке, кашель. Результаты КТ органов грудной клетки (сентябрь 2019 г.) представлены на рисунке 2.
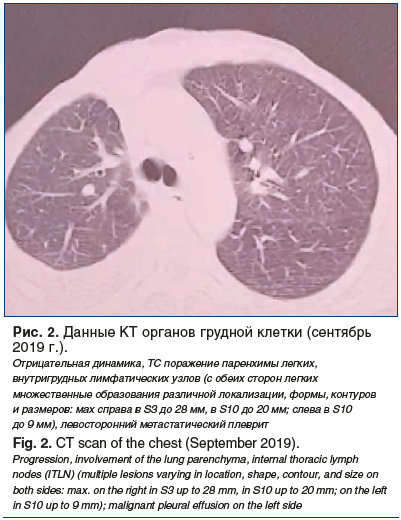
В ноябре 2019 г. — апреле 2020 г. проведена гормонотерапия первой линии: фулвестрант 500 мг 5 курсов. В апреле 2020 г. у пациентки отмечены: дыхательная недостаточность, усиление одышки, кашель, нарастание метастатического плеврита, метастатическое поражение головного мозга, увеличение размеров метастазов в легких. Результаты КТ органов грудной клетки (апрель 2020 г.) представлены на рисунке 3.
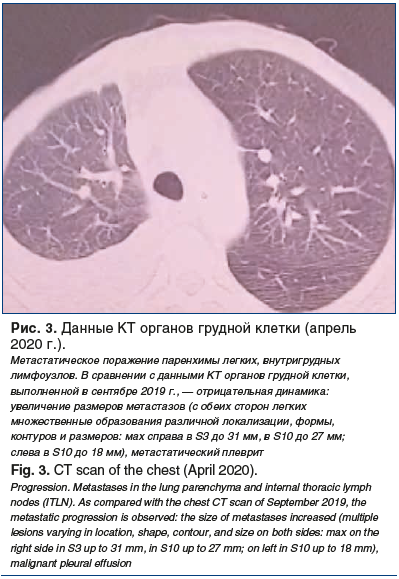
У пациентки появились неврологические признаки в виде атаксического синдрома и нарастание когнитивных нарушений. КТ головного мозга (апрель 2020 г.): метастатическое поражение головного мозга, образования в левой лобной доле (18 мм) и правой гемисфере мозжечка (7 мм) метастатического характера.
В апреле 2020 г. выполнена паллиативная лучевая терапия на весь объем головного мозга. Состояние было расценено как висцеральный криз.
Проводимая терапия. С апреля 2020 г. по настоящее время пациентка получает ХТ первой линии: перорально винорелбин 60 мг/м2 первые 3 нед. (100 мг), далее 80 мг/м2 (130 мг) еженедельно.
В начале терапии отмечалась положительная динамика (по данным КТ органов грудной клетки с июля 2020 г. по январь 2021 г.), в настоящий момент наблюдается стабилизация процесса (по данным КТ органов грудной клетки с апреля 2021 г. по апрель 2022 г.).
В представленном клиническом наблюдении выбор противоопухолевой терапии позволил пациентке не только сохранить качество жизни, но и увеличить ее продолжительность (к настоящему моменту на 26 мес.).
Применяемый препарат винорелбин в капсулах в качестве первой линии ХТ у пациентки c мРМЖ (HR+, HER2neu-) обеспечил длительный контроль заболевания. Винорелбин хорошо переносится, побочных и нежелательных явлений, требующих отмены препарата или понижения дозировки, не отмечено. Пероральный прием химиотерапевтического препарата позволил избежать постинъекционных осложнений и сохранить качество жизни. Клинически удалось добиться улучшения общего самочувствия и психоэмоционального статуса пациентки.
Клиническое наблюдение пациента мужского пола (Е.В. Артамонова)
Пациент N., 55 лет, соматически не отягощен, впервые обратил внимание на уплотнение в левой грудной железе в 2015 г., но за медицинской помощью не обращался. В 2020 г. стал отмечать постепенный рост данного образования, деформацию железы, появление плотных узловых образований в левой подмышечной области.
Самостоятельно обратился в ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России в марте 2020 г., где при комплексном обследовании был установлен и морфологически верифицирован диагноз рака левой грудной железы T4N3M0. Маммографическое исследование с УЗИ показало утолщение кожи всей железы, наличие опухолевого образования неправильной формы до 5,5 см, инфильтрирующего грудную мышцу. В левой аксиллярной области определялись множественные измененные лимфатические узлы до 2,4 см и конгломерат размером 4,0×3,0 см. В левой подключичной области — цепочка метастатически пораженных лимфатических узлов до 1,2 см в диаметре. При комплексном обследовании отдаленных метастазов не выявлено. Мутаций в генах BRCA1/2 также не выявлено.
Иммуногистохимия: РЭ — 8; РП — 7; ki-67 — 40%; негативный статус по онкогену — Her2/neu 2+ (необходима FISH-реакция).
Учитывая люминальный подтип опухоли с неопределенным статусом HER2, на время ожидания результатов FISH-исследования пациенту был назначен тамоксифен в дозе 20 мг 1 р/сут ежедневно, имеющий преимущество перед ингибиторами ароматазы. Лечение осложнилось гнойным маститом с формированием свища, проводилось хирургическое вмешательство. На фоне терапии тамоксифеном в течение 1,5 мес. отмечалось уменьшение первичной опухоли и метастазов в лимфоузлах в рамках минимальной регрессии (-25%).
Диагноз: РМЖ (левой) T4N3M0 люминальный, подтип Her2+.
Учитывая выраженную положительную динамику, люминальный подтип опухоли с высокой экспрессией гормональных рецепторов и желание получать максимально щадящее лечение, на консилиуме было принято решение: продолжить гормонотерапию тамоксифеном с добавлением двойной анти-Her2-блокады в стандартном режиме: пертрузимаб + трастузумаб каждые 3 нед.
С апреля 2020 г. пациенту было проведено 8 курсов таргетной терапии трастузумабом 6 мг/кг (нагрузочная доза 8 мг/кг) и пертузумабом 420 мг (нагрузочная доза 840 мг) каждые 3 нед., продолжен прием тамоксифена. Лечение переносил удовлетворительно, с периодическими диареями в пределах 2-й степени. После 4 циклов терапии зафиксирована частичная регрессия опухоли: отек кожи уменьшился, размеры опухолевого узла сократились до 3,0×1,8 см, лимфатические узлы в подключичной области перестали определяться, в аксиллярной области сократились до 1,4 см, конгломерат перестал определяться (-76%). Достигнутый эффект сохранялся на протяжении лечения.
В октябре 2020 г. выполнена радикальная мастэктомия слева с пластикой подмышечно-подключично-подлопаточной области композитным мышечным трансплантатом.
При гистологическом исследовании: остаточная опухоль 3,5×3×2,5 см представлена инфильтративным раком неспецифического типа с признаками лечебного патоморфоза RCB-III. Клеточность опухоли — 96%, отмечено врастание опухоли в кожу соска, признаки ангиолимфатической и периневральной инвазии. Стромальные TIL — 4%. Лимфатических узлов с метастазами — 6 из 9.
Иммуногистохимия: РЭ — 7, РП — 5, HER2/neu 2+, ki-67 — 23%.
Учитывая полученные данные, было рекомендовано проведение адъювантной химиотаргетной терапии по схеме 4 курса антрациклинов каждые 3 нед., далее 4 курса по схеме доцетаксел 75 мг/м2 + трастузумаб 6 мг/кг + пертузумаб 420 мг каждые 3 нед. с продолжением терапии до года (от ее начала).
Первый блок терапии был проведен в запланированном режиме и осложнился астенией 2-й степени, нейтропенией 2-й степени, тошнотой 1-й степени и гастроинтестинальной токсичностью 1-й степени.
Первый цикл второго блока, несмотря на проводимую Г-КСФ профилактику, осложнился фебрильной нейтропенией, агранулоцитозом, мукозитом 3-й степени, диареей 2-й степени, астенией 2-й степени, в связи с чем пациент был экстренно госпитализирован, проводилась антибактериальная, противогрибковая терапия, терапия октреотидом. В течение 5 дней нежелательные явления были купированы.
Ввиду осложнившегося 1-го курса 2-го блока терапии 2-й курс проведен с редукцией дозы доцетаксела на 30%. Несмотря на это, лечение осложнилось нейтропенией 2-й степени, астенией 2-й степени, стоматитом 2-й степени, обострением мочекаменной болезни, по поводу чего потребовалась экстренная госпитализация в урологический стационар. Перерыв в лечении составил более 6 нед.
От дальнейшего проведения ХТ пациент категорически отказался. Пертузумаб отменен из-за диареи. Проведен курс адъювантной лучевой терапии на левую половину грудной стенки и зоны лимфооттока. Адъювантная терапия трастузумабом была завершена в июне 2021 г.
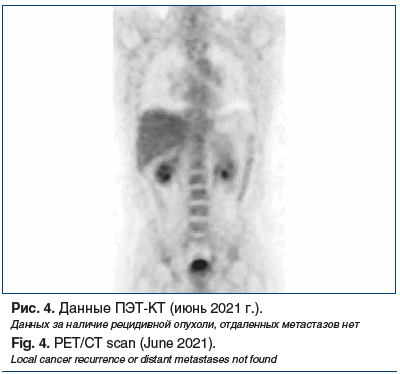
По данным ПЭТ-КТ (июнь 2021 г.), признаки болезни отсутствовали, продолжена терапия тамоксифеном (рис. 4). Через 6 мес. в ноябре 2021 г. при ПЭТ-КТ выявлено прогрессирование: метастаз в лимфоузле корня левого легкого, 22×20 мм, с повышенным метаболизмом радиофармпрепарата SUVmax=5,75 (рис. 5).
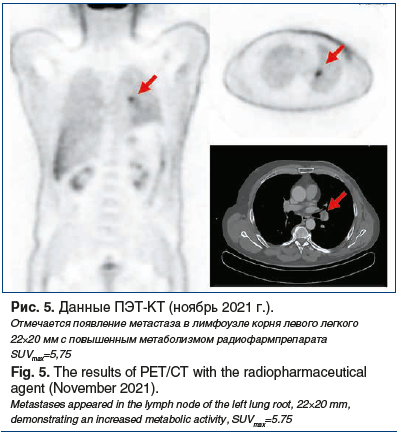
После обсуждения побочных эффектов пациент отказался от проведения:
терапии т-ДМ1;
стандартной терапии первой линии Her2-позитивного мРМЖ в режиме доцетаксел + трастузумаб + пертузумаб (план адъювантной терапии не был выполнен);
проведения двойной анти-HER2-терапии с гормонотерапией первой линии, аналог ЛГРГ + ингибиторы ароматазы.
В качестве компромиссного решения, с приоритетным сохранением высокого качества жизни, выбрана терапия в режиме: винорелбин в капсулах (60 мг/м2 внутрь 1 раз в 7 дней первые 3 нед., после оценки переносимости эскалация дозы до 80 мг/м2 еженедельно) + таргетная терапия трастузумабом. Пертузумаб не использован в связи с повышенным риском диареи. Лечение в данном режиме было начато в декабре 2021 г. Значимых нежелательных явлений зарегистрировано не было, периодически отмечалась небольшая слабость (1-й степени), доза винорелбина, согласно рекомендациям, была эскалирована до 80 мг/м2, нежелательных явлений не отмечено.
В январе — феврале 2022 г. лечение было прервано на 4 нед. в связи с COVID-19 среднетяжелого течения, с двусторонним поражением паренхимы легких до 40%. После стихания симптомов противоопухолевая системная терапия возобновлена в прежнем режиме. Несмотря на перерыв, при контрольном обследовании в апреле 2022 г. (ПЭТ-КТ) ранее выявленный лимфатический узел корня левого легкого сократился в размерах до 14×9 мм (-37%), без признаков патологического накопления радиофармпрепарата. В паренхиме легких с двух сторон сохраняются поствоспалительные изменения в фазе неполной репарации, новых метастатических очагов не выявлено (рис. 6).
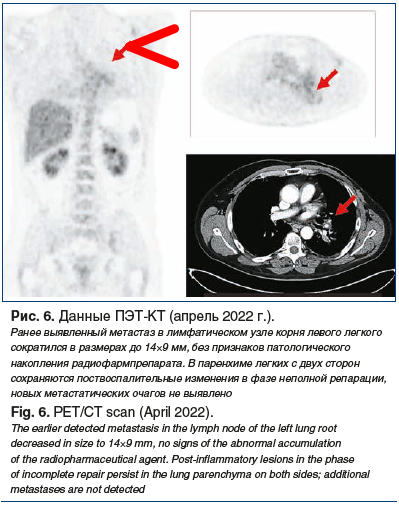
В представленном клиническом примере пациент в течение последних 6 мес. получает эффективную терапию: винорелбин (Навельбин капсулы) + таргетная терапия трастузумабом. Проводимая терапия хорошо переносится, пациент ведет активный образ жизни.
На данный момент клинических признаков прогрессии болезни не отмечено. В случае сохранения достигнутого эффекта при очередном контрольном обследовании, учитывая олигометастатический характер болезни, планировалось обсуждение локального лучевого воздействия на лимфатический узел корня левого легкого (данные ASCO 2022).
Итак, у пациента с HER2+ РМЖ с ранее проведенной неоадъювантной гормонотерапией, адъювантной ХТ + таргетной терапией, адъювантной гормонотерапией и ранним прогрессированием после окончания адъювантной терапии трастузумабом, с крайне тяжелой переносимостью ХТ в анамнезе комбинация Навельбин капсулы и трастузумаб в первой линии терапии обеспечила частичный ответ, время без прогрессирования болезни более 6 мес. и высокое качество жизни.
Заключение
При терапии мРМЖ основной целью становится не только эффективность, но и в большей мере качество жизни пациента. При сопоставимой эффективности лечения пациенты предпочитают пероральную форму, которая позволяет им сохранить привычный образ жизни. Винорелбин капсулы по эффективности терапии сопоставим с таксанами и обеспечивает длительный контроль заболевания, предоставляя пациентам все преимущества пероральной формы. Таким образом, винорелбин является хорошим выбором для первой линии химиотерапии при мРМЖ.
Сведения об авторах:
Артамонова Елена Владимировна — д.м.н., заведующая отделением химиотерапии № 1 ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России; 115522, Россия, г. Москва, Каширское ш., д. 24; профессор кафедры онкологии и лучевой терапии РНИМУ им. Н.И. Пирогова Минздрава России; 117321, Россия, г. Москва, ул. Островитянова, д. 1; заведующая кафедрой онкологии и торакальной хирургии ФПК ГБУЗ МО МОНИКИ им. М.Ф. Владимирского; 129110, Россия, г. Москва, ул. Щепкина, д. 61/2; ORCID iD 0000-0001-7728-9533.
Ткаченко Елена Викторовна — к.м.н., заведующая отделением краткосрочной химиотерапии ФГБУ «НМИЦ онкологии им Н.Н. Петрова» Минздрава России; 197758, Россия, г. Санкт-Петербург, пос. Песочный, ул. Ленинградская, д. 68; ORCID iD 0000-0001-6375-8335.
Фрейер Жиль — профессор, отделение медицинской онкологии Онкологического института группы паллиативных учреждений; 69006, Франция, г. Лион, наб. Шарля де Голля, д. 200; ORCID iD 0000-0001-6001-164X.
Чернядьева Светлана Николаевна — врач-онколог отделения химиотерапии № 1 КОГКБУЗ «Центр онкологии и медицинской радиологии»; 610045, Россия, г. Киров, пр-т Строителей, д. 23.
Контактная информация: Артамонова Елена Владимировна, e-mail: artamonovae@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 01.08.2022.
Поступила после рецензирования 17.08.2022.
Принята в печать 24.08.2022.
About the authors:
Elena V. Artamonova — Dr. Sc. (Med.), Head of Department of Chemotherapy No. 1, N.N. Blokhin National Medical Research Center of Oncology; 24, Kashirskoe road, Moscow, 115478, Russian Federation; Professor of the Department of Oncology and Radiation Therapy, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; Head of the Department of Oncology and Thoracal Surgery, M.F. Vladimirskiy Moscow Regional Research and Clinical Institute; 61/2, Shchepkin str., Moscow, 129110, Russian Federation; ORCID iD 0000-0001-7728-9533.
Elena V. Tkachenko — C. Sc. (Med.), Head of the Department of Short-Course Chemotherapy, N.N. Petrov National Medical Research Center of Oncology; 68, Leningradskaya str., settl. Pesochny, Saint Petersburg, 197758, Russian Federation; ORCID iD 0000-0001-6375-8335.
Gilles Freyer — Professor, Medical Oncology Department, Centre Hospitalier Lyon Sud, 200 Quai Charles de Gaulle, 69006, Lyon, France; ORCID iD 0000-0001-6001-164X.
Svetlana N. Chernyad’eva — Oncologist, Chemotherapy Department No. 1, Center of Oncology and Medical Radiology; 23 Stroiteley av., Kirov, 610045, Russian Federation.
Contact information: Elena V. Artamonova, e-mail: artamonovae@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 01.08.2022.
Revised 17.08.2022.
Accepted 24.08.2022.
Информация с rmj.ru