Введение
Одно из фундаментальных свойств всех организмов — это способность тканей к их восстановлению после повреждения [1]. У взрослых людей, в отличие от плода (до 24 нед. гестации), кожные раны заживают в виде рубцов [2]. В рубцовой ткани снижается биомеханическая и физиологическая функциональность из-за изменения клеточного состава и строения внеклеточного матрикса, в частности изменения строения и расположения коллагеновых волокон [3].
Репарация раны — хорошо организованный процесс с участием клеточных и внеклеточных компонентов [4]. При этом клетки формируют внеклеточный матрикс, а внеклеточный матрикс активно контролирует форму, поведение и функции клеток. Поэтому внеклеточный матрикс играет фундаментальную роль в точно регулируемом восстановлении тканей у взрослых людей и является ключевым элементом, определяющим эффективность и степень выраженности процесса восстановления [5]. Взаимодействие фибробластов с внеклеточным матриксом осуществляется по типу аутокринной регуляции, которая имеет решающее значение в процессе заживления ран. Фибробласт должен постоянно создавать новые матриксные белки для надлежащего заживления кожной раны, одновременно регулируясь белками собственного производства [6]. Можно выделить следующие факторы, формирующие гипертрофические и келоидные рубцы: чрезмерная выработка коллагена и других компонентов внеклеточного матрикса; потеря или подавление ключевых стоп-сигналов; дисфункция в разрешении и подавлении деградирующих ферментов, участвующих в ремоделировании грануляционной ткани [5].
Частота развития гипертрофических рубцов, по данным разных авторов, варьирует от 15 до 70% после хирургических вмешательств [7–9]. Одним из важных факторов прогнозирования гипертрофических рубцов является время полного заживления: уменьшение времени снижает вероятность гипертрофических рубцов [10].
Ранее основные исследования по заживлению ран были больше сконцентрированы на клеточном компоненте, новые исследования отводят центральное место внеклеточному матриксу в управлении фенотипами клеток в процессе репарации [11].
В настоящее время предложено множество способов для контроля и улучшения заживления после повреждения кожи, включая применение инвазивных (инъекции тромбоцитарной плазмы, ботулинического токсина типа А, глюкокортикостероидов (ГКС), 5-фторурацила, интерферона и блеомицина) и неинвазивных методов (лазерная терапия, кремы с факторами роста и цитокинами, силиконами) [10, 12, 13]. Однако «золотого стандарта» на сегодняшний день нет, что связано как с неполным представлением о точке приложения разных методов и недостатком проспективных исследований, так и с некоторыми побочными эффектами применения препаратов. Так, применение ГКС может привести к боли и атрофии окружающих тканей, телеангиоэктазиям, остеопорозу. Ряд авторов считают, что они должны быть отнесены к препаратам второй линии (когда более простые методы неэффективны) [14, 15].
Компоненты внеклеточного матрикса кожи обеспечивают взаимодействие между различными клетками из-за своего специфического трехмерного расположения. Такое взаимодействие влияет на прикрепление, миграцию, дифференциацию и морфогенетические признаки. Нарушение структуры внеклеточного матрикса снижает его регулирующую и репарационную роль, что приводит к нарушению рубцевания [16].
Одним из перспективных методов контроля и улучшения репарации раны является применение коллагена. Так, на ранних сроках заживления ран коллаген способствует интенсивной пролиферации стволовых клеток эпидермиса и фибробластов с дальнейшей обратимой дифференцировкой фибробластов в миофибробласты, способствуя сужению раны. Также было показано, что коллаген стимулирует миграцию клеток и ускоряет заживление. При гистологическом исследовании было отмечено, что на 8-й день в группе с применением коллагена обнаружено меньше воспалительных клеток, а к 13-му дню — больший ангиогенез (в сравнении с группой с применением физиологического раствора) [17]. Коллаген действует как естественный субстрат для прикрепления клеток, он может опосредовать множество физиологических взаимодействий, способствующих регенерации, во время сложного процесса заживления ран, начиная от ангиогенеза и заканчивая реэпителизацией [18].
Примерами препаратов на основе нативного коллагена являются медицинские изделия, содержащие коллаген I типа нативный нереконструированный, — КОЛЛОСТ® гель 7 и 15% («БиоФАРМАХОЛДИНГ», Россия), на основе фибрилл коллагена [19]. Далее мы рассмотрим клинические наблюдения применения данного препарата у пациенток на разных стадиях заживления раны после травмы и после оперативного вмешательства (письменное согласие пациенток на публикацию получено).
Клиническое наблюдение 1
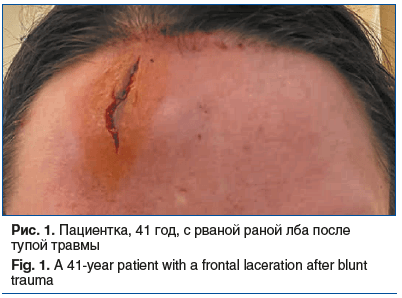
Пациентка, 41 год, обратилась с рваной раной лба после тупой травмы (рис. 1). Хирургом был наложен шов. На второй день после травмы (рис. 2) было инъецировано медицинское изделие, содержащие коллаген I типа нативный нереконструированный 7%, по краям раны и вдоль шва.
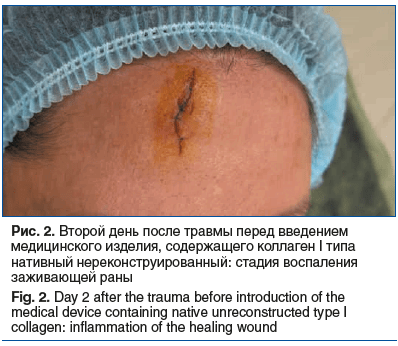
На 17-е сутки после травмы видна образовавшаяся грануляционная ткань без признаков избыточного воспаления (рис. 3). Была выполнена 2-я процедура введения медицинского изделия по краям и в центре заживающей раны для создания условий миграции фибробластов.
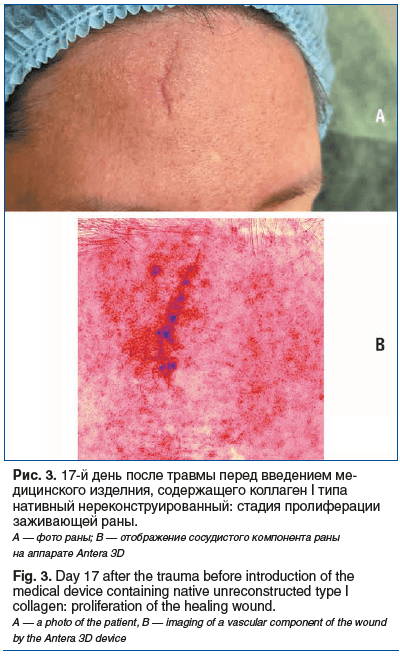
На 34-е сутки после травмы рана находится в стадии ремоделирования: образовавшаяся ранее грануляционная ткань замещается постоянным матриксом (рис. 4). Была выполнена 3-я процедура введения медицинского изделия, содержащего коллаген I типа нативный нереконструированный, по краям и в центре заживающей раны.
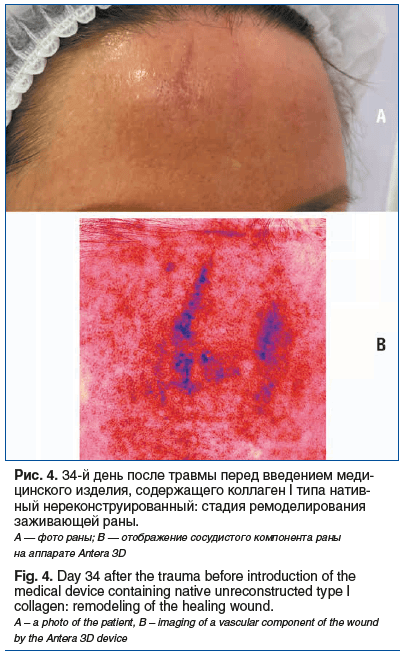
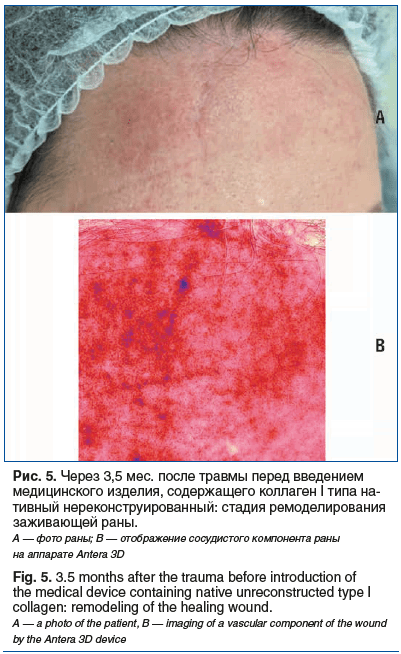
В настоящее время проведено 4 процедуры лечения раны медицинским изделием, содержащим коллаген I типа нативный нереконструированный. При осмотре раны через 3,5 мес. после получения травмы (перед 4-й процедурой) отмечено значительное улучшение состояния раны без признаков воспаления, цвет близкий к окружающим тканям (рис. 5). В настоящее время пациентка находится под наблюдением.
Клиническое наблюдение 2
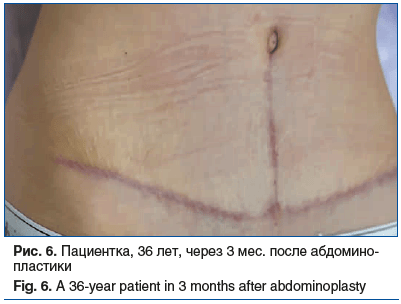
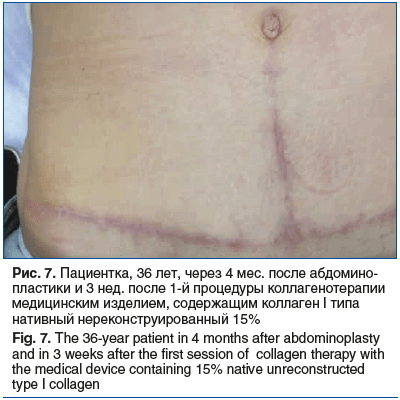
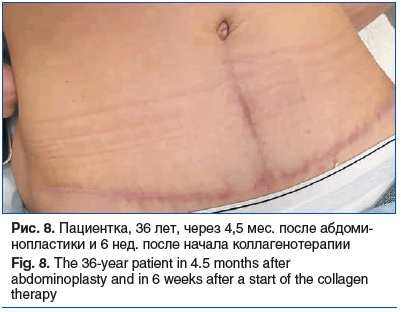
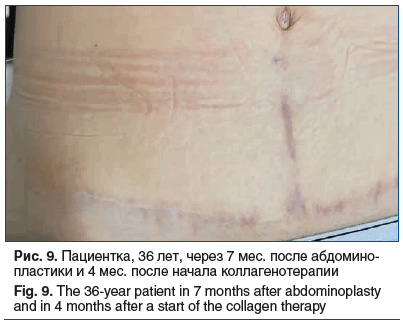
Пациентка, 36 лет, через 3 мес. после абдоминопластики обратилась с жалобами на зуд, «стягивание» и уплотнение в области послеоперационного рубца (рис. 6). Пациентке было инъецировано медицинское изделие, содержащее коллаген I типа нативный нереконструированный 15%, интрарубцово на протяжении всего рубца. Через неделю пациентка отметила отсутствие зуда и ощущения «стягивания» в области рубца. При осмотре через 3 нед. отмечено уменьшение плотности рубца и небольшое снижение интенсивности покраснения (рис. 7). Через 3 нед. после 1-й процедуры было выполнено следующее введение медицинского изделия, содержащего коллаген I типа нативный нереконструированный 7%, еще через 3 нед. выполнена 3-я процедура введения медицинского изделия, содержащего коллаген I типа нативный нереконструированный 7% (рис. 8), и через 4 мес. после начала лечения (рис. 9) проведена 4-я процедура введения медицинского изделия, содержащего коллаген I типа нативный нереконструированный 7%. При осмотре через 4 мес. после начала лечения отмечено значительное улучшение состояния рубца: снижение плотности, уменьшение интенсивности окраски. В настоящее время пациентка находится под наблюдением.
Обсуждение
Проблема гипертрофических рубцов остается чрезвычайно актуальной. Несмотря на большое количество работ по данной тематике, единого «золотого стандарта» лечения и профилактики нет. Однако можно отметить смещение фокуса внимания с применения ГКС (как монотерапии) в сторону методик, в целом улучшающих регенерацию, а также переключение основного внимания с клеточных компонентов процесса репарации в сторону внеклеточного матрикса [10–15].
Одним из относительно новых направлений тактики ведения пациентов является применение инъекционных медицинских изделий на основе коллагена. На клеточных культурах (в присутствии коллагена) была показана стимуляция миграции клеток, ускорение заживления, менее выраженное воспаление и более эффективный ангиогенез [17].
В другом исследовании на модели экспериментальных животных (крысы) было показано снижение выраженности воспаления, улучшение ангиогенеза и уменьшение сроков репарации при внутрикожном введении и введении в полость раны медицинского изделия КОЛЛОСТ® гель 7% [20].
В представленных клинических наблюдениях отмечена эффективность применения медицинского изделия КОЛЛОСТ® гель 7 и 15% на разных сроках после операции и после травмы. Данные экспериментального исследования на животных не могут полностью служить обоснованием использования изделия у человека. Однако медицинское изделие КОЛЛОСТ® гель 7% имеет большую доказательную базу применения у пациентов, по данным исследований было отмечено улучшение состояния внеклеточного матрикса [21, 22]. В любом случае возможность применения коллагенотерапии для улучшения репарации кожи после хирургических вмешательств нуждается в дополнительных исследованиях для создания четких алгоритмов применения.
Заключение
Коллаген служит основным компонентом внеклеточного матрикса кожи. Он участвует в ряде физиологических процессов, способствующих регенерации в ходе сложного процесса заживления ран. Применение коллагена является перспективным направлением исследований в сфере регенерации ран в связи с рядом преимуществ. Так, применение коллагена не связано с побочными эффектами, наблюдаемыми при использовании ГКС (боль и атрофия кожи, телеангиоэктазии). Также коллаген не только действует на рубцовую ткань, но и улучшает регенерацию окружающих тканей. Дополнительным преимуществом является доступность препарата в сравнении с новейшими разработками в сфере заживления ран (генно-модифицированные технологии, использование стволовых клеток и др.). В клинических наблюдениях продемонстрирована эффективность применения препаратов на основе нативного коллагена для контроля и улучшения заживления ран после травмы и операции.
Сведения об авторах:
Борзых Ольга Борисовна — д.м.н., врач дерматолог, косметолог ООО «Артис»; 394030, Россия, г. Воронеж, ул. Пролетарская, д. 87; ORCID iD 0000-0002-3651-4703
Петрова Марина Михайловна — д.м.н., профессор, заведующая кафедрой поликлинической терапии и семейной медицины с курсом ПО ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-Ясенецкого Минздрава России; 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; ORCID iD 0000-0002-8493-0058
Шнайдер Наталья Алексеевна — д.м.н., профессор, главный научный сотрудник, заместитель руководителя Института персонализированной психиатрии и неврологии, ФГБУ «НМИЦ ПН им. В.М. Бехтерева» Минздрава России; 192019, Россия, г. Санкт-Петербург, ул. Бехтерева, д. 3; ведущий научный сотрудник центра коллективного пользования «Молекулярные и клеточные технологии» ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-Ясенецкого Минздрава России; 660022, Россия, г. Красноярск, ул. Партизана Железняка, д. 1; ORCID iD 0000-0002-2840-837X
Данилова Светлана Витальевна — к.м.н., врач дерматолог, косметолог, физиотерапевт ООО «Параллелепипед»; 119049, Россия, г. Москва, Якиманский пер., д. 6; ORCID iD 0009-0001-4549-7749
Контактная информация: Борзых Ольга Борисовна, e-mail: kurumchina@mail.ru
Источник финансирования: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 10.03.2025.
Поступила после рецензирования 02.04.2025.
Принята в печать 25.04.2025.
About the authors:
Olga B. Borzykh — D. Sc. (Med.), Dermatologist, Cosmetologist, Artis LLC; 87, Proletarskaya str., Voronezh, 394030, Russian Federation; ORCID iD 0000-0002-3651-4703
Marina M. Petrova — D. Sc. (Med.), Professor, Head of the Department of Outpatient Therapy and General Practice with a PE course, Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University; 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0002-8493-0058
Natalia A. Sсhnayder — D. Sc. (Med.), Professor, Chief Researcher, Deputy Head of the Institute of Personalized Psychiatry and Neurology, V.M. Bekhterev National Medical Research Center for Psychiatry and Neurology; 3, Bekhterev str., St. Petersburg, 192019, Russian Federation; Leading Researcher of the Center of Collective Usage «Molecular and Cellular Technologies», Prof. V.F. Voino-Yasenetsky Krasnoyarsk State Medical University; 1, Partizan Zheleznyak str., Krasnoyarsk, 660022, Russian Federation; ORCID iD 0000-0002-2840-837X
Svetlana V. Danilova — C. Sc. (Med.), Dermatologist, Cosmetologist, Physiotherapist, Parallelepiped LLC; 6, Yakimansky lane, Moscow, 119049, Russian Federation; ORCID iD 0009-0001-4549-7749
Contact information: Olga B. Borzykh, e-mail: kurumchina@mail.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 10.03.2025.
Revised 02.04.2025.
Accepted 25.04.2025.
Информация с rmj.ru






