ведение
Несмотря на широкое применение профилактических мероприятий, туберкулез (ТБ) в XXI в. сохраняет свою актуальность.
Стоит отметить, что ТБ входит в так называемую инфекционную триаду «лидеров» (наравне с ВИЧ-инфекцией и вирусным гепатитом С) по уровню смертности населения и экономического ущерба, наносимого государству. Только в 2021 г. бюджет России потерял свыше 380 млрд рублей в связи с вышеупомянутыми инфекциями [1].
Несмотря на ежегодно затрачиваемые колоссальные финансовые ресурсы, которые выделяются на борьбу с ВИЧ-инфекцией, вирусным гепатитом С и ТБ, эпидемиологические индикаторы при стабильном снижении уровней заболеваемости и смертности [2, 3] последнего продолжают вызывать озабоченность, особенно относительно детско-подросткового контингента [4].
По данным ВОЗ, в 2022 г. количество заболевших ТБ в возрасте до 15 лет составило около 1,3 млн человек. В 2022 г. количество умерших от ТБ ВИЧ-негативных детей составило приблизительно 183 тыс. [5].
Как было упомянуто, в настоящий момент на территории РФ отмечается устойчивая тенденция к снижению эпидемиологической напряженности по ТБ среди детско-подросткового контингента. В то же время среди детей раннего возраста (до 1 года жизни) в 2021 г. на территории РФ уровень заболеваемости вырос на 26,62% [1]. По данным Роспотребнадзора, в 2021 г. на территории РФ часть регионов задекларировала увеличение числа заболевших ТБ детей по сравнению с предыдущим периодом. В 2022 г. отмечен небольшой, но значимый рост заболеваемости ТБ в возрастной группе 7–14 лет, по всей видимости, связанный с увеличением контакта в очагах инфекции во время пандемии COVID-19, а также активными миграционными потоками с территорий с высокой заболеваемостью ТБ [6].
Настороженность вызывает постепенное увеличение доли детей, больных ТБ с лекарственной устойчивостью (ЛУ) возбудителя [7]. Лечение детей и подростков с ЛУ ТБ характеризуется определенными трудностями в связи с ограниченными возможностями применения некоторых противотуберкулезных препаратов, недостаточной приверженностью химиотерапии (ХТ), анатомо-физиологическими особенностями детского организма. Исходя из этого, немаловажное значение в комплексном лечении больных ТБ занимает адекватная диетотерапия.
Потребности ребенка в энергии и нутриентах при пересчете на массу тела выше, чем у взрослых. Особенно это выражено в периоды так называемых скачков роста — в возрасте до 1 года и в период пубертата. При этом присутствие в организме ребенка специфического микроорганизма и развитие инфекционно-воспалительного процесса способствуют дезадаптации, истощению и нарушению роста. Поэтому очень важно обеспечивать ребенка, больного ТБ, достаточным количеством энергии, макро- и микроэлементами, особенно в период болезни.
Общепризнано, что усиленное питание является важным фактором, определяющим клинический исход при ТБ. Для ТБ, как и для многих других инфекций, характерно формирование порочного круга, когда гиперкатаболическое состояние и снижение поступления нутриентов по причине потери аппетита, нарушения процессов переваривания и всасывания, диареи и тошноты, других метаболических нарушений приводит к недостаточному поступлению макро- и микронутриентов на фоне повышенной потребности в них, усилению недостаточности питания, снижению реактивности иммунной системы и усугублению инфекционного процесса. В связи с этим не всегда удается гарантированно компенсировать возросшие потребности детей в белке и энергии, не прибегнув к специализированным способам нутритивной поддержки.
Цель исследования: оценить в условиях реальной клинической практики влияние дополнительной нутритивной поддержки (ДНП) на нутритивный статус детей с ТБ, которым была начата ХТ, а также возможное влияние ДНП на эффективность и переносимость ХТ.
Материал и методы
В двух клинических центрах — отделении для больных ТБ органов дыхания (детском) ГБУЗ НО «НОКПД» (г. Нижний Новгород) и отделении для детей, больных ТБ органов дыхания, ГБУЗ АО «Областной клинический противотуберкулезный диспансер» (г. Астрахань) проведено ретроспективно-проспективное несплошное когортное поперечное (период наблюдения с 07.08.2022 по 02.11.2023) исследование. В исследование включали детей, удовлетворяющих критериям включения. Исследование проводилось в соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации. Пациенты (их законные представители), участвовавшие в исследовании, подписывали добровольное информированное согласие.
Критерии включения: дети в возрасте от 1 года до 10 лет (включительно) с подтвержденным диагнозом ТБ легких, отсутствие других тяжелых заболеваний, недостаточная масса тела I–III степени (-2 < Z-score < -1, -3 < Z-score < -2 и Z-score < -3).
Критерии исключения: тяжелые сопутствующие заболевания, внелегочная локализация ТБ, распространенный ТБ, неинфекционная природа поражения легких, непереносимость любого компонента продукта ДНП, включая аллергию к белкам коровьего молока.
Пациенты, которые удовлетворяли критериям включения, составили основную группу (проспективная группа). Пациенты данной группы помимо сбалансированной госпитальной диеты, подобранной индивидуально на основании рекомендаций лечащего врача, получали ДНП гиперкалорийной полимерной смесью с пищевыми волокнами «PediaSure Здоровейка» («Эбботт Лэбораториз», Голландия) в количестве 100 мл 2 р/сут ежедневно (300 ккал/сут).
В группу сравнения (ретроспективная группа) вошли пациенты, которые соответствовали исходным характеристикам пациентов, включенных в основную группу, и были отобраны на основании анализа медицинской документации. Дети данной группы получали сбалансированную госпитальную диету, рассчитанную индивидуально, и не получали продукты ДНП.
Было запланировано 2 обследования (две временные точки для ретроспективной группы) — в момент включения в исследование и через 3 мес. (±5 дней). Оценивали следующие показатели: массу тела пациента, рост, толщину кожной складки в подлопаточной области (ТКСПЛ), индекс массы тела (ИМТ) с конвертацией в Z-score, уровень гемоглобина, общего белка в крови, удельный вес мочи, переносимость ХТ и переносимость продукта ДНП (по данным законного представителя и медицинского персонала, ведущего уход за ребенком).
Статистический анализ данных осуществляли с помощью программного обеспечения IBM SPSS Statistics 27 64-bit (IBM Corp., США). Соответствие выборок нормальному распределению оценивали с помощью критериев Шапиро — Уилка, асимметрии (As) и эксцесса (E), построения графика квантилей (Q-Q plot). При неподчинении полученных показателей закону нормального (Гауссова) распределения использовали непараметрические критерии анализа.
Нормально распределенные данные представлены в виде среднего, стандартного отклонения и 95% доверительного интервала (ДИ) (M±SD (95% ДИ)), непараметрически распределенные показатели — в виде медианы и нижнего и верхнего квартилей (Me [Q1; Q3]). Возраст представлен в виде медианы и разброса показателя (Me (min–max)). Качественные показатели представлены в виде P±σp (95% ДИ), где P — процентная доля, σp — стандартное отклонение процентной доли.
Оценку статистической значимости различий между группами (количественные данные) проводили с помощью U-критерия Манна — Уитни (U-test), критерия Уилкоксона (W), непарного и парного t-критериев Стьюдента.
Для выявления статистических различий (качественные данные) между выборками применяли таблицы сопряженности, критерий χ2 Пирсона, критерий χ2 Пирсона с поправкой на правдоподобие, гамма (γ)-критерий Гудмана — Краскела и отношение шансов (ОШ) с расчетом его 95% ДИ. Расчет ДИ для частот осуществляли с помощью метода Клоппера — Пирсона.
Уровень статистической значимости различий при проверке гипотез (р) был ≤0,05.
Результаты исследования
В период с 07.08.2022 по 02.11.2023 под наблюдением в клинических центрах находились 49 детей с установленным диагнозом ТБ легких, критериям включения соответствовали 26 детей, из них в основную группу было включено 23 ребенка. Трое детей не были включены в исследуемую группу в связи с отказом родителей от подписания добровольного информированного согласия. В группу сравнения было отобрано 20 детей, которые соответствовали основным характеристикам пациентов основной группы и имели подписанное добровольное информированное согласие.
Все дети получали ХТ как по режиму лечения для лекарственно-чувствительного ТБ (не менее 60 доз или 60 дней терапии), так и по режиму лечения ТБ с множественной ЛУ (не менее 180 доз или 180 дней терапии).
Основные демографические характеристики пациентов приведены в таблице 1.
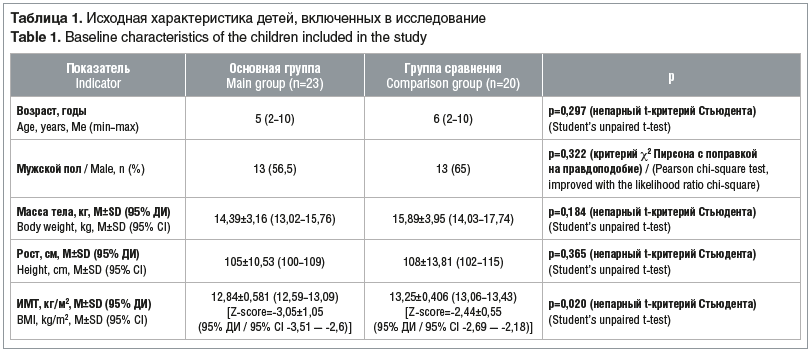
За 3 мес. в обеих группах отмечено увеличение основных антропометрических показателей. При этом в основной группе констатировали статистически значимое увеличение всех изученных антропометрических показателей по сравнению с исходными, в то время как у детей группы сравнения достоверно увеличились масса тела, рост, ИМТ, но уменьшилась ТКСПЛ (табл. 2).
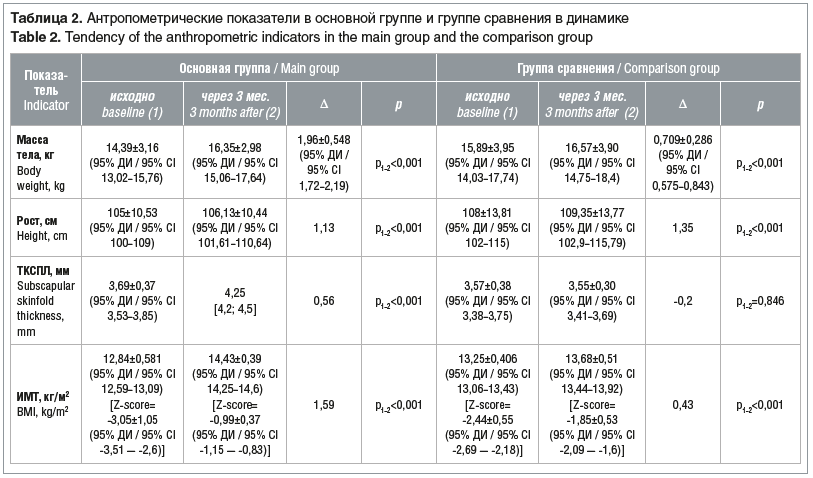
Прием ДНП был связан с более выраженным увеличением ИМТ. Так, отсутствие приема специализированной смеси увеличивало риск снижения ИМТ на 98,4% (γ-критерий=-0,984, p<0,001). При сравнении двух показателей: прибавка в массе тела и прием специализированной смеси — ОШ 7,333 (95% ДИ 11,889–13,264), что подтверждает гипотезу о влиянии специализированной смеси на стабилизацию ИМТ (шанс нормализации ИМТ был выше в 7,3 раза среди детей основной группы, получавших ДНП).
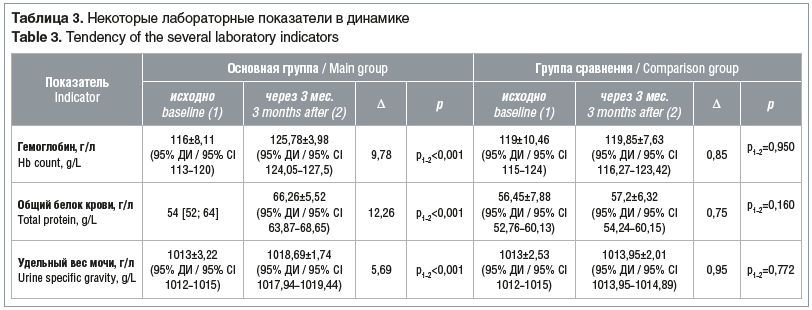
Кроме антропометрических показателей мы оценили влияние ДНП на уровни гемоглобина, общего белка крови и удельную плотность мочи. В группе ДНП все указанные показатели значимо улучшились через 3 мес. наблюдения, в то время как в группе сравнения показатели статистически значимо не изменились (табл. 3).
Переносимость ХТ
По прошествии 3 мес. лечения среди пациентов основной группы неудовлетворительная переносимость (рвота, жидкий стул, диспепсия и пр.) ХТ была зарегистрирована только у 4 (17,4±7,9% (95% ДИ 6,2–36,2)) детей, удовлетворительная (без каких-либо побочных эффектов) — у 19 (82,6±7,9% (95% ДИ 63,8–93,8)) детей, среди пациентов группы сравнения — у 14 (70%±10,2 (95% ДИ 48,3–86,4)) и у 6 (30%±10,2 (95% ДИ 13,6–51,7)) детей соответственно.
При сравнении двух групп по признаку переносимости ХТ были обнаружены статистически значимые различия (χ2=43, df=3, p<0,001). Использование в рационе диетического питания специализированной смеси уменьшало риск развития побочных реакций при ежедневном приеме ХТ на 65,2% (γ-критерий=0,652, p<0,001).
Переносимость специализированной смеси у подавляющего большинства пациентов — 91,3±5,9% (95% ДИ 74,9–98,1) оценена удовлетворительно (без каких-либо нареканий), лишь у 2 (8,7±5,9% (95% ДИ 1,9–25,1)) детей — неудовлетворительно. У одного пациента периодически отмечались аллергические проявления и до начала ДНП, полностью связать их с приемом данного продукта не представляется возможным, но при отмене продукта аллергические кожные проявления уменьшились; один ребенок отказался от приема ДНП из-за вкусовых предпочтений.
Наша работа продемонстрировала, что ДНП специализированной полимерной гиперкалорийной смесью, которая вводилась дополнительно к госпитальной лечебной диете, была более эффективна, чем только диета, причем не только в отношении улучшения нутритивного статуса детей (ИМТ в первую очередь), получавших ХТ, но и улучшения переносимости последней.
Обсуждение
Высокий риск неудачи ХТ, смерти и инфицирования ЛУ ТБ связан с тяжестью заболевания, коинфицированием ВИЧ, а также недостаточностью питания. В недавно опубликованном метаанализе [8] продемонстрировано, что недостаточность питания в 3 раза снижает вероятность терапевтического успеха ХТ ТБ. Учитывая растущую распространенность ЛУ ТБ в РФ, важно отметить, что у детей с такой формой ТБ наличие даже незначительной недостаточности питания (Z-score масса тела / возраст <-1) было значимым предиктором смерти или неудачи терапии [9]. При этом даже удачная ХТ ТБ не улучшает нутритивный статус ребенка c недостаточностью питания, поэтому организация нутритивной поддержки для таких пациентов может рассматриваться как необходимый компонент активного лечения ТБ [10].
Интересно, что опубликованные систематические обзоры и метаанализы не находят четкой связи между клиническими исходами ТБ (излечение или смерть) через 6 и 12 мес. после начала предоставления еды бесплатно, или гиперкалорийного дополнительного питания, или мультивитаминов [11]. Вероятно, это связано с большим разнообразием оцениваемых подходов влияния на недостаточность питания. При этом авторы отмечают, что при оценке влияния только дополнительного гиперкалорийного питания (в отличие от приема мультивитаминов) оно, несомненно, оказывает положительное влияние на набор массы тела, и это было связано с положительными клиническими исходами. В систематическом обзоре, сравнивавшем предоставление ДНП с отсутствием ДНП, было показано положительное влияние ДНП на прекращение бактериовыделения и положительную рентгенологическую динамику у взрослых пациентов с ТБ легких, и это было связано напрямую с увеличением ИМТ [12]. Несмотря на то, что в нашем исследовании мы не оценивали клинические исходы ТБ, мы продемонстрировали, что достижение нормативного уровня ИМТ происходило в 7 раз чаще в группе детей, получавших ДНП гиперкалорийной полимерной смесью, чем в группе детей, ее не получавших.
Второй важный момент, который определяет эффективность ХТ, — это ее переносимость. Плохая переносимость ХТ связана с низкой приверженностью лечению пациентов и их родителей/опекунов, более высокой вероятностью смерти или развития ЛУ ТБ [13]. Нежелательные явления со стороны ЖКТ — самые распространенные НЯ, связанные с ХТ ТБ. ДНП с помощью специализированной смеси, содержащей нерастворимые пищевые волокна, уменьшало риск развития побочных реакций при ежедневном приеме противотуберкулезных препаратов на 65,2% (γ-критерий=0,652, p<0,001). Похожие результаты были продемонстрированы в других исследованиях данной смеси у детей с выраженной недостаточностью питания [14].
Наше исследование имело некоторые ограничения, которые необходимо принимать во внимание при оценке его результатов. В первую очередь это наблюдательный проспективно-ретроспективный характер, достаточно небольшая выборка, отсутствие оценки клинических исходов, а также оценки суточного поступления энергии и макронутриентов в основной группе и группе сравнения. При этом мы наблюдали за детьми достаточно продолжительный промежуток времени, оценивали переносимость ХТ и специализированной смеси в условиях реальной клинической практики в двух разных клинических центрах, расположенных в разных климатических зонах. Поэтому полученные результаты с большой долей вероятности могут быть подтверждены в лечебных учреждениях схожего профиля.
Заключение
Применение ДНП специализированной гиперкалорийной полимерной смесью, содержащей нерастворимые пищевые волокна, оказывает достоверное положительное влияние на нутритивный статус (масса тела, рост, ИМТ) детей с недостаточностью питания, получавших активную ХТ ТБ. Кроме антропометрических показателей, ДНП специализированным продуктом способствовала статистически значимому увеличению уровней гемоглобина и общего белка крови, нормализации удельного веса мочи в отличие от группы сравнения, где эти показатели достоверно не улучшились. При хорошей переносимости специализированного продукта продемонстрировано уменьшение риска развития побочных реакций при ежедневном приеме ХТ на 65,2% в группе ДНП в сравнении с группой, не получавшей ДНП. Данные результаты говорят в пользу назначения ДНП всем детям с недостаточностью питания и ТБ, особенно начинающим ХТ.
Благодарность
Авторы статьи выражают благодарность за помощь в исследовании и подготовке статьи: Швец Ю.А. — студентке 6-го курса педиатрического факультета ФГБОУ ВО «ПИМУ» Минздрава России, Наумовой Т.А. — студентке 3-го курса юридического факультета Нижегородского государственного университета им. Н.И. Лобачевского, Лещиловской А.А. — практическому психологу, Лещиловскому Е.М. — журналисту.
Сведения об авторах:
Барболина Светлана Федоровна — ассистент кафедры фтизиатрии им. И.С. Николаева ФГБОУ ВО «ПИМУ» Минздрава России; 603005, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; врач-фтизиатр высшей категории детского отделения ГБУЗ НО «НОКПД»; Россия, г. Нижний Новгород, ул. Родионова, д. 198.
Наумов Алексей Георгиевич — ассистент кафедры фтизиатрии им. И.С. Николаева ФГБОУ ВО «ПИМУ» Мин-здрава России; 603005, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; врач-фтизиатр первой категории терапевтического отделения ГБУЗ НО «НОКПД»; Россия, г. Нижний Новгород, ул. Родионова, д. 198; ORCID iD 0000-0003-0412-6877.
Овчинникова Ольга Александровна — врач-диетолог ГБУЗ АО «Областной клинический противотуберкулезный диспансер»; 414004, Россия, г. Астрахань, Началовское ш., д. 7.
Бикбаев Рафаэль Ришатович — заведующий стационарным отделением № 3 ГБУЗ АО «Областной клинический противотуберкулезный диспансер»; 414004, Россия, г. Астрахань, Началовское ш., д. 7.
Контактная информация: Барболина Светлана Федоровна, e-mail: svetlanabarbolina@yandex.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 10.11.2023.
Поступила после рецензирования 23.11.2023.
Принята в печать 30.11.2023.
About the authors:
Svetlana F. Barbolina — Assistant Professor of the I.S. Nikolaev Department of Phthisiology, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky Square, Nizhny Novgorod, 603005, Russian Federation; phthisiologist of the highest category of the Children’s Department, Nizhny Novgorod Regional Clinical Tuberculosis Dispensary; 198, Rodionova str., Nizhny Novgorod, 603163, Russian Federation.
Alexey G. Naumov — Assistant Professor of the I.S. Nikolaev Department of Phthisiology Privolzhsky Research Medical University; 10/1, Minin and Pozharsky Square, Nizhny Novgorod, 603005, Russian Federation; phthisiologist of the first category of the Therapeutic Department, Nizhny Novgorod Regional Clinical Tuberculosis Dispensary; 198, Rodionova str., Nizhny Novgorod, 603163, Russian Federation; ORCID iD 0000-0003-0412-6877.
Olga A. Ovchinnikova — nutritionist, Regional Clinical Tuberculosis Dispensary; 7, Nachalovskoe High Road, Astrakhan, 414004, Russian Federation.
Rafael R. Bikbaev — Head of Inpatient Department No. 3, Regional Clinical Tuberculosis Dispensary; 7, Nachalovskoe High Road, Astrakhan, 414004, Russian Federation.
Contact information: Svetlana F. Barbolina, e-mail: svetlanabarbolina@yandex.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 10.11.2023.
Revised 23.11.2023.
Accepted 30.11.2023.
Информация с rmj.ru






