Содержание статьи
Введение
Мочевая кислота (МК) является конечным продуктом метаболизма пуриновых оснований, и ее концентрация в крови может увеличиваться у людей, человекообразных обезьян и некоторых видов собак в результате произошедших в процессе эволюции генетических мутаций [1]. Повышение уровня МК в сыворотке крови выше 7 мг/дл (420 мкмоль/л) у мужчин и женщин после менопаузы и выше 6 мг/дл (360 мкмоль/л) у женщин до менопаузы определяется как гиперурикемия (ГУ). Уровень МК в крови регулируется тремя механизмами: эндогенным синтезом, экскрецией и реабсорбцией в почках и кишечнике [2]. В физиологических условиях производство и выведение МК находятся в состоянии баланса, а при его нарушении развивается ГУ. Генетически обусловленное нарушение реабсорбции [3] или экскреции [4] МК может приводить к гипо- или гиперурикемии, соответственно демонстрируя двунаправленность транспорта уратов в эпителии проксимальных канальцев почек. При повышении уровня МК и отсутствии признаков подагрического артрита ГУ считается бессимптомной.. Согласно клиническим рекомендациям Ассоциации ревматологов России (АРР) по диагностике и лечению подагры [5] выделяют две последовательные стадии бессимптомной ГУ (БГУ): без депозитов моноурата натрия (МУН) и с наличием депозитов МУН, но без симптомов или анамнеза подагры (отсутствие приступов артрита и тофусов).
В последние десятилетия во многих странах мира наблюдается тенденция к увеличению встречаемости ГУ [6–11], что связано с ростом продолжительности жизни в экономически развитых странах мира, снижением физической активности, увеличением частоты метаболических нарушений (избыточной массы тела и ожирения, патологии углеводного и липидного обмена), а также увеличением потребления в пищу продуктов питания, богатых пуринами (мясо и морепродукты), сладких безалкогольных напитков и алкоголя [12–15]. В США с 1960-х по 1990-е годы распространенность ГУ выросла более чем в 2 раза и продолжала неуклонно расти до 2007–2008 гг., достигнув 21,4% (на 3,2% выше, чем в 1988–1994 гг..,), а по данным за 2015–2016 гг.. она составляет 20,1% [6]. В Италии распространенность ГУ увеличилась с 8,54% в 2005 г. до 11,93% в 2009 г. [7]. В Японии она составляет около 30% среди мужского населения, а среди женщин — 1–3% в зависимости от возраста [8]. В Ирландии ГУ определяется у 19,9% населения [9]. В Китае, в зависимости от района исследования, ГУ встречается с частотой от 5,5% до 23,55%, в среднем составляя 13,3% [10]. Распространенность ГУ в Российской Федерации составляет 16,8% (примерно 14,9 млн взрослого населения). При этом среди мужчин она встречается в 25,3% случаев, а среди женщин — в 11,3%. Уровень МК более 416,5 мкмоль/л выявляется у 9,8% населения Российской Федерации [11].
Увеличение сывороточного уровня МК происходит в результате взаимодействия множества факторов, таких как пол, возраст, генетические особенности, образ жизни (ОЖ) (курение, физическая активность, пищевое поведение, употребление алкоголя), окружающая среда, наличие коморбидных заболеваний и др. (рис.. 1) [16].
![Рис. 1. Основные причины ГУ (адаптировано из [17]) Рис. 1. Основные причины ГУ (адаптировано из [17])](https://medblog.su/wp-content/uploads/2021/12/vliyanie-bessimptomnoj-giperurikemii-na-komorbidnye-zabolevaniya-i-vozmozhnosti-ee-korrektsii-mazurov-v-i-bashkinov-r-a-gajdukova-i-z-fonturenko-a-yu.png)
Имеется тенденция к увеличению встречаемости ГУ среди женщин после менопаузы, что связано со снижением уровня эстрогенов. Известно, что высокий уровень эстрогенов может способствовать более эффективной экскреции уратов [18]. Доказательством влияния женских половых гормонов на метаболизм МК служит исследование, в котором у мужчин, получавших эстрогены, отмечалось снижение уровня уратов в крови [19]. В экспериментальной модели эстрадиол играл более значимую роль в экспрессии генов — транспортеров МК (URAT1, GLUT9 и ABCG2) по сравнению с прогестероном [20]. Целый ряд лекарственных средств может способствовать развитию ГУ: некоторые дезагреганты (низкие дозы ацетилсалициловой кислоты (АСК), тикагрелор), β-адреноблокаторы, диуретики (тиазидные, петлевые, антагонисты минералокортикоидных рецепторов (спиронолактон)). Напротив, прием гиполипидемических препаратов (ингибиторы ГМГ-КоА-редуктазы (статины), фибраты), лозартана и сахароснижающих препаратов (ингибиторы натрий-глюкозного котранспортера 2-го типа (SGLT-2)) способствует снижению уровня МК [21].
Проводимые в последние годы полногеномные исследования продемонстрировали важную роль генетической предрасположенности к нарушению пуринового обмена. В частности, полиморфизмы генов, кодирующих уратные транспортеры в почках и кишечнике (SLC2A9, SLC22A12, ABCG2 и др..), могут быть причиной повышения уровня МК, т. е. значимым фактором риска (ФР) возникновения подагры и ГУ (рис. 2) [22]..
![Рис. 2. Обмен МК в эпителии проксимальных канальцев почек (адаптировано из [22]) Рис. 2. Обмен МК в эпителии проксимальных канальцев почек (адаптировано из [22])](https://medblog.su/wp-content/uploads/2021/12/1638837733_195_vliyanie-bessimptomnoj-giperurikemii-na-komorbidnye-zabolevaniya-i-vozmozhnosti-ee-korrektsii-mazurov-v-i-bashkinov-r-a-gajdukova-i-z-fonturenko-a-yu.png)
Несмотря на то, что наличие ГУ является необходимым условием для возникновения подагры, далеко не у всех пациентов с повышением МК дебютирует суставной синдром. Так, по данным наблюдательного исследования, 5-летняя кумулятивная заболеваемость подагрой мужчин c БГУ составила 18,83% [23]. E.W. Campion et al. [24] кумулятивную заболеваемость подагрическим артритом оценивают в 22% при уровне МК 9 мг/дл (540 мкмоль/л) или более.. В другом наблюдательном исследовании за 7,5 года наблюдения подагра дебютировала у 3,1% пациентов с БГУ [25]. Несмотря на это, ГУ имеет широкий диапазон влияния на развитие и прогрессирование целого ряда патологий терапевтического профиля.
Влияние ГУ на сердечно-сосудистую систему
Экспериментальные исследования показали, что повышенный уровень МК способствует развитию сердечно-сосудистых заболеваний (ССЗ), проатерогенным процессам, субклиническому воспалению, эндотелиальной дисфункции (ЭД) и окислительному стрессу. Активные формы кислорода, продуцируемые после активации ксантиноксидазы (КСО), являются одной из основных причин, вызывающих ЭД и поражение сердечно-сосудистой системы [26]. Описано несколько механизмов, объясняющих возможное участие МК в формировании ССЗ. Так, результаты исследования R.J. Johnson et al. [27] показали, что повышение уровня МК может вызывать гломерулотубулярные повреждения, способствующие активации ренин-ангиотензин-альдостероновой системы (РААС) и повышению артериального давления (АД), при этом данные изменения могут регрессировать после устранения ГУ.. L.G. Sanchez-Lozada et al. [28] продемонстрировали, что высокое содержание МК может индуцировать повреждение сосудистой стенки, которое регрессирует при использовании препарата аллопуринол.. Более того, показано, что ГУ вызывает спазм сосудов почек, провоцируя активацию РААС [28, 29], и является значимым фактором развития ЭД [30]. Другие потенциальные механизмы, с помощью которых ГУ и/или повышенная активность фермента КСО могут способствовать сосудистому повреждению, включают адгезию тромбоцитов, пролиферацию гладкомышечных клеток сосудов и стимуляцию воспалительного процесса [31]. Следует отметить, что кристаллы МУН могут депонироваться в аорте и коронарных артериях, тем самым участвуя в образовании бляшек и кальцификации сосудов [32]. Таким образом, доказано, что МК может принимать непосредственное участие в патогенезе целого ряда ССЗ и атеросклероза..
Эпидемиологические исследования показали, что повышение концентрации МК является предиктором развития артериальной гипертензии (АГ) [33]. Данные метаанализа 18 исследований [34] демонстрируют увеличение на 13% частоты впервые возникшей АГ на каждый 1% повышения уровня МК.. Исследование PAMELA [35] подтвердило, что увеличение уровня МК на 1 мг/дл (60 мкмоль/л) связано со значительным повышением риска развития впервые возникшей АГ. ГУ является значимым ФР развития ишемической болезни сердца (ИБС), острого инфаркта миокарда, острой сердечной недостаточности (СН), сердечно-сосудистой и общей смертности [36–39]. Двенадцатилетнее исследование PIUMA [40], в котором приняли участие 1720 пациентов с АГ, также показало, что уровень МК — сильный предиктор смертности.. В метаанализе данных 8776 пациентов с острым коронарным синдромом и сопутствующей ГУ было выявлено повышение риска неблагоприятных сердечно-сосудистых событий, общей и сердечно-сосудистой смертности после корректировки на другие известные ФР [41]. У пациентов с хронической СН была показана прямая связь между повышением уровня МК, снижением фракции выброса левого желудочка и уровнем NT-proBNP [42]. В литературе представлены доказательства взаимосвязи ГУ и острого нарушения мозгового кровообращения (ОНМК) [43]. Более того, среди пациентов, перенесших ОНМК и имеющих ГУ, отмечалось увеличение смертности [44]. Нарушения ритма сердца также ассоциированы с ГУ, в частности, описаны пути патологического влияния МК на формирование фибрилляции предсердий [45].
Гиперурикемия и метаболические нарушения
Доказано, что более высокая концентрация МК в сыворотке крови тесно связана с повышением уровня липидов, триглицеридов, глюкозы в крови и метаболическим синдромом (МС) [46]. Инсулинорезистентность (ИР) и повышенный уровень лептина могут быть связующим звеном между ожирением, дислипидемией и ГУ [47]. Установлена ассоциация подагры с ожирением и дислипидемией [48], причинами которой в большинстве случаев являются ИР и гиперинсулинемия [49]. Результаты исследования C. Lie et al. [50] подтверждают предположение о том, что ИР занимает центральное место в причинно-следственной связи между МС и ГУ.. ИР ассоциируется не только с патогенезом МС, но и с повышением синтеза пуринов, который является результатом энергетического обмена с участием гипертриглицеридемии, играющей важную роль в данном механизме [51]. Избыточная масса тела и центральное ожирение тесно связаны с повышенным уровнем МК. Было показано, что нарастание индекса массы тела
на 4 единицы увеличивает уровень МК в крови на 0,5 мг/дл (30 мкмоль/л) и риск развития ГУ на 7,5% [52].
В данный момент актуальность проблемы неалкогольной жировой болезни печени (НАЖБП) заметно повысилась.. Как показал метаанализ 13 исследований [53], ГУ связана с повышенным риском развития НАЖБП в азиатских популяциях.. По данным обзора 5 наблюдательных исследований, пациенты с ГУ и НАЖБП имели более высокий уровень индекса активности НАЖБП (≥5 баллов), более того, повышенный уровень МК был связан с более тяжелым поражением печени при гистологическом исследовании [54].
Влияние ГУ на почки
Гиперурикемия является сильным независимым ФР развития хронической болезни почек (ХБП) [55–58]. Риск поражения почек быстро увеличивается, когда концентрация МК в сыворотке достигает 7 мг/дл (420 мкмоль/л) и более [59]. После того, как у пациентов развивается поражение почек, уровень МК в сыворотке становится более вариабельным, и некоторые исследователи предполагают, что ГУ является независимым предиктором ухудшения течения ХБП [56, 60]. Имеются свидетельства того, что биологические эффекты МК, вызывающие заболевание почек, могут быть в большей степени опосредованы ее внутриклеточными эффектами [61]. Внутриклеточные уровни могут быть выше в условиях стимуляции синтеза МК, что может наблюдаться при высокой активности КСО. В свою очередь, активность КСО в крови связана с прогрессированием ХБП и сердечно-сосудистыми исходами независимо от уровня МК [62, 63].
Считается, что ГУ вызывает повреждение почек за счет как кристаллозависимых, так и кристаллонезависимых механизмов [63]. Кристаллозависимый путь включает отложение кристаллов МУН в канальцах или интерстиции почек, что приводит к хроническому воспалению и повреждению канальцев [63]. С другой стороны, повышенный уровень МК в сыворотке умеренно и независимо связан с повышенным риском развития мочекаменной болезни (МКБ) [64]. Интересно, что наличие микрокристаллической нефропатии не было связано с выявлением кристаллов уратов в мочевом осадке, что подтверждает независимость двух патофизиологических механизмов [65]. Растворимая внутриклеточная МК может вызывать ХБП через кристаллонезависимый процесс. Это может происходить либо за счет повышенного уровня МК в сыворотке крови, либо за счет эндогенного синтеза [66]. Механизм включает повышение как системного, так и внутриклубочкового давления в сочетании с афферентной артериолярной вазоконстрикцией и нарушением почечного кровотока, которое опосредуется активацией системы РААС, снижением биодоступности эндотелиального оксида азота и индукцией окислительного стресса [67, 68]. С другой стороны, происходит пролиферация гладкомышечных клеток сосудов, вызывающая артериолопатию с нарушением ауторегуляции, а также воздействие на канальцы, включая эпителиально-мезенхимальные и воспалительные изменения [69, 70].
В конечном итоге ишемия становится одним из основных результатов патологии почек у лиц, страдающих ГУ и подагрой [71].
Влияние уратснижающей терапии на течение коморбидных заболеваний
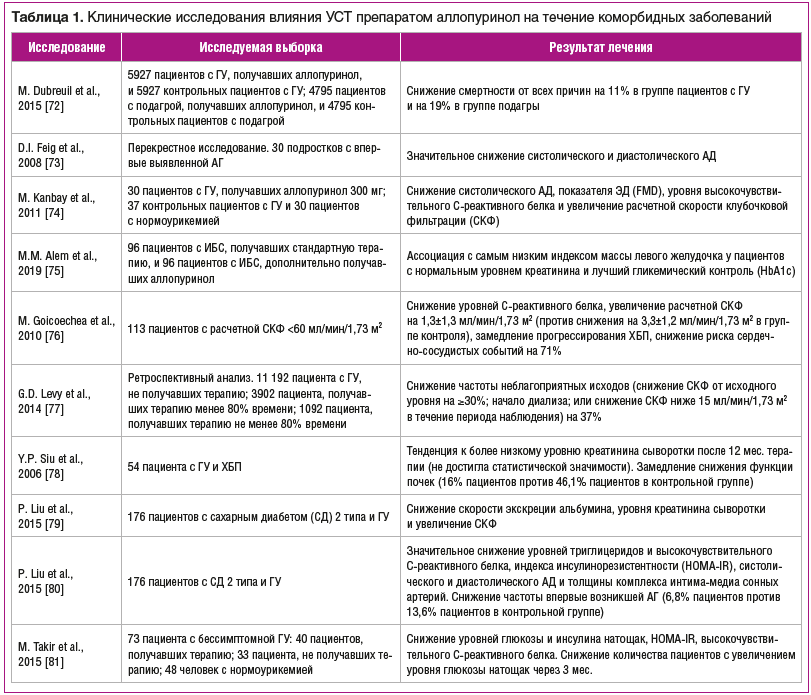
Ввиду значимого влияния ГУ на возникновение и течение сердечно-сосудистой, нефрологической и метаболической патологии было проведено довольно большое количество экспериментальных и рандомизированных клинических исследований влияния уратснижающей терапии (УСТ) ингибиторами КСО, а именно препаратом аллопуринол, на их течение (табл. 1).
Бессимптомная ГУ и депозиты МУН
Существует три основных патологии, связанные с депонированием кристаллов МУН: подагра, уратная нефропатия и МКБ. Стойкая БГУ — это ФР развития вышеперечисленных клинических событий, и эти риски связаны с выраженностью и продолжительностью ГУ. Взаимодействие кристаллов МУН с различными клетками сустава приводит к синтезу широкого спектра провоспалительных цитокинов, таких как интерлейкин (ИЛ)-1 [82], фактор некроза опухоли альфа (ФНО-α) [83], ИЛ-8, хемокины [84], метаболиты арахидоновой кислоты, супероксидные кислородные радикалы, протеиназы. Имеются исследования, демонстрирующие, что ГУ сопровождается системным повышением продукции ФНО-α, ИЛ-6, ИЛ-8, микроРНК-155, локальной экспрессией моноцитарного хемотаксического белка 1 в почках и циклооксигеназы 2-го типа в кровеносных сосудах [85].
Современные визуализационные методы диагностики, такие как ультразвуковое исследование (УЗИ) и двухэнергетическая компьютерная томография (ДЭКТ), продемонстрировали патофизиологическую связь между ГУ и отложением депозитов МУН в опорно-двигательном аппарате еще до дебюта суставного синдрома [85–95]. Было показано, что данные методы обследования предоставляют возможность выявлять депозиты МУН, устанавливать их локализацию и количество, а также проводить динамическое наблюдение во время УСТ. В ряде случаев отложения МУН в виде видимых или выявленных при помощи визуализационных методов тофусов в области кожи, суставов, сухожилий при отсутствии артрита, безболезненны и бессимптомны. При УЗИ кристаллы МУН, покрывающие суставной хрящ, могут быть обнаружены как симптом «двойного контура», тофусы (скопление кристаллов МУН, окруженных организованным клеточным ободком и фиброваскулярной зоной) или в виде гиперэхогенных включений в полости сустава (вид «метели») [96]. ДЭКТ, имеющая два источника рентгеновского излучения и два детектора, способна определять, включает ли химический состав исследуемой области кристаллы МУН, и с помощью программного обеспечения оценивает их объем..
В попытке доказать наличие депозитов МУН у лиц с БГУ многие исследователи [85–95] проводили инструментальное обследование данной категории пациентов.. По полученным данным, субклинические отложения депозитов МУН в структурах опорно-двигательного аппарата определялись у 42% пациентов с БГУ при помощи УЗИ и ДЭКТ.. В исследовании [86] отложения МУН в области суставов и сухожилий стоп по ДЭКТ наблюдались у 24% пациентов. P. Wang et al. [87] у 15% пациентов обнаружили отложения кристаллов МУН по данным ДЭКТ со средним общим объемом 0,13±0,14 см3. Y. Sun et al. [88] с помощью ДЭКТ выявили 80 областей отложений депозитов МУН среди 19 пациентов с БГУ, при этом среднее количество участков отложения составило 3. В работе [89] симптом «двойного контура» при УЗИ был выявлен в 25% первых плюснефаланговых суставов (1ПлФС) стоп и 17% тазобедренных суставов, а внутрисуставные тофусы были обнаружены у 16% пациентов с БГУ. Симптомы отложений МУН по данным УЗИ были выявлены у 42% пациентов, причем у 82% пациентов наличие кристаллов МУН было подтверждено при поляризационной микроскопии синовиальной жидкости [90]. J.G. Puig et al. [91] у 34% пациентов при УЗИ выявили тофусы в области сухожилий, синовиальной оболочки или мягких тканей, воспалительная реакция в области тофусов наблюдалась у 23% пациентов.. M. Andes et al. [92] по данным УЗИ коленных, голеностопных и 1ПлФС обнаружили гиперэхогенные включения, симптом «двойного контура» и тофусы у 53,3, 26,7 и 10% пациентов соответственно, а у 14,8% пациентов при поляризационной микроскопии синовиальной жидкости были выявлены кристаллы МК. Отложения МУН по данным УЗИ коленных суставов и 1ПлФС присутствовали у 29% пациентов [93]. M.A. Reuss-Borst et al. [94] выявили при УЗИ в 14% исследуемых суставов патологические изменения (из них 8% c симптомом «двойного контура»). А. Abhishek et al. [95] обследовали 131 человека (сыновья пациентов с подагрой): уровень МК был не менее 6 мг/дл (360 мкмоль/л) у 64,1% и не менее 7 мг/дл (420 мкмоль/л) у 29%, а у 29,8% пациентов были обнаружены изменения по УЗИ не менее чем в 1 суставе. В работе [85] частота синовита и симптома «двойного контура» при УЗИ составляла 67% и 27% соответственно у пациентов с БГУ и подагрой и была выше, чем в контрольной группе, а пациенты с отложениями депозитов МУН имели более высокие уровни ИЛ-6 и микроРНК-155.
Подходы к терапии БГУ
В рекомендациях некоторых профессиональных ревматологических сообществ по ведению пациентов с подагрой (Япония, Тайвань, Китай и Португалия) высказывается мнение, что БГУ подлежит медикаментозному лечению при неэффективности нефармакологических методов терапии, высоком уровне МК в крови и наличии сопутствующей патологии сердечно-сосудистой системы, почек и метаболических нарушений [97]. Так, согласно Японским национальным рекомендациям, при уровне МК не менее 9 мг/дл
(540 мкмоль/л) медикаментозную терапию следует рассматривать независимо от модификации ОЖ, кроме того, применение УСТ возможно, когда уровень МК в сыворотке достигает 8 мг/дл (480 мкмоль/л) и более, если у пациента имеются сопутствующие заболевания, в особенности патология почек (ХПБ, МКБ) [98]. В Португалии у пациентов с уровнем сывороточной МК не менее 9 мг/дл (540 мкмоль/л) фармакологическое лечение рассматривают после индивидуальной оценки соотношения риска и пользы, в частности при профилактике подагры [99]. A. Brucato et al. [100] рекомендуют следующие показания к применению аллопуринола: стойкие уровни МК выше 13 мг/дл (780 мкмоль/л) у мужчин или 10 мг/дл (600 мкмоль/л) у женщин (эти значения повышают риск нефротоксичности, а УСТ может замедлять прогрессирование заболеваний почек и предотвращать эти риски); экскреция МК почками, превышающая 1100 мг/сут (это связано с увеличением риска осаждения МК в виде камней на 50%, который предотвращается посредством снижения ее экскреции почками до 800 мг/сут); подготовка пациента к лучевой или химиотерапии (профилактика нефропатии и других проявлений синдрома лизиса опухоли).
Однако имеется и противоположная точка зрения относительно необходимости проведения УСТ у пациентов с БГУ.. Так, клиническими рекомендациями Европейской антиревматической лиги (EULAR) [101], Американской коллегии ревматологов (ACR) [102] и АРР [5] не рекомендуется проведение медикаментозной терапии пациентам с БГУ в плане профилактики подагры, несмотря на уровень МК и наличие или отсутствие коморбидных заболеваний.
В реальной клинической практике, по данным Городского регистра Санкт-Петербурга пациентов с подагрой и БГУ, среди 400 пациентов с остеоартритом, БГУ и обширным перечнем сопутствующих заболеваний (АГ — 84%, СД — 31,8%, ХБП — 48,8%, ожирение — 45%, гиперхолестеринемия — 65,7% и т. д.) УСТ получали лишь 36,8% пациентов, при ее эффективности всего в 20,4% случаев [103].
Следует отметить, что в клинических рекомендациях Европейского общества кардиологов (ESC, 2018) [104] и Российского кардиологического общества (РКО, 2020) [105] по ведению пациентов с АГ обозначено, что МК является значимым прогностическим фактором при данной патологии, а также отмечается наличие доказанной связи между ГУ и повышением сердечно-сосудистой смертности, в связи с чем определение ее уровня в крови является обязательным для всех пациентов, страдающих АГ (уровень убедительности рекомендаций (УУР) A; уровень достоверности доказательств (УДД) 2).
Более того, экспертами в области кардиологии Европы (C. Borghi et al.) и Российской Федерации (РМОАГ) был опубликован консенсус по ведению пациентов с ГУ и высоким сердечно-сосудистым риском (ССР), рекомендующий проведение УСТ препаратом аллопуринол при неэффективности немедикаментозных методов лечения [27, 106, 107]. Согласно данному документу рекомендуется придерживаться следующего пошагового алгоритма действий [27]:
Шаг 1. Оценить уровень МК в сыворотке крови, считать высоким уровень более 360 мкмоль/л (в пересмотре C. Borghi et al. от 2021 г. [107]: у пациентов с наличием минимум двух из следующих ФР: АГ, СД, дислипидемия, поражение органов-мишеней или пережитые сердечно-сосудистые события — более 300 мкмоль/л).
Шаг 2. Оценить наличие сопутствующих заболеваний, у пациентов с высоким ССР целевым считать уровень МК в сыворотке крови ниже 300 мкмоль/л
(в пересмотре C. Borghi et al. от 2021 г. [107]: у пациентов с наличием минимум двух из следующих ФР: АГ, СД, дислипидемия, поражение органов-мишеней или пережитые сердечно-сосудистые события — менее 300 мкмоль/л, у иных пациентов — менее 360 мкмоль/л).
Шаг 3. Информировать пациента о фармакологических и эпидемиологических факторах, влияющих на ГУ, сопутствующих заболеваниях и сердечно-сосудистых ФР. Рекомендовать изменения ОЖ, диеты (в пересмотре C. Borghi et al. от 2021 г. [107]: ограничение потребления пуринов, в том числе красного мяса, морепродуктов, продуктов с высоким содержанием фруктозы, сахаросодержащих безалкогольных напитков и алкоголя; регулярная физическая активность; употребление кофе, молочнокислых продуктов, вишни и аскорбиновой кислоты и снижение массы тела, а также строгая приверженность рекомендуемому лечению. Отменить по возможности препараты, влияющие на уровень МК в сыворотке крови (в пересмотре C. Borghi et al. от 2021 г. [107]: рекомендуется применение лозартана; по возможности отмена/замена диуретиков, низких доз АСК (при первичной профилактике ССЗ); в то же время не рекомендуется переход с других блокаторов рецепторов ангиотензина на лозартан; прекращение приема низких доз АСК у пациентов со вторичной профилактикой ССЗ; переход со статинов на фенофибрат).
Шаг 4. Начать терапию аллопуринолом в дозировке 100 мг с последующей титрацией до 300–600 мг/сут, до достижения целевого уровня МК (в пересмотре C. Borghi et al. от 2021 г. [107]: — максимальная доза 900 мг/сут).
Шаг 5. Контролировать уровень МК в крови не реже 2 раз в год. У пациентов с АГ, ИБС, ОНМК в анамнезе, СД и ХБП, не достигших целевого уровня МК, рассмотреть возможность комбинированной терапии (аллопуринол + препарат с урикозурическим эффектом) (в пересмотре
C. Borghi et al. от 2021 г. [107]: при достижении целевых значений МК не прекращать лечение).
Консенсус Объединенной академии эндокринологии и диабета (IDEA) [108] рекомендует начинать УСТ при БГУ до уровня МК 9 мг/дл (540 мкмоль/л) с наличием сопутствующей ХБП III–IV стадии и/или МКБ, при этом терапия аллопуринолом также рекомендована при уровне МК выше 9 мг/дл (540 мкмоль/л) и нормальной функции почек (целевой уровень — менее 360 мкмоль/л).
В клинических рекомендациях Ассоциации нефрологов России (2021) по ведению пациентов с ХБП [109] всем пациентам с данной патологией рекомендовано исследование и мониторирование уровня МК в крови, которое при необходимости должно быть дополнено исследованием уровня МК в моче и расчетом ее суточной экскреции для выявления и дифференциальной диагностики ГУ, оценки ассоциированных рисков и выбора терапии (УУР — A, УДД — 1). D. Viggiano et al. [110] предлагают в качестве обследования идентифицировать пациентов с высоким риском прогрессирования ХБП уратного генеза путем анализа исследования мочевого осадка (на предмет наличия кристаллов уратов), УЗИ опорно-двигательного аппарата (на предмет наличия депозитов кристаллов МУН) и динамического наблюдения за функцией почек. По мнению коллектива авторов, УСТ целесообразно начинать пациентам с наличием кристаллов уратов в осадке мочи и депозитов МУН в области опорно-двигательного аппарата, а также отрицательной динамикой расчетной СКФ за 6 мес.
По данным актуальных международных клинических рекомендаций, препаратом первой линии для УСТ при подагре и БГУ является ингибитор КСО аллопуринол (Милурит®, «ЭГИС»). Милурит® — единственный в Российской Федерации препарат, имеющий в качестве официального показания к применению не только подагру, но и различные виды ГУ.. Применение аллопуринола более предпочтительно для пациентов с ССР, так как, по данным исследования CARES (Goutand Cardiovascular Morbidities), смертность от всех причин и от ССЗ на фоне приема аллопуринола в сравнении с фебуксостатом ниже на 22% и 34% соответственно [111].
Заключение
Не вызывает сомнений тот факт, что ГУ служит ключевым ФР возникновения подагры. Однако применение УСТ при БГУ, протекающей в сочетании с различными КЗ, до сих пор является предметом дискуссий.. Наряду с этим в настоящее время доказаны прямые патогенетические связи ГУ с формированием и прогрессированием патологии сердечно-сосудистой системы, поражением опорно-двигательного аппарата, болезнями почек и метаболическим синдромом. Именно поэтому в рекомендациях РМОАГ, IDEA и ряде других медицинских сообществ представлены показания для инициации УСТ при БГУ, в перечень которых входят высокие риски сердечно-сосудистых событий в группе пациентов с АГ и ИБС, а также ХБП и МС. Вместе с тем назрела необходимость в разработке междисциплинарного консенсуса по ведению пациентов с БГУ и наличием коморбидных заболеваний, который базировался бы на результатах клинических исследований и анализе данных отечественных и зарубежных регистров..
Благодарность
Авторы и редакция благодарят ООО «ЭГИС-РУС» за предоставление полных текстов иностранных статей, требовавшихся для подготовки данной публикации.
.
Информация с rmj.ru






