В статье описана тактика лечения ятрогенных повреждений и стриктур внепеченочных желчных путей.
Увеличение частоты холецистэктомий при ЖКБ приводит к увеличению количества интраоперационных повреждений внепеченочных желчных ходов (ВПЖХ) и достигает 3,0% от общего числа оперированных пациентов по поводу желчнокаменной болезни [1–4]. После повторных операций на желчных путях в отдаленном периоде рубцовые стриктуры анастомозов развиваются у 20–30% больных [5–9]. В настоящее время отдаленные результаты при реконструктивных и восстановительных вмешательствах не удовлетворяют хирургов, что диктует необходимость поиска новых подходов к оперативному лече-
нию [3, 10–12]. В последние десятилетия наблюдается тенденция к увеличению количества мини-инвазивных вмешательств при патологии желчных путей, а именно баллонных пластик и стентирований [5, 13–15]. Однако не все авторы считают такие вмешательства целесообразными, что и определяет актуальность проблемы реконструктивной и восстановительной хирургии при интраоперационных повреждениях и рубцовых стриктурах ВПЖХ [1, 3, 5, 6].
: дифференцировка показаний к открытым и мини-инвазивным операциям при реконструктивной билиарной хирургии.
Под нашим наблюдением находились 76 пациентов, проходивших лечение в хирургическом отделении БМУ КОКБ по поводу ятрогенных повреждений ВПЖХ и рубцовых стриктур протоков и билиодигестивных анастомозов в период с 1994 по 2017 г. В общем числе больных было 13 (17,1%) мужчин и 63 (82,9%) женщины, преимущественно работоспособного возраста от 40 до 65 лет — 56 (73,68%) человек, старше 60 лет были 24 (31,57%) человека.
Пациентов разделили на 2 группы: в 1-ю группу вошли 36 (47,36%) пациентов с ятрогенными повреждениями; 2-ю группу составили 40 (52,64%) больных со стриктурами ВПЖХ и билиодигестивных анастомозов.
У 25 (69,4%) больных 1-й группы (n=36) повреждения ВПЖХ возникли после видеолапароскопической холецистэктомии, у 10 (27,8%) пациентов — при лапаротомной холецистэктоми и у 1 (2,8%) пациента — после холецистэктомии из мини-доступа. При этом повреждение ВПЖХ произошло у 21 (58,3%) пациента при проведении видеолапароскопической холецистэктомии (ВЛХЭ) в ЦРБ Курской области. Больные были доставлены в БМУ КОКБ с механической желтухой или наружными желчными свищами для дообследования и определения дальнейшей тактики лечения.
Следует отметить, что повреждение ВПЖХ у 32 (88,9%) пациентов происходило на фоне выраженного воспалительного инфильтрата в области печеночно-дуоденальной связки, короткого пузырного протока, выраженного спаечного процесса и невозможности дифференцировать элементы треугольника Кало. Это было связано с длительным периодом от начала заболевания до первого оперативного вмешательства (холецистэктомии).
У 23 (63,9%) из 36 больных повреждение ВПЖХ диагностировано во время операции по появлению желчи в операционном поле, а у 13 (36,1%) — в послеоперационном периоде. Сроки диагностики ятрогенного повреждения ВПЖХ в послеоперационном периоде приведены на рисунке 1.
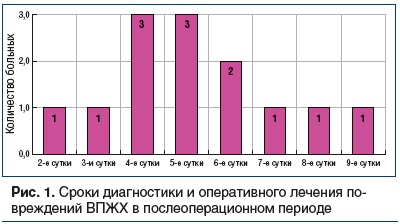
Всем больным проводили обследование, включающее биохимический анализ крови, ультразвуковое исследование с определением выраженности желчной гипертензии, МРТ-холангиографию, ретроградную панкреатохолангиографию (РПХГ) с целью уточнения уровня повреждения. Первым (диагностическим и лечебным) этапом 14 (38,9%) больным, переведенным из ЦРБ, с целью купирования желчной гипертензии наложили перкутанную холангиостому, что дало возможность провести антеградную холангиографию для уточнения верхней границы уровня блока; 8 больным выполнена РПХГ, 7 больным эти два исследования выполнены одновременно.
При малых повреждениях ВПЖХ (в 9 случаях) произведено ушивание дефекта на дренаже Кера. Гепатикоеюноанастомоз (ГЕА) по Ру на дренаже Прадери наложен 19 больным. Показанием к каркасному дренированию был малый диаметр и тонкая стенка протока. Бигепатикоеюноанастомоз по Ру на дренаже Прадери наложен 4 пациентам с целью длительной декомпрессии желчных путей и профилактики несостоятельности ГЕА. ГЕА по Ру на дренаже Фелькера наложен 4 больным. Каркасное дренирование по Фелькеру проводилось в условиях выраженного спаечного процесса между диафрагмой и диафрагмальной поверхностью печени.
У 9 (25%) больных в раннем послеоперационном периоде диагностировали подпеченочные и поддиафрагмальные биломы, которые санировали дренированием под УЗ-контролем.
Летальность в 1-й группе составила 5,56% (2 пациента). В одном случае в послеоперационном периоде на фоне ишемической болезни сердца у больного возникла тромбоэмболия легочной артерии с развитием правосторонней инфаркт-пневмонии, сопровождавшейся выраженной острой дыхательной недостаточностью. Больной умер от сердечно-легочной недостаточности. В другом случае у больного через 3 сут вследствие несостоятельности ГЕА развился желчный перитонит, по поводу которого выполнена релапаротомия. На 4-е сут развилась ранняя послеоперационная спаечная тонкокишечная непроходимость, по поводу которой выполнены релапаротомия, назоеюнальная интубация. Послеоперационный период осложнился развитием двусторонней нозокомиальной пневмонии, которая привела к полиорганной недостаточности и летальному исходу.
В среднем длительность пребывания в стационаре составила 26±7 койко-дней.
Анализ результатов показал, что из 13 пациентов, поступивших в сроки более 4 сут после ятрогенных повреждений, у 9 (25%) возникли осложнения в виде несостоятельности анастомозов и билом. В значительной степени осложнения были связаны с увеличением временнÓго интервала (5,4±2,3 сут) между первичной и реконструктивной операциями. Одному из двух погибших больных на 3-и сут выполнили ГЕА, в раннем послеоперационном периоде развилась его несостоятельность, которая привела к биломе и перитониту. В связи с этим была выполнена ререлапаротомия, усугубившая общее состояние и приведшая к полиорганной недостаточности. Это позволяет считать оптимальным сроком проведения реконструктивной операции менее 3–4 сут после ятрогенного повреждения желчных путей.
Во 2-й группе (n=40) со стриктурами анастомозов было 15 (37,5%) больных, которым ранее выполняли гепатикоеюностомию по Ру на дренаже Прадери по поводу ятрогенного повреждения протоков во время ВЛХЭ; со стриктурами ВПЖХ после ранее проведенных вмешательств на холедохе по поводу холедохолитиаза — 22 (55%) больных, с синдромом Миризи после холедохолитотрипсии — 3 (7,5%). Следует отметить, что у 27 (67,5%) пациентов мы не могли определить точные сроки и количество оперативных вмешательств. Этим больным оперативные вмешательства по поводу ятрогенных повреждений ВПЖХ (со слов) проводили более чем через 5 сут после первичной операции.
Срок от наложения билиодигестивного анастомоза (БДА) до появления его стриктуры в этой группе больных составил от 6 мес. до 7 лет.
При поступлении всем больным проводили УЗИ, при котором были выявлены признаки желчной гипертензии, связанной с нарушением оттока желчи. Первым этапом
23 (57,5%) пациентам выполнено декомпрессионное дренирование желчного дерева под УЗ-контролем, направленное на купирование желчной гипертензии, проведена антеградная холангиография и дальнейшая баллонная пластика. Дополнительное проведение РПХГ с целью уточнения нижней границы уровня блока потребовалось 16 (40%) больным. Это позволило выявить тип стриктуры, что определило дальнейшую хирургическую тактику.
У 21 (52,5%) из 40 пациентов стриктура ВПЖХ клинически проявилась механической желтухой, сопровождавшейся повышением уровня прямого билирубина с выраженным цитолитическим синдромом. У 7 (17,5%) пациентов механическая желтуха сопровождалась явлениями холангита, а у 12 (30%) — наблюдалось повышение прямой фракции билирубина выше нормального уровня без клинических проявлений.
Все больные были прооперированы: в 47% случаев были произведены открытые операции, в 53% — мини-инвазивные.
Структура оперативных вмешательств представлена в таблице 1.
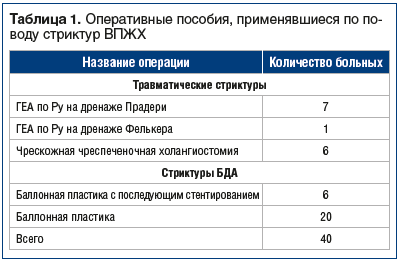
В группе больных с травматическими стриктурами ВПЖХ предпочтение отдавали операции с наложением ГЕА по Ру на дренаже Прадери, а из мини-инвазивных вмешательств в группе больных со стриктурами БДА — баллонной пластике зоны стриктуры. Наиболее частым осложнением после открытого оперативного вмешательства был холангит (8,47%), что потребовало проведения ревизии дренажа с его промыванием, антибактериальной, дезинтоксикационной терапией.
Баллонную пластику стриктур после реконструктивных операций у пациентов 2-й группы в 20 (50%) случаях проводили через 9,11±3,1 мес. Повторную антеградную баллонную дилатацию стриктур БДА проводили 9 (22,5%) пациентам. Интервал времени между баллонными пластиками составил 4,6±2,1 мес. При дальнейшем динамическом наблюдении через 10,75±5,7 мес. 4 пациента (10%) нуждались в дополнительной эндобилиарной коррекции БДА.
По нашим данным, после баллонной пластики стриктур БДА осложнений не наблюдалось.
Анализ отдаленных результатов показал, что часть больных были оперированы в других ЛПУ, часть больных не выходили на контакт, от прогрессирования сопутствующей патологии умерли 3 пациента.
Средний срок нахождения в стационаре больных 2-й группы составил 11,8±6 койко-дней.
Заключение
В результате проведенных исследований нами отмечено, что наиболее частой причиной повреждения ВПЖХ были воспалительные изменения в зоне печеночно-дуоденальной связки с наличием выраженного спаечного процесса на фоне деструктивного холецистита.
Реконструктивные операции в виде наложения БДА с применением каркасного дренирования являются эффективным способом восстановления пассажа желчи с относительно длительным безрецидивным периодом при соблюдении оптимальных сроков (менее 4 сут) от наступления ятрогении до операции. Это позволяет снизить частоту послеоперационных осложнений и предотвратить развитие стриктур в раннем послеоперационном периоде. Мини-инвазивные вмешательства в виде баллонной пластики в ряде случаев могут являться окончательным методом лечения.
Применение баллонной пластики в группе больных со стриктурами ранее наложенных БДА дает возможность избежать открытой операции, уменьшить число осложнений и не допустить летальных исходов.
Информация с rmj.ru





