Введение
Инфекции дыхательных путей являются одними из наиболее распространенных заболеваний у детей и подростков и представляют собой одну из основных причин госпитализации в этой популяции. Частые рецидивы респираторных заболеваний создают психологический и физический дискомфорт для детей и родителей, снижают качество жизни, нередко приводят к назначению антибактериальных препаратов, в том числе необоснованному (что особенно актуально в условиях растущей антибиотикорезистентности), а также несут значительные финансовые расходы как для семьи, так и для государства [1–5]. В литературе обсуждалась связь рецидивирования респираторных инфекций с различными факторами, в том числе с состоянием иммунной системы [6], аллергическими заболеваниями [7], нарушениями микробиоты кишечника [8, 9], герпесвирусными инфекциями [10] и др. Согласно современным представлениям пациент с рецидивирующими респираторными инфекциями (РРИ) в половине случаев — это нормальный ребенок, который переносит ОРВИ 8–12 раз в год, реже — ребенок с атопическим заболеванием (30%), другими хроническими заболеваниями (10%), иммунодефицитом (10%)1.
Для практикующих врачей РРИ представляют проблему как с точки зрения диагностики, так и с позиций подхода к лечению. С учетом преимущественно вирусной этиологии заболевания, а также возрастных аспектов выбор препаратов ограничен. На первый план выходят профилактические подходы, которые позволяют минимизировать частоту эпизодов острых респираторных инфекций (ОРИ) и снизить их тяжесть, избежав развития осложнений и необходимости назначения антибактериальных препаратов.
Препарат инозин пранобекс имеет многолетнюю историю применения и эффективен в отношении вирусных инфекций, в том числе герпесвирусных инфекций (ГВИ) [11], а в последние годы описано применение инозина пранобекса у пациентов с коронавирусной инфекцией [12–14]. C.R. Jayanthi et al. в 2022 г. [15] показали, что у пациентов с COVID-19 легкой и средней тяжести препарат улучшает клинические показатели, увеличивает цитотоксичность, опосредованную естественными клетками-киллерами, инфицированных вирусом клеток в качестве раннего иммунного ответа на вирусную инфекцию и усиливает экспрессию лиганда NKG2D.
Ранее нами проводились исследования эффективности различных схем лечения детей с ГВИ и ежемесячными ОРИ. Была показана необходимость лечения детей с РРИ и активными ГВИ, а также подтверждена эффективность препарата Нормомед® у данной категории пациентов с активной инфекцией ВГЧ-6А/В [16] и другими активными ГВИ как в моноварианте, так и при их сочетанных формах. Однако оценка эффективности более длительного курса терапии препаратом Нормомед® (согласно инструкции производителя) с использованием критерия Уилкоксона и в более крупных выборках пациентов не проводилась.
Цель исследования: оценка эффективности препарата инозин пранобекс (Нормомед®) в терапии детей с РРИ и активными ГВИ.
Материал и методы
Под наблюдением находились пациенты, обратившиеся амбулаторно с жалобами на рецидивирующие инфекции органов респираторного тракта с лабораторно подтвержденной активной ГВИ. Было обследовано 96 пациентов, из них 50 (52,1%) девочек, в возрасте от 3 до 17 лет: 58 (60,4%) детей младше 7 лет, 38 (39,6%) детей в возрасте 7 лет и старше (медиана возраста 6 (Q1; Q3: 3; 8) лет).
Проводились комплексное клинико-лабораторное обследование, оценка активности ГВИ (вирус простого герпеса 1-го типа (ВПГ-1), вирус Эпштейна — Барр (ВЭБ), цитомегаловирус (ЦМВ), вирус герпеса человека типа 6А/В (ВГЧ-6А/В)). Лабораторная диагностика указанных ГВИ осуществлялась посредством прямых и косвенных методов: определение ДНК вирусов в крови и мазках из ротоглотки методом ПЦР с гибридизационно-флуоресцентной детекцией результатов анализа в режиме реального времени в образцах периферической крови; детекция ранних антигенов вируса в крови и мазках из ротоглотки (быстрый культуральный метод (vero, u937)), поздних антигенов (непрямая реакция иммунофлюоресценции), определение вирус-специфических IgМ и IgG. Активная инфекция устанавливалась при наличии виремии, латентная — при повышении уровня IgG без виремии и/или детекции ДНК вируса в мазке из ротоглотки при отсутствии в крови.
Критерии включения в исследование: возраст от 3 до 17 лет; ежемесячные респираторные инфекции за прошедшие 6 мес.; лабораторно подтвержденная активная форма ГВИ, установленная на момент включения в исследование; подписанное информированное согласие родителей или законных представителей.
Критерии невключения в исследование: хронические заболевания в стадии декомпенсации (органическое поражение ЦНС, патология сердечно-сосудистой системы, почечная и печеночная недостаточность), онкологические заболевания, иммунодефицитные состояния, индивидуальная гиперчувствительность к компонентам исследуемого препарата.
Всем пациентам назначали препарат инозин пранобекс (Нормомед®, АО «Валента Фарм», Россия, ЛП-004700, ЛП-№(002470)-(РГ-RU)) в дозировке 50–75 мг/кг/сут в зависимости от тяжести состояния (с учетом выраженности интоксикации, длительности заболевания и выраженности катарального синдрома) курсами по 10 дней: 83 (86%) ребенка получали таблетки, 13 (14%) детей — сироп. Всего проведено 3 курса с перерывами по 10 дней (суммарно продолжительность курса терапии составила 50 дней). Через 5±1 нед. после завершения терапии выполняли контрольное обследование, включавшее клинический анализ крови, выделение ДНК ВЭБ, ВГЧ-6А/В, ЦМВ, ВПГ-1 прямыми методами в крови и материале мазков из ротоглотки и определение специфических IgM и IgG в сыворотке крови методом иммуноферментного анализа. Также проводилось повторно УЗИ органов брюшной полости для оценки выраженности гепатолиенального синдрома как одного из проявлений ГВИ.
Задачи исследования:
-
Оценка клинической эффективности препарата инозин пранобекс (Нормомед®) у детей.
-
Оценка симптомов интоксикационного, катарального и лимфопролиферативного синдромов у детей с РРИ до и после терапии.
-
Оценка количества активных герпесвирусов у детей с РРИ до и после терапии.
-
Оценка доли пациентов с активной инфекцией каждого из изучаемых герпесвирусов до и после терапии.
На момент включения в исследование у всех детей были выявлены активные формы ГВИ. При этом у 57,3% (55 детей) — моногерпесвирусная инфекция и у 42,7% (41 ребенок) — ГВИ сочетанной этиологии. Наиболее часто выявлялся активный ВГЧ-6А/В — у 75 (78,1%) детей, вторым по частоте был ВЭБ — 44 (45,8%), ВПГ-1 выявлен у 14 (14,6%) детей, ЦМВ — у 9 (9,4%). В этиологической структуре ГВИ наиболее часто встречались моноинфекция ВГЧ-6А/В — 35 (36,5%) случаев, сочетание ВГЧ-6А/В + ВЭБ — 23 (24,0%) случая и моноинфекция ВЭБ — 16 (16,7%) случаев, несколько реже обнаруживалась сочетанная инфекция ВГЧ-6А/В + ВПГ — у 9 (9,4%) пациентов (рис. 1).
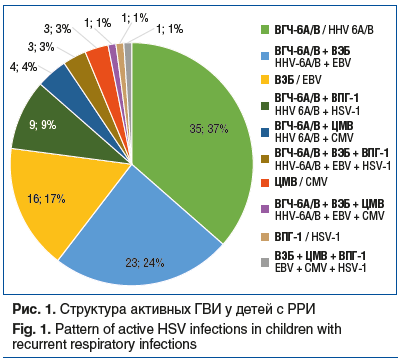
Для статистической обработки данных использовали программу StatTech v. 3.1.8 (ООО «Статтех», Россия). Количественные переменные представлены как медиана (Me) и квартили (Q1; Q3), для категориальных переменных указаны абсолютные значения и доли (%). Проводили анализ связанных совокупностей с использованием критерия Уилкоксона, теста Макнемара. Различия считали статистически значимыми при p<0,05.
Результаты исследования
В соответствии с поставленными задачами мы проводили оценку эффективности терапии в несколько этапов. На первом этапе оценивали общую клиническую эффективность проводимой нами терапии. Для этого определяли количество и качество ОРИ в течение всего периода наблюдения.
Улучшение фиксировали при отсутствии острых респираторных заболеваний в течение периода от начала терапии (3 мес.); частичное улучшение — в случае уменьшения числа эпизодов и/или снижения тяжести течения ОРИ. При сохраняющихся ежемесячных респираторных заболеваниях констатировали отсутствие эффекта. В подавляющем большинстве наблюдений удалось добиться улучшения состояния (рис. 2).
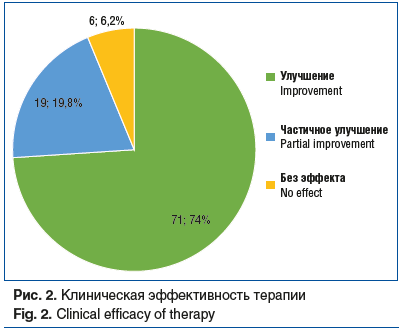
В целом курсовое применение препарата Нормомед® приводило к снижению частоты и тяжести респираторных заболеваний у детей в течение 3 мес. от начала терапии в 93,8% (n=90) наблюдений.
Для решения второй задачи был проведен анализ динамики клинических проявлений.
До лечения повышение температуры имело место у 10 детей: субфебрильная температура — у 9 (9,4%) детей, из них у 5 в течение 1 мес. и более, фебрильная — у 1 (1%) ребенка. После терапии в этой группе у 7 (70%) детей наблюдалась нормализация, у 3 (30%) — сохранялось повышение температуры (табл. 1).
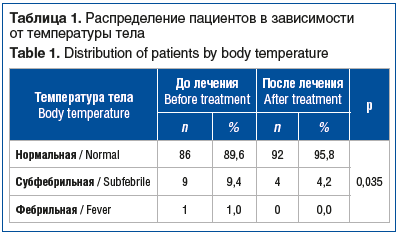
Таким образом, на фоне курса терапии препаратом Нормомед® мы наблюдали достоверное уменьшение выраженности лихорадочного синдрома: купирование фебрильной лихорадки и уменьшение доли пациентов с субфебрилитетом в 2 раза.
Динамику катарального синдрома у детей с РРИ мы оценивали на основании изменений фарингоскопической картины, полученной при осмотре детей.
Выраженность гиперемии ротоглотки у пациентов была минимальной и не имела статистически значимых изменений в динамике (р=0,127). Гиперемия ротоглотки отсутствовала у 78 (81,2%) детей на начальном этапе наблюдения и у 86 (89,6%) при повторном осмотре. Выраженность симптома несколько снизилась, после лечения отсутствовали пациенты с яркой гиперемией (рис. 3).
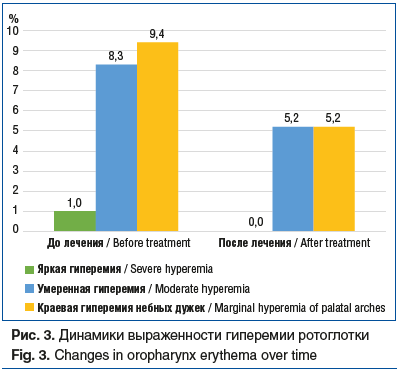
Среди тех 18 пациентов, у которых наблюдалась гиперемия, были отмечены положительные изменения: в 12 (66,7%) случаях состояние ротоглотки нормализовалось, у 5 (27,8%) детей динамика отсутствовала.
Для анализа выраженности гранулярного фарингита были использованы следующие критерии:
-
единичные лимфоидные фолликулы;
-
лимфоидные фолликулы покрывают менее 1/3 видимой части задней стенки глотки (ЗСГ);
-
лимфоидные фолликулы покрывают от 1/3 до 1/2 видимой части ЗСГ;
-
лимфоидные фолликулы покрывают более 1/2 видимой части ЗСГ
.
На начальном этапе проявления гранулярного фарингита наблюдались у большинства (85 (88,6%)) детей. После проведенного лечения доля детей с единичными фолликулами увеличилась до 25 (26%), а выраженность гранулярного фарингита снизилась (p<0,001; табл. 2).
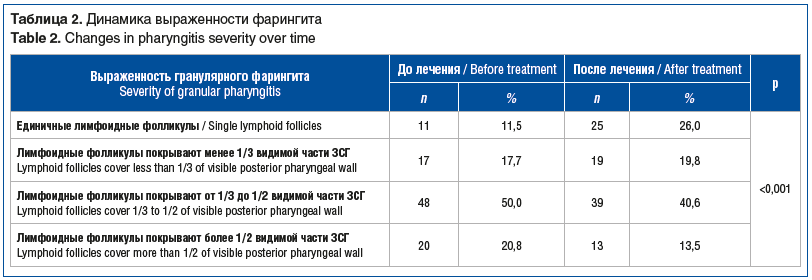
Среди тех пациентов, которые имели проявления гранулярного фарингита до назначения терапии, наблюдались следующие изменения: состояние нормализовалось у 16 (18,8%), положительная динамика отмечена у 13 (15,3%), отсутствовали изменения у 51 (60%) ребенка.
Таким образом, у 34,1% пациентов мы наблюдали уменьшение зернистости ЗСГ на фоне проводимого курса терапии.
Лимфопролиферативный синдром является одним из ведущих проявлений активной ГВИ у детей, длительно сохраняющимся даже после уменьшения числа эпизодов ОРИ. Он включает гипертрофию лимфоидной ткани аденотонзиллярной зоны, регионарную и генерализованную лимфоаденопатию, гепатолиенальный синдром. В нашем исследовании не было технической возможности оценить выраженность гипертрофии аденоидов у всех пациентов. Однако все остальные проявления лимфопролиферативного синдрома были проанализированы (табл. 3).
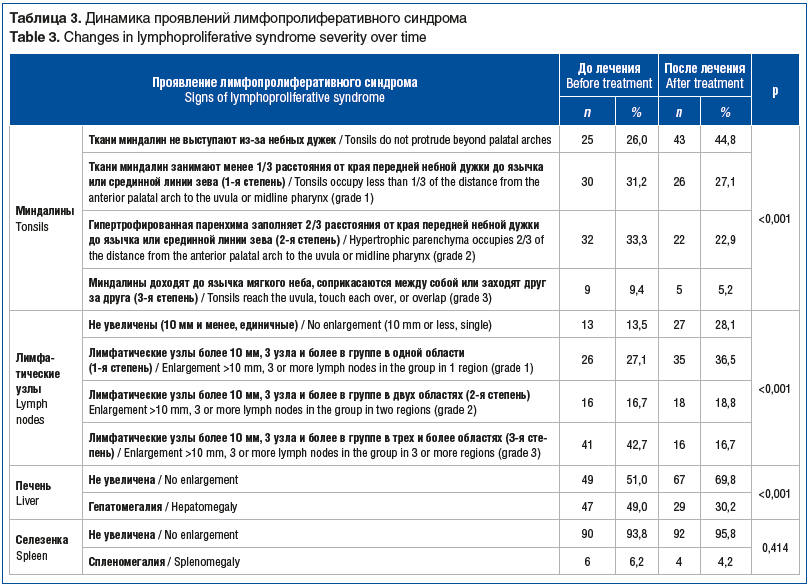
Гипертрофия миндалин была распространенным симптомом у детей с РРИ и активной ГВИ. Только у 25 (26%) пациентов ткани миндалин не выступали из-за небных дужек. Большинство детей имели увеличение миндалин до 1-й или 2-й степени (см. табл. 3). После лечения снизилась доля пациентов с гипертрофией, а также наблюдалось уменьшение выраженности увеличения миндалин (p<0,001). Среди детей с гипертрофией у 20 (28,2%) наблюдалась полная нормализация размеров миндалин после лечения, у 17 (23,9%) — значительная положительная динамика. В 30 (42,3%) случаях размеры миндалин не изменились.
Проведен анализ динамики выраженности лимфоаденопатии. Увеличение лимфатических узлов имело место более чем у 85% детей, у большинства из них (41–42,7%) — до 3-й степени (лимфатические узлы более 10 мм, 3 узла и более в группе в трех и более областях). На фоне этиотропной терапии не только увеличилась доля (27 (28,1%)) детей с нормальными размерами лимфатических узлов, но и сократилась выраженность лимфоаденопатии. Только у 16 (16,7%) детей сохранялось увеличение до 3-й степени. Положительная динамика наблюдалась у 25 (30,1%) детей, нормализация показателя — у 17 (20,5%).
Увеличение печени имело место у половины детей до противовирусной терапии, у трети пациентов — после проведенного лечения (р<0,001). Динамика размеров печени на фоне противовирусного лечения препаратом Нормомед® характеризовалась нормализацией у 15 (31,9%) детей, улучшением у 11 (23,4%), размеры печени не изменились у 19 (40,4%) пациентов.
Увеличение селезенки у пациентов наблюдалось редко (менее чем в 10% случаев) и не имело статистически значимых изменений в динамике. Из 6 детей со спленомегалией на начальном этапе у 4 (66,7%) наблюдалась нормализация размеров селезенки после проведенного лечения.
Результаты оценки динамики клинических проявлений представлены на рисунке 4.
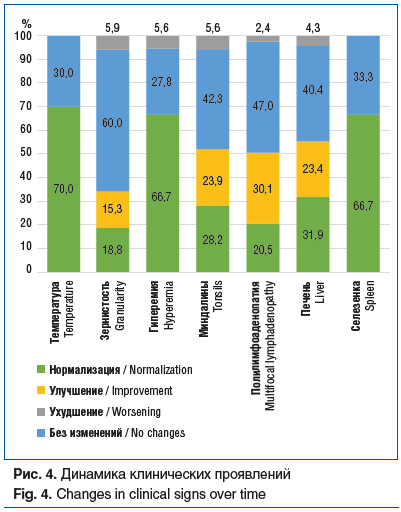
Таким образом, у пациентов зарегистрирована значимая положительная динамика не только по количеству эпизодов ОРИ, но и по отдельным симптомам активных ГВИ. Достоверные различия зафиксированы в динамике лихорадки (купирование фебрильной и уменьшение доли субфебрильной в 2 раза), состояния слизистых ротоглотки (в 66,7%), сокращения размеров миндалин (52,1%), лимфатических узлов (50,6%) и печени (54,3%).
Для решения третьей задачи мы оценивали противовирусную эффективность терапии на основании специально разработанных критериев.
При отсутствии лабораторных маркеров активной ГВИ после окончания курса терапии диагностировалось улучшение. У пациентов с сочетанной инфекцией переход одного из прежде активных вирусов в латентную форму свидетельствовал о частичном улучшении.
После проведенного лечения препаратом Нормомед® улучшение имело место у 85 (88,6%) детей (рис. 5).
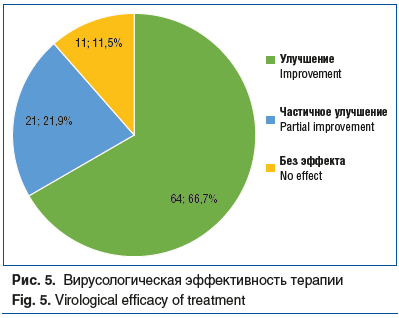
Таким образом, на фоне лечения уменьшение активности ГВИ регистрировали несколько реже, чем клиническое улучшение. Подобный факт объясняется «запаздыванием» лабораторных показателей активности ГВИ относительно клинических проявлений заболевания.
Для решения последней, четвертой, задачи был проведен анализ активности каждого из вирусов до и после лечения (табл. 4).
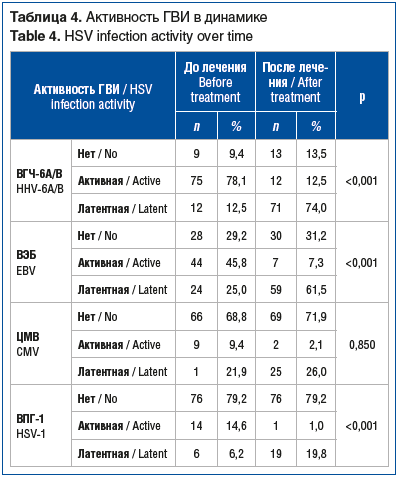
Основным критерием включения в исследование была верификация активной формы ГВИ, однако у 41,7% детей мы верифицировали ГВИ сочетанной этиологии, при которой часть вирусов находилась в латентной форме, а другие были активны.
Таким образом, продемонстрирована противовирусная активность препарата Нормомед® в отношении всех изучаемых видов герпесвирусов: ВПГ-1, ВГЧ-6А/В, ВЭБ, ЦМВ.
Также было проанализировано общее количество активных ГВИ на двух этапах наблюдения (рис. 6).
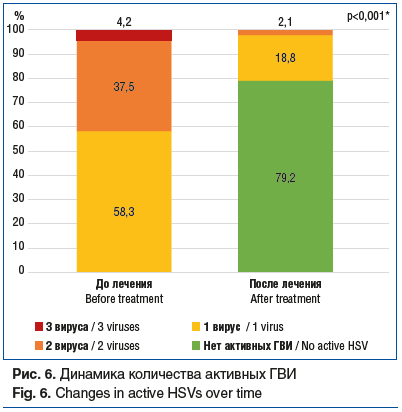
На начальном этапе все дети имели активные ГВИ, тогда как после завершения курс этиотропной терапии у 76 (79,2%) пациентов не было зафиксировано активных ГВИ (p<0,001). У детей с РРИ и ГВИ чаще выявляются ВГЧ-6А/В, ВЭБ и их сочетания. При динамическом наблюдении после проведенного лечения наблюдалось статистически значимое снижение доли пациентов с активными формами ВГЧ-6А/В (с 78,1 до 12,5%), ВЭБ (с 45,8 до 7,3%), ВПГ-1 (с 14,6 до 1,0%). Также достоверно снижалось количество активных вирусов. Если до терапии у 41,7% пациентов зарегистрированы ГВИ сочетанной этиологии, то после терапии их количество уменьшилось в 2 раза (до 20,9%) и отсутствовали сочетания сразу трех активных герпесвирусов. Следовательно, можно говорить о вирусологической активности препарата в отношении всех анализируемых вариантов герпесвирусов.
Обсуждение
Проблема РРИ у детей является не только медицинской, но и социальной. У детей с РРИ младше 7 лет без своевременной диагностики и выявления причин этого состояния формируется хроническая соматическая патология более чем в половине случаев уже к 16 годам.
Причины РРИ у детей могут быть самыми различными: аллергические заболевания, врожденные пороки, заболевания органов и систем не диагностированные ранее, а также первичные иммунодефицитные состояния [6–9]. Однако при исключении вышеперечисленных причин практикующий врач сталкивается с ситуацией, когда более чем в половине случаев дети с рекуррентными ОРИ не имеют хронических заболеваний, но тем не менее продолжают болеть каждый месяц.
Герпесвирусные инфекции являются пантропными, повсеместно распространенными и первично-хроническими. Инфицированность ГВИ у детей с РРИ достигает 96% [17, 18]. Однако доказанную роль в возникновении повторных эпизодов ОРИ могут играть только активные их формы, доля которых составляет не более 40% [19]. В связи с этим вопросы своевременной комплексной диагностики ГВИ у детей являются актуальными в педиатрической практике.
Инозин пранобекс — комплексный препарат, обладающий противовирусным и иммуномодулирующим эффектами. Его эффективность была продемонстрирована в целом ряде доклинических и клинических исследований в отношении различных вирусов: респираторной группы, кори, герпесвирусов, вирусов гепатита, ВИЧ. В нашей стране подобные исследования проводились и ранее [20–22] и продемонстрировали клиническую эффективность инозина пранобекса.
В настоящем исследовании с участием 96 детей, обратившихся к врачу педиатру-инфекционисту с жалобами на ежемесячные респираторные инфекции с подтвержденными активными формами ГВИ, была проведена оценка эффективности трех курсов инозина пранобекса (Нормомед®) как с клинической точки зрения (частота выявления интоксикационного, катарального и лимфопролиферативного синдромов различной степени выраженности), так и с точки зрения противовирусной активности.
Особенностью настоящего исследования является комплексная оценка клинических и вирусологических показателей у обследованных детей на фоне проводимой терапии с использованием методов, предназначенных для связанных выборок, что позволило установить достоверные различия между соматическим и вирусологическим статусом пациентов до и после терапии.
Выводы
-
Назначение курса терапии препаратом инозин пранобекс (Нормомед®) приводило к снижению частоты и тяжести респираторных заболеваний у детей в течение 3 мес. от начала терапии в 94% (90) наблюдений.
-
На фоне курса терапии достоверно уменьшается выраженность лихорадочного синдрома: купирование фебрильной лихорадки и уменьшение доли пациентов с субфебрилитетом в 2 раза.
-
Применение препарата Нормомед® приводило к нормализации состояния слизистых ротоглотки: уменьшению гиперемии ротоглотки в 12/66,7% наблюдений и уменьшению зернистости задней стенки глотки в 34,1% случаев.
-
Через 3 мес. после начала терапии препаратом инозин пранобекс (Нормомед®) мы фиксировали положительные изменения в отношении лимфопролиферативного синдрома у 60/62,5% пациентов. Так, положительная динамика в отношении гипертрофии небных миндалин отмечена в 52,1% случаев, в отношении лимфоаденопатии — в 50,6%, гепатомегалии — в 55,3%, спленомегалии — в 66,7%.
-
На фоне лечения препаратом Нормомед® мы регистрировали уменьшение активности ГВИ у 88,6% (85) детей.
-
После проведенного лечения наблюдалось статистически значимое снижение доли пациентов с активными формами ВГЧ-6А/В (с 78,1 до 12,5%), ВЭБ (с 45,8 до 7,3%) и ВПГ-1 (с 14,6 до 1,0%).
-
У пациентов, получавших инозин пранобекс (Нормомед®),достоверно снижалось количество активных герпесвирусов. Если до терапии у 42,7% (41) пациентов зарегистрированы ГВИ сочетанной этиологии, то после терапии их количество уменьшилось в 2 раза (20,9%) и отсутствовали сочетания сразу трех активных герпесвирусов.
1Approach to the child with recurrent infections, 2022. (Electronic resource.) URL: https://www.uptodate.com/contents/approach-to-the-child-with-recurrent-infections (access date: 01.08.2023).
Сведения об авторах:
Мелехина Елена Валериевна — д.м.н., доцент по специальности «педиатрия», ведущий научный сотрудник клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; врач-педиатр инфекционного отделения ГАУЗ МО «Химкинская ОБ»; 141407, Россия, г. Химки, Куркинское ш., д. 11; ORCID iD 0000-0002-9238-9302.
Преображенская Дарья Владимировна — клинический ординатор 2-го года обучения ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0009-0000-6152-0251.
Музыка Анна Драгиевна — к.м.н., старший научный сотрудник клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0002-2269-2533.
Солдатова Евгения Юрьевна — младший научный сотрудник клинического отдела инфекционной патологии ФГБНУ ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0002-0683-8010.
Горелов Александр Васильевич — член-корр. РАН, д.м.н., профессор, заместитель директора по научной работе ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; профессор кафедры детских болезней ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-9257-0171.
Контактная информация: Мелехина Елена Валериевна, e-mail: e.melekhina@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов: отсутствует.
Статья поступила: 09.09.2023.
Поступила после рецензирования: 03.10.2023.
Принята в печать: 26.10.2023.
Информация с rmj.ru






