Введение
В практическом здравоохранении актуальна проблема развития остеопении и остеопороза в молодом возрасте, что диктует необходимость их ранней, своевременной диагностики [1]. Вопросы метаболических нарушений костной системы и их последствий у недоношенных детей на сегодняшний день изучены мало. Известно, что метаболические нарушения могут быть связаны с патологиями беременности, внутриутробной задержкой роста и заболеваниями перинатального периода [2–4].
Одним из основных параметров оценки прочности костей является минеральная плотность костной ткани (МПКТ). В клинической практике широко применяется неинвазивный способ измерения МПКТ и определения вероятности ее переломов — денситометрия.
Для определения эффективности терапевтических и профилактических методов, применяемых у детей с дефицитом потребления минеральных веществ, особенно рожденных после применения экстракорпорального оплодотворения (ЭКО) и недоношенных, необходимы знания возрастной анатомии, физиологии костно-мышечного аппарата и способов оценки предикторов, оказывающих на него воздействие. Несмотря на актуальность вопроса профилактики нарушений минерализации скелетной системы у этих детей в развитых странах и имеющийся опыт в нашей стране, до сих пор отмечаются очевидный недостаток в подобных научных исследованиях и отсутствие методов их ранней диагностики и принципов их коррекции и профилактики в зависимости от возраста и фактической обеспеченности детей нутриентами.
Цель работы: оценить состояние МПКТ с помощью скрининговой ультразвуковой (УЗ) денситометрии у недоношенных детей, рожденных после применения ЭКО или рожденных без применения ЭКО с массой тела менее 1500 г.
Материал и методы
Проведено обследование 189 недоношенных детей на базе отделения патологии новорожденных и недоношенных детей неонатального центра в ГБУЗ РДКБ (г. Уфа).
Критерии включения: согласие родителей на участие ребенка в исследовании, возраст от 1 года до 3 лет; масса тела при рождении 1500 г и менее, сопутствующие заболевания легкой степени.
Критерии исключения: отзыв согласия на участие в исследовании, нарушение протокола исследования или врачебной инструкции.
В зависимости от того, были дети рождены после применения ЭКО или после естественного зачатия, их распределили в 2 группы. В зависимости от массы тела при рождении каждую группу разделили на 2 подгруппы: подгруппы А составляли дети с очень низкой массой тела (ОНМТ), подгруппы Б — дети с экстремально низкой массой тела (ЭНМТ).
Таким образом, 1-ю группу (n=101), основную, составили дети, рожденные после проведения ЭКО, из них в подгруппы 1А и 1Б вошли 52 и 49 детей соответственно; 2-ю группу (n=88), группу сравнения, составили дети, рожденные после естественного зачатия, из них в подгруппы 2А и 2Б вошли 46 и 42 ребенка соответственно. МПКТ измеряли методом УЗ-остеоденситометрии, в основе которого лежит измерение скорости ультразвуковой волны (Speed of Sound, SOS) при прохождении через костную ткань.
При помощи УЗ-остеоденситометра Sunlight Omnisense® 7000 (Израиль) проводилась оценка SOS и стандартизированного Z-критерия (Z-score), представляющего прочность кости ребенка относительно средневозрастной нормы для того же пола и возраста (стандартное отклонение (SD) на большеберцовой кости). При этом методе исследования в соответствии с инструкцией применялся специальный датчик, который располагали между пяткой и коленным суставом. Продолжительность измерения одного участка скелета составляла 1 мин.
Полученные результаты костной прочности по Z-критерию сопоставлены с базой данных прибора. Показателем дефицита костной прочности считали Z-score <-1 SD (SOS <10‰ и >3‰) (группа риска снижения прочности кости), клинически значимым снижением прочности кости — Z-score <-2 SD (SOS <3‰). Последующий анализ выполнялся при сравнении с перцентильными таблицами средневозрастных показателей SOS [5].
Статистическая обработка полученных результатов проводилась при помощи цифровых программ Microsoft Excel 2013 и Statistica 12.0.
Результаты и обсуждение
Результаты исследования представлены в таблицах 1–3. Нормальная прочность кости была зарегистрирована у 39 (38,6%) детей 1-й группы и 58 (65,9 %) детей 2-й группы (p>0,05). У детей 1-й группы статистически значимо чаще встречалось снижение прочности кости (<-1SD), чем у детей 2-й группы (49 (48,5%) против 21 (23,8%) соответственно, p<0,05). Снижение прочности кости (<-2SD) зарегистрировали у 13 (12,8%) детей 1-й группы и 9 (10,2 %) детей 2-й группы (p>0,05).
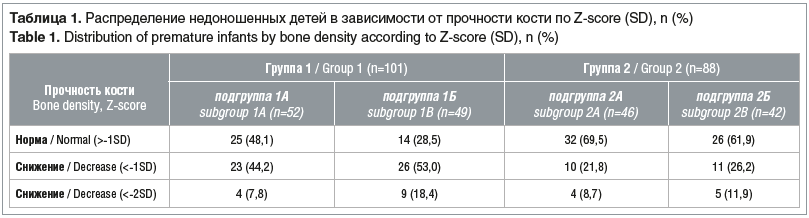

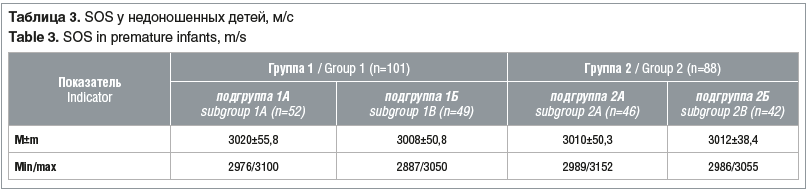
Не выявили существенных различий при сравнении долей детей с нормальными или сниженными показателями Z-score в подгруппах 1А и 1Б, 2А и 2Б.
Сравнивая показатели костной прочности (см. табл. 2) с данными литературы [5–7], мы установили, что нормальный показатель Z-score характерен для доношенных детей в возрасте ближе к 1,5–2 годам (нашим детям 3 года), что еще раз характеризует снижение костной прочности у недоношенных детей, рожденных с ЭНМТ или ОНМТ после ЭКО или после естественного зачатия. Можно сделать вывод о наличии взаимосвязи возрастных изменений и данных SOS (r=0,86, р=0,000). Во время развития ребенка происходит поэтапное нарастание прочности костей [5, 6].
При изучении полученных в результате анализа показателей SOS большеберцовой кости в сравнении с центильными таблицами средневозрастных показателей SOS установлено снижение костной прочности относительно данных российских исследователей [5]. Клинически значимое снижение прочности кости (SOS <3‰) у детей, рожденных после применения ЭКО, отмечали в 13 (12,8%) случаях. ЭНМТ у детей, рожденных с помощью ЭКО, является фактором риска развития остеопении и остеопороза (χ2=4,5, p<0,03, отношение рисков 4,5, 95% доверительный интервал от 3,6 до 5,5).
В настоящее время для измерения плотности костной ткани используются следующие методы: двухэнергетическая рентгеновская абсорбциометрия, по результатам которой МПКТ определяется как значение плотности, измеряемой в г/см2 на уровне L1–L4 или проксимального отдела бедра [8]; количественная КТ; двухэнергетическая КТ (наиболее современный метод диагностики остеопороза, позволяющий максимально точно определять уровень МПКТ, выраженность остеопороза) [9], УЗ-остеоденситометрия — способ оценки МПКТ путем измерения скорости ультразвуковой волны при ее прохождении через костную ткань.
Диагностическая способность рентгеновской денситометрии заключается в определении трех параметров: минерального содержания кости (МСК) (г), площади проекции исследуемого участка (см2) и проекционной минеральной плотности кости (г/см2). Последняя величина клинически наиболее значимая. Она вычисляется делением МСК на площадь проекции [10]. Уменьшение минеральной плотности скелетного аппарата клинически определяют как остеопению (состояние субнормально минерализованной кости) или остеопороз (патологически низкая масса костной ткани с ухудшением ее архитектуры) [11]. Необходимо отметить, что МПКТ достигает максимальной величины в подростковом возрасте, а именно в период полового созревания [12, 13].
Раннее выявление остеопении может осуществляться безопасным способом — УЗ-денситометрией. Она может применяться для оценки МПКТ у детей. Для УЗ-денситометрии применяется портативное оборудование. Метод характеризуется незначительной лучевой нагрузкой, быстротой выполнения, низкой стоимостью, что делает его основным в обследовании недоношенных детей.
Заключение
У детей с ОНМТ и ЭНМТ, рожденных после применения ЭКО, выявлено существенное снижение прочности кости (SOS <10‰ и >3‰) по сравнению с показателями у детей, рожденных после естественного зачатия. При оценке денситометрических показателей выявлено снижение прочности кости на 3‰ (клинически значимое снижение) у недоношенных детей, рожденных с ЭНМТ после ЭКО, в 12,8% случаев. Результаты исследования, показывающие высокий процент уменьшения МПКТ у недоношенных детей (рожденных после ЭКО или после естественного зачатия), обосновывают необходимость разработки региональных референтных баз данных.
Раннее выявление остеопении осуществляется с применением УЗ-денситометрии, которая безопасна для детей, поскольку сопровождается незначительной лучевой нагрузкой. В будущем возможно применение УЗ-денситометрии в качестве скринингового метода ранней диагностики патологических изменений костной системы.
Сведения об авторах:
Мерзлякова Динара Рафкатовна — ассистент кафедры педиатрии с курсом института дополнительного профессионального образования ФГБОУ ВО БГМУ Минздрава России; 450008, Россия, г. Уфа, ул. Ленина, д. 3; врач-педиатр кабинета катамнеза ГБУЗ РДКБ; 450054, Россия, г. Уфа, ул. Степана Кувыкина, д. 98; ORСID iD 0000-0001-9037-7124.
Хафизова Наиля Римовна — к.м.н., доцент кафедры педиатрии с курсом института дополнительного профессионального образования ФГБОУ ВО БГМУ Минздрава России; 450008, Россия, г. Уфа, ул. Ленина, д. 3; ORCID iD 0000-0002-1452-9998.
Вахитова Гульназ Абрековна — к.м.н., доцент кафедры педиатрии с курсом института дополнительного профессионального образования ФГБОУ ВО БГМУ Минздрава России; 450008, Россия, г. Уфа, ул. Ленина, д. 3; ORCID iD 0000-0001-9452-0901.
Шангареева Зилия Асгатовна — к.м.н., доцент кафедры факультетской педиатрии с курсом педиатрии, неонатологии и симуляционным центром института дополнительного профессионального образования ФГБОУ ВО БГМУ Минздрава России; 450008, Россия, г. Уфа, ул. Ленина, д. 3; ORCID iD 0000-0001-8745-9989.
Гилязова Гульнара Газимовна — заведующая отделением лабораторной диагностики ГБУЗ РДКБ; 450054, Россия, г. Уфа, ул. Степана Кувыкина, д. 98; ORСID iD 0000-0002-1210-6588.
Назарова Альфия Идрисовна — к.м.н., доцент кафедры терапии и сестринского ухода за больными ФГБОУ ВО БГМУ Минздрава России; 450008, Россия, г. Уфа, ул. Ленина, д. 3; ORCID iD 0000-0002-6943-3096.
Контактная информация: Мерзлякова Динара Рафкатовна, e-mail: Dinara-merzlyakova@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 27.04.2022.
Поступила после рецензирования 26.05.2022.
Принята в печать 21.06.2022.
About the Authors:
Dinara R. Merzlyakova — assistant of the Department of Pediatrics with a course of the Institute of Additional Professional Education, Bashkir State Medical University; 3, Lenin str., Ufa, 450008, Russian Federation; pediatrician of the Prospective Follow-Up Room, Republican Children’s Clinical Hospital; 98, Stepana Kuvykina str., Ufa, 450106, Russian Federation; ORСID iD 0000-0001-9037-7124.
Nailya R. Khafizova — C. Sc. (Med.), associate professor of the Department of Pediatrics with a course of the Institute of Additional Professional Education, Bashkir State Medical University; 3, Lenin str., Ufa, 450008, Russian Federation; ORCID iD 0000-0002-1452-9998.
Gulnaz А. Vakhitova — C. Sc. (Med.), associate professor of the Department of Pediatrics with a course of the Institute of Additional Professional Education, Bashkir State Medical University; 3, Lenin str., Ufa, 450008, Russian Federation; ORCID iD 0000-0001-9452-0901.
Ziliya А. Shangareeva — C. Sc. (Med.), associate professor of the Department of Faculty Pediatrics with a course of pediatrics, neonatology and simulation center of the Institute of Additional Professional Education, Bashkir State Medical University; 3, Lenin str., Ufa, 450008, Russian Federation; ORCID iD 0000-0001-8745-9989.
Gulnara G. Gilyazova — Head of the Laboratory Diagnostics Department, Republican Children’s Clinical Hospital; 98, Stepana Kuvykina str., Ufa, 450106, Russian Federation; ORСID iD 0000-0002-1210-6588.
Alfiya I. Nazarova — C. Sc. (Med.), associate professor of the Department of Therapy and Nursing Care, Bashkir State Medical University; 3, Lenin str., Ufa, 450008, Russian Federation; ORCID iD 0000-0002-6943-3096.
Contact information: Dinara R. Merzlyakova, e-mail: Dinara-merzlyakova@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 27.04.2022.
Revised 26.05.2022.
Accepted 21.06.2022.
Информация с rmj.ru






