Ключевые слова: анемия, искусственные клапаны сердца, сердечно-сосудистая хирургия, послеоперационная анемия, механический гемолиз, шистоциты.
Для цитирования: Николенко Л.А. Приобретенная механическая гемолитическая анемия, вызванная дисфункцией имплантированных сердечных клапанов // РМЖ. 2018. №1(II). С. 126-128
Nikolenko L.A.
Federal Center of Cardiovascular Surgery, Chelyabinsk
Surgical correction of the heart valves makes urgent the problem of postoperative anemia, which can have a different character. The course of the postoperative period in such patients largely depends on the possibility of developing the acquired mechanical hemolytic anemia. In connection with the improvement of the methodology of surgical interventions, as well as with the modernization of prosthetic heart valve (HV), cardiovascular risk in heart operations during the last decades has significantly decreased in all age groups. Using a new generation of prostheses has reduced the frequency of hemolytic anemia to 1%. In modern conditions, the most frequently expressed signs of hemolysis are caused by the prosthesis dysfunction, for example, due to the formation of para-valvular fistula. The destruction of erythrocytes with the development of hemolysis is associated with a violation of blood flow through the defective prosthesis and an increased damage to erythrocytes by the valves. The syndrome of mechanical hemolysis is confirmed by the detection the fragments of erythrocytes (Fragmentes Red Cell (FRC)) or schistocytes in the patient’s blood smear.
Key words: anemia, prosthetic heart valves, cardiovascular surgery, postoperative anemia, mechanical hemolysis, schistocytes.
For citation: Nikolenko L.A. Acquired mechanical hemolytic anemia, caused by dysfunction of implanted heart valves (with a description of clinical cases) // RMJ. 2018. № 1(II). P. 126–128.
Статья посвящена проблеме приобретенной механической гемолитической анемии, вызванной дисфункцией имплантированных сердечных клапанов. Показано, что в современных условиях наиболее часто выраженные признаки гемолиза наблюдаются при дисфункции протеза, например, вследствие образования параклапанной фистулы. Представлены клинические случаи.
В настоящее время благодаря современным возможностям сердечно-сосудистой хирургии операция протезирования клапанов сердца стала повседневной в работе специализированных кардиохирургических центров. В мире живут десятки тысяч пациентов с имплантированными сердечными протезами. В условиях хирургической коррекции клапанов становится актуальной проблема послеоперационной анемии, которая может носить различный характер. Вероятность развития у такого рода больных приобретенной механической гемолитической анемии во многом определяет течение послеоперационного периода. Большое значение в достижении хороших отдаленных результатов приобретают квалифицированный контроль и лечение этих пациентов у врача поликлиники по месту жительства [1].
Данные о воздействии протезов на эритроциты и на возникновение гемолиза противоречивы. По данным некоторых исследователей, гемолиз бывает клинически невыраженным, в других работах имеются указания на значительные клинические проявления гемолиза [1–4]. Степень клинических проявлений гемолиза зависит как от состояния самих эритроцитов, так и от механических свойств протезов [5, 6]. Несомненно, играют роль не только обработка протеза и материал, из которого он сделан, но и гемодинамические условия: скорость кровотока в области протеза, образование завихрений.
В связи с улучшением методологии оперативных вмешательств, а также с модернизацией искусственных клапанов сердца (ИКС) сердечно-сосудистый риск при операциях на сердце в течение последних десятилетий существенно снизился во всех возрастных группах. В 1960–1970-е гг. после введения в практику протезирования клапанов сердца гемолитическая анемия развивалась у 5–15% прооперированных пациентов, особенно после имплантирования механических шаровых протезов [2, 5]. Использование протезов нового поколения снизило частоту гемолитической анемии до 1% [2, 6]. Современные искусственные клапаны сердца разработаны на основе клинических данных использования нескольких поколений протезов. Они изготовлены из новейших материалов и имеют уникальную конструкцию [7, 8]. Однако компенсированный гемолиз может возникнуть при любом типе протеза. Наиболее часто выраженные признаки гемолиза наблюдаются при нарушении функции протеза, например, вследствие образования параклапанной фистулы. Разрушение эритроцитов с развитием гемолиза связано с нарушением кровотока через дефектный протез и увеличением повреждения эритроцитов его створками [3, 7]. Клинически гемолиз может проявляться симптомами сердечной недостаточности и анемии. Наблюдаются бледность кожных покровов, желтуха, моча может приобретать коричневый или черный цвет. Содержание билирубина повышено, особенно непрямая фракция, могут быть ретикулоцитоз, повышение активности лактатдегидрогеназы (ЛДГ) и уровня свободного гемоглобина в плазме крови. Синдром механического гемолиза подтверждается обнаружением в мазке крови больного фрагментов (обломков) эритроцитов (Fragmentes Red Cell (FRC)) или шистоцитов (син. — шизоциты). Наблюдаются анизопойкилоцитоз (изменение формы и размеров эритроцитов), полихромазия (способность окрашиваться как основными, так и кислыми красителями). При длительно протекающем гемолизе развивается дефицит железа.
В отечественной и зарубежной литературе описано очень мало случаев макроангиопатической гемолитической анемии, связанной с механическим повреждением эритроцитов у пациентов с ИКС. Мы приводим собственные наблюдения о гемолизе, вызванном дисфункцией механического двустворчатого протеза МедИнж (ЗАО НПП «МедИнж», Россия).
Пациентка, 65 лет.
Диагноз: сочетанный приобретенный порок митрального, аортального и трикуспидального клапанов. Проведено протезирование аортального (МедИнж 23) и митрального (МедИнж 29) клапанов, аннулопластика трикуспидального клапана по Де Вега-2.
До оперативного вмешательства у пациентки показатели красной крови не выходили за пределы соответствующих референтных интервалов: эритроциты — 4,16×1012/л; гемоглобин — 124 г/л; гематокрит — 36%; средний объем эритроцитов — 86,6 фл; среднее содержание гемоглобина в эритроците — 29,8 пг; средняя концентрация гемоглобина в эритроците — 344 г/л; ширина распределения эритроцитов по объему — 13,7%. На 10-е сут после операции у нее наблюдалась нормохромная анемия: эритроциты — 2,74×1012/л; гемоглобин — 83,2 г/л; гематокрит — 23,7%; средний объем эритроцитов — 86,7 фл; среднее содержание гемоглобина в эритроците — 30,4 пг; средняя концентрация гемоглобина в эритроците — 351 г/л; ширина распределения эритроцитов по объему — 16,1%. Через 1 мес. признаки анемии сохранялись: эритроциты — 2,54×1012/л; гемоглобин — 80,2 г/л; гематокрит — 23%; средний объем эритроцитов — 82,3 фл; среднее содержание гемоглобина в эритроците — 27,4 пг; средняя концентрация гемоглобина в эритроците — 351 г/л; ширина распределения эритроцитов по объему — 17,1%. На фоне приема сульфата железа и аскорбиновой кислоты 200 мг/сут эффекта не наблюдалось.
Пациентку беспокоили одышка при минимальной физической нагрузке, в положении лежа, отеки, повышенная утомляемость. Через 6 мес. после операции в связи с сохранением жалоб, признаков анемии (гемоглобин — 70–80 г/л) находилась на лечении в терапевтическом отделении. У пациентки был повышен уровень непрямого билирубина (40,4 мкмоль/л), проба Кумбса отрицательная, отмечалось периодическое выделение мочи черного цвета. Эффекта от преднизолона не было. Была обследована у гематолога, диагностирована приобретенная гемолитическая анемия, обусловленная механическим повреждением эритроцитов протезированными клапанами сердца. Направлена в кардиохирургический стационар для решения вопроса о повторном оперативном вмешательстве.
При поступлении в стационар состояние тяжелое. Кожные покровы бледные, желтушные. Живот увеличен за счет асцита. Пастозность стоп, лодыжек. Тоны сердца приглушены, аритмичные. Мелодия протеза четкая, систолический шум во всех точках. На эхокардиографии: в проекции аортального клапана протез без признаков дисфункции; в проекции митрального клапана диагностирована трансклапанная регургитация 1–2 степени, по задней части протеза — параклапанная фистула 2 степени. Показатели красной крови: эритроциты — 2,76×1012/л; гемоглобин — 90 г/л; гематокрит — 26,3%; средний объем эритроцитов — 95,6 фл; среднее содержание гемоглобина в эритроците — 32,2 пг; средняя концентрация гемоглобина в эритроците — 342 г/л; ширина распределения эритроцитов по объему — 24,3%, при микроскопии окрашенного мазка — полихромазия, шистоциты (2,0%) (рис. 1), ретикулоциты — 2,5%. Билирубин общий — 98,5 мкмоль/л, билирубин непрямой — 50,4 мкмоль/л, свободный гемоглобин — 0,6 г/л.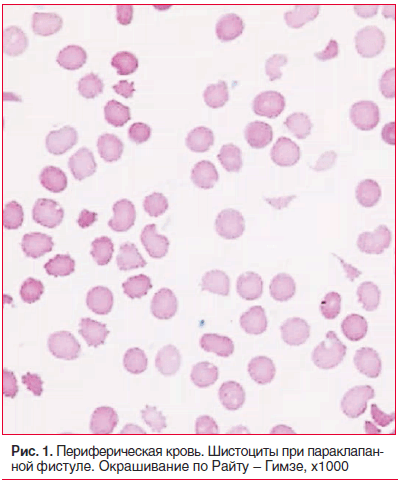
К сожалению, ввиду наличия у пациентки аортального протеза эндоваскулярное закрытие параклапанной фистулы митрального протеза было технически невыполнимо. В настоящее время пациентка наблюдается у кардиолога и гематолога по месту жительства. При снижении гемоглобина ниже 60 г/л ей проводятся трансфузии эритроцитосодержащих компонентов крови.
Пациентка, 60 лет. Диагноз: приобретенный порок митрального и трикуспидального клапанов. Проведены протезирование митрального (МедИнж 29) клапана, аннулопластика трикуспидального клапана по Де Вега.
Через 1 год после оперативного вмешательства у пациентки наблюдалось ухудшение состояния: одышка при минимальной физической нагрузке, отеки на ногах, последние 6 мес. — желтушность склер. В анализах, выполненных по месту жительства, — билирубин до 134 мкмоль/л. По данным чреспищеводной эхокардиографии в проекции митрального клапана — параклапанная фистула 1 степени.
Пациентка была госпитализирована в кардиохирургический стационар для устранения дефекта. При поступлении: билирубин — 110 мкмоль/л, непрямой билирубин — 22,7 мкмоль/л, свободный гемоглобин — 0,3 г/л. Наблюдалась гипохромная анемия: эритроциты — 4,6×1012/л; гемоглобин — 100 г/л; гематокрит — 36%; средний объем эритроцитов — 73,9 фл; среднее содержание гемоглобина в эритроците — 21,7 пг; средняя концентрация гемоглобина в эритроците — 291 г/л; ширина распределения эритроцитов по объему — 24,4%, шистоциты — 1,3%. Пациентке было проведено эндоваскулярное закрытие параклапанной фистулы окклюдером с положительной динамикой, с постепенным снижением уровня общего и непрямого билирубина, повышением уровня гемоглобина. При выписке гемоглобин — 128 г/л.
Таким образом, при подозрении на гемолиз у больных с ИКС всегда необходимо исключать механическую причину повреждения эритроцитов. Степень анемии в зависимости от степени и выраженности гемолиза может быть различной. Чаще всего анемия нормохромная, но при длительно протекающем гемолизе может носить гипохромный характер, с изменением морфологии красных клеток крови и присутствием шистоцитов либо только с присутствием шистоцитов как изолированным проявлением пойкилоцитоза. Рабочая группа Международного совета стандартизации в гематологии (МССГ (ICSH)) подготовила рекомендации для стандартизации, идентификации, подсчета и описания шистоцитов. Рекомендации определяют морфологическое описание шистоцитов, основанное на соответствующих критериях (в виде шлема; маленькие, неправильной треугольной формы, с наличием 2–3 углов; в форме полумесяца, с заостренными выступами, а также с отсутствием просветления в центре) [9–11]. В качестве полезного дополнения к микроскопу рекомендуется автоматизированный подсчет FRC. К сожалению, не все современные гематологические анализаторы демонстрируют сигналы тревоги («флаги»), сигнализирующие о наличии шистоцитов, а тем более проводят их подсчет. Да и специфичность автоматического метода очень низка (около 20%), требуется микроскопическое исследование для их подтверждения [9]. Поэтому общий анализ крови у пациентов с ИКС при подозрении на гемолиз необходимо дополнять микроскопией окрашенного мазка крови с описанием морфологии эритроцитов.
Выявленный шистоцитоз требует от врача-клинициста безотлагательных действий по установлению диагноза. При наличии клинической картины, лабораторных признаков гемолиза, нарастании в динамике процентного содержания шистоцитов диагноз механического разрушения эритроцитов становится очевидным. При подтверждении механической гемолитической анемии оправданным методом лечения является своевременное репротезирование клапанов сердца.
Литература
1. Таричко Ю.В., Веретник Г.И., Файбушевич А.Г. Острый внутрисосудистый гемолиз после протезирования аортального клапана протезом Карбоникс // Хирургия. 2004. № 1. 2004. С. 52–53 [Tarichko Yu.B., Veretnik G.I., Faibushevich A.G. Ostrij vnutrisosudistij gemolis posle protesirovaniya aortalnogo klapana protesom Karboniks // Xirurgija. 2004. № 1. S. 52–53 (in Russian)].
2. Филатов Л.Б., Томилов А.Ф., Алексеева Т.А. Гемолитическая анемия, вызванная фрагментацией эритроцитов // Клиническая онкогематология. 2011. № 4. С. 346–355 [Filatov L.B., Tomilov A.F., Alekseeva T.A. Gemoliticheskaja anemija, visvannaja fragmentaciei eritrocitov // Klinicheskaja onkogematologija. 2011. № 4. S. 346–355 (in Russian)].
3. Фридман М.Л. Гемолитическая анемия. Болезни крови у пожилых / пер. с англ. / под ред. М.Д. Дэнхема, И. Чанарина. М.: Медицина, 1989. 352 с. [Fridman M.L. Gemoliticheskaja anemija. Bolesni krovi u posilix. Per. s angl. Pod red. M.D. Denxema, I. Chanarina. M.: Medicina, 1989. 352 s. (in Russian)].
4. Baker K.R., Moake J. Hemolytic anemia resulting from physical injuri to red cells // Ch. 49. In: Williams Hematology, 2007. Р. 1856.
5. Лапицкая О.И., Моргунова В.В. и др. Состояние периферического звена эритрона и метаболический статус эритроцитов (по данным цитохимии) у больных с пороками сердца и после замены митрального и аортального клапанов дисковыми протезами // Актуальные вопросы кардиологии. 1994. № 8. С. 75–76 [Lapickaja O.I., Morgunova V.V. Sostojanie perifericheskogo zvena eritrona i metabolicheskiji status eritrositov( po dannim citoximii) u bolnix s porokami serdsa i posle sameni mitralnogo i aortalnogo klapanov diskovimi protesami // Aktualnie voprosi kardiologii. № 8. 1994. S. 75–76 (in Russian)].
6. Gott V., Alejo D., Cameron D. Mechanical heart valves: 50 years of evolution // Ann.Thorac.Surg. 2003. Vol. 76. P. 52230–52239.
7. Мохаммад А., Кестутис Р., Виргилиус Т., Гинтарас Т. Преимущества и недостатки искусственных клапанов сердца // Наука, техника, образование. 2015. № 7(13). С. 93–100 [Moxammad A., Kestutis P., Virgilius T., Gintaras T. Preimushestva i nedostatki iskusstvennix klapanov serdsa // Nauka, technika, obrasovanie. 2015. № 7 (13). S. 93–100 (in Russian)].
8. Орловский П.И. Искусственные клапаны сердца. СПб.: ОЛМА Медиа Групп, 2007. 448 с. [Orlovskiji P.I. Iskusstvennie klapani serdsa. SPb.: OLMA Media Grupp, 2007. 448 s. (in Russian)].
9. Zini G., D’Onofrio G., Briggs C. et al. ICSH Recommendations for identification, diagnostic value and quantitation of schistocytes // Int. J. Lab. Hematol. 2012. Vol. 34(2). P. 107–116.
10. Palmer L., Briggs C., Mcfadden S. et al. ICSH Recommendations for the stardardization of nomenclature and grading of peripherial blood cell morphological features // Int. J. Lab. Hematol. 2015. Vol. 37. P. 287–303.
11. Schapkaitz E., Mezgebe M.H. The Clinicsl Significance of schistocyte: A prospective evalution of the International council for standardization in hematology schistocyte guidelines // Turk. J Hematol. 2017. Vol. 34. P. 59–63.
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
Информация с rmj.ru






