Содержание статьи
Введение
Во всем мире отмечается тенденция к старению населения. В середине XX в. лиц пожилого возраста насчитывалось около 600 млн человек. В соответствии с динамикой старения населения в середине XXI в. число лиц старше 60 лет достигнет 2 млрд. Это ставит новые задачи перед обществом, наукой и медициной — в частности, задачу разработки мер, направленных на лечение и профилактику инвалидизации и ранней смертности среди пожилых пациентов [1]. Известно, что с возрастом увеличивается риск развития некоторых заболеваний, что кардинально меняет стратегические и тактические задачи лечения, контроля и реабилитации пожилых пациентов.
Проблема полиморбидности с медицинской точки зрения включает в себя три основных направления деятельности: создание стройной системы борьбы с основными факторами риска, формирование окружающей среды для пациента с максимальными приоритетами психического и физического благополучия, определение наиболее эффективного и безопасного медицинского сопровождения [2–4]. Еще 30 лет назад в реальной клинической практике мы выделяли основное заболевание и старались максимально изменить его течение в целях улучшения прогноза. Сегодня изменилось само понятие эффективности лечения, так как у полиморбидного пациента более сложные медицинские потребности, которые включают в себя лечение множественных заболеваний и сложные схемы лечения [4].
Врач старается в целях сохранения безопасности лечения назначить лекарственные средства в минимальных дозах без активной титрации, что в последующем становится огромной проблемой в плане достижения целевых показателей терапии любого состояния. Основными причинами становятся боязнь побочных эффектов при увеличении доз препаратов, непонимание возможностей препарата в плане действия на различные органы-мишени и отсутствие глубоких знаний по вопросу лекарственного взаимодействия используемого препарата.
Применению лекарственных средств фармакологической группы ингибиторов ангиотензинпревращающего фермента (ИАПФ), которая наиболее часто назначается пациентам с сердечно-сосудистыми заболеваниями (ССЗ), посвящается данная статья.
У амбулаторного врача на приеме чаще всего встречаются полиморбидные пациенты. Наличие 3 и более заболеваний диагностируется у 13–95% пациентов, выраженность полиморбидности зависит от возраста и наличия первого основного заболевания, которое запускает сердечно-сосудистый континуум [5, 6]. Наиболее часто в российской популяции встречается сочетание артериальной гипертонии (АГ), сахарного диабета (СД), фибрилляции предсердий (ФП), ишемической болезни сердца (ИБС). К указанным заболеваниям могут присоединиться хроническая болезнь почек (ХБП), патология легких или желудочно-кишечного тракта, а в возрасте старше 60–65 лет у пациентов резко увеличивается риск формирования хронической сердечной недостаточности (ХСН). Последние 10 лет в структуре полиморбидности все чаще встречаются онкологические заболевания
[12, 13]. С 2020 г. у полиморбидных пациентов выявляются осложнения после перенесенной коронавирусной инфекции [7–11]. Таким образом, чаще всего в реальной клинической практике встречается полиморбидный пациент с высоким риском обострения любого заболевания, увеличения выраженности побочных явлений при повышении дозы препарата и наличия лекарственных взаимодействий.
Применение ИАПФ у пациентов с ССЗ и ХБП
Исследования ПИФАГОР IV [14] и ЭПОХА-АГ [15] установили, что в России для лечения основных ССЗ в качестве препаратов первой линии выбора используются ИАПФ, на долю которых приходится 25–35% фармацевтического рынка всех сердечно-сосудистых лекарственных средств. У больных АГ частота назначения ИАПФ достигает 65%. Какой же ИАПФ является наиболее безопасным и изученным на российской популяции?
Основной вопрос для практикующего врача: насколько препарат и его метаболиты опасны при высоких концентрациях для организма и его органов-мишеней на этапе выведения? Ответ напрашивается сам собой: когда у препарата несколько путей выведения, он является максимально безопасным. Наиболее изученный препарат среди всех ИАПФ, который имеет двойной путь выведения (50% — с желчью через печень, 50% — через почки), независимо от возраста, пола, — это фозиноприл и его метаболит фозиноприлат. Сравнительные исследования [16–19] среди больных молодого возраста и пожилых пациентов показали наличие одинаковой скорости выведения метаболитов в обеих группах. Период его полувыведения составляет около 11,5 ч, а среди полиморбидных пациентов данный показатель достигает 14 ч [16]. При этом снижение выведения при наличии поражения одной из систем увеличивает активность элиминации через вторую систему [19].
Исследование [17] у наиболее тяжелых полиморбидных пациентов, имеющих ХСН II–IV функционального класса (ФК) и ХБП с клиренсом креатинина (CrCl) <30 мл/мин, показало, что увеличение дозы фозиноприла оказалось более безопасным по показателям площади под кривой (AUC) и индексу кумуляции по сравнению с таковым на фоне приема эналаприлата и лизиноприла. Большее накопление эналаприлата и лизиноприла у пациентов с ХСН и ХБП, ассоциированное с более высокими значениями индекса кумуляции, может свидетельствовать о необходимости коррекции дозы у полиморбидных пациентов, имеющих один превалирующий путь выведения. Двойная элиминация фозиноприлата, о чем свидетельствуют низкие значения индекса накопления препарата, позволяет избежать необходимости коррекции дозы даже у наиболее тяжелых пациентов. Данная тактика титрации ИАПФ нашла отображение в рекомендациях 2019 г. по ведению пациентов в амбулаторной практике [18] (табл. 1): только один ИАПФ — фозиноприл не требовал снижения терапевтической дозы даже при V стадии ХБП.
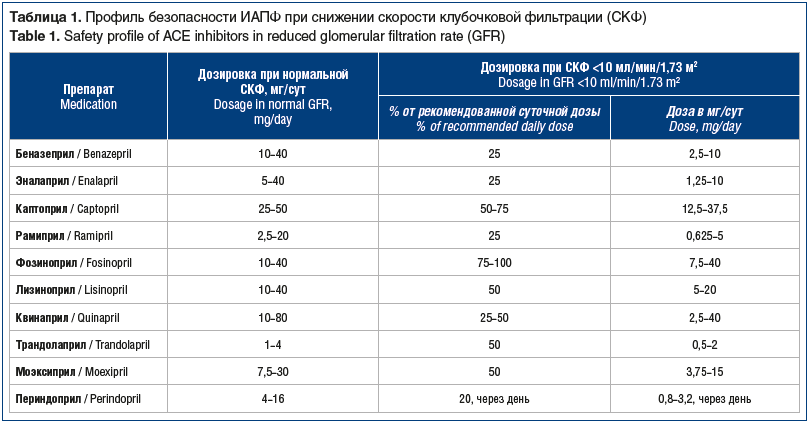
В 2021 г. вышли новые рекомендации KDIGO [20] по лечению АГ при ХБП II–IV стадий, наличии протеинурии А2–3-й степени, которые предусматривают для данной категории пациентов снижение артериального давления (АД) ниже 120/80 мм рт. ст. В целях уменьшения полипрагмазии предлагается увеличение дозы препаратов до максимально переносимой в соответствии с уровнем безопасности (табл. 2). В рекомендациях KDIGO 2021 г. доза фозиноприла увеличена до 80 мг/сут (в инструкцию препарата измененные данные о максимально допустимой суточной дозе еще не внесены) без корректировки дозы при любом уровне снижения CrCl. После принятия текста рекомендаций нефрологическими обществами США и стран Европы рекомендованную дозу будут назначать пациентам с ХБП V стадии. В РФ на сегодня инструкция препарата фозиноприл не изменена, поэтому возможно назначение только дозы 40 мг/сут в качестве максимальной. Практикующий врач должен понимать, что безопасность препарата настолько высока, что доза 40 мг может быть назначена при ХБП IV–V стадий.
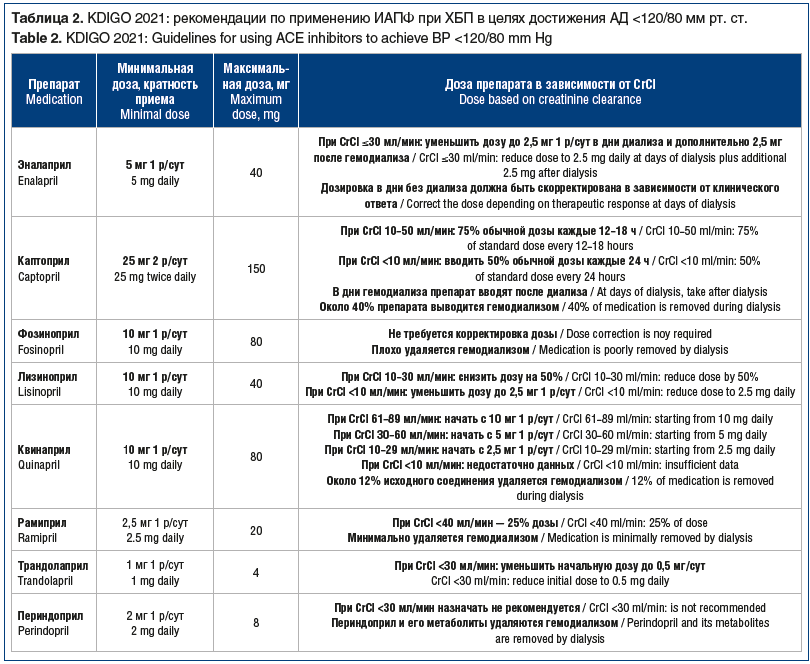
Таким образом, эксперты пришли к выводу, что наиболее безопасным среди лекарственных средств группы ИАПФ является фозиноприл, который может применяться у полиморбидных пациентов со снижением СКФ любой степени.
Показания и безопасность применения фозиноприла
Современные антигипертензивные средства должны подтвердить свою эффективность снижения АД, органопротекцию и профилактику сердечно-сосудистых осложнений.
Основными показаниями к применению фозиноприла являются АГ и ХСН. Международные исследования по безопасности препарата были проведены среди пациентов с АГ (FLIGHT) [21], включая пожилых (FOPS) [22], или с наличием микро- и макропротеинурии (PREVENT-IT) [23]; больных СД (FASET) [24] или с поражением почек (ESPIRAL) [25]. Также препарат изучался в комбинации со статинами в профилактике атеросклероза (PHYLLIS) [26], при остром инфаркте миокарда (FAMIS) [27] и ХСН (FHF study) [28] и (FEST) [29]. Полученные результаты показали высокую безопасность применения препарата, особенно среди пожилых пациентов, при очень низкой частоте клинических и лабораторных нежелательных явлений [30–32]. Важным преимуществом фозиноприла оказался факт более редкой частоты кашля по сравнению с таковой на фоне приема других препаратов группы ИАПФ. При смене ранее принимаемого ИАПФ на фозиноприл частота кашля оказалась значимо ниже [33, 34].
Многочисленные исследования [23–25, 35–38] подтвердили органопротекцию фозиноприла у пациентов с АГ, СД и протеинурией. Применение данного ИАПФ позволило замедлить прогрессирование заболевания у пациентов с III–IV стадией ХБП. При формирующейся микроальбуминурии (МАУ) у пациентов трудоспособного возраста с высоким нормальным АД и минимальным риском сердечно-сосудистых осложнений или СД (не более 3,0%) в исследовании PREVENT-IT [23] была подтверждена гипотеза о нефропротекции фозиноприла. У пациентов с выраженной МАУ >50 мг/сут длительная терапия (не менее 3 мес.) фозиноприлом приводила к снижению риска развития сердечно-сосудистых осложнений на 45% (р=0,04), а также к значимой профилактике прогрессирования протеинурии в течение всего периода наблюдения [37, 38]. Следует отметить, что у пациентов с МАУ <50 мг/сут значимой органопротекции не было обнаружено ни через 4 года, ни через 10 лет наблюдения [38].
В исследовании ESPIRAL [25] была продемонстрирована органопротекция на фоне терапии фозиноприлом у наиболее тяжелых пациентов с почечной патологией (первичный гломерулонефрит, нефросклероз и поликистоз почек) без СД. В еще одном исследовании [39] назначение фозиноприла привело к значимому снижению 2-кратного повышения уровня креатинина в сыворотке крови и потребности в диализе на 21% (р=0,01), что было ассоциировано со снижением протеинурии на 53% (р=0,002).
В исследовании [40], посвященном безопасности применения ИАПФ при гемодиализе, сравнивались 2 группы ИАПФ в зависимости от диализируемости: 1-я группа — препараты с низкой диализируемостью (фозиноприл и рамиприл), 2-я группа — с высокой диализируемостью (эналаприл, лизиноприл и периндоприл). Фозиноприл оказался сравнимым по уровню смертности от всех причин и сердечно-сосудистых осложнений в течение 1 года гемодиализа с ИАПФ высокой диализируемости (p=0,6), также не был обнаружен эффект накопления препарата в крови в течение периода наблюдения.
Экспериментальные исследования [41, 42] на животных с СД, вызванным стрептозотоцином, показали, что использование фозиноприла снижало концентрации креатинина в крови, азота мочевины, белка в суточной моче, хемерина и белка фактора роста эпителия сосудов (ФРЭС). Исследователи [41] продемонстрировали, что фозиноприл может защищать почечную ткань при СД, подавляя экспрессию хемерина и белка ФРЭС. Также было выявлено профилактическое влияние на развитие тактильной аллодинии у крыс с СД, что позволяет предполагать: фозиноприл может снижать риски возникновения диабетической невропатической боли [42].
В исследовании PHYLLIS [26] фозиноприл усиливал эффекты статинов в плане замедления прогрессирования атеросклероза на основании изменения толщины комплекса интима-медиа. Замедление атеросклероза было установлено в группах использования фозиноприла, правастатина и их комбинации. Также была выявлена метаболическая нейтральность фозиноприла при тенденции к снижению уровней общего холестерина и холестерина липопротеинов низкой плотности. При комбинированном применении статина и фозиноприла снижение показателей липидограммы было значимо выраженнее, чем в группе монотерапии статином.
В недавнем исследовании [43] фозиноприл показал более существенное потенцирующее действие в профилактике судорожного синдрома с некоторыми противоэпилептическими препаратами, особенно с карбамазепином, фелбаматом, ламотриджином, топираматом и вальпроатом, по сравнению с эналаприлом, зофеноприлом, лизиноприлом. Эксперты пришли к выводу, что возможно использование ИАПФ, особенно фозиноприла, в целях увеличения терапевтической эффективности комбинированных противоэпилептических средств.
Применение фозиноприла при ХСН
Наибольшее число исследований [27–29, 44–50] по изучению эффективности фозиноприла было проведено среди пациентов с ХСН. Положительное гемодинамическое действие препарата было выявлено в исследовании FAMIS [27] при острой сердечной недостаточности на фоне острого инфаркта миокарда (ОИМ). Пациенты включались в исследование через 9 ч от начала ОИМ независимо от уровня системного АД. Титрация дозы фозиноприла начиналась с 2,5 мг 2 р/сут в случае диагностированной гипотонии, в последующем стабилизация основного патологического процесса дала возможность увеличить дозу фозиноприла до 40 мг/сут. Данная тактика приводила к улучшению гемодинамических показателей, повышению физической активности и увеличению реабилитационного потенциала в течение 2 лет. Применение высоких доз фозиноприла после ОИМ привело к снижению риска развития ХСН III–IV ФК в течение 2 лет на 34,1% (р=0,05) и комбинированной точки (смертность или любая ХСН) на 29,1% (р=0,04). Установлено сохранение конфигурации и объемов полостей миокарда на фоне терапии, что ассоциировано с улучшением прогноза [45].
Согласно рекомендациям специалистов по сердечной недостаточности [46, 47] у стабильных пациентов с ХСН и нормальным или высоким уровнем АД начальная доза фозиноприла составляет 10 мг/сут. При одновременном приеме диуретиков начальная доза не должна быть выше 5 мг/сут. Также специалисты рекомендуют осуществлять контроль за показателями гемодинамики в течение 2–6 ч после первого приема препарата. При отсутствии интенсивного снижения АД следует начать титрацию дозы фозиноприла, если отмечается гипотония — сохранить первоначальную дозу до стабилизации АД. Следующий шаг — снижение дозы диуретика в целях минимизации рисков гипотонии.
У пациентов с ХСН с низкой фракцией выброса (ФВ) (25±7%) прием фозиноприла позволял значимо уменьшить клинические симптомы, увеличить ФВ и толерантность к физическим нагрузкам [48, 49]. Рандомизированное исследование FEST [29] включало стабильных пациентов с ХСН и низкой ФВ (26,5±6,9%), которым в течение 12 нед. проводились велотренировки. Критерий исключения — способность выполнения тренировки на велотренажере более 10 мин. На фоне терапии фозиноприлом через 12 нед. время тренировки на велотренажере значимо увеличилось — более чем на 38 с (р=0,01). Клиническая симптоматика (одышка, утомляемость, слабость) значимо уменьшилась, а риски прогрессирования ХСН и потребность в увеличении дозы диуретиков значимо снизились по сравнению с плацебо (р=0,001). Была выявлена прямая корреляционная связь между снижением риска прогрессирования ХСН и увеличением дозы фозиноприла до 40 мг/сут. Аналогичная закономерность была выявлена среди пациентов с ХСН и низкой ФВ, не принимающих дигиталис [48].
Фозиноприл также исследовался у пациентов после трансплантации сердца. Полученные результаты показали безопасность комбинации фозиноприла с иммуносупрессивными препаратами, хорошую гипотензивную эффективность с суточным контролем АД и усиление действия статинов в плане достижения целевого уровня общего холестерина и холестерина ЛПНП. В послеоперационном периоде применение фозиноприла достоверно быстрее приводило к стабилизации почечной функции по сравнению с плацебо [50].
Доказательная база эффективности фозиноприла на российской популяции
В России фозиноприл был изучен в программе ТРИ-Ф [51]: у больных с неосложненной АГ (ФЛАГ [52]), с осложненной АГ (ФАГОТ [53]) и с ХСН (ФАСОН [54, 55]). Если в исследование ФЛАГ [52] были включены пациенты с различной степенью повышения АД и не анализировалась полиморбидность, то в исследование ФАГОТ [53] включались пациенты с АГ и с СД, ХСН, МАУ, ХБП, хронической обструктивной болезнью легких. Исследования [52, 53] были многоцентровыми и проводились в 20 различных регионах страны. Общее количество пациентов составило 4334. Интенсивность снижения АД зависела от дозы фозиноприла, степени АГ, наличия факторов риска и сопутствующих заболеваний. Целевое АД было достигнуто у 62,1% пациентов на фоне низкодозовой терапии фозиноприлом (10 мг/сут). В группе пациентов, которые принимали фозиноприл в дозе 20–30 мг/сут, достижение целевого АД составило 86,4%. В среднем уровень снижения САД был равен 28,7 мм рт. ст., ДАД — 16,2 мм рт. ст. Использование фозиноприла в комбинации с тиазидным диуретиком оказалось более экономически выгодным по сравнению с любой другой комбинацией гипотензивных средств.
В исследование ФАСОН [54], которое было посвящено определению эффективности и безопасности титрации фозиноприла до 20 мг/сут, включались пациенты с ХСН и ФВ <40%. Проводилась последующая фармакоэкономическая оценка лечения. Динамика клинической симптоматики, изменения ФВ и класса ХСН были аналогичными данным исследований FEST [29] и FHF study [28]. Суммарные затраты на лечение больных с ХСН снизились на 54% за счет уменьшения числа госпитализаций, вызовов скорой медицинской помощи и числа принимаемых препаратов [55].
Программа ТРИ-Ф [51], включившая в себя 5779 пациентов, ответила на очень важный вопрос: каким пациентам в первую очередь следует назначать фозиноприл? Это пациенты с наличием факторов риска и АГ, что соответствует начальной стадии ССЗ; пациенты с осложненной АГ с перенесенным ОИМ, с СД, ХБП, ХСН; больные с ХСН с различными показателями гемодинамики. Таким образом, исследовались пациенты с ССЗ всех стадий с различными поражениями органов-мишеней. Полученные результаты подтвердили высокую степень органопротекции фозиноприла, предсказуемую динамику снижения АД, улучшения качества жизни и низкую частоту побочных явлений (кашель на фоне приема ИАПФ, гипотония при быстрой титрации дозы).
Заключение
Современные рекомендации [56, 57] предусматривают применение препаратов с разнонаправленностью фармакологического действия. Борьба с полипрагмазией становится приоритетом современной стратегии лечения пациентов пожилого возраста, имеющих комбинацию различных заболеваний. Предпочтение отдают лекарственным средствам с хорошей доказательной базой у различных категорий пациентов, имеющим минимальные побочные эффекты и высокий уровень безопасности при одновременном применении в различных комбинациях.
Многочисленные отечественные и зарубежные исследования доказали, что фозиноприл проявляет органопротекцию независимо от уровня снижения АД у коморбидных пациентов с СД, ХБП, асимптомным атеросклерозом, ХСН и после перенесенного ОИМ, что ассоциировалось со снижением риска развития инсульта и сердечно-сосудистых осложнений.
Сведения об авторе:
Фомин Игорь Владимирович — д.м.н., доцент, заведующий кафедрой госпитальной терапии и общей врачебной практики им. В.Г. Вогралика ФГБОУ ВО «ПИМУ» Минздрава России; 603005, Россия, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1; ORCID iD 0000-0003-0258-5279.
Контактная информация: Фомин Игорь Владимирович, e-mail: fomin-i@yandex.ru.
Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 11.01.2022.
Поступила после рецензирования 03.02.2022.
Принята в печать 01.03.2022.
About the author:
Igor V. Fomin — Dr. Sc. (Med.), Head of V.G. Vogralik Department of Hospital Therapy & General Medical Care, Privolzhsky Research Medical University; 10/1, Minin and Pozharsky sq., Nizhny Novgorod, 603950, Russian Federation; ORCID iD 0000-0003-0258-5279.
Contact information: Igor V. Fomin, e-mail: fomin-i@yandex.ru.
Financial Disclosure: the author has no a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 11.01.2022.
Revised 03.02.2022.
Accepted 01.03.2022.
.
Информация с rmj.ru






