Введение
Вакцинопрофилактика инфекционных заболеваний — приоритетная задача современного здравоохранения. Активная специфическая иммунопрофилактика является одним из ключевых методов эффективного предупреждения инфекционных заболеваний. По данным Всемирной организации здравоохранения (ВОЗ), в настоящее время ежегодно в мире предотвращается 3,5–5,0 млн случаев смерти благодаря прививкам против дифтерии, столбняка, коклюша, гриппа и кори. При этом эксперты ВОЗ особо подчеркивают, что с точки зрения затрат иммунизация относится к самым эффективным профилактическим мероприятиям в области общественного здравоохранения и одним из наиболее продуктивных видов инвестирования в охрану здоровья людей. Кроме этого, прививки лежат в основе глобальной безопасности в области здравоохранения и будут оставаться жизненно важным инструментом в борьбе с устойчивостью патогенных микроорганизмов к противомикробным препаратам. Учитывая чрезвычайную важность вакцинации, ВОЗ призывает признать иммунизацию одним из основных компонентов права человека на здоровье1,2.
Особо следует отметить, что в Российской Федерации, где проводится планомерная и последовательная работа по вакцинопрофилактике инфекционных заболеваний, достигнуты колоссальные успехи3,4,5. Так, в 2002 г. Российской Федерации был выдан сертификат ВОЗ о ликвидации полиомиелита, и благодаря системно проводимым мероприятиям, в том числе по иммунизации детей, до настоящего времени поддерживается статус страны, свободной от полиомиелита. С 2017 г. Российская Федерация признана Европейским региональным бюро ВОЗ территорией, свободной от эндемичной краснухи4. Особо следует подчеркнуть, что в целом благодаря иммунизации в Российской Федерации значительно снижена не только заболеваемость всеми вакциноуправляемыми инфекциями, но и количество смертельных случаев5.
Однако успехи вакцинопрофилактики могут быть нивелированы широко распространенным в Российской Федерации в настоящее время прививочным нигилизмом [1–5]. При этом одними из факторов, способствующих отказу населения от иммунизации, являются ложные представления о высокой частоте вакцинальных осложнений и значительная переоценка роли прививочных реакций в развитии различных патологических состояний [5, 6]. Особую тревогу у родителей при этом вызывает возможное повышение температуры тела у ребенка в ответ на вакцинацию [6, 7]. Несмотря на то, что современные вакцинные препараты имеют значительно меньшую реактогенность по сравнению с используемыми ранее вакцинами, в ряде случаев при иммунизации действительно возможно повышение температуры тела в ответ на прививку [6–9]. Принимая во внимание обеспокоенность этим фактом родителей, а также учитывая, что гипертермия при вакцинации может стать триггером фебрильных судорог, был проведен целый ряд клинических исследований, направленных на изучение эффективности и безопасности профилактического применения анальгетиков-антипиретиков для снижения риска развития лихорадки при иммунизации детей. Детальный анализ результатов этих исследований представлен ниже.
Содержание статьи
- 1 Поствакцинальная гипертермия: вопросы и ответы
- 2 Повышение температуры тела в поствакцинальный период: реакция на прививку или проявление интеркуррентного заболевания?
- 3 С чем связано развитие поствакцинальной гипертермии?
- 4 Может ли профилактический прием антипиретиков предупредить поствакцинальную гипертермию и фебрильные судороги без ущерба для формирования иммунного ответа на прививку?
- 5 Заключение
Поствакцинальная гипертермия: вопросы и ответы
Повышение температуры тела в поствакцинальный период: реакция на прививку или проявление интеркуррентного заболевания?
Следует помнить, что гипертермия после вакцинации не всегда непосредственно связана с прививкой или является ее следствием, она может быть случайным по времени совпадением с развитием самостоятельного заболевания, чаще всего инфекционной этиологии. Поэтому для уточнения генеза лихорадки, возникшей на фоне прививки, целесообразно рассматривать весь перечень возможных причин: непосредственно иммунизацию, спровоцированное вакцинацией обострение хронических заболеваний, а также интеркуррентные инфекции. Для этого в каждом конкретном случае, когда у ребенка в поствакцинальном периоде имеет место повышение температуры тела, детализируют все клинические особенности, а также уточняют время манифестации гипертермии и ее продолжительность.
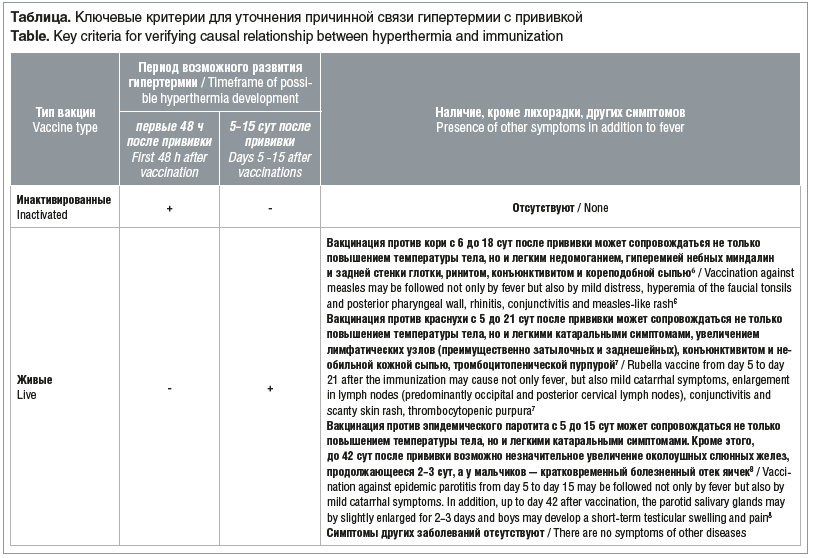
Установлено, что повышение температуры тела, развившееся в результате вакцинации, как правило, кратковременное (не более 48 ч) и не сопровождается другими клиническими проявлениями. Кроме этого, необходимо обратить внимание на хронологическую связь вакцинации и гипертермии. При этом отмечено, что время манифестации гипертермии зависит от типа применяемой вакцины. Так, при использовании инактивированных вакцин повышение температуры тела возможно в первые 48 ч после иммунизации. В тех же случаях, когда после иммунизации инактивированной вакциной гипертермия развивается через 48 ч и более, то вероятность, что прививка является причиной повышения температуры тела, очень низкая. В свою очередь, для живых вакцин возможное развитие лихорадочной реакции характеризуется другими временными интервалами. При использовании живых вакцин гипертермия, обусловленная прививкой, манифестирует в период с 5-го по 15-й день после иммунизации [6]. Следовательно, в тех ситуациях, когда при введении живой вакцины гипертермия развивается в первые 4 дня или после 15 дней с момента прививки, нельзя связывать ее с иммунизацией, необходимо искать другую причину повышения температуры тела. При этом особо следует отметить, что даже в тех случаях, когда лихорадка развивается в регламентируемые сроки поствакцинального периода, но сохраняется более 2–3 сут и при этом имеются патологические проявления, отличительные от ожидаемых побочных явлений (см. таблицу), причинная связь гипертермии с прививкой также маловероятна. В этих случаях, как правило, повышение температуры тела у ребенка обусловлено переносимым интеркуррентным заболеванием, чаще всего инфекционного генеза [6].
С чем связано развитие поствакцинальной гипертермии?
Анализ результатов исследований, направленных на поиск причин повышения температуры тела после проведенной иммунизации, позволил сделать вывод о том, что в основе развития прививочной лихорадки могут лежать как особенности самой вакцины, так и особенности реактивности организма вакцинируемого ребенка [6, 8, 9]. Так, установлено, что наибольшей реактогенностью обладают инактивированные корпускулярные вакцины. Кроме того, отмечено, что риск поствакцинальной гипертермии и развития на этом фоне фебрильных судорог повышается при использовании некоторых комбинированных вакцин, по сравнению с применением отдельных их компонентов. Установлено, что введение вакцины против кори, краснухи и эпидемического паротита одновременно с вакциной против ветряной оспы, а также применение четырехкомпонентной комбинированной вакцины (корь, краснуха, эпидемический паротит, ветряная оспа) характеризуются большей частотой фебрильных судорог, чем их раздельное использование [10].
Особо следует отметить, что развитие гипертермии после прививки и степень ее выраженности зависят не только от типа вакцинных препаратов и их состава, но также и от индивидуальных особенностей ребенка. Последнее находит все больше доказательств при верификации генеза фебрильных судорог, которые развились на фоне поствакцинальной лихорадки [11–13]. Так, при проведении полногеномного секвенирования, проведенного у 929 детей с фебрильными судорогами, развившимися в результате вакцинации против кори, краснухи и эпидемического паротита, была установлена связь изучаемого явления с локусами, содержащими интерферон-стимулируемый ген IFI44L [11]. В то же время указанные генетические особенности отсутствовали в группах сравнения (1070 детей с фебрильными судорогами, не связанными с прививкой) и контроля (4118 детей без фебрильных судорог). Следует особо отметить, что у детей с вакцино-ассоциированными фебрильными судорогами, по сравнению с контрольной группой, была также выявлена связь фебрильных пароксизмов с локусом, содержащим ген рецептора CD46. Кроме этого, у всех детей с фебрильными судорогами, независимо от этиологии пароксизмов, были выявлены особенности генов SCN1A, SCN2A и ANO3, регулирующих работу различных ионных каналов [11]. В свою очередь, у детей с синдромом Драве (рефрактерный эпилептический синдром, первым триггером которого в 50% случаев является поствакцинальное повышение температуры тела, а в дальнейшем — гипертермия независимо от ее этиологии), по сравнению с контрольной группой, были установлены особенности цитокинового профиля в ответ на прививку [12]. Отмечено, что вектор продукции цитокинов мононуклеарами периферической крови у детей с синдромом Драве после вакцинации существенно смещается в провоспалительном направлении, в отличие от контроля, и характеризуется повышением продукции интерлейкина (ИЛ) 1β, ИЛ-6 и фактора некроза опухоли α при одновременном снижении продукции противовоспалительного цитокина ИЛ-10 [12]. Выявленные у детей с фебрильными судорогами генетические, а также иммунологические особенности позволяют объяснить тот факт, что в их семейном анамнезе припадки на фоне гипертермии наблюдаются в 5,2 раза чаще, чем у лиц с неотягощенной наследственностью [6]. Таким образом, гипертермия после прививки и развитие на этом фоне фебрильных судорог определяются не только характеристиками вакцинного препарата (реактогенность, состав и др.), но и индивидуальными особенностями самого ребенка [6, 8–10, 11–13].
Может ли профилактический прием антипиретиков предупредить поствакцинальную гипертермию и фебрильные судороги без ущерба для формирования иммунного ответа на прививку?
Высокая частота поствакцинальной лихорадки, имевшая место в предшествующие десятилетия, когда использовались более реактогенные вакцины (наиболее наглядный пример — комбинированная вакцина против коклюша, столбняка и дифтерии, в составе которой присутствовал цельноклеточный коклюшный компонент), явилась причиной профилактического назначения антипиретиков. При этом жаропонижающие при вакцинации назначались не только для уменьшения частоты и выраженности гипертермии, но и для снижения риска фебрильных судорог [14–16]. Антипиретик при этом назначали в момент иммунизации и продолжали прием с интервалом в 6–8 ч на протяжении последующих 48–72 ч. При этом в качестве антипиретика было рекомендовано использовать ацетаминофен (парацетамол). Внедрение превентивного применения ацетаминофена при вакцинации в повседневную практику действительно сопровождалось уменьшением частоты развития выраженной гипертермии. В то же время некоторые исследователи при этом высказывали мнение, что рутинное использование антипиретиков у детей во время вакцинации может оказать негативное влияние на иммунный ответ [15]. Действительно, клинические исследования, проведенные в последующие годы, подтвердили высказанные ранее опасения — оказалось, что напряженность поствакцинального иммунитета у детей, профилактически принимавших парацетамол при иммунизации, была ниже, чем у детей, не использовавших при этом антипиретики [17–21].
Следует особо отметить работу R. Prymula et al. [17], в которой представлены наиболее показательные результаты, свидетельствующие о том, что профилактическое использование ацетаминофена во время иммунизации неблагоприятно влияет на формирование вакцинального иммунитета. Так, были проведены два последовательных (первичных и бустерных) рандомизированных контролируемых открытых исследования по изучению влияния профилактического применения парацетамола при вакцинации против дифтерии, столбняка, коклюша, гепатита B, полиомиелита, гриппа, пневмококковой, гемофильной инфекции и ротавирусной инфекции на частоту и выраженность лихорадки, а также на формирование иммунитета к вакцинным антигенам у 459 здоровых детей первого года жизни [17]. При этом дети основной группы (n=226) профилактически принимали парацетамол каждые 6–8 ч в течение первых 24 ч после прививки. Группу контроля составили 233 здоровых ребенка аналогичного возраста, которым парацетамол при вакцинации не назначался. Анализ результатов проведенных исследований показал, что процент детей с повышением температуры тела более 38 °С был существенно ниже в основной группе. В то же время именно у детей, которым профилактически во время иммунизации назначали парацетамол, среднегеометрический титр антител к большинству вакцинных антигенов был значительно ниже по сравнению с группой контроля (как при первичной, так и при бустерной иммунизации). При обсуждении результатов исследования высказываются следующие ключевые положения: несмотря на то, что частота выраженных лихорадочных реакций при использовании парацетамола значительно уменьшилась, профилактическое его введение во время вакцинации не следует рутинно рекомендовать, так как гуморальные иммунные реакции на некоторые вакцинные антигены были снижены. На основании полученных данных авторы делают вывод о том, что исследования, направленные на поиск оптимальной тактики по предупреждению значимой гипертермии при иммунизации, но сохранении при этом адекватного иммунного ответа на прививку, должны быть продолжены [17].
Учитывая сохраняющуюся актуальность рассматриваемой проблемы, в последующие годы клинические исследования по изучению эффективности антипиретиков и оценке их влияния на формирование иммунного ответа были продолжены [22–24]. При этом в настоящее время имеются результаты законченных клинических исследований, в которых в качестве антипиретика при вакцинации использовали ибупрофен, разрешенный для применения у детей, начиная с трехмесячного возраста. Ибупрофен относится к нестероидным противовоспалительным препаратам, в основе механизма действия которых лежит ингибирование циклооксигеназы, благодаря чему угнетается синтез простагландинов и достигается противовоспалительный эффект. Кроме этого, ибупрофен обратимо ингибирует агрегацию тромбоцитов и обладает обезболивающим эффектом. При этом анальгезирующее действие ибупрофена максимально проявляется в тех случаях, когда в основе болевого синдрома лежит воспаление [25, 26]. Результаты систематического обзора и метаанализа, проведенного M. Tan et al. [26] на основании изучения 19 клинических исследований (из них 11 рандомизированных), посвященных безопасности и эффективности ацетаминофена и ибупрофена при лихорадке и/или боли у детей в возрасте до 2 лет (n=241 138), показали, что ибупрофен характеризуется более быстрым антипиретическим действием при одинаковом с ацетаминофеном профиле безопасности.
Одним из наиболее хорошо зарекомендовавших себя препаратов ибупрофена по эффективности и безопасности в педиатрической практике является Нурофен® для детей. Препарат с успехом используется для купирования гипертермии и болевого синдрома при различных инфекционно-воспалительных заболеваниях. В отечественной педиатрической практике, как и во всем мире, Нурофен® для детей применяют в качестве одного из препаратов выбора при лихорадке различной этиологии, в том числе и при вакцино-ассоциированном повышении температуры тела. Так, анализ результатов исследования О.В. Шамшевой и соавт. [27] свидетельствует о том, что применение препарата Нурофен® для детей почти в 2 раза снижает риск развития вакцинальных осложнений. При этом все исследователи отмечают хорошую переносимость и высокую клиническую эффективность препарата.
Отдельно необходимо обсудить вопросы, связанные с возможным применением ибупрофена для предупреждения и лечения поствакцинальной гипертермии. Результаты рандомизированного контролируемого исследования по изучению влияния профилактического назначения ибупрофена и парацетамола на формирование прививочного иммунитета к пневмококку, дифтерии, столбняку, коклюшу, полиомиелиту, папилломавирусной и гемофильной (тип В) инфекции изучали у 895 детей первого года жизни [23]. На основании полученных в данном исследовании результатов авторы делают вывод о том, что профилактическое назначение антипиретиков при иммунизации оказывает отрицательное воздействие на иммунный ответ. При этом установлено, что у детей первого года жизни парацетамол оказывает негативное влияние на формирование иммунитета на антигены пневмококка, а ибупрофен может снижать иммунный ответ на антигены коклюша и столбняка. В связи с этим использование жаропонижающих средств для профилактики лихорадки во время вакцинации младенцев требует исключительно индивидуального подхода [23].
Систематический обзор, подготовленный E. Koufoglou et al. [24] на основе изучения пяти рандомизированных контролируемых исследований (2775 детей), посвященных изучению влияния парацетамола и ибупрофена на формирование прививочного иммунитета, также свидетельствует о том, что профилактическое назначение антипиретиков при вакцинации негативно влияет на иммунный ответ. Авторы в связи с этим делают вывод о том, что использование антипиретиков для профилактики вакцинальной гипертермии заслуживает тщательного рассмотрения в каждом конкретном случае и не должно стать рутинной практикой.
Считаем целесообразным подчеркнуть, что в последние годы были внесены также изменения в подходы профилактики фебрильных судорог, связанных с вакцинацией. Если в предшествующие десятилетия существовала установка, что все дети с фебрильными судорогами в анамнезе должны обязательно профилактически принимать антипиретики до и во время иммунизации, то в настоящее время использование жаропонижающих рекомендуется только в тех случаях, когда прививка сопровождается повышением температуры тела. Это связано с тем, что получены убедительные данные о том, что фебрильные судороги, возникающие в результате вакцинации, нельзя предупредить превентивным назначением антипиретиков [28, 29].
Заключение
Таким образом, результаты представленных выше исследований стали основанием для пересмотра тактики применения антипиретиков (парацетамол, ибупрофен) при вакцинации. Учитывая риск неблагоприятного влияния профилактического назначения жаропонижающих на формирование прививочного иммунитета и отсутствие эффекта по предупреждению вакцино-ассоциированных фебрильных судорог, в настоящее время рекомендуется использовать жаропонижающие только в случаях развития гипертермии. При этом препаратами выбора для купирования лихорадки у детей являются ацетаминофен (парацетамол) и ибупрофен.
1WHO. The Sixty-fifth World Health, 26 May 2012. Agenda item 13.12 Assembly Global vaccine action plan.
2WHO. Vaccines and immunization. (Electronic resource.) URL: https://www.who.int/health-topics/vaccines-and-immunization#tab=tab_1 (access date: 02.03.2023).
3Сертификация ликвидации полиомиелита. Пятнадцатое совещание Европейской региональной комиссии по сертификации. Копенгаген, 2002.
4Measles and rubella elimination country profile: Russian Federation. (Electronic resource.) URL: https://apps.who.int/iris/handle/10665/346511 (access date: 02.03.2023).
5Распоряжение Правительства РФ от 18 сентября 2020 г. No 2390-р «Об утверждении Стратегии развития иммунопрофилактики инфекционных болезней на период до 2035 года». (Электронный ресурс.) URL: https://www.garant.ru/products/ipo/prime/doc/74591684/ (дата обращения: 02.03.2023).
Сведения об авторах:
Заплатников Андрей Леонидович — д.м.н., профессор, проректор по учебной работе, заведующий кафедрой неонатологии им. проф. В.В. Гаврюшова, профессор кафедры педиатрии им. акад. Г.Н. Сперанского ФГБОУ ДПО РМАНПО Минздрава России; 123995, Россия, Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0000-0003-1303-8318.
Гирина Асия Ахмедовна — к.м.н., доцент кафедры фармакологии, педиатрии и инфекционных болезней БУ «Ханты-Мансийская государственная медицинская академия»; 628011, Россия, г. Ханты-Мансийск, ул. Мира, д. 40; ORCID iD 0000-0002-5281-1564.
Леписева Инга Владимировна — главный врач ГБУЗ «ДРБ»; 185000, Россия, г. Петрозаводск, ул. Парковая, д. 58; ORCID iD 0000-0001-8989-6103.
Свинцицкая Виктория Иосифовна — к.м.н., доцент кафедры педиатрии им. акад. Г.Н. Сперанского ФГБОУ ДПО РМАНПО Минздрава России; 123995, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0000-0002-9272-2339.
Лешик Мария Владимировна — ассистент кафедры педиатрии им. акад. Г.Н. Сперанского ФГБОУ ДПО РМАНПО Минздрава России; 123995, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0000-0002-9331-1419.
Фурсова Анна Дмитриевна — ординатор кафедры неонатологии имени профессора В.В. Гаврюшова ФГБОУ ДПО РМАНПО Минздрава России; 123995, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1.
Контактная информация: Заплатников Андрей Леонидович, e-mail: zaplatnikov@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 03.03.2023.
Поступила после рецензирования 27.03.2023.
Принята в печать 17.04.2023.
About the authors:
Andrey L. Zaplatnikov — Dr. Sc. (Med.), professor, Vice-Rector for Academic Affairs, Head of the Prof. V.V. Gavryushov Department of Neonatology, Professor of the Acad. G.N. Speransky Department of Pediatrics, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0003-1303-8318.
Asiya A. Girina — C. Sc. (Med.), associate professor of the Department of Pharmacology, Pediatrics and Infectious Diseases, Khanty-Mansiysk State Medical Academy; 40, Mira str., Khanty-Mansiysk, 628011, Russian Federation; ORCID iD 0000-0002-5281-1564.
Inga V. Lepiseva — Chief Physician, Children’s Republican Hospital; 58, Parkovaya str., Petrozavodsk, 185000, Russian Federation; ORCID iD 0000-0001-8989-6103.
Victoria I. Svintsitskaya — C. Sc. (Med.), associate professor of the Acad. G.N. Speransky Department of Pediatrics, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0002-9272-2339.
Maria V. Leshik — assistant of the Acad. G.N. Speransky Department of Pediatrics, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; ORCID iD 0000-0002-9331-1419.
Anna D. Fursova — resident of the Prof. V.V. Gavryushov Department of Neonatology, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation.
Contact information: Andrey L. Zaplatnikov, e-mail: zaplatnikov@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 03.03.2023.
Revised 27.03.2023.
Accepted 17.04.2023.
Информация с rmj.ru


