Введение
Подагра — наиболее распространенное воспалительное заболевание суставов в мире, частота выявления которого продолжает неуклонно расти. Традиционно клиническая картина дебюта подагры ассоциируется с острым моноартикулярным поражением первого плюснефалангового сустава, реже — с вовлечением голеностопного или коленного сустава. Однако за последние полтора десятилетия появляется все больше данных о том, что подагра является системным заболеванием, способным вовлекать в патологический процесс аксиальный скелет, включая поражение позвоночника (чаще поясничный отдел) и крестцово-подвздошных сочленений (КПС) [1–3].
Возрастающий интерес к данному вопросу неслучаен и может быть объяснен некоторыми факторами. Во-первых, недооценкой распространенности — врачи-ревматологи и терапевты редко целенаправленно опрашивают пациентов с подагрой на предмет болей в спине и крестце, в связи с чем истинная распространенность аксиальной подагры, вероятно, значительно выше регистрируемой [4]. Во-вторых, диагностическими затруднениями — симптоматика аксиальной подагры часто имитирует другие заболевания, такие как анкилозирующий спондилит, спондилоартропатии, дегенеративные заболевания позвоночника или инфекции, что, в свою очередь, приводит к длительным диагностическим поискам, неправильному лечению и хронизации боли. В-третьих, «невидимостью» при стандартном обследовании — рентгенография позвоночника и КПС часто малоинформативна на ранних стадиях, а специфические изменения, такие как эрозии и тофусы, могут долго оставаться незамеченными. Более того, артроцентез, выполняемый с целью получения синовиальной жидкости с последующей поляризационной микроскопией, направленной на обнаружение кристаллов моноуратов натрия (МУН), в случае поражения КПС представляется технически сложной задачей [5]. В-четвертых, влиянием на качество жизни — поражение осевого скелета сопровождается хроническим болевым синдромом, скованностью и ограничением подвижности, что существенно снижает качество жизни пациентов и приводит к стойкой утрате трудоспособности.
Данные о распространенности поражения позвоночника и КПС при подагре варьируют. По данным различных исследований, частота сакроилиита при подагре составляет от 13 до 17% [5]. Поражение позвоночника (спондилодисцит, артрит дугоотростчатых суставов, образование тофусов в позвоночном канале) встречается с частотой от 14 до 35% при целенаправленном обследовании с помощью визуализационных методов диагностики [4, 6, 7].
Патогенез аксиальной подагры не отличается от такового при поражении периферических суставов — ключевым звеном является отложение кристаллов МУН в структурах осевого скелета. Этому способствуют особенности кровоснабжения (хрящевая ткань межпозвонковых дисков и суставных поверхностей КПС аваскулярна, что создает условия для персистенции кристаллов), механическая нагрузка на позвоночник и КПС, которая может провоцировать микроповреждения и последующее депонирование кристаллов МУН [8].
Клинические проявления при поражении осевого скелета разнообразны и неспецифичны [2]:
хроническая боль в нижней части спины (пояснично-крестцовой области), ягодицах. Боль может быть одно- или двусторонней, усиливаться в покое и ночью, уменьшаться при движении (что сходно с воспалительной болью при спондилоартритах), усиливаться после физической нагрузки (механический характер). В отличие от классического подагрического артрита с атаками острейшей боли, локальной гиперемией и выраженной припухлостью поражение позвоночника и КПС обычно протекает хронически, с преобладанием деструктивных, а не воспалительных изменений, что затрудняет своевременную диагностику, так как врачи редко связывают хроническую боль в спине с подагрой. По мнению R.M. Konatalapalli et al. [1], сакроилиит при подагре может протекать субклинически, являясь случайной находкой при исследовании;
-
утренняя скованность в позвоночнике;
-
при формировании тофусов в позвоночном канале или компрессии корешков возможно развитие радикулопатий, миелопатии, синдрома конского хвоста. Это является грозным, хотя и редким, осложнением;
-
как правило, аксиальная симптоматика возникает на фоне длительного анамнеза хронической тофусной подагры, высокой гиперурикемии, снижения скорости клубочковой фильтрации (СКФ), при отсутствии адекватной уратснижающей терапии.
В последнее время в литературе все чаще стали встречаться описания поражения позвоночника и КПС вследствие хронической тофусной подагры, нередко протекающие под маской других заболеваний, симулирующие анкилозирующий спондилит [5, 9], псориатический спондилоартрит [10, 11], ревматоидный артрит [12], опухоль грудного отдела позвоночника [13] и др.
Поскольку вовлечение КПС в патологический процесс при подагре встречается относительно редко, в реальной клинической практике могут возникнуть сложности в диагностике подагрического сакроилиита и анкилозирующего спондилита. Подтверждением этого может служить пример из нашей клинической практики.
Содержание статьи
Клиническое наблюдение
Пациент В., 53 года, был направлен на консультацию к врачу-ревматологу нейрохирургом из-за сохраняющихся на протяжении 4 нед. болей механического характера в нижней части спины и впервые выявленного двустороннего сакроилиита по результатам магнитно-резонансной томографии (МРТ).
Из анамнеза заболевания известно, что в возрасте 37 лет было диагностировано морбидное ожирение: при росте 186 см масса тела пациента составила 174 кг (индекс массы тела (ИМТ) 50,3 кг/м2). В том же возрасте впервые развился эпизод острого артрита с локализацией в области первого плюснефалангового сустава правой стопы, который в последующем неоднократно рецидивировал, приступы артрита пациент самостоятельно купировал приемом нестероидных противовоспалительных препаратов (НПВП). В анализах крови обнаруживалась гиперурикемия, которая оставалась без должного внимания. Диагноз подагры был установлен лишь спустя 8 лет от момента первого приступа артрита врачом-эндокринологом, к которому пациент обратился по поводу снижения массы тела. Тогда же впервые был назначен аллопуринол на постоянной основе, однако больной пренебрег врачебными рекомендациями и принимал уратснижающий препарат на протяжении последующих 5 лет нерегулярно. Также был рекомендован прием агониста рецептора глюкагоноподобного пептида-1, что позволило снизить массу тела на 31 кг. Из-за учащения подагрических атак, присоединения артритов в области первого плюснефалангового сустава левой стопы, мелких суставов правой кисти пациент в феврале 2023 г. (в 53 года) был вынужден впервые обратиться к врачу-ревматологу.
На момент осмотра имели место ожирение (масса тела — 138 кг), варикозно расширенные вены нижних конечностей с трофическими расстройствами, припухлость первых плюснефаланговых суставов без явлений локальной гиперемии и гипертермии кожи над пораженными суставами, а также дефигурация в области межфалангового сустава 1 пальца и проксимального межфалангового сустава 5 пальца правой кисти с ограничением объема активных движений в указанных суставах. Также отмечалась болезненность при пальпации в проекции суставной щели обоих коленных суставов с медиальной стороны и их варусная деформация (в исходе посттравматического остеоартрита). Из-за неоднократных спортивных травм пациенту в возрасте 28 лет была выполнена артротомия и резекция внутренних менисков обоих коленных суставов.
В легких выслушивалось везикулярное дыхание, хрипов на момент осмотра не было. Артериальное давление — 130/80 мм рт. ст. (на фоне регулярного приема валсартана и амлодипина). Перкуторно левая граница относительной тупости сердца определялась на 1,0 см кнаружи от срединно-ключичной линии, правая — по правому краю грудины, верхняя — в третьем межреберье. Тоны сердца аритмичные, на верхушке сердца выслушивался систолический шум. Живот увеличен в объеме за счет избыточного развития подкожно-жировой клетчатки, при пальпации — безболезненный, нижний край печени определялся по краю реберной дуги. Стул и диурез — в норме.
Обращал на себя внимание отягощенный анамнез жизни — у пациента ранее были диагностированы комбинированный митральный порок с преобладанием митральной недостаточности 2-й степени (как проявление хронической ревматической болезни сердца), артериальная гипертензия, ишемическая болезнь сердца: стенокардия напряжения (функциональный класс 2), постоянная форма фибрилляции предсердий, язвенная болезнь луковицы двенадцатиперстной кишки.
По данным лабораторных исследований были выявлены: повышение острофазовых белков (скорость оседания эритроцитов (СОЭ) 38 мм/ч, С-реактивный белок (СРБ) 65,4 мг/л), гиперурикемия (мочевая кислота 423 мкмоль/л), гипергликемия (глюкоза натощак 6,1 ммоль/л), увеличение индекса HOMA (Homeostatis Model Assessment) до 6,2 (диагностический критерий инсулинорезистентности — 2,7 и более) и гликозилированного гемоглобина до 6,1% (диагностический критерий сахарного диабета — 6,5% и более). Уровень креатинина составил 60 мкмоль/л, расчетная СКФ по CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) — 109 мл/мин/1,73 м2. Холестерин липопротеинов низкой плотности 1,42 ммоль/л (на фоне приема розувастатина 20 мг/сут). Ревматоидный фактор 2,3 МЕ/мл, антитела к циклическому цитруллинированному пептиду менее 7 Ед/мл (при верхней границе нормы до 17 Ед/мл).
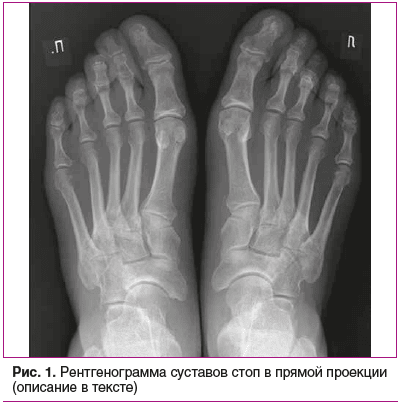
На рентгенограмме суставов стоп определялись невыраженное сужение суставной щели плюснефаланговых суставов первых пальцев, их вальгусная девиация, единичные кистовидные просветления костной ткани, локализованные в головках первых плюсневых костей, небольшое уплотнение мягких тканей в области первых плюснефаланговых суставов (рис. 1). На рентгенограмме суставов кистей в прямой проекции костно-суставной патологии выявлено не было.
При проведении ультразвукового исследования суставов стоп был обнаружен умеренно выраженный аваскулярный синовит первых плюснефаланговых суставов стоп с участками уплотнения синовиальной оболочки и мелкими гиперэхогенными включениями; суставов кистей — признаки умеренного синовита 5 пальца правой кисти без патологической гиперваскуляризации синовия.
При проведении МРТ обеих стоп были выявлены дегенеративно-дистрофические изменения предплюсне-плюсневых (на уровне III-IV-V) и межпредплюсневых сочленений с наличием мелких краевых разрастаний, мелких субхондральных узур и кист с признаками перифокального асептического отека костного мозга дегенеративного характера, невыраженный отек прилежащих мягких тканей.
По результатам МРТ суставов правой кисти определялись минимальный синовит луче-ладьевидного, ладьевидно-головчатого, второго запястно-пястного суставов, локальные зоны отека костного мозга в головках второй и третьей пястных костей.
В пунктате синовиальной жидкости, полученной из первого плюснефалангового сустава правой стопы, при проведении поляризационной микроскопии кристаллы МУН не были обнаружены (исследование было выполнено на фоне приема аллопуринола).
Ввиду отсутствия достаточного критерия (наличие кристаллов МУН в синовиальной жидкости) для установления диагноза подагры (согласно классификационным критериям Американской коллегии ревматологов (ACR — American College of Rheumatology) и Европейского альянса ревматологических ассоциаций (EULAR — European Alliance of Associations for Rheumatology)) [14] пациенту было рекомендовано проведение двухэнергетической компьютерной томографии (ДЭКТ) стоп.
Исследование было выполнено на мультиспиральном рентгеновском компьютерном томографе SIEMENS SOMATOM Definition Flash по программе DUAL ENERGE FOOT GOUT с дальнейшей реконструкцией изображений в разных режимах, позволившее обнаружить немногочисленные субмиллиметровые участки отложений солей мочевой кислоты в мягких тканях правой стопы, единичные — в левой стопе (в области ногтевого ложа не учитывались) (рис. 2).
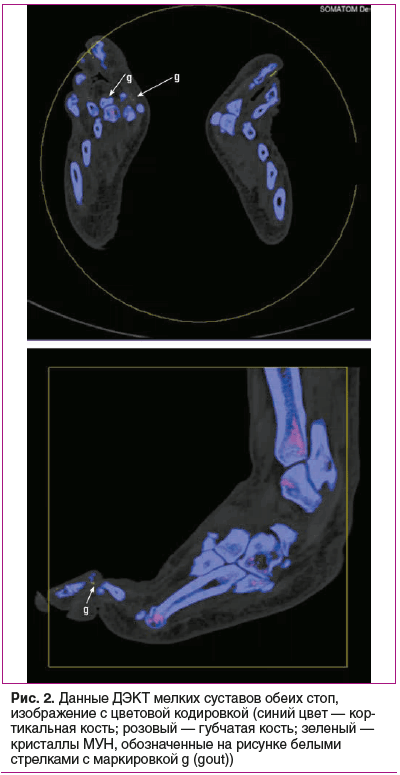
Таким образом, пациенту на основании клинико-лабораторно-визуализационных данных (по критериям ACR/EULAR [14] — 11 баллов при минимальном пороговом уровне, равном 8 баллов) был выставлен клинический диа-гноз первичной подагры хронического течения, хронического артрита бестофусной формы.
Рекомендован прием аллопуринола в стартовой дозе 100 мг/сут с постепенным повышением дозы до достижения целевого уровня мочевой кислоты менее 300 мкмоль/л (с учетом очень высокого кардиоваскулярного риска)1. Вместе с уратснижающей терапией для профилактики рецидивов подагрического артрита был назначен колхицин в дозе 1,0 мг/сут.
Эндокринологом продолжено лечение ожирения, в частности, последовательно были назначены лираглутид 3 мг и cемаглутид 7 мг, прием данных препаратов привел к дальнейшему снижению массы тела еще на 37 кг (в настоящее время ИМТ — 30,6 кг/м2). Также пациенту врачом-кардиологом были подобраны антигипертензивные, антиангинальные и антикоагулянтный препараты (последний был назначен под прикрытием гастропротекторов).
Первый эпизод болей в нижней части спины механического характера (интенсивность болей по числовой рейтинговой шкале оценивалась пациентом на 7–8 баллов) зафиксирован в марте 2023 г. после перенесенной новой коронавирусной инфекции. В течение 2 нед. пациент по рекомендации врача-невролога принимал НПВП (напроксен), толперизон и комплексный препарат, содержащий витамины группы В. Ввиду недостаточного эффекта от проведенного консервативного лечения больному была проведена локальная инъекционная терапия глюкокортикоидами (препараты вводились пресакрально и паравертебрально) с эффектом последействия в течение 2 нед. В апреле 2023 г. пациенту была выполнена радиочастотная нуклеопластика межпозвонкового диска L4-L5 с радиочастотной денервацией фасеточных суставов на уровне L3-L4-L5-S1 сегментов с обеих сторон. Из-за рецидива болей в спине спустя 1 год пациенту повторно была выполнена нейрохирургическая операция — радиочастотная денервация фасеточных суставов на уровне сегментов L2-L3-L4-L5-S1 с обеих сторон.
При проведении МРТ поясничного отдела позвоночника (апрель 2024 г.) был обнаружен отек костного мозга суставных поверхностей КПС с обеих сторон с наличием неравномерного сужения суставных щелей, преимущественно в верхних отделах (рис. 3).

Вследствие выявления МР-признаков активного двустороннего сакроилиита пациент был направлен нейрохирургом на повторную консультацию к врачу-ревматологу для исключения дебюта анкилозирующего спондилита.
Для уточнения природы поражения КПС пациенту было рекомендовано проведение иммуногенетического исследования, в ходе выполнения которого аллели HLA B27 и HLA Cw6 не были обнаружены. Также была выполнена ДЭКТ КПС (май 2024 г.), которая позволила обнаружить множественные участки отложения кристаллов МУН в области КПС (рис. 4, 5), в местах прикрепления мышц таза, дугоотростчатых суставов в поясничном отделе позвоночника, вдоль передней и задней продольных связок, в местах энтезисов головки и шейки бедренных костей (рис. 5). Также были выявлены КТ-признаки перенесенного сакроилиита с обеих сторон (в смежных отделах сочленяющихся костей определяются обширные зоны склероза толщиной в крестце до 1,1 см, в подвздошной кости — до 1,4 см, суставная щель была неравномерно расширена, с краевыми эрозиями подвздошной кости справа) (рис. 6).


Сопоставление клинической картины с полученными лабораторными и инструментальными данными складывалось в пользу подагрического характера поражения поясничного отдела позвоночника и КПС (подагрический сакроилиит). Предположительный диагноз анкилозирующего спондилита не был подтвержден. Пациенту была продолжена терапия аллопуринолом с титрованием дозы до 400 мг/сут (на фоне приема колхицина 0,5 мг/сут), что позволило достигнуть целевых значений мочевой кислоты (282 мкмоль/л). В течение последующего года эпизодов выраженных болей в спине не наблюдалось. При выполнении ДЭКТ КПС в динамике спустя 11 мес. (в апреле 2025 г.) какой-либо существенной динамики не отмечалось — объем депозитов уратов сохранялся прежним, отмечалось только перераспределение данных отложений.
Обсуждение
Представленное клиническое наблюдение демонстрирует сложный в диагностическом плане случай хронической подагры с относительно редкой локализацией уратных депозитов в структурах пояснично-крестцового отдела позвоночника и КПС, что симулировало клинико-рентгенологическую картину анкилозирующего спондилита. Наше описание клинического наблюдения развития подагрического сакроилиита не является уникальным, на поражение КПС указывают и другие авторы [5, 9–11, 15, 16].
Как подчеркивают R.M. Konatalapalli et al. [1], сакроилиит при подагре чаще всего протекает субклинически, являясь случайной находкой при исследовании. Возникшая интенсивная механическая боль в спине и выявленный по данным МРТ двусторонний сакроилиит закономерно вызвали у врачей подозрение на дебют анкилозирующего спондилита, что в такой ситуации представляется диагностической дилеммой [9, 10, 15]. В этой связи отметим, что признаки отека костного мозга, верифицируемые при проведении МРТ КПС, имеют неспецифический характер и могут быть проявлением различных заболеваний, в том числе и спондилоартритов [5].
У пациента в течение многих лет отмечалась неадекватно контролируемая гиперурикемия на фоне нерегулярной уратснижающей терапии, что, вероятно, создало предпосылки для тяжелого течения заболевания с формированием хронического артрита и внесуставных отложений кристаллов МУН. Несмотря на типичный анамнез (острый моноартрит первого плюснефалангового сустава, рецидивирующее течение), прямое подтверждение диагноза — обнаружение кристаллов МУН в синовиальной жидкости — оказалось негативным, что обусловило необходимость применения более чувствительных визуализационных методов.
Верификация подагрического генеза сакроилиита стала возможной благодаря применению ДЭКТ. ДЭКТ — это быстрый и неинвазивный метод исследования, заключающийся в спектральной дифференцировке материалов с помощью сканирования определенного участка тела двумя типами рентгеновского излучения, отличающимися по энергии, без использования контрастных веществ, характеризующийся высокой специфичностью (93,7%) и чувствительностью (84,7%) [17]. Т.В. Ким и соавт. [18] в своем исследовании продемонстрировали еще более высокую чувствительность ДЭКТ у пациентов с более длительным стажем подагры, превышающим 10 лет (95%). Продолжительность подагры в описываемом нами клиническом наблюдении на момент верификации природы сакроилиита составила около 15 лет. По мнению М.С. Елисеева и Я.И. Кузьминой [19], у пациентов с длительным анамнезом подагры в случае аксиальных проявлений (наличия жалоб со стороны позвоночника и тазобедренных суставов) для верификации причины боли и исключения атипичного течения болезни следует использовать ДЭКТ. Также подчеркнем, что ДЭКТ является предпочтительным методом для выявления отложения кристаллов МУН в нетипичных местах, где сложно подтвердить наличие кристаллов с помощью аспирации и последующего микроскопического исследования синовиальной жидкости или где недостаточно биоматериала для диагностической аспирации. Однако высказываются опасения, что получить изображение крупных проксимальных суставов (тазобед-ренных и плечевых) и осевого скелета может быть непросто из-за наличия шумов и артефактов в наборе данных с напряжением 80 кВ [20].
Двухэнергетическая компьютерная томография обладает высокой специфичностью в визуализации кристаллов МУН. Применение данного визуализационного исследования в нашем случае позволило идентифицировать уратные депозиты в области КПС, дугоотростчатых суставов, энтезисах и по ходу связок позвоночника. Выявленные изменения (отек костного мозга по данным МРТ, эрозии и склероз по данным КТ) в КПС были интерпретированы как проявление перенесенного и, вероятно, хронического воспаления, индуцированного отложениями уратов, что расширяет спектр причин боли в нижней части спины, особенно у пациентов с длительно текущей неконтролируемой подагрой.
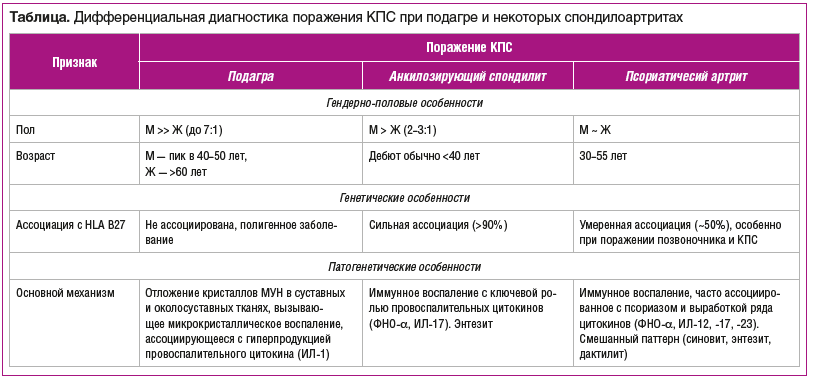
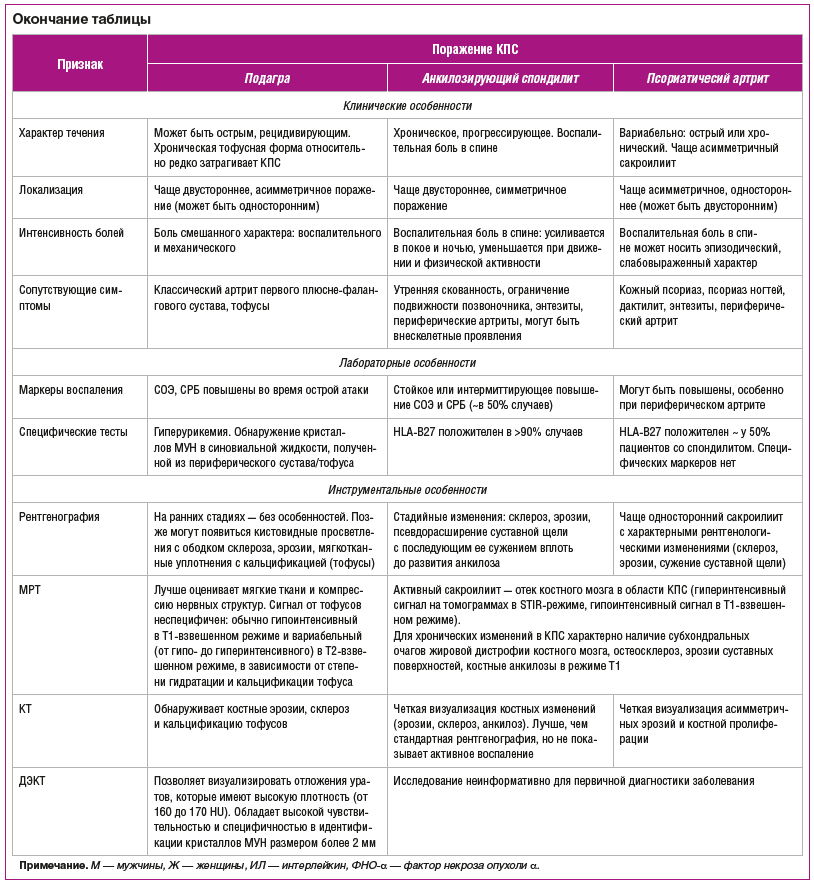
Дифференциально-диагностические признаки поражения КПС при подагре2 [2, 4, 5, 12, 18], анкилозирующем спондилите и псориатическом артрите представлены в таблице.
Достижение стойкой нормоурикемии на фоне адекватной уратснижающей терапии привело к значительному клиническому улучшению — исчезновению выраженных болей в спине в течение последующего года, что является важным аргументом в пользу правильности установленного диагноза. Отсутствие существенной динамики в объеме уратных депозитов по данным контрольной ДЭКТ через 11 мес. ожидаемо, так как для резорбции тофусов, особенно в костной ткани, требуются годы непрерывной адекватной уратснижающей терапии.
Заключение
Данное клиническое наблюдение наглядно иллюстрирует, что подагра является системным заболеванием, способным поражать не только периферические суставы, но и осевой скелет. Ключевой проблемой стала дифференциальная диагностика с анкилозирующим спондилитом, учитывая обнаруженные по данным МРТ признаки сакроилиита. При наличии у пациента с хронической подагрой упорного болевого синдрома в спине и визуализационных признаков сакроилиита необходимо включать подагрическое поражение КПС в круг дифференциальной диагностики. Отрицательный статус по HLA-B27 и, что наиболее важно, выявление множественных отложений кристаллов МУН в области КПС и энтезисов с помощью ДЭКТ позволили подтвердить подагрическую природу заболевания. Успешное достижение целевого уровня мочевой кислоты на фоне подобранной уратснижающей терапии привело к стойкому купированию выраженного болевого синдрома в спине в течение 1 года, что доказывает эффективность контроля гиперурикемии даже при структурных изменениях. Таким образом, своевременная диагностика и назначение адекватной долгосрочной терапии являются залогом успешного контроля над заболеванием и предотвращения его прогрессирования и осложнений.
1Клинические рекомендации. Подагра. 2018. (Электронный ресурс.) URL: https://library.mededtech.ru/rest/documents/cr_174/ (дата обращения: 02.08.2025).
2Клинические рекомендации. Идиопатическая подагра. 2025. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/preview-cr/936_1 (дата обращения: 02.08.2025).
Информация с rmj.ru




