Введение
Гиперплазия эндометрия (ГПЭ) представляет собой гинекологическое заболевание, при котором вследствие пролиферации желез, увеличения железисто-стромального соотношения поражается эндометрий матки [1–3]. Согласно данным, представленным в печати в 2022 г. (основаны на материалах 29 различных исследований), заболеваемость ГПЭ среди женщин в пременопаузе увеличивается с возрастом и может достигать в различных популяциях от 121 случая на 100 000 женщин-лет (у южнокорейских женщин в возрасте 46–50 лет) до 270 случаев на 100 000 женщин-лет (у американских женщин в возрасте 45–49 лет) [1]. Частота ГПЭ у пациенток с бесплодием находится в пределах от 0,9 до 3,0%, а среди индивидуумов с аномальными маточными кровотечениями ГПЭ регистрируется значительно чаще (3,4–26,5%) [1]. Наличие ГПЭ (особенно атипичных форм) у женщины существенно повышает риск возникновения рака эндометрия [3, 4].
Известными факторами риска развития ГПЭ являются возраст, ожирение, раннее менархе / поздняя менопауза, сахарный диабет, хроническая ановуляция, пролонгированная перименопауза, постменопаузальный статус и др. [1–4]. Ключевое значение для этиопатогенеза ГПЭ имеют гормональные факторы (гиперэстрогения, дисбаланс эстрогенов и прогестерона, эффекты андрогенов и др.), которые оказывают пролиферативное влияние на эндометрий матки [2–8]. Значимая роль в возникновении заболевания отводится и генетическим факторам [9–13]. При этом важно отметить, что данные о генетических детерминантах ГПЭ, известные в мире на сегодня, крайне малочисленны и нередко неоднозначны; до настоящего времени не проведено ни одного полногеномного ассоциативного исследования (genome-wide association study, GWAS) ГПЭ, что однозначно указывает на необходимость более активного изучения молекулярно-генетических основ данного заболевания.
Цель исследования: изучить ассоциацию полиморфных вариантов, связанных с уровнем половых гормонов в организме, с риском развития ГПЭ у женщин с нормальным индексом массы тела (ИМТ).
Материал и методы
Работа выполнена на выборке 766 женщин с ИМТ <25 кг/м2, среди которых 196 пациенток с ГПЭ и 570 контрольных индивидуумов. Все обследуемые являлись русскими, родились (и проживали) в центральной части России, без родственных связей друг с другом [14]. Выборка формировалась в перинатальном центре ОГБУЗ «Белгородская областная клиническая больница Святителя Иоасафа» в 2008–2013 гг.: в группу пациенток включали женщин с гистологически подтвержденным диагнозом ГПЭ (простая без атипии форма) [9]; в группу контроля — женщины, у которых отсутствовали клинические и УЗИ-данные о пролиферативных заболеваниях органов малого таза [15]. Показатели возраста (36,21±8,62 года (ГПЭ) и 35,28±8,13 года (контроль), p>0,05) и ИМТ (21,61±1,81 кг/м2 (ГПЭ) и 21,42±1,83 кг/м2 (контроль), p>0,05) сравниваемых групп не отличались.
Проведено генотипирование пяти полиморфизмов, связанных с уровнем половых гормонов (эстрадиол, тестостерон, глобулин, связывающий половые гормоны (ГСПГ), фолликулостимулирующий гормон (ФСГ), индекс свободных андрогенов) в организме, согласно данным ранее проведенных GWAS: rs11031005 FSHB (T>C) (тестостерон [16–18], ФСГ [19], индекс свободных андрогенов [18]), rs1641549 TP53 (C>T) (ГСПГ [19]), rs117585797 ANO2 (C>A) (эстрадиол [19]), rs117145500 CHD9 (A>C) (индекс свободных андрогенов [19]), rs727428-SHBG (C>T) (ГСПГ [20–22], эстрадиол [17], тестостерон [16, 21]). Генотипирование SNP выполняли в режиме real-time PCR (полимеразная цепная реакция в реальном времени) на амплификаторе CFX96 Touch (Bio-Rad, США) с использованием специально изготовленных для данного исследования наборов реагентов (ООО «ТЕСТ ГЕН ЛАБОРАТОРИЯ», г. Ульяновск), которые содержат специфические нуклеотидные последовательности праймеров и зондов, по протоколу фирмы-производителя. Полученные результаты по распределению генотипов рассмотренных локусов в изученных группах оценивали на основе закона Харди — Вайнберга.
Поиск ассоциаций SNP c ГПЭ выполняли методом логистической регрессии, имплементированным в программе gPLINK [23], в рамках четырех генетических моделей (аллельная, аддитивная, доминантная, рецессивная) с обязательным включением в анализ ковариат (возраст и ИМТ) и проведением пермутационного тестирования [24] при установленном уровне статистической значимости pperm<0,05. Направленность и силу ассоциации оценивали на основе общепринятых в генетико-эпидемиологических исследованиях показателях OR (odds ratio, отношение шансов) и 95% СI (confidence interval, доверительный интервал). Для локуса rs11031005 FSHB (T>C), показавшего значимые связи с ГПЭ (и сильно сцепленных с ним SNP rs11031006 и rs74485684) методом анализа in silico c использованием баз данных HaploReg (версия 4.2; дата обращения: 01.02.2024) [25] и GTEx portal (дата обращения: 10.02.2024) [26] изучена функциональная значимость.
Результаты и обсуждение
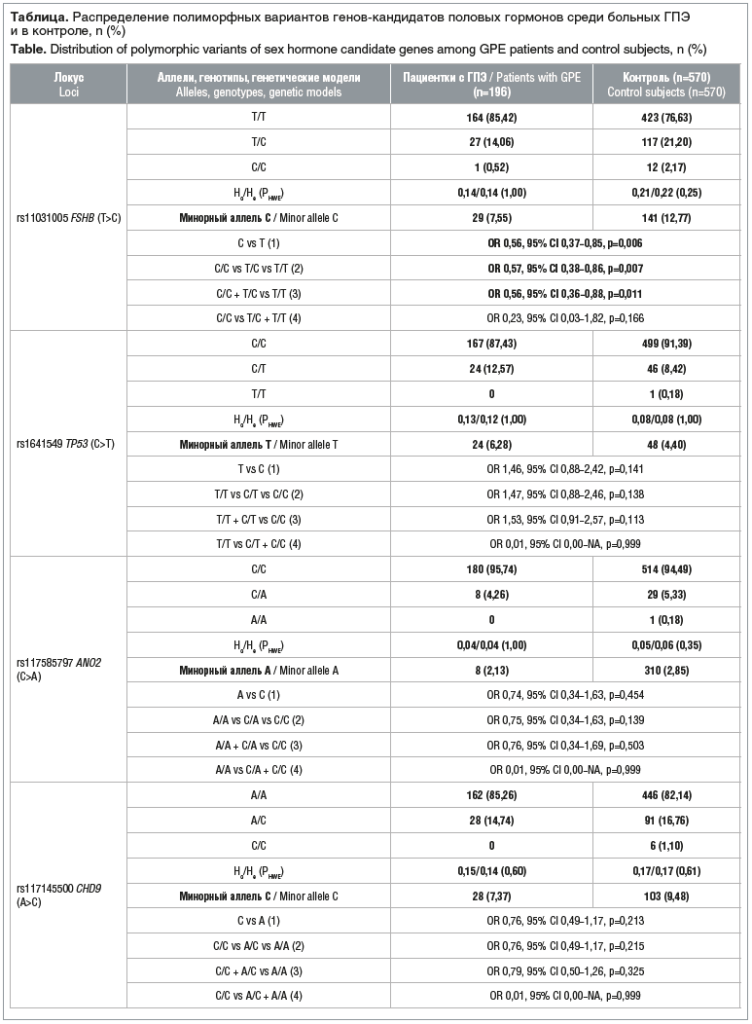
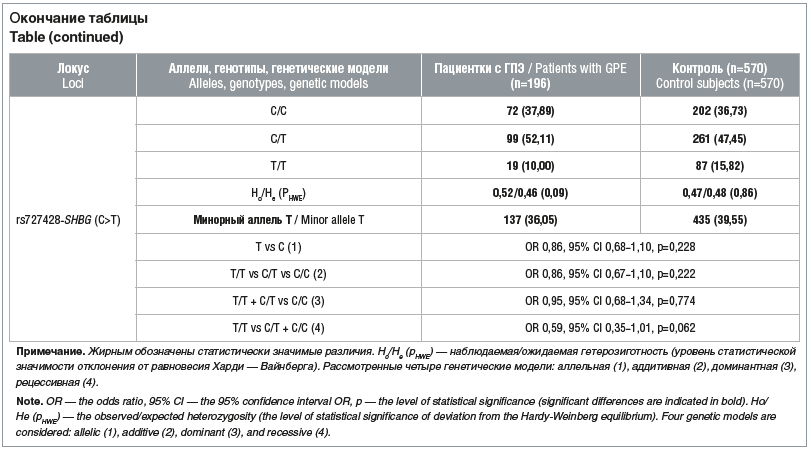
В изучаемых группах женщин с ИМТ <25 кг/м2 (пациентки с ГПЭ, контроль) распределение анализируемых полиморфизмов подчинялось закону Харди — Вайнберга: pHWE≥0,085 (пациентки с ГПЭ) и pHWE≥0,184 (контроль). Частоты альтернативных аллелей варьировали в интервале от 0,021 (rs117585797 ANO2 (C>A)) до 0,361 (rs727428 SHBG (C>T)) среди пациенток с ГПЭ и от 0,028 (rs117585797 ANO2 (C>A)) до 0,396 (rs727428 SHBG (C>T)) в контроле (см. таблицу).
Среди изученных пяти полиморфизмов связь с заболеванием была зарегистрирована для локуса rs11031005 FSHB (T>C) в трех генетических моделях: аллельной (OR 0,56; 95% СI 0,37–0,85; р=0,006, рperm=0,006), аддитивной (OR 0,57; 95% СI 0,38–0,86; р=0,007, рperm=0,008), доминантной (OR 0,56; 95% СI 0,36–0,88; р=0,011, рperm=0,012) (см. таблицу). На основании полученных данных можно заключить, что аллельный вариант С rs11031005 FSHB имеет протективное значение при формировании ГПЭ у женщин с нормальным ИМТ (OR<1).
Согласно базе HaploReg (версия 4.2; дата обращения: 13.02.2024) полиморфизм rs11031005 FSHB, расположенный в предполагаемой промоторной области гена FSHB (26kb 5′ этого гена), влияет на взаимодействие ДНК с двумя факторами транскрипции (ФТ) — Otx2, Zfp281. При этом протективный для возникновения ГПЭ аллельный вариант С этого полиморфизма повышает «чувствительность» ДНК к влияниям ФТ Zfp105 и снижает аффинность ДНК к действию ФТ Otx2. Важно отметить, что два сильно сцепленных с rs11031005 FSHB полиморфизма — rs11031006 (r2=1,00; D’=1,00) и rs74485684 (r2=0,81; D’=0,99) также находятся в регионах взаимодействия ДНК более чем с 20 ФТ: для rs11031006 — 11 ФТ (ERalpha-a, FXR, Foxj2, Foxl1, HNF4, LRH1, NR4A, RORalpha1, RXRA, SF1, Sox), для rs74485684 — 10 ФТ (Foxa, Foxd1, Foxf2, Foxj1, Foxk1, Foxo, HDAC2, MZF1, Spz1, р300).
По данным базы GTEx portal, SNP rs11031005 FSHB ассоциирован с транскрипцией гена ARL14EP в подкожной жировой ткани, причем минорный аллельный вариант C rs11031005 связан с более высокой транскрипционной активностью гена ARL14EP (NES=0,25; р=5,3e-6). Важно, что с уровнем экспрессии этого же гена в подкожной жировой ткани связаны и два сильно сцепленных с rs11031005 FSHB SNP — rs11031006 (NES=0,26; р=1,3e-6) и rs74485684 (NES=0,27; р=2,2e-8).
Итак, полиморфный вариант rs11031005 FSHB (T>C) и два сильно сцепленных с ним SNP (rs11031006 и rs74485684) обладают значимыми функциональными эффектами (располагаются в промоторном регионе гена FSHB, взаимодействующего более чем с 20 ФТ и влияющего на экспрессию гена ARL14EP в подкожной жировой ткани), что может являться медико-биологической основой установленной нами ассоциации этого локуса с риском возникновения ГПЭ в изучаемой группе женщин с ИМТ <25 кг/м2.
В ранее проведенных GWAS показана важная роль SNP rs11031005 FSHB (T>C) в формировании гормонального профиля организма: выявлена его связь с содержанием ФСГ [19], общего и биодоступного тестостерона [18–20], соотношением тестостерон/ГСПГ [18]. Исходя из этого, одним из потенциальных механизмов, определяющих связь локуса rs11031005 FSHB (T>C) с ГПЭ, установленную в нашем исследовании, может быть его влияние на содержание в организме общего и биодоступного тестостерона, причем минорный аллель С rs11031005 (протективный фактор развития ГПЭ, по нашим данным) связан с более высокими концентрациями общего и биодоступного тестостерона [16–18] и низким соотношением тестостерон/ГСПГ [18].
Современные данные литературы, основанные на большом числе экспериментальных исследований, свидетельствуют о существенном влиянии андрогенов (тестостерон, дегидроэпиандростерон, андростендион, дигидротестостерон (ДГТ)) на физиологию женской репродуктивной системы [7, 8]. Эти воздействия андрогенов могут быть как самостоятельными (за счет связывания со своими специфическими андрогеновыми рецепторами (androgen receptor, AR) и влияния на экспрессию генов-мишеней (например, таргетными генами в эндометрии являются CITED2, ACSS2, PPFIBP2, MAOA и др. [27])), так и опосредованными (за счет влияния на эстрогены и прогестерон), что приводит к сложной сети взаимодействий стероидных гормонов и играет важную регуляторную роль в менструальном цикле, биологии эндометрия и развитии фолликулов в яичниках [8]. У женщин 80% андрогенов связываются с ГСПГ, 19% — с сывороточным альбумином и только 1% свободный; лишь свободные андрогены являются активными [7]. Кроме того, андрогены преобразуются ароматазой в эстрогены и уже за счет этого могут реализовать свои биологические эффекты [7].
Тестостерон, повышая экспрессию инсулиноподобного фактора роста 1, стимулирует рост и созревание примордиальных фолликулов, метаболизм ооцитов, рекрутинг фолликулов и извлечение ооцитов, усиливает реакцию фолликулов на ФСГ [8, 28, 29]. Вместе с этим на поздних стадиях развития фолликулов андрогены ингибируют рост фолликулов и выработку эстрогенов, стимулируют апоптоз клеток гранулезы и переход к созреванию фолликулов [30], а также развитие антральной полости [31]. Кроме того, передача сигналов андрогенами в яичниках стимулирует образование желтых тел посредством усиления экспрессии рецептора ФСГ, таким образом также оказывая косвенное стимулирующее влияние на выработку прогестерона [32, 33].
На экспериментальных моделях трансгенных животных убедительно показано, что при нокауте рецепторов андрогенов наблюдаются значительные нарушения в работе яичников (нарушение развития фолликулов, более длительные эстральные циклы, меньшее количество желтых тел, повышенная атрезия фолликулов, нарушение извлечения яйцеклеток и др.) [8, 34], что имеет первостепенное значение в патогенезе ГПЭ [4].
Весьма интересны данные, представленные в литературе, по вопросу влияния тестостерона на пролиферацию клеток эндометрия. Считается, что экспрессия рецепторов андрогенов происходит преимущественно в стромальных клетках эндометрия и она повышается в конце пролиферативной и начале секреторной фазы [8, 35]. С одной стороны, в экспериментах in vivo (мыши с овариэктомией и трансгенные мыши) показаны прямые связи между введением тестостерона, ДГТ и пролиферацией клеток эндометрия (за счет активизации сигнальных путей инсулиноподобного фактора роста 1) [8, 36, 37]. С другой стороны, в ряде исследований in vitro продемонстрированы ингибирующие эффекты андростендиона, тестостерона и ДГТ на пролиферацию клеток эндометрия человека (как стромальных, так и железистых) [27, 38–40] в противовес пролиферативным эффектам эстрогенов [8]. Также показано, что использование экзогенного тестостерона (выше нормальных физиологических уровней) для лечения женщин приводило к атрофии эндометрия и снижению пролиферации клеток [41, 42]. В экспериментах in vitro установлено, что ДГТ значительно снижает активность каспаз в стромальных клетках эндометрия человека, что имеет важное значение для стромально-железистых эпителиальных взаимодействий и регуляции андроген-зависимого клеточного апоптоза [27].
Таким образом, вышеприведенные данные литературы содержат достаточно убедительные аргументы, позволяющие обосновать протективные эффекты по отношению к ГПЭ минорного аллеля SNP rs11031005 FSHB (T>C) (обнаружены в нашем исследовании), связанного, согласно данным GWAS [16–18], с повышенным содержанием общего и биодоступного тестостерона в организме. Важно подчеркнуть, что сильно сцепленные с рассматриваемым нами локусом rs11031005 FSHB (T>C) полиморфизмы также демонстрируют значимые ассоциации как с уровнем тестостерона (rs12294104 [16]), так и с таким тестостерон-значимым заболеванием, как синдром поликистозных яичников (rs11031006 [43–45], rs10835638 [45], rs11031010 [46]).
Следует отметить, что многочисленные данные, представленные как в экспериментальных работах (в том числе основанных на GWAS) [43–54], так и в обзорных статьях [55–57], убедительно демонстрируют выраженную связь достаточно большого числа и других SNP (rs11031006, rs10835638, rs74485684, rs1782507, rs11031010, rs555621 и др.), расположенных в промоторном регионе гена FSHB (0,21–40 Kb 5′ участка гена FSHB) с различными гормон-зависимыми признаками (заболеваниями).
Более чем в 10 различных GWAS показана связь rs11031006 гена FSHB с такими репродуктивно значимыми фенотипами, как уровень ФСГ [53], концентрация лютеинизирующего гормона (ЛГ) и синдром поликистозных яичников [43], содержание ФСГ и рождение дизиготных близнецов [48], возраст менархе [49] и возраст менопаузы [44], характеристики менструального цикла (продолжительность, наличие чрезмерных, частых и нерегулярных менструаций) и овариэктомия (билатеральная) [50], миома матки [54], миома матки и обильные менструальные кровотечения [51], эндометриоз, возраст менархе и продолжительность менструального цикла (плейотропные связи, выявленные методом менделеевской рандомизации) [52], синдром поликистозных яичников [45, 47]. Следует отметить, что rs11031006 находится на расстоянии 72 пары нуклеотидов от изучаемого нами rs11031005 и сильно сцеплен с ним при r2=1 и D’=1.
Не менее важное медико-биологическое значение (связь с гормон-зависимыми репродуктивно значимыми показателями) показано в ряде работ и для полиморфизма rs10835638 гена FSHB (место локализации — 210bp 5′ данного гена), расположенного на расстоянии 26 kb от изучаемого нами rs11031005 и сцепленного с ним (r2=0,62/D’=0,79). Так, в работе K.S. Ruth et al. [58] выявлена связь rs10835638 с содержанием ЛГ, продолжительностью менструального цикла, возрастом менопаузы, развитием бесплодия у женщин с эндометриозом. В исследовании B. Bianco et al. [59] обнаружена ассоциация этого локуса с уровнем ЛГ у пациенток с эндометриозом, страдающих бесплодием. По данным K. Rull et al. [60], полиморфизм rs10835638 (-211 G>T FSHB) был связан с концентрацией ФСГ и ЛГ у женщин с аменореей и бесплодием. Значимые связи данный генетический вариант показал с уровнем ЛГ, реакцией на контролируемую гиперстимуляцию яичников, числом полученных антральных фолликулов, яйцеклеток, эмбрионов [61], а также синдромом поликистозных яичников [45] и уровнем ФСГ при идиопатическом мужском бесплодии [62].
На связь других полиморфизмов, локализованных в регионе регуляторных участков гена FSHB, с гормон-зависимыми фенотипами также указывается в значительном количестве различных научных публикаций: возраст менархе (rs1782507 [8,7kb 5′ гена FSHB], rs555621 [16kb 5′ гена FSHB]) [63], возраст менархе, уровень ЛГ и синдром поликистозных яичников (rs11031010 [12kb 5′ гена FSHB]) [46, 63], возраст менопаузы, концентрация тестостерона, уровень ЛГ и соотношение ЛГ/ФСГ (rs12294104 [23kb 3′ гена C11orf46], расположен на расстоянии 156,5 kb от rs11031005 и сильно сцеплен с ним при r2=0,37/D’=0,66) [16, 64–67], миома матки (rs76959488 [17kb 3′ гена C11orf46], расположен на расстоянии 149,9 kb от rs11031005 и сильно сцеплен с ним при r2=0,42/D’=0,68) [68], эндометриоз (rs74485684 [10kb 5′ гена FSHB]) [69]. Важно отметить, что для выборки женщин из популяции Центрально-Черноземного региона России (изучается в настоящей работе) ранее были показаны связи полиморфизмов rs1782507, rs11031010, rs555621 промоторного региона гена FSHB (8,7-16 kb 5′ данного гена) с такими гормон-зависимыми признаками, как масса тела новорожденного (rs1782507, rs555621) [70], ГПЭ [9].
Таким образом, на основании полученных нами результатов и вышеуказанных многочисленных данных литературы можно утверждать, что функционально значимые полиморфные локусы гена FSHB (rs11031002, rs11031005, rs11031006, rs10835638, rs74485684, rs1782507, rs12294104, rs11031010, rs76959488, rs555621) играют ключевую роль в детерминации гормонального статуса женского организма и формировании гормон-зависимых фенотипов (нормальных признаков и заболеваний), что позволяет считать данный ген «синтропным геном» для множества гормон-связанных признаков/патологий. Это раскрывает широкие перспективы как для дальнейших медико-генетических исследований SNP гена FSHB в отношении других гормон-зависимых фенотипов организма (недостаточно изученных к настоящему времени), так и для использования полиморфизмов этого гена в практической медицине (предиктивное тестирование) в качестве генетических маркеров повышенного риска развития гормон-зависимых заболеваний.
Заключение
Результаты настоящего исследования подтверждают связь GWAS-значимого для содержания половых гормонов в организме (концентрации общего и биодоступного тестостерона, соотношение тестостерон/ГСПГ, уровень ФСГ) полиморфизма rs11031005 FSHB (T>C) с риском развития ГПЭ у женщин с нормальным ИМТ (минорный аллель С является протективным фактором развития заболевания, OR 0,56–0,57). Локус rs11031005 FSHB (T>C) и два сильно сцепленных с ним SNP (rs11031006 и rs74485684) обладают значимыми функциональными эффектами (располагаются в промоторном регионе гена FSHB, взаимодействующего более чем с 20 ФТ (ERalpha-a, FXR, Foxj2, Foxl1, HNF4, LRH1, NR4A, RORalpha1, RXRA, SF1, Sox, Foxa, Foxd1, Foxf2, Foxj1, Foxk1, Foxo, HDAC2, MZF1, Spz1, р300) и влияющего на экспрессию гена ARL14EP в подкожной жировой ткани).
Сведения об авторах:
Чурносов Владимир Иванович — аспирант кафедры медико-биологических дисциплин медицинского института ФГАОУ ВО «Белгородский государственный национальный исследовательский университет»; 308015, Россия, г. Белгород, ул. Победы, д. 85; ORCID iD 0009-0007-8519-4594
Пономаренко Ирина Васильевна — д.м.н., профессор кафедры медико-биологических дисциплин медицинского института ФГАОУ ВО «Белгородский государственный национальный исследовательский университет»; 308015, Россия, г. Белгород, ул. Победы, д. 85; ORCID iD 0000-0002-5652-0166
Чурносов Михаил Иванович — д.м.н., профессор, заведующий кафедрой медико-биологических дисциплин медицинского института ФГАОУ ВО «Белгородский государственный национальный исследовательский университет»; 308015, Россия, г. Белгород, ул. Победы, д. 85; ORCID iD 0000-0003-254-6134
Контактная информация: Пономаренко Ирина Васильевна, e-mail: ponomarenko_i@bsuedu.ru
Источник финансирования: исследование выполнено за счет гранта Российского научного фонда № 25-25-00034, https://rscf.ru/project/25-25-00034/
Конфликт интересов: отсутствует.
Статья поступила 15.04.2025.
Поступила после рецензирования 08.05.2025.
Принята в печать 02.06.2025.
Информация с rmj.ru





