Новый коронавирус был выделен и идентифицирован в 2019 г. в Ухане, Китай. 11 марта 2020 г. ВОЗ объявила о пандемии этого заболевания [1]. Было установлено, что заболевание вызвано новым одноцепочечным РНК-вирусом (ss-RNA, 29903 bp), относящимся к группе коронавирусов (CoV). Новый коронавирус был обозначен как SARS-CoV2 – severe acute respiratory syndrome coronavirus 2 [2], а вызываемое им заболевание названо COVID-19 – coronavirus disease2019. По данным ВОЗ, на начало июня 2020 г. в мире было уже более 7 млн подтвержденных случаев заболевания, в том числе более 400 тыс. с летальным исходом. Для проникновения в клетки вирус SARS-CoV2, как и SARS-CoV, экспрессирует рецептор для ангиотензинпревращающего фермента (АПФ) 2. У человека AПФ2 экспрессируется большинством органов и тканей, наиболее уязвимыми к новой коронавирусной инфекции являются легкие и нижние отделы дыхательных путей, сердце, почки, кишечник, а также гладкомышечные клетки сосудистой стенки (преимущественно микроциркуляторное русло) и ЦНС [3].
Биохимическими маркерами активной инфекции и неблагоприятного прогноза инфекции служат повышение уровня СРБ, D-димера (ДД) и гомоцистеина. Опубликовано динамическое наблюдение за пациентами с COVID-19 для оценки прогностической значимости различных показателей компьютерной томографии (КТ), характеризующих поражение легких. Средний возраст 273 пациентов COVID-19, поступивших с прогрессированием КТ-изменений, был выше, чем у пациентов без такого прогрессирования (р=0,006). Уровень лейкоцитов, тромбоцитов, нейтрофилов и кислотного гликопротеина был снижен у пациентов с прогрессированием по данным визуализации (все р<0,05), а моноцитов увеличен (р=0,025). Содержание гомоцистеина и СРБ было статистически значимо выше у пациентов с прогрессированием заболевания (р<0,05). Логистические модели показали, что в 1-ю неделю после инфицирования COVID-19 возраст, уровень гомоцистеина и период от начала инфекции до поступления пациентов в стационар являлись независимыми факторами для прогнозирования прогрессирования изменений в легких по данным КТ [4, 5].
Пока не существует лекарственного средства или вакцины против коронавируса человека и животных. Ингибирование фермента гидролазы 3CL обеспечивает перспективный терапевтический принцип для разработки методов лечения CoViD-19. Как известно, 3clpro (Mpro) участвует в противодействии врожденному иммунному ответу хозяина. В экспериментальном исследовании с использованием молекулярного докинга Autodock был показан ингибирующий эффект некоторых природных соединений против основного фермента вируса – гидролазы 3CL. Выявлено три агентакандидата, которые ингибируют основную протеазу коронавируса: хиспидин, лепидин Е и фолиевая кислота [6]. Фолиевая кислота является естественным фактором, уменьшающим выраженность гомоцистеинемии.
Отечественным препаратом, содержащим адекватную дозу фолиевой кислоты, является Ангиовит (производство АО «Алтайвитамины»). Ангиовит – комплексный препарат, в состав которого входят витамины группы В и фолиевая кислота (пиридоксина гидрохлорид 4 мг, фолиевая кислота 5 мг, цианокобаламин 6 мкг). Препарат способен активировать в организме ключевые ферменты транссульфурации и реметилирования метионина – метилентетрагидрофолатредуктазу и цистатион-В-синтетазу, в результате чего происходит ускорение обмена метионина и снижение в крови концентрации гомоцистеина. Гипергомоцистеинемия является важным фактором риска развития атеросклероза и артериального тромбоза, а также инфаркта миокарда, ишемического инсульта мозга, диабетической ангиопатии. Возникновению гипергомоцистеинемии способствует дефицит в организме фолиевой кислоты и витаминов В6 и В12 [7].
Цель настоящего пилотного исследования – оценка влияния Ангиовита в составе комплексной терапии острой стадии инфекции COVID-19, проявляющейся пневмонией или острой респираторной вирусной инфекцией (ОРВИ) с лихорадкой.
Пациенты и методы. В исследование включено 50 больных с острой стадией COVID-19-инфекции. У всех больных диагноз коронавирусной инфекции подтвержден с помощью полимеразной цепной реакции. Ангиовит получали 25 пациентов со средней степенью тяжести инфекции (женщин 13; 52%), средний возраст – 39,4 года, которые поступили в среднем на 3-й день заболевания. По методу случайной рандомизации к ним были подобраны 25 пациентов группы сравнения, не отличавшихся по полу, возрасту и особенностям клинического проявления COVID-19-инфекции, но поступившие чуть позже – на 3,3 день болезни.
В табл. 1 приведены демографические показатели пациентов основной группы и группы сравнения. Показатели базовых КТ-изменений по 5-балльной шкале выраженности (от 0 до 4 баллов) и степени дыхательной недостаточности (ДН) по 4-балльной шкале выраженности (от 0 до 3 баллов) значимо не различались в двух группах. Распределение по доминирующему синдрому (пневмония или ОРВИ) оказалось также практически равнозначным в группах, но в целом все показатели тяжести были незначительно выше в группе сравнения, чем в основной группе. Больные основной группы получали Ангиовит в дозе 3 таблетки в день на протяжении не менее 10 дней в дополнение к стандартной терапии, в том числе включавшей эноксапарин; ни одному из 50 пациентов не назначали глюкокортикоиды.

Исследование лабораторных показателей (СРБ, ДД, международное нормализованное отношение – МНО, активированное частичное тромбопластиновое время – АЧТВ) и клинический анализ крови, включавший определение форменных элементов, гемоглобина, гематокрита, субпопуляций лейкоцитов, проводили на биохимическом анализаторе Сапфир-500, иммунохимическом анализаторе Immulite-2000, коагулометре CA-660, гематологическом анализаторе МЕК-7300. Уровень гомоцистеина в крови определяли методом иммуноферментного анализа у 10 больных (по 5 из каждой группы), отобранных методом простой рандомизации.
Статистическая обработка результатов проводилась с помощью программного обеспечения SPSS и Microsoft Excel. Статистическое сравнение результатов исследования осуществляли с использованием непараметрического критерия Манна–Уитни (U-критерий Манна–Уитни), который применяется для оценки различий между двумя малыми выборками по уровню количественно измеряемого признака.
Результаты. Динамика клинических показателей на фоне лечения представлена в табл. 2. Больные получали Ангиовит в дополнение к базовой терапии, согласно Временным методическим рекомендациям Минздрава России по профилактике, диагностике и лечению новой коронавирусной инфекции (CОVID-19), версия 6 [8]. При приеме Ангиовита отмечено значимое уменьшение длительности лихорадочного периода (4,12 дня по сравнению с 5,88 дня без Ангиовита), пациенты значимо меньше дней провели в стационаре – длительность госпитализации составила 13,0 и 16,8 дней соответственно.

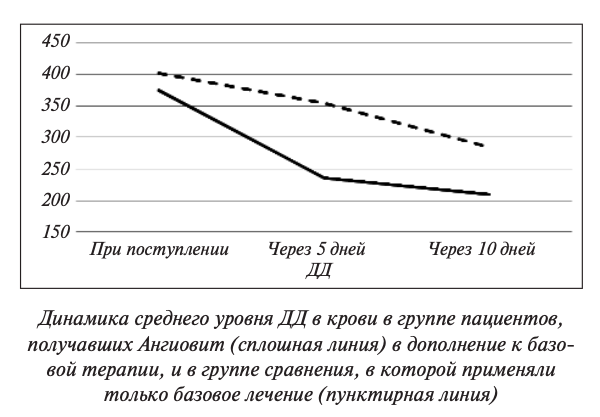
На фоне лечения лабораторные показатели стабилизировались и приближались к референсным значениям (табл. 3). В обеих группах отмечено уменьшение уровня СРБ и ДД в крови, повышение содержания лейкоцитов и лимфоцитов. У пациентов, получавших Ангиовит, наблюдалось более значимое снижение уровня СРБ и ДД, причем показатели ДД контролировали 3 раза, и его снижение произошло уже на 5-й день лечения.
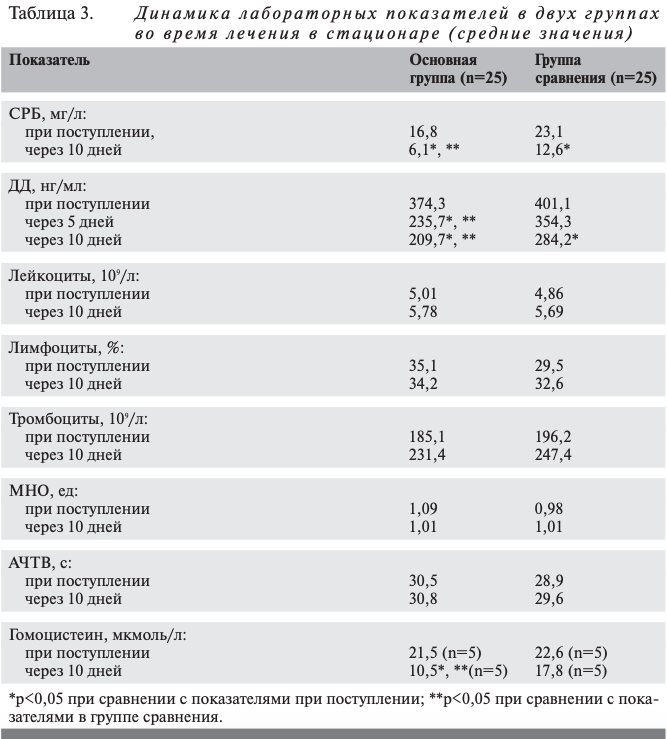
На рисунке показана динамика уровня ДД на фоне терапии Ангиовитом и без таковой. В группе, получавшей Ангиовит, статистически значимое снижение уровня ДД наблюдалось уже на 5-й день лечения, а в группе сравнения – только на 10-й день. Статистически значимой динамики других показателей в этой выборке не получено. Только в основной группе при добавлении Ангиовита зафиксировано значимое снижение уровня гомоцистеина на 10-й день.
Обсуждение. Одним из важных факторов развития эндотелиальной дисфункции (ЭД) при различных состояниях считается увеличение содержания в плазме крови гомоцистеина – серосодержащей кислоты, являющейся продуктом метаболизма метионина. Метаболизм гомоцистеина осуществляется двумя основными путями: транссульфурированием в цистеин и реметилированием в метионин. Ключевыми ферментами для обеспечения этих метаболических путей служат соответственно цистатионин-β-синтетаза и метилентетрагидрофолат редуктаза. Метаболизм гомоцистеина в значительной степени определяется содержанием фолиевой кислоты, витамина В12, витамина В6 (являющегося коферментом в реакции деметилирования гомоцистеина), которые выступают в качестве кофакторов реметилирования [9].
В настоящее время показано наличие нескольких основных механизмов негативного влияния гомоцистеина при ЭД [10]. Гомоцистеин, в отличие от других аминотиолов (цистеина, глутатиона, N-ацетилцистеина), вызывает окислительный стресс посредством различных механизмов (прямого и опосредованного), роль которых пока недостаточно исследована. Это, в свою очередь, приводит к развитию ЭД и формированию протромбогенного состояния. В клетках небольшая часть гомоцистеина превращается в тиолактонную форму, которая легко проникает через мембраны и обладает высокой биологической активностью. Так, показано, что тиолактон гомоцистеина ингибирует Na+/K+-АТФазу [11] и лизилоксидазу [12], однако пока роль этих механизмов в развитии ЭД неясна. При повышении внутриклеточной концентрации гомоцистеина реакция разложения его предшественника – S-аденозилгомоцистеина (S-Adenosyl-L-homocysteine, SAH) тормозится. Избыток SAH ингибирует реакции трансметилирования белков, ДНК и других субстратов, что ведет к множественным изменениям экспрессии генов. Гипометилирование, в свою очередь, тормозит экспрессию цистатион-γ-лиазы – фермента пути транссульфурации, который участвует в удалении избытка гомоцистеина и синтезе вазодилататора H2S [13, 14]. На сегодняшний день считается, что гипометилирование играет ключевую роль в гомоцистеин-опосредованной ЭД. Кроме того, гомоцистеин стимулирует пролиферацию гладкомышечных клеток в сосудистой стенке [15, 16].
Учитывая, что в патогенезе сосудистых осложнений инфекции COVID-19 важную роль играет дисрегуляция ангиотензиновой системы [17], снижение уровня гомоцистеина может оказать положительный эффект, поскольку имеются данные, свидетельствующие о тесной взаимосвязи гомоцистеина с активностью ангиотензина II. Во-первых, были показаны возможность прямой активации рецепторов ангиотензина (AT1R) гомоцистеином и важная роль этого механизма в ремоделировании сосудов на модели гипергомоцистеинемии у мышей [18]. Позднее прямая активация (орто- и аллостерическая) AT1R при связывании с гомоцистеином была подтверждена методом молекулярной динамики и in vitro [19]. Во-вторых, на экспериментальной модели гипергомоцистеинемии у крыс установлено, что применение фолиевой кислоты снижало как уровень гомоцистеина, так и его гипертензивный эффект. На этой модели было также выявлено, что гомоцистеин вызывал гиперэкспрессию АПФ1, а также AT1R и что эти эффекты тоже устранялись фолиевой кислотой [20].
Заключение. Наше первое пилотное исследование показало, что Ангиовит с содержащейся в нем фолиевой кислотой в составе комплексной терапии статистически значимо снижает уровень гипергомоцистеинемии в острый период заболевания COVID-19 и способствует нормализации клинико-лабораторных показателей, в частности, ускоряя нормализацию уровня ДД. Дальнейшие исследования на большем числе больных необходимы для определения места этого препарата в лечении и профилактике COVID-19.
Заявление о конфликте интересов/Conflict of Interest Statement
Исследование не имело спонсорской поддержки. Конфликт интересов отсутствует. Авторы несут полную ответствен- ность за предоставление окончательной версии рукописи в печать. Все авторы принимали участие в разработке концепции статьи и написании рукописи. Окончательная версия рукописи была одобрена всеми авторами.
The investigation has not been sponsored. There are no conflicts of interest. The authors are solely responsible for submitting the final version of the manuscript for publication. All the authors have participated in developing the concept of the article and in writing the manuscript. The final version of the manuscript has been approved by all the authors.
Статья впервые опубликована: Неврология, нейропсихиатрия, психосоматика. 2020;12(3):82–86
https://nnp.ima-press.net/nnp/article/view/1363/1054
.
Информация с rmj.ru