Статья посвящена современным аспектам терапии острых респираторных вирусных инфекций.
Введение
Острые респираторные вирусные инфекции (ОРВИ) являются самой распространенной формой острых заболеваний, составляющих в РФ 80–90% от всех регистрируемых инфекций. Не менее 1 раза в год болеет практически каждый житель страны [1]. Причинами этого являются высокая контагиозность возбудителей, разнообразие их видового состава (рис. 1) (известно более 200 вирусов — возбудителей ОРВИ, образующих различные группы (вирусы парагриппа, гриппа, аденовирусы, риновирусы, энтеровирусы и т. д.) при генетической лабильности многих возбудителей, приводящей к постоянному образованию новых штаммов [1]. Способствовать хронизации процесса, затяжному и/или осложненному течению заболевания могут также представители семейства Herpesviridae [2]. Одновременное коинфицирование несколькими возбудителями приводит к более тяжелому течению заболевания (рис. 2).![Рис. 1. Частота выделения возбудителя у детей с ОРВИ при моно- и коинфицировании (2013–2017) [3] Рис. 1. Частота выделения возбудителя у детей с ОРВИ при моно- и коинфицировании (2013–2017) [3]](https://medblog.su/wp-content/uploads/2020/10/ostrye-respiratornye-virusnye-infektsii-aktualnyj-vzglyad-na-problemu-i-sovremennyj-podhod-k-lecheniyu-belan-e-b-sadchikova-t-l.png)
![Рис. 2. Тяжесть риновирусной инфекции при моно- и коинфицировании [6] Рис. 2. Тяжесть риновирусной инфекции при моно- и коинфицировании [6]](https://medblog.su/wp-content/uploads/2020/10/1601619261_73_ostrye-respiratornye-virusnye-infektsii-aktualnyj-vzglyad-na-problemu-i-sovremennyj-podhod-k-lecheniyu-belan-e-b-sadchikova-t-l.png)
Классификация
Для различных форм ОРВИ предусмотрены следующие коды в МКБ-10:
J00 Острый назофарингит
J02 Острый фарингит
J04 Острый ларингит и трахеит
J04.0 Острый ларингит
J04.1 Острый трахеит
J04.2 Острый ларинготрахеит
J06 Острые инфекции дыхательных путей множественной и неуточненной локализации
J06.0 Острый ларинготрахеит
J06.9 Острая инфекция верхних дыхательных путей неуточненная
Особые проблемы — отсутствие средств этиотропной терапии для большинства возбудителей или резистентность к имеющимся средствам, высокая частота вирусно-бактериальных ассоциаций, сопровождающихся более тяжелыми формами заболевания. По данным О. Kurskaya et al. [3], частота вирусных ассоциаций у госпитализированных больных составляла до 30%.
Несмотря на то, что заболевание в большинстве случаев носит саморазрешающийся характер, непосредственной причиной смерти обычно является развитие на фоне респираторной вирусной инфекции тяжелых осложнений (пневмонии, бронхита, синусита, острого среднего отита, энцефалопатии, бронхиальной астмы, многочисленных сердечно-сосудистых и обменных нарушений) [4, 5].
Особенности течения
Инкубационный период большинства ОРВИ составляет 2–7 дней. Максимальное выделение вируса происходит на 3-й день после заражения (этот же период характеризуется и наиболее выраженными симптомами), резко снижается к 5-му дню заболевания (появляется вирусспецифический IgM), хотя у некоторых больных вирус может выделяться до 2 нед. (до достижения титра вирусспецифических IgG, достаточного для элиминации возбудителя) [7].
Основным симптомокомплексом при ОРВИ является катаральное воспаление дыхательных путей. Вместе с тем развитие симптомов является не столько следствием повреждающего действия возбудителя в отношении эпителиальных клеток, сколько результатом их десквамации и реакции иммунной системы, прежде всего факторов врожденного иммунитета. Синтез провоспалительных цитокинов (IL-1, IL-6, IL-8 и др.) способствует развитию пирогенной реакции при инфекционных болезнях, индуцирует системную и локальную воспалительные реакции. Повышение проницаемости сосудов слизистой дыхательных путей при ОРВИ связано с гиперсекрецией слизи, исчезновение прозрачности назального секрета и возможное появление желтоватого или зеленоватого оттенка — с миграцией активированных лейкоцитов в очаг реакции. Подобные симптомы необязательно свидетельствуют о присоединении бактериальной инфекции и необходимости назначения антибиотиков [7]. Несмотря на участие иммунных механизмов в развитии клинических симптомов ОРВИ, их следует рассматривать в качестве патогенетического, но не патогенного фактора, необходимо обеспечить нормальное функционирование иммунной системы при заболевании.
Диагностика ОРВИ базируется на клинико-эпидемиологических данных, результатах инструментального и лабораторного обследования [5, 7].
Несмотря на сходство клинических проявлений ОРВИ различной этиологии, существуют особенности клинических проявлений гриппа, респираторно-синцитиальной вирусной инфекции (РСВ) и т. д. (табл. 1) [8].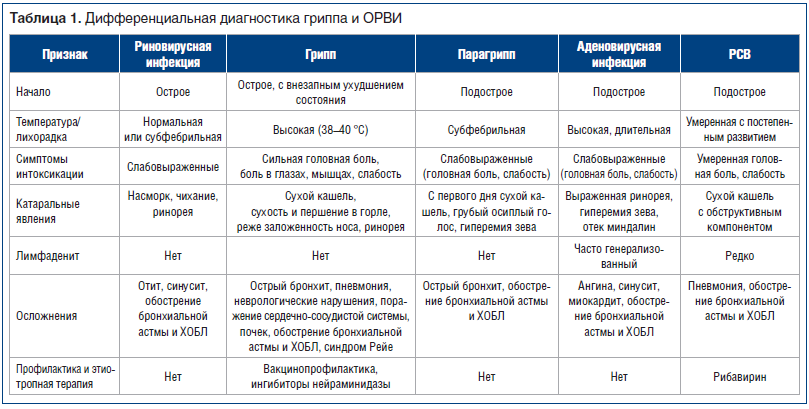
Методы исследования
Целью лабораторного обследования при ОРВИ является обнаружение бактериальных очагов, не определяемых клиническими методами, у детей, а у взрослых — приведшей к ухудшению течения коморбидной патологии.
Клинический анализ крови у взрослых относится к обязательным методам исследования (типичны нормоцитоз и ускорение СОЭ), у детей целесообразен только при выраженных общих симптомах с лихорадкой [5, 7].
Клинический анализ мочи у взрослых является обязательным методом исследования (при неосложненном течении ОРВИ не должно быть изменений), у детей — рекомендуется проводить при наличии лихорадки без катаральных явлений [5, 7].
Определение уровня С-реактивного белка (СРБ) рекомендовано для исключения тяжелой бактериальной инфекции у детей с фебрильной лихорадкой (повышение температуры выше 38 °С), особенно при отсутствии видимого очага инфекции (вероятность 85% при уровне СРБ >30–40 мг/л) [7].
Плановые вирусологическое и бактериологическое исследования в настоящее время не рекомендуются, поскольку они требуют дополнительных визитов в лечебно-профилактическое учреждение, сопряжены с дополнительными затратами, часто не дают немедленного ответа, а результаты не влияют на выбор тактики лечения больных. Исключение составляют экспресс-тесты на грипп у пациентов с высокой лихорадкой и на стрептококк при подозрении на острый стрептококковый тонзиллит.
Инструментальные исследования (рентгенография органов грудной клетки при подозрении на пневмонию; рентгенография придаточных пазух носа при подозрении на развитие синусита; ЭКГ при наличии кардиальных симптомов) при неосложненном течении не проводят. Детям с симптомами острого ринофарингита не рекомендуется проводить рентгенографию пазух носа в первые 12 дней болезни. У взрослых консультация врача-оториноларинголога показана при подозрении на развитие синусита или отита, детям отоскопия рекомендована во всех случаях ОРВИ. При тяжелом/среднетяжелом течении или отказе от госпитализации рекомендована консультация врача-инфекциониста.
Лечение
Несмотря на то, что ОРВИ могут существенно ухудшать качество жизни, пациентов следует информировать о доброкачественности течения заболевания в большинстве случаев и необходимости избегать полипрагмазии.
Этиотропную терапию ОРВИ проводить сложно ввиду отсутствия средств, влияющих на репродуктивный цикл многих возбудителей. К настоящему времени наиболее широкий спектр препаратов имеется для лечения гриппа (ингибиторы нейраминидазы, производные адамантана, умифеновир). Наиболее целесообразно использование ингибиторов нейраминидазы (в РФ зарегистрированы осельтамивир и занамивир), которые максимально эффективны при раннем назначении (желательно в первые часы заболевания).
Производные адамантана (римантадин, адамантан) на протяжении многих лет были препаратами выбора для профилактики и лечения гриппа А [9]. Механизм противовирусного действия средств данной группы связан с ингибированием М2-протеина, в результате чего нарушается высвобождение рибонуклеопротеида в процессе репликации вируса в клетке хозяина. Римантадин и адамантан в последние годы не рекомендованы в качестве препаратов выбора при лечении гриппа в связи с развитием резистентности возбудителя к препаратам данной группы [10]. Так, вирус, циркулировавший в США в сезон 2005–2006 гг. (H3N5), в 92,3% случаев имел мутации в гене М2, в результате чего наблюдалось снижение (или потеря) чувствительности вируса гриппа к адамантанам [11, 12].
Противовирусное действие умифеновира заключается в том, что он подавляет слияние липидной оболочки вируса с клеточной мембраной, специфически ингибирует вирусы гриппа А и В [9].
По данным фармакоэкономического исследования в Австралии, стоимость 5-дневного курса терапии дженериками амантадина составляет 13 долл., аналогичный курс лечения пероральным осельтамивиром (75 мг 2 р./сут) — около 53 долл., ингаляционным занамивиром (10 мг 2 р./сут) — 45 долл. [13]. Вакцинация против гриппа и терапия ингибиторами нейраминидазы в настоящее время сопоставимы по экономическим затратам, однако с учетом низкой реактогенности современных вакцин приоритетным направлением в профилактике гриппа должна оставаться специфическая иммунизация пациентов [9]. Тем не менее она не всегда позволяет достичь желаемого уровня контроля заболеваемости гриппом вследствие отказа части населения от вакцинации, ее неэффективности у части пациентов, а также возможного несовпадения антигенной структуры циркулирующего штамма и штамма, использованного при производстве вакцины. Химиопрофилактика и химиотерапия не являются альтернативой вакцинации и не влияют на ее эффективность. При развившемся заболевании противовирусные препараты являются средством этиотропной терапии, и их необходимо включать в комплексную терапию.
Многие вирусы, в т. ч. и некоторые новые высокопатогенные штаммы гриппа, обладают способностью подавлять выработку интерферонов, что может приводить к снижению иммунного ответа и развитию тяжелых форм заболевания, сопровождающегося бактериальными осложнениями. Поэтому необходимо рассматривать целесообразность включения в терапевтический комплекс препаратов интерферона или его индукторов [5, 14, 15].
В целом в настоящее время заболеваемость и течение респираторных инфекций рассматривают в неотрывной связи с состоянием иммунной системы пациента [16, 17], а различные варианты иммунотропной терапии — в качестве патогенетического лечения при инфекционных заболеваниях дыхательных путей [16–18]. В частности, экспертами Cochrane Collaboration показано, что иммуностимулирующая терапия на 40% снижает количество эпизодов респираторных инфекций у восприимчивых к ним детей [18, 19].
Дискутабельным является вопрос о целесообразности назначения при ОРВИ препаратов цинка, витамина D3, фитопрепаратов, гомеопатических средств и т. д., относящихся к категории средств с недоказанной эффективностью (что не является эквивалентом доказанной неэффективности) [20, 21].
В настоящее время отсутствуют исчерпывающие объяснения механизма действия препаратов, применяемых в так называемой комплементарной медицине, однако их повсеместное массовое применение в последние годы требует проведения серьезных исследований с соблюдением методологии, принятой в клинических исследованиях аллопатических средств.
Одной из таких работ является международное многоцентровое контролируемое исследование по оценке эффективности включения в комплексную терапию ОРВИ гомеопатических средств, проведенное M. Thinesse-Mallwitz et al. (2015). В исследуемую группу вошли 523 больных в возрасте от 1 года до 65 лет (265 — основная группа и 258 — группа сравнения). Результаты достоверно продемонстрировали (p
Аналогичные данные были показаны в неинтервенционном открытом рандомизированном контролируемом обсервационном исследовании эффективности и безопасности препарата Афлубин® в симптоматической терапии ОРВИ в параллельных группах. Афлубин® является гомеопатическим комбинированным препаратом, содержащим пять гомеопатических разведений растительной и (в одном случае) минеральной природы, изготовленных в соответствии с технологией, описанной в Европейской и Гомеопатической фармакопее Германии. Лекарственный препарат представлен в виде таблеток подъязычных, в состав которых входят: горечавка желтая (Gentiana) D1; аконит аптечный (Aconitum) D6; бриония двудомная (Bryonia) D6; железа фосфат (Ferrum phosphoricum) D12; молочная кислота (Acidum sarcolacticum) D12.
132 пациента (мужчины и женщины, возраст — от 18 до 75 лет) с диагнозом ОРВИ (в т. ч. грипп) были рандомизированно разделены на 2 группы по 66 человек в каждой. Пациенты группы сравнения получали только стандартную терапию, пациентам основной группы дополнительно назначали терапию препаратом Афлубин®, таблетки подъязычные гомеопатические. В ходе исследования планировалось 5 визитов — в 1 (скрининг и начало терапии), 3, 5, 7 (окончание терапии) и 10-й день (оценка эффективности и безопасности терапии).
В качестве первичной контрольной точки рассматривали определение скорости регрессии клинических симптомов:
общие клинические симптомы (лихорадка, озноб, общее недомогание, головная боль / головокружение, мышечная/суставная боль);
местные клинические симптомы (затруднение носового дыхания, чихание, боль в горле, насморк, кашель);
лабораторные показатели (лейкоцитарная формула, СОЭ).
Одним из важных симптомов ОРВИ, существенно снижающих качество жизни больных, является нарушение носового дыхания. В данном исследовании на завершающем этапе (визит 5) различия между группами по рассматриваемому показателю были статистически значимы (p®, на этапе визита 5 затруднения носового дыхания отсутствовали (0 баллов у 100% пациентов), тогда как в группе сравнения данный симптом был выявлен у 9,09% пациентов.
Статистически достоверно (p®, падало уже на 2-й день лечения, и с 3-го дня терапии у пациентов основной группы регистрировалась только субфебрильная температура (37,20 [36,90; 37,40] °C).
Частота и выраженность головокружения были сопоставимыми между группами в начале и конце периода наблюдения, однако уже на начальных этапах в основной группе имела место достоверно (p
Динамика головной боли была сопоставимой между группами, однако следует отметить, что в основной группе к концу исследования она не регистрировалась ни у одного пациента, а в группе сравнения сохранялась у 4,6% больных. Частота и выраженность мышечных болей при ОРВИ и их динамика к визиту 5 были сопоставимыми между группами, однако со 2-го дня их интенсивность в группе сравнения достоверно (p®. Несмотря на отсутствие достоверных различий между группами по частоте и выраженности миалгий, у получавших Афлубин® они к 5-му дню не регистрировались ни в одном случае, в то время как в группе сравнения имели место у 4,55% [23].
Таким образом, полученные данные позволяют сделать вывод о некотором ускорении регрессии симптомов ОРВИ и уменьшении степени выраженности интоксикационного синдрома при включении в базисную терапию гриппа и ОРВИ гомеопатического препарата Афлубин®. Одновременно происходит уменьшение выраженности катарального синдрома, который также регрессирует на 2 дня раньше, чем при проведении общепринятой терапии больных ОРВИ. Афлубин® сочетается с препаратами других фармакологических групп, а в качестве средства для монотерапии рекомендуется при легком и среднетяжелом течении ОРВИ.
Профилактика ОРВИ должна включать вакцинацию против возможных возбудителей заболевания (вирус гриппа) и его осложнений (пневмококк), в остальных случаях основной акцент необходимо делать на неспецифических превентивных мероприятиях. Фармакотерапевтический комплекс при ОРВИ должен быть минимизирован и формироваться на основе средств с доказанной эффективностью. В отношении остальных групп препаратов целесообразно провести качественные исследования, по результатам которых должно быть определено их возможное место (или его отсутствие) в существующей программе помощи больным ОРВИ.
.
Информация с rmj.ru





