Введение
Заболевания суставно-мышечной системы имеют широкую распространенность в популяции, часто приводят к временной или стойкой утрате трудоспособности, связаны со значительными материальными затратами на ведение пациентов [1, 2]. На сегодняшний день установлен целый ряд факторов риска поражения суставов, однако мероприятия по их коррекции недостаточно эффективны, требуется проведение длительной медикаментозной терапии и, нередко, оперативного лечения [3]. Наличие широкого спектра сопутствующей патологии, с одной стороны, ухудшает течение суставно-мышечных заболеваний, с другой — повышает лекарственную нагрузку на организм и риск развития лекарственных взаимодействий [4, 5].
Одна из ведущих проблем современной медицины — дорсалгия (синдром боли в нижней части спины), которая является одной из наиболее распространенных жалоб пациентов на приеме у невролога, терапевта, ревматолога, врача общей практики, ортопеда-травматолога и представляет собой междисциплинарную проблему. Дорсалгия — одна из наиболее частых причин увеличения числа лет, прожитых с заболеванием, и снижения качества жизни в большинстве стран, в том числе в России [2, 6].
Дорсалгия обусловлена дисфункцией мышечно-связочного аппарата и дегенеративно-дистрофическими изменениями дугоотростчатых суставов и межпозвонковых дисков. Патологические изменения в значительной степени обусловлены нарушением обмена веществ в хрящевой ткани, в частности деполимеризацией и уменьшением содержания протеогликанов, которые являются ее главными структурными компонентами [7]. Возникают и прогрессируют нарушения васкуляризации межпозвонкового диска, ускоренный катаболизм протеогликанов опережает их синтез, нарушается целостность коллагенового каркаса, что способствует дегенерации межпозвонкового диска и замыкательных пластинок тел позвонков [8]. Вследствие снижения концентрации хондроитина сульфата (ХС) пульпозное ядро утрачивает гидростатические свойства и перестает выполнять амортизирующие функции, что приводит к повышению мощности механических воздействий на фиброзное кольцо и возникновению в нем трещин и разрывов.
Вследствие гибели хондроцитов и клеток синовиальной сумки, накопления продуктов разрушения межклеточного матрикса активируются процессы воспаления в поврежденных структурах позвоночника (дугоотростчатые суставы, межпозвонковый диск, мышцы, сухожилия, связки). Выраженность и прогрессирование дегенеративного поражения тканей также обусловлены включением механизмов запрограммированной клеточной гибели (пироптоз, апоптоз, ферроптоз), активацией процессов образования свободных радикалов, поддержания хронического воспаления [9, 10]. Одним из следствий указанных процессов является активация процессов нейропластичности с арборизацией отростков чувствительных нейронов и образованием новых болевых рецепторов в области воспаления [11].
Постоянный приток болевой импульсации приводит к изменению деятельности заднего рога спинного мозга, постепенно утрачивающего способность блокировать прохождение сигналов от болевых рецепторов. В последующем, при длительном персистировании болевого синдрома, наблюдается структурно-функциональная перестройка подкорковых и корковых систем анализа и восприятия болевых сигналов, что создает основу для развития хронического болевого синдрома, который может приобретать характеристики нейропатического [12].
С учетом этого консервативное лечение неспецифической скелетно-мышечной боли должно включать препараты, которые не только купируют боль, но и тормозят воспалительные процессы и дегенеративные изменения основных компонентов фиброзного кольца и пульпозного ядра и тем самым предупреждают прогрессирование дегенеративно-дистрофических изменений в хрящевой ткани [6, 13]. В этой связи исключительный интерес представляют препараты замедленного действия симптоматической терапии остеоартрита (ОА) (англ.: Symptomatic Slow Acting Drugs for OsteoArthritis, SYSADOA), которые ранее широко применялись в ревматологии и нейрологии, при этом основным механизмом их действия считалась способность предупреждать прогрессирующее поражение хрящевой ткани, вследствие чего они рассматривались исключительно как хондропротекторы [14, 15].
Современные исследования значительно расширили представления о механизмах действия препаратов SYSADOA. Было установлено, что их клинический эффект связан со стимуляцией хондроцитов, угнетением процессов хронического воспаления низкой интенсивности, снижением активности лизосомальных ферментов (матриксных металлопротеиназ), медиаторов воспаления, индукторов апоптоза хондроцитов, увеличением резистентности хондроцитов к воздействию провоспалительных цитокинов, активацией анаболических процессов в матриксе хряща и созданием предпосылок для формирования устойчивого хряща [16, 17]. Данные свойства препаратов SYSADOA представляются исключительно важными, учитывая доказанную роль воспалительного компонента в патогенезе различных форм дорсалгии [18, 19].
Одним из хондропротекторов с обширной доказательной базой является глюкозамин, который оказывает влияние на экспрессию генов в хрящевой ткани, обладает антикатаболической активностью, уменьшает продукцию простагландина E2, препятствует активации сигнального пути ядерного фактора κB [20]. Глюкозамин входит в состав матрикса хрящевой ткани, участвует в синтезе клеточной мембраны, коллагена и костного матрикса, а также в синтезе гликолипидов, гликопротеинов, гликозаминогликанов, суставных протеогликанов, муцина и гиалуроновой кислоты. Глюкозамин in vitro ингибирует внутриклеточный каскад сигнальных цитокинов в хондроцитах, стимулирует синтез протеогликанов, ингибирует их деградацию и стимулирует регенерацию хряща после экспериментально вызванных повреждений [20]. Установлено, что длительное введение глюкозамина сульфата (ГС) уменьшает разрушение хряща и экспрессию матриксных металлопротеиназ и матричной РНК (мРНК) в моделях in vitro [21].
Хондроитина сульфат (ХС) обеспечивает восстановление нормального метаболизма костной и хрящевой ткани, торможение процессов воспаления, предупреждение оксидативного поражения плазменной мембраны, уменьшение активности циклооксигеназы 2-го типа и подавление экспрессии простагландина E2 [22]. Противовоспалительный эффект ХС обусловлен подавлением клеточного компонента воспаления. ХС способствует активизации синтеза гиалуроновой кислоты и протеогликанов на фоне угнетения их катаболизма [23].
Установлено выраженное симптом-модифицирующее действие ГС и ХС, позволяющее добиться уменьшения интенсивности болевого синдрома и улучшения функций сустава, при этом большинство исследований было посвящено возможности применения указанной комбинации препаратов при патологии крупных суставов (коленного, тазобедренного) [24–26]. Результаты метаанализа ряда рандомизированных плацебо-контролируемых исследований продемонстрировали клиническую эффективность и хорошую переносимость SYSADOA при дегенеративно-дистрофических заболеваниях суставов, наличие у них выраженных противоболевого и противовоспалительного эффектов [25, 26]. Показана эффективность парентерального введения ХС и ГС при хронической суставной боли и дорсалгии в условиях реальной клинической практики [26]. В открытом сравнительном клиническом исследовании с применением интермиттирующей схемы введения ХС и ГС в течение 6 нед. группе из 70 пациентов с распространенным ОА было показано, что применение в комплексном лечении SYSADOA позволило добиться обезболивания у 91,4% пациентов, тогда как монотерапия нестероидными противовоспалительными препаратами (НПВП) обеспечила эффективное обезболивание только у 62,9% больных.
Следует отметить, что сведений о возможности применения препаратов SYSADOA у пациентов с дорсалгией значительно меньше, лишь единичные исследования посвящены изучению данной проблемы [27, 28]. Результаты экспериментальных исследований, а также значительный клинический опыт применения позволили установить высокую эффективность препаратов Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг® при лечении пациентов с суставной патологией [29].
Исходя из этого, было предпринято настоящее исследование, цель которого — оценить клиническую эффективность и переносимость инъекционной терапии препаратами Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг® у пациентов с ОА различной локализации.
Содержание статьи
Материал и методы
Дизайн исследования. В наблюдательное проспективное неинтервенционное исследование-программу «ХондроЭффект» были включены пациенты с первичным или вторичным ОА различной локализации. У всех пациентов имелась дорсалгия, которая сочеталась с болевыми скелетно-мышечными синдромами другой локализации.
Критерии включения в исследование: мужчины и женщины с достоверным диагнозом ОА (I–III рентгенологических стадий по Kellgren и Lawrence); возраст от 18 до 70 лет включительно; интенсивность боли >40 мм по ВАШ в анализируемом (целевом) суставе; назначение одного из препаратов: Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг®; подписанное информированное согласие на участие в исследовании и использование медицинских данных в обезличенном виде для научных целей.
Критерии невключения в исследование: внутрисуставное введение любых препаратов в течение 6 нед. до начала исследования и потребность в их введении (в т. ч. синовит); непереносимость компонентов исследуемого препарата (в т. ч. лидокаина); прием медленно действующих препаратов для лечения ОА (SYSADOA, хондропротекторы) в течение 4 мес., предшествующих исследованию; хроническая сердечная недостаточность, нарушение сердечной проводимости, мерцательная аритмия, артериальная гипотония; эпилепсия; тяжелые нарушения функции печени и почек; бронхиальная астма; некомпенсированный сахарный диабет; сопутствующий прием глюкокортикостероидов; отказ от подписания информированного согласия на участие в исследовании.
Критерии исключения из исследования: решение пациента прекратить участие в исследовании и отзыв информированного согласия; решение исследователя из-за возникновения у пациента нежелательной реакции (НР), требующей медикаментозного вмешательства или отмены/смены проводимого лечения, либо развитие состояния, требующего применения лекарственного препарата, не разрешенного к одновременному применению с препаратами Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг® в соответствии с инструкцией по их медицинскому применению.
Препараты Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг® назначали исходя из клинической картины ОА, результатов клинического обследования и соотношения потенциальной пользы и риска для пациентов. Препараты назначали в строгом соответствии показаниям к применению в инструкции по медицинскому применению лекарственных препаратов.
Готовность пациента принимать участие в наблюдательной программе не оказывала влияния на решение лечащего врача о назначении того или иного препарата. Назначение терапии проводилось следующим образом (один из нижеперечисленных режимов):
препарат Эльбона® (р-р А + р-р Б) внутримышечно в одном шприце трижды в неделю через день (например: понедельник, среда, пятница) в течение 6 нед.;
препарат Сусталонг® вводился внутримышечно в одном шприце трижды в неделю (по аналогичной схеме) в течение 6 нед.;
препарат ЭЛТУФЛОП® БИО вводился внутримышечно по 2 мл через день, всего 10 инъекций.
В соответствии с протоколом были предусмотрены два визита:
Визит 1: оценка соответствия критериям включения/невключения, оценка клинического состояния (в т. ч. по визуально-аналоговой шкале, ВАШ), характера сопутствующей разрешенной терапии (какой препарат назначен, тип применяемого НПВП), антропометрических параметров (рост, масса тела), подписание информированного согласия.
Визит 2: после окончания курса терапии (зависел от характера проводимой терапии и продолжительности курса лечения) — оценка клинического состояния (в т. ч. по ВАШ), потребности в дополнительном приеме НПВП), регистрация НР, определение их тяжести и возможной связи с проводимой терапией.
Критерии оценки эффективности терапии:
динамика болевого синдрома по ВАШ. В соответствии с результатами оценки по ВАШ, выделяли следующие категории болевого синдрома: 0 — боль отсутствует; 1–3 см — легкая боль; 4–5 см — умеренная непостоянная боль; 6–7 см — умеренная постоянная боль; 8–9 см — сильная боль; 10 см — невыносимая боль.
На визите 2 — эффекты терапии по следующим категориям: эффект от лечения сохранился; эффект от лечения усилился; эффект от лечения уменьшился.
На визите 2 — потребность в приеме НПВП по следующим категориям: потребность в приеме сохраняется; потребность в приеме увеличилась; потребность в приеме уменьшилась.
Частота и характер НР, связанных с применением в/м инъекционных форм Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг®.
Всего анализу подвергнуты результаты обследования 495 пациентов из 14 городов различных субъектов Российской Федерации, которые находились под наблюдением 55 специалистов различного профиля (неврологи, ревматологи, хирурги, травматологи-ортопеды, врачи общей практики). У 182 пациентов имелся гонартроз, у 159 — коксартроз I–III стадии, у 154 — поражение мелких суставов кисти, у 198 (40%) пациентов имел место сочетанный ОА нескольких суставов, в том числе проявлявшийся дорсалгией. Средний возраст включенных в исследование пациентов — 57,6±10,1 года, из них 205 (41,4%) мужчин и 290 (58,6%) женщин. Пациенты 1-й группы (n=167) получали препарат Эльбона®, 2-й группы (n=175) — Сусталонг®, 3-й группы (n=153) — ЭЛТУФЛОП® БИО. Существенных отличий представленности поражения различных суставов в группах исследования не было.
Статистический анализ. Размер выборки был рассчитан в соответствии с требуемым доверительным интервалом 95% для первичной переменной — доли пациентов со снижением интенсивности боли по ВАШ на визите 2 на фоне лечения в реальной клинической практике. Было рассчитано, что для достижения цели исследования необходимо провести анализ результатов обследования 495 пациентов. Для определения соответствия распределения данных нормальному использовали критерий Колмогорова — Смирнова. Показатели с нормальным распределением представлены в виде среднего и стандартного отклонения (M±m), показатели, распределение которых отлично от нормального, — в виде медианы и верхнего и нижнего квартилей (Me [Q1; Q3]). Качественные признаки представлены в виде абсолютных значений и доли (n (%)). Для сравнения количественных признаков в независимых группах применяли критерий Манна — Уитни, для сравнения признаков в зависимых группах — критерии Уилкоксона и Мак-Немара. Для анализа различий частот признаков в группах применяли критерий χ2. Для статистического анализа использовали пакеты для статистической обработки и визуализации данных: numpy, scipy, а также MS Office Excele и R version 4.4.1.
Результаты исследования
Исходный характер жалоб наблюдавшихся больных представлен в таблице 1. У пациентов 1-й и 2-й групп наблюдалось статистически значимое преобладание жалоб на затруднение/ограничение движений в суставах при движении (p<0,05), тогда как у больных 3-й группы статистически значимо преобладали жалобы на хруст в суставах при движении и умеренной интенсивности периодические боли после значительной физической нагрузки (p<0,05).

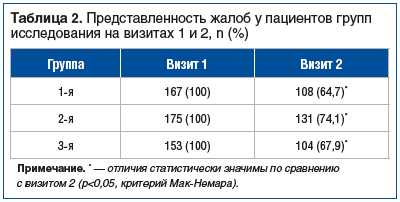
На фоне проведенного лечения во всех группах имело место уменьшение числа пациентов, предъявляющих жалобы (табл. 2), при этом отличия носили статистически значимый характер по сравнению с исходным уровнем.
На визите 2 у пациентов всех 3 групп имело место значительное уменьшение выраженности имеющихся жалоб, которые, если и сохранялись, то были статистически значимо менее выражены по сравнению с исходным уровнем (p<0,05, табл. 3).

На визите 2 болевой синдром отсутствовал у 15 (9,0%) пациентов 1-й группы, у 14 (8,0%) — 2-й и у 16 (10,5%) — 3-й группы.
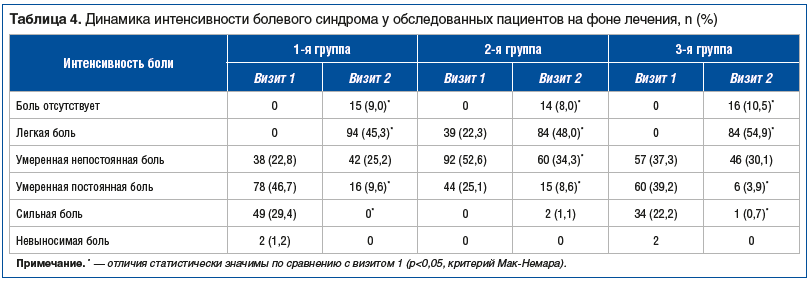
На фоне проведенной терапии во всех группах была зарегистрирована сопоставимая динамика — статистически значимо уменьшилось число пациентов с эпизодической или постоянной умеренной интенсивности болью (p<0,05), притом что также статистически значимо увеличилось число больных, у которых боль значительно уменьшилась или исчезла вовсе (p<0,05) (табл. 4).
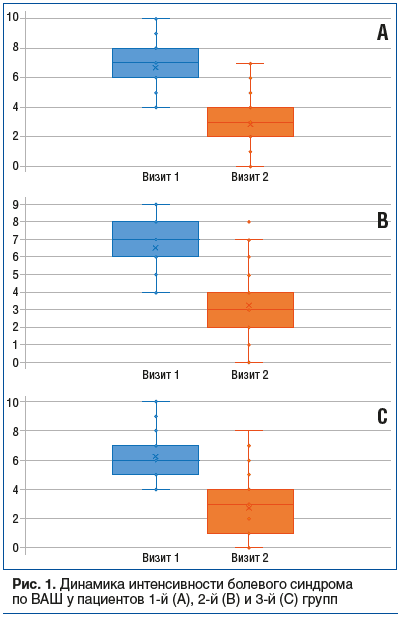
Результаты количественной оценки интенсивности болевого синдрома по ВАШ позволили установить, что во всех группах имело место уменьшение ее интенсивности на визите 2 по сравнению с визитом 1 (рис. 1). Все отличия носили статистически значимый характер по сравнению с исходным уровнем (p<0,05).
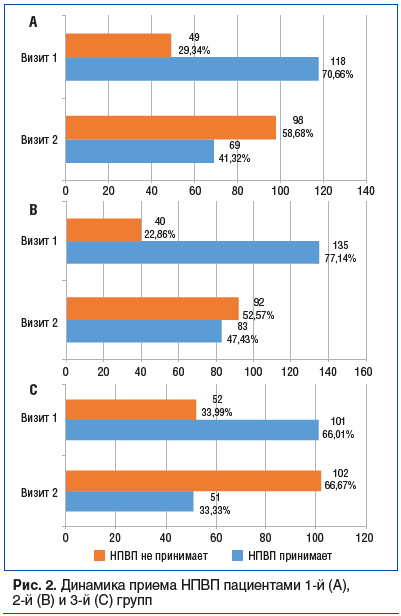
В результате проведенного лечения во всех группах больных статистически значимо уменьшилось число пациентов, которым требовался дополнительный прием НПВП (рис. 2). Отличия во всех группах носили статистически значимый характер (p<0,05, критерий Мак-Немара).
Период времени, необходимый для наступления стойкого противоболевого эффекта терапии и уменьшения / полного прекращения приема НПВП, у пациентов 1-й группы составил 30,0 [28,0; 32,0] сут, 2-й группы — 30,0 [28,0; 32,0] сут, 3-й группы — 38,0 [27,0; 31,0] сут. Статистически значимые отличия скорости наступления клинического эффекта между 1-й и 2-й группами отсутствовали, притом что эффект наступал статистически значимо позже у пациентов 3-й группы по сравнению с 1-й и 2-й группами (p=0,04 и p<0,01 соответственно, критерий Манна — Уитни).
При анализе частоты НР, возникших на фоне проводимой терапии, оказалось, что она была практически равной во всех группах исследования (табл. 5). Наиболее частыми НР были локальная болезненность и гиперемия в месте введения препарата. Изменения режима приема препаратов или дополнительных врачебных назначений указанные НР не потребовали. Статистически значимых отличий между группами частоты развития НР выявлено не было (p=0,54, критерий χ2). Серьезных НР в ходе проведенного исследования выявлено не было.

Обсуждение
Результаты проведенного исследования свидетельствуют о том, что препараты Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг® продемонстрировали высокую эффективность при применении в условиях реальной клинической практики. Результаты настоящего исследования подтверждают данные, полученные в результате экспериментальных исследований [29]. Назначение указанных препаратов пациентам с ОА различных суставов, проведенное в трех сопоставимых по основным клинико-демографическим показателям группах, продемонстрировало свою высокую эффективность. Назначение каждого из трех препаратов сопровождалось снижением интенсивности болевого синдрома, о чем свидетельствовало статистически значимое уменьшение значений по ВАШ по сравнению с исходным уровнем, а также статистически значимое снижение потребности в дополнительном использовании НПВП. Существенных отличий эффективности трех препаратов по рассматриваемым показателям отмечено не было, однако применение препарата Сусталонг® приводило к несколько более позднему наступлению клинического эффекта, о чем свидетельствовало более позднее уменьшение потребности в дополнительном приеме НПВП.
Применение препаратов Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг® характеризовалось хорошей переносимостью. НР в процессе лечения возникали редко, носили преимущественно легкий характер и не требовали прекращения лечения или дополнительных лекарственных назначений. В процессе проведения исследования не было зарегистрировано ни одного случая лекарственных взаимодействий.
Заключение
Результаты проведенного исследования продемонстрировали эффективность препаратов Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг® у пациентов со скелетно-мышечными болевыми синдромами, в том числе с дорсалгией. Ограничениями исследований являются его открытый характер и отсутствие плацебо-контроля. Вместе с тем результаты, полученные при наблюдении за репрезентативной группой пациентов в условиях реальной клинической практики, представляются важными и имеющими значительную ценность, они свидетельствуют о достаточной эффективности и хорошей переносимости препаратов Эльбона®, ЭЛТУФЛОП®БИО и Сусталонг® и позволяют рекомендовать их применение у пациентов с патологией суставов.
Источник финансирования: исследование проведено при поддержке компании «ЭЛЛАРА» (Россия).
Информация с rmj.ru






