Ключевые слова: когнитивные расстройства, умеренные когнитивные нарушения, деменция, биомаркеры, нейропсихологическое тестирование, шкалы.
Для цитирования: Ткачева О.Н., Чердак М.А., Мхитарян Э.А. Обследование пациентов с когнитивными нарушениями // РМЖ. 2017. №25. С. 1880-1883
Tkacheva O.N.1, Cherdak M.A.1, Mkhitaryan E.A.1,2
1 Russian gerontological scientific and clinical center, Moscow
2 First Moscow State Medical University named after I.M. Sechenov
Cognitive functions impairment is a frequent impairment in elderly and senile people. The most severe form of cognitive impairment (CI) is dementia, which disrupts the patient’s professional, daily and social activity. The CI is characterized by a frequent combination with non-cognitive disorders — emotional affective and behavioral disorders, which can distort the clinical picture of the disease and cause choosing a wrong treatment for the patient. Diagnosis and determination of the etiology of the CI at the pre-existing stage are crucial for the timely initiation of therapy in order to prolong the period with a higher level of functioning, which not only facilitates the patient’s own life, but also reduces the burden on carers, as well as the socioeconomic burden for the whole society. The article discusses modern approaches to CI classification, issues of their etiology, presents clinical and paraclinic methods of CI diagnosis, and suggests an algorithm for examining patients with possible CI.
Key words: cognitive disorders, mild cognitive impairment, dementia, biomarkers, neuropsychological testing, scales.
Fot citation: Tkacheva O.N., Cherdak M.A., Mkhitaryan E.A. Examination of patients with cognitive impairments // RMJ. 2017. № 25. P. 1880–1883.
В статье обсуждаются современные подходы к классификации когнитивных нарушений, вопросы их этиологии, методы диагностики, а также предложен алгоритм обследования пациентов с возможными когнитивными нарушениями.
Под термином «когнитивные» (познавательные), как правило, подразумеваются наиболее сложные функции головного мозга, участвующие в процессе рационального познания мира [1, 2]. К когнитивным функциям относится память (способность запечатлевать, сохранять и многократно воспроизводить нужную информацию), речь (способность к вербальной коммуникации как в устной, так и в письменной форме), праксис (способность приобретать, сохранять и использовать какие-либо двигательные навыки), гнозис (способность распознавать и интегрировать чувствительные образы различных модальностей), а также управляющие функции (способность контролировать свою познавательную деятельность и поведение). К управляющим (регуляторным, исполнительным) функциям тесно примыкает понятие «интеллект», суть которого в узком смысле заключается в способности к вынесению суждений и логических умозаключений. Нередко в качестве самостоятельной функции также выделяют внимание, произвольное и непроизвольное.
Нарушение когнитивных функций относится к частым расстройствам у лиц пожилого и старческого возраста. По мере старения распространенность когнитивных расстройств (КР) существенно нарастает от 13–22% среди лиц в возрасте 60–69 лет до 43% и выше у лиц старше 85 лет [3, 4]. В последние десятилетия с увеличением продолжительности жизни населения увеличивается количество людей пожилого и старческого возраста, вместе с этим возрастает доля пациентов с деменцией и недементными КР [5].
Деменция (слабоумие) – это тяжелое расстройство когнитивных функций, которое нарушает профессиональную, бытовую и социальную активность пациента. Деменция является одной из ведущих причин формирования зависимости пожилых людей во всем мире, а также оказывает физическое, психологическое, социальное и экономическое воздействие на членов семьи пациентов и общество в целом. Данное состояние вызывает дополнительные трудности для диагностики и лечения сопутствующих заболеваний. Развитие деменции в большинстве случаев представляет долгий процесс и начинается задолго до появления первых клинических признаков [6]. Кроме того, зачастую ранние симптомы деменции или более легких форм когнитивных нарушений, особенно при их развитии у лиц пожилого и старческого возраста, традиционно пытаются объяснять «нормальным» проявлением старения. Все это способствует поздней диагностике КР. В то же время в исследованиях с длительным наблюдением за больными с «нормальным» возрастным снижением когнитивных функций было показано, что с течением времени у большинства из них формируется деменция [7].
Развитию деменции предшествует стадия недементных нарушений, когда наиболее оправданы меры, направленные на сохранение функционального статуса пациента, замедление прогрессирования заболевания [8, 9]. В 2005 г. академиком Н.Н. Яхно была предложена классификация когнитивных нарушений с выделением легкой, умеренной и тяжелой форм [10]. Легкие и умеренные когнитивные нарушения соответствуют недементным нарушениям. Легкие когнитивные нарушения (ЛКН) могут быть констатированы при снижении в одной или нескольких когнитивных сферах исходно более высокого индивидуального уровня, они не влияют на бытовую, профессиональную и социальную деятельность. Считается, что ЛКН могут быть как проявлением физиологического процесса старения, так и наиболее ранней стадией органического церебрального заболевания.
Умеренные когнитивные нарушения (УКН, «mild cognitive impairment») проявляются снижением одной или нескольких когнитивных функций, которые осознаются пациентом и/или заметны окружающим и подтверждаются с помощью объективных методов исследования, но не вызывают профессиональной или бытовой дезадаптации. Диагностические критерии УКН [11] представлены в таблице 1.
Самой частой причиной тяжелых КР в мире является болезнь Альцгеймера (БА) (40–70%), вторыми по распространенности идут сосудистые КР, а также смешанные состояния в виде сочетания сосудистых и нейродегенеративных факторов [12–14]. Деменция – необратимое состояние, но у части пациентов в основе тяжелых когнитивных нарушений лежат потенциально курабельные заболевания, коррекция которых приводит к уменьшению тяжести КР (нормотензивная гидроцефалия, дефицит витамина В12, гипотиреоз, инфекционные заболевания центральной нервной системы). Кроме того, в обсервационном исследовании пациентов после перенесенного инсульта было показано, что полноценная вторичная профилактика инсульта способствовала существенному снижению частоты постинсультных КР [15]. Отдельно следует рассматривать случаи псевдодеменции, которые имитируются наличием сопутствующих тяжелых эмоционально-волевых расстройств (депрессии, апатии).
Диагностика КР включает клинические и параклинические методы, цель которых заключается в определении этиопатогенетической причины КР у конкретного пациента. Учитывая потенциально обратимый характер части заболеваний, приводящих к КР, а также эффективность превентивных мер у лиц с сосудистыми КР, ранняя диагностика и правильный анализ характера и выраженности КР у каждого конкретного пациента имеют первостепенное значение. Это позволяет не только облегчить жизнь самих пациентов и их родственников, но и уменьшить социально-экономическое бремя для общества [16, 17].
Клинические методы диагностики когнитивных нарушений
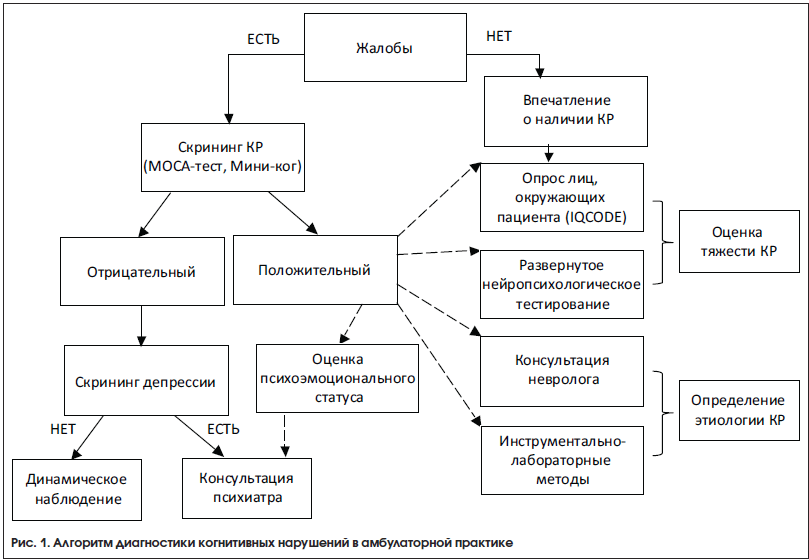
Диагностика состояния когнитивной сферы начинается с оценки жалоб пациента. Как правило, для пациентов с деменцией характерно постепенное снижение критического отношения к своему состоянию, это приводит к отсутствию у них каких-либо жалоб когнитивного характера, либо эти жалобы не коррелируют с тяжестью объективных нарушений и степенью бытовой дезадаптации. Это указывает на важность получения информации о пациенте не только с его слов, но и из дополнительных источников, включая медицинскую документацию и опрос близких пациента или знакомых с ним в течение длительного времени людей, для чего используется опросник IQCODE (Informant Questionnaire on Cognitive Decline in the Elderly) [18]. Данный опросник позволяет, с одной стороны, более объективно оценить динамику когнитивных нарушений с течением времени, с другой стороны, он нашел широкое применение в диагностике КР до и после инсульта [19]. Жалобы на нарушение памяти являются одними из самых распространенных у работоспособных лиц среднего возраста. У части из них даже самое тщательное нейропсихологическое обследование не позволяет выявить каких-либо отклонений от возрастной нормы, в таком случае речь идет о «субъективных когнитивных нарушениях» [20]. У других лиц объективно определяются ЛКН или УКН, часто ассоциированные с тревожно-депрессивными, астеническими состояниями. Показано, что УКН сами по себе не оказывают существенного влияния на повседневную жизнь человека за исключением самых сложных профессиональных функций. Однако динамика УКН с течением времени меняется, установлено, что риск развития деменции через 5 лет после постановки диагноза «УКН» составляет 55–70% [9]. Таким образом, даже при отсутствии тяжелых КР подобные пациенты нуждаются в пристальном динамическом наблюдении.
Клиническая диагностика КР базируется на оценке неврологического, нейропсихологического и психоэмоционального статуса пациента.
Целью неврологического обследования является диагностика неврологических синдромов (двигательных, чувствительных, вегетативных нарушений), характерных для отдельных заболеваний ЦНС, сопровождающихся нарушением когнитивных функций. Особое внимание, с учетом особенностей патогенеза расстройств, следует уделять оценке экстрапирамидных нарушений, нарушений равновесия, походки, тазовых функций. При наличии жалоб на головокружение в числе прочего должны проводиться тесты для исключения ортостатической гипотензии.
Нейропсихологическое обследование подразумевает исследование состояния таких функций, как память, речь, восприятие, праксис, мышление и внимание, с проведением соответствующих тестов. В зависимости от этапа и цели оказания помощи больному возможно использование как скрининговых шкал (например, MMSE [21], Монреальской шкалы оценки когнитивных функций [22], Мини-ког [23] и т. д.), так и проведение более детального нейропсихологического тестирования.
Использование скрининговых шкал уместно и в амбулаторных условиях, и в стационаре. Как правило, их применение не занимает много времени (2–15 мин) и не требует наличия у врача специфических навыков. Их могут использовать не только неврологи или психиатры, но также терапевты, врачи общей практики, гериатры. Применение скрининговых шкал не позволяет ответить на вопрос об этиологии КР, но подтверждает их наличие (Мини-ког) и косвенно свидетельствует о тяжести нарушений.
Важным этапом является оценка психоэмоционального статуса, с учетом влияния сопутствующих эмоциональных и поведенческих расстройств пациента на выраженность когнитивного дефекта. Краткая оценка может быть выполнена с применением стандартных шкал и опросников (Гериатрическая шкала депрессии [24], шкала Спилбергера – Ханина [25], Госпитальная шкала тревоги и депрессии [26]). При подозрении на выраженные тревожно-депрессивные расстройства, при поведенческих расстройствах требуется консультация психиатра.
Следующий этап заключается в определении тяжести КР с анализом влияния определяемых нарушений на повседневную (профессиональную, социальную, бытовую) жизнь пациента. Стоит предостеречь от прямого переноса результатов тестирования, особенно скрининговых шкал, на функциональный статус пациента в быту, поскольку результаты тестирования могут быть искажены психоэмоциональной реакцией пациента на обследование, с другой стороны, в определенных ситуациях чувствительность некоторых шкал к тяжелым КР бывает недостаточной. Примером может служить шкала MMSE, не обладающая достаточной чувствительностью в диагностике КР сосудистого генеза [27].
Параклинические методы диагностики когнитивных нарушений
Всем пациентам с когнитивными нарушениями в обязательном порядке необходимо проведение развернутого общего анализа крови с определением уровня эритроцитов и гемоглобина (для исключения микро- и макроцитарной анемии), скорости оседания эритроцитов, лейкоцитарной формулы (для исключения воспалительных реакций); определение уровня электролитов (натрий, кальций, калий), глюкозы, печеночных ферментов, креатинина, мочевины, гормонов щитовидной железы (свободного Т4 и ТТГ), серологического исследования крови на сифилис. Одним из важных факторов развития нервно-психических расстройств является дефицит витамина В12 и/или фолиевой кислоты, встречающийся у 3% лиц среднего возраста и более чем у 10% пациентов старше 70 лет, что указывает на необходимость проверять их концентрацию в сыворотке крови у всех пациентов с когнитивными нарушениями вне зависимости от наличия у них анемии [28].
При развитии деменции неясной этиологии у молодых пациентов требуется более детальное серологическое обследование для исключения возможных нейроинфекций, включая ВИЧ, боррелиоз, токсоплазмоз, вирусы герпеса и т. д. [29].
Исследование ликвора проводится при подозрении на нейроинфекционное заболевание, кроме того, для анализа биомаркеров нейродегенеративных заболеваний (бета-амилоида, общего и фосфорилированного тау-протеина). Известно, что перечисленные соединения напрямую связаны с патогенезом БА, изменения концентрации данных биомаркеров в цереброспинальной жидкости отмечается еще на недементной стадии БА [30]. Было показано, что соотношение концентрации бета-амилоида и фосфорилированного тау-протеина обладает высокой специфичностью и чувствительностью в отношении БА [31]. Вместе с тем в настоящее время их использование ограничено преимущественно научными целями, в частности в исследованиях превентивной терапии БА.
При наличии сосудистых факторов риска (сердечно-сосудистых заболеваний, артериальной гипертонии, гиперхолестеринемии) необходимо кардиологическое обследование методами электрокардиографии и эхокардиографии, а также исследование магистральных сосудов головы при помощи дуплексного или триплексного сканирования. С появлением методов двухмерного (дуплексного) и трехмерного (триплексного) сканирования сосудов ультразвуковая допплерография потеряла свою диагностическую значимость [1].
Важнейшее место в диагностике деменции играют методы нейровизуализации – магнитно-резонансная томография (МРТ) и, при невозможности ее выполнения, компьютерная томография (КТ). Эти методы необходимы для определения выраженности и локализации структурных изменений головного мозга (сосудистого поражения, атрофических процессов), исключения потенциально курабельных причин (опухоли, субдуральной гематомы, гидроцефалии). Для диагностики нейродегенеративных заболеваний используются такие методы, как функциональная МРТ, позитронно-эмиссионная томография (ПЭТ) с фтордезоксиглюкозой или специфическими лигандами амилоида (например, питтсбургским веществом – PIB) [32, 33]. Как правило, данные нейровизуализационные техники являются дорогостоящими, что ограничивает их использование в рутинной практике. В то же время наиболее типичный морфологический признак БА – атрофию медиальных отделов височных долей и гиппокампов – можно оценить и при структурной МРТ, для чего разработаны простые в использовании шкалы [34].
Электроэнцефалография не обладает особой диагностической значимостью у пациентов с КР. Ее необходимо проводить только при подозрении на эпилепсию и болезнь Крейтцфельдта – Якоба.
Перечень методов параклинического обследования пациентов с когнитивными нарушениями приведен в таблице 2. Приблизительный алгоритм обследования пациентов с возможными когнитивными нарушениями представлен на рисунке 1.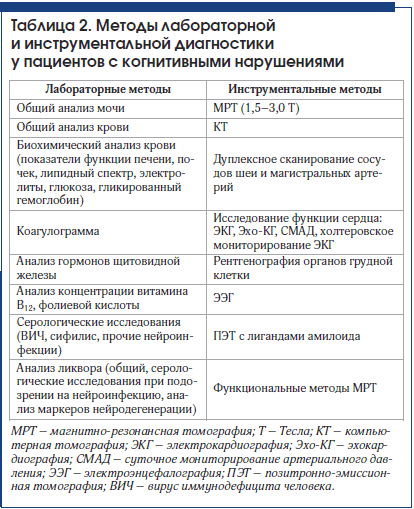
Литература
1. Яхно Н.Н., Захаров В.В., Локшина А.Б. и др. Деменции. М.: МЕДпресс-информ; 2011. 272 с. [Jahno N.N., Zaharov V.V., Lokshina A.B. i dr. Demencii. M.: MEDpress-inform; 2011. 272 s. (in Russian)].
2. Захаров В.В., Вознесенская Т.Г. Нервно-психические нарушения: диагностические тесты. М.: МЕДпресс-информ, 2013. 320 с. [Zaharov V.V., Voznesenskaja T.G. Nervno-psihicheskie narushenija: diagnosticheskie testy. M.: MEDpress-inform, 2013. 320 s. (in Russian)].
3. Rodríguez-Sánchez E., Mora-Simón S., Patino-Alonso M.C. et al. Prevalence of cognitive impairment in individuals aged over 65 in an urban area: DERIVA study // BMC Neurology. 2011. Vol. 11. Р.147. doi:10.1186/1471-2377-11–147
4. Waldron N., Laws H., James K. et al. The Prevalence of Cognitive Impairment among Older Adults in Jamaica // WIMJ. 2015. Vol. 2(2). P.71–76. doi: 10.7727/wimjopen.2014.003
5. Prince M.J., Wimo A., Guerchet M.M. et al. World Alzheimer Report 2015 – The Global Impact of Dementia: An analysis of prevalence, incidence, cost and trends. London: Alzheimer’s Disease International. 2015. 84 p.
6. Garre-Olmo J., Genis Batlle D., Del Mar Fernandes M. et al. Registry of Dementia of Girona Study Group (ReDeGi Study Group). Incidence and subtypes of early-onset dementia in a geographically defined general population // Neurology. 2010. Vol. 5(14). P.1249–1255.
7. Petersen R.C., Smith G.E., Waring S.C. et al. Aging, memory, and mild cognitive impairment // Int. Psychogeriatr. 1997. Vol. 9 (Suppl 1). P.65–69.
8. Яхно Н.Н., Захаров В.В., Коберская Н.Н. и др. «Предумеренные» (субъективные и легкие) когнитивные расстройства // Неврол. журн. 2017. Т.22. №4. С.198–204 [Jahno N.N., Zaharov V.V., Koberskaja N.N. i dr. «Predumerennye» (sub’ektivnye i ljogkie) kognitivnye rasstrojstva // Nevrol. zhurn. 2017. T.22. №4. S.198–204 (in Russian)].
9. Захаров В.В. Эволюция когнитивного дефицита: легкие и умеренные когнитивные нарушения // Неврология, нейропсихиатрия, психосоматика. 2012. №2. С.16–21 [Zaharov V.V. Jevoljucija kognitivnogo deficita: legkie i umerennye kognitivnye narushenija // Nevrologija, nejropsihiatrija, psihosomatika. 2012. №2. S.16–21 (in Russian)].
10. Яхно Н.Н. Когнитивные расстройства в неврологической клинике // Неврол. журн. 2006. Т.11. Прил. №1. С.4–12 [Jahno N.N. Kognitivnye rasstrojstva v nevrologicheskoj klinike // Nevrol. zhurn. 2006. Т.11. Рril. №1. S. 4–12 (in Russian)].
11. Petersen R., Touchon J. Consensus on mild cognitive impairment: EADC – ADCS // Research and Practice in Alzheimer’s Disease. 2005. Vol.10. P.38–46.
12. Захаров В.В. Всероссийская программа исследований эпидемиологии и терапии когнитивных расстройств в пожилом возрасте («Прометей») // Неврол. журн. 2006. T.11. C.27–32 [Zaharov V.V. Vserossijskaja programma issledovanij jepidemiologii i terapii kognitivnyh rasstrojstv v pozhilom vozraste («Prometej») // Nevrol. zhurn. 2006. T.11. S.27–32 (in Russian)].
13. Яхно Н.Н., Преображенская И.С., Захаров В.В. и др. Распространенность когнитивных нарушений при неврологических заболеваниях (анализ работы специализированного амбулаторного приема) // Неврология, нейропсихиатрия, психосоматика. 2012. №2. С.30–35 [Jahno N.N., Preobrazhenskaja I.S., Zaharov V.V. i dr. Rasprostranennost’ kognitivnyh narushenij pri nevrologicheskih zabolevanijah (analiz raboty specializirovannogo ambulatornogo priema) // Nevrologija, nejropsihiatrija, psihosomatika. 2012. №2. S.30–35 (in Russian)].
14. Rizzi L., Rosset I., Roriz-Cruz M. Global Epidemiology of Dementia: Alzheimer’s and Vascular Types // BioMed Research International. 2014. Vol. 3. P.1–8. doi:10.1155/2014/908915
15. Douiri A., McKevitt C., Emmett E.S. et al. Long–term effects of secondary prevention on cognitive function in stroke patients. // Circulation. 2013. Vol. 128(12). P.1341–1348. doi: 10.1161/CIRCULATIONAHA.113.002236
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
Информация с rmj.ru






