Механизмы развития и поддержания трепетания и фибрилляции предсердий в детском возрасте
М. А. Школьникова, доктор медицинских наук, профессор
Е. П. Дикевич
Е. К. Ерастова
НИИ педиатрии и детской хирургии, Москва
Трепетание и фибрилляция предсердий в детском возрасте являются редкими, но в то же время опасными нарушениями ритма, приводящими к развитию осложнений, таких как сердечная недостаточность, тромбоэмболии (в том числе ишемические инсульты), аритмогенная кардиомиопатия и даже внезапная сердечная смерть [1–4]. До настоящего времени именно эти аритмии с точки зрения распространенности, особенностей клинического течения и прогноза у детей и подростков остаются наименее изученными среди всех нарушений ритма, а их описаниям в детском возрасте посвящены единичные публикации [5–10]. Несмотря на то, что с электрофизиологической точки зрения трепетание предсердий (ТП) и фибрилляция предсердий (ФП) у детей и у взрослых не различаются, есть основания полагать, что имеются существенные особенности как со стороны этиологических факторов, так и патофизиологических механизмов развития и поддержания этих аритмий в детском возрасте. В то время как трепетание и особенно фибрилляция предсердий у взрослых лидируют по числу научных исследований и публикаций, ведение каждого ребенка, страдающего данными нарушениями ритма, все еще остается трудной клинической задачей. Алгоритмы лечения разработаны и совершенствуются в настоящее время только для взрослых пациентов [11–13]. Необходимы специальные исследования, которые позволят предложить педиатрические критерии оценки риска развития жизнеугрожающих состояний при ТП и ФП у детей и адаптировать к детскому возрасту разработанные для взрослых пациентов методы медикаментозного и интервенционного лечения. Целью настоящей публикации является обобщение данных об особенностях ТП и ФП в детском возрасте, как на основании опубликованных исследований, так и собственного клинического опыта.
Суммарная распространенность ТП и ФП в общей популяции составляет 0,5–0,6% [14]. При этом она не превышает 1% в возрастной группе моложе 50 лет, составляет около 5% среди лиц старше 50 лет и достигает 10% у лиц старше 80 лет [15].
Распространенность ФП и ТП в детской популяции не известна. По данным ЭКГ-скрининга практически здоровых российских детей в возрасте до 18 лет ТП было выявлено у одного из 5387 обследованных, что составило 0,02% в исследуемой когорте [16]. Имеются немногочисленные данные о частоте встречаемости мерцательной аритмии у детей, страдающих различными заболеваниями, что позволяет получить некоторое представление о группах риска по ее развитию. Дети с оперированными врожденными пороками сердца (ВПС) представляют наиболее обширную группу риска по развитию ТП и ФП. Отмечается, что распространенность этих аритмий после хирургической коррекции ВПС увеличивается в среднем по группе на 10% и на 30% — в подгруппе пациентов после операций Fontan, Mustard и Senning [17, 18]. Наиболее вероятным у детей с ВПС является развитие инцизионного ТП [19]. ФП наблюдается у 20% взрослых и 4% детей при синдроме Вольфа–Паркинсона–Уайта (ВПУ) [20], что, благодаря возможности проведения импульсов высокой частоты на желудочки, сопряжено с риском развития жизнеугрожающих аритмий при пароксизме ФП [9, 20, 21]. ФП и ТП у детей могут быть проявлением поражения сердца в рамках системной миопатии, наиболее часто — миотонической дистрофии и мышечной дистрофии Эмери–Дрейфуса. В последнем случае распространенность ФП может достигать 60% [22, 23]. Кроме того, есть данные о роли ФП, в том числе как триггера желудочковых аритмий, у детей с первичными электрическими заболеваниями сердца — синдромом укороченного интервала QT [24] и катехоламинергической желудочковой тахикардией (ЖТ) [25], а также у больных с кардиомиопатиями [26].
Таким образом, низкая распространенность мерцательной аритмии в детском возрасте не уменьшает ее клинического значения, поскольку аритмия часто ассоциируется с тяжелыми патологическими состояниями или с другими нарушениями ритма и повышает вероятность неблагоприятного прогноза.
Классические подходы к классификации ФП и ТП не отличаются у детей и взрослых и учитывают этиологию, клинические проявления и патофизиологические механизмы. Может иметь место идиопатический и вторичный характер аритмии, при котором ФП или ТП осложняют течение других сердечно-легочных заболеваний. В отличие от взрослых пациентов, у которых ФП чаще всего развивается на фоне ишемической болезни сердца, когда участки ишемизированного или фиброзно-измененного миокарда создают анатомический субстрат для циркуляции возбуждения по предсердиям [27, 28], в детском возрасте высока вероятность выявления данной аритмии у лиц со структурно нормальным сердцем. По данным нашей клиники, в 61% случаев дети с мерцательной аритмией не имели признаков органического поражения сердца. Ремоделирование миокарда является основой развития ФП у детей с кардиомиопатиями (КМП). При этом относительно медленное прогрессирование заболеваний обусловливает манифестацию ФП преимущественно на 2–4 декадах жизни, т. е. у подростков и лиц молодого возраста [22, 26, 29]. Гистологические исследования выявили признаки вялотекущего воспалительного процесса в тканях предсердий у более чем 50% больных с ФП, считавшейся ранее идиопатической [30, 31]. По данным J. Maixent с соавторами у 60% пациентов с так называемой идиопатической пароксизмальной ФП обнаруживаются циркулирующие антитела к тяжелой цепи миозина [32]. В то же время для острых миокардитов, наоборот, ФП не характерна [33].
Среди фетальных аритмий доля ТП достигает 26%, и развитие этой аритмии у плода нередко связано с наличием ВПС, таких как атриовентрикулярный канал, гипоплазия левых отделов сердца, атрезия легочной артерии [34]. От 25% до 32% ФП и ТП у детей регистрируется при ВПС, наиболее часто при дефектах межпредсердной перегородки, врожденной митральной недостаточности, аномальном дренаже легочных вен, дефектах межжелудочковой перегородки, транспозиции магистральных сосудов, тетраде Фалло, аномалии Эпштейна [6]. Согласно данным M. Damjanovic аномалия Эпштейна сочетается с синдромом ВПУ и пароксизмальной формой ФП в 50% случаев [8]. Особенно часто у больных с ВПС отмечаются инцизионные формы этих тахиаритмий, развивающиеся как раннее или позднее осложнение вмешательств на открытом сердце вследствие блокады проведения и появления дисперсии рефрактерности миокарда вокруг послеоперационных рубцов [19]. Вероятность развития ТП повышается с увеличением возраста оперированных пациентов с ВПС [7].
Основой развития ФП у детей могут быть и другие органические заболевания сердца: опухоли, фиброэластоз эндокарда, структурные изменения в рамках синдрома Марфана и других соединительнотканных дисплазий, инфекционный эндокардит [35, 36]. Наши наблюдения также включают детей с врожденным кардитом, дилятационной КМП, аневризмой правого предсердия, катехоламинергической ЖТ (рис. 1). Предрасполагающим фактором для развития ФП и ТП как у взрослых, так и у детей со структурными заболеваниями сердца является ремоделирование с расширением предсердий и растяжением устьев легочных вен [17, 29].
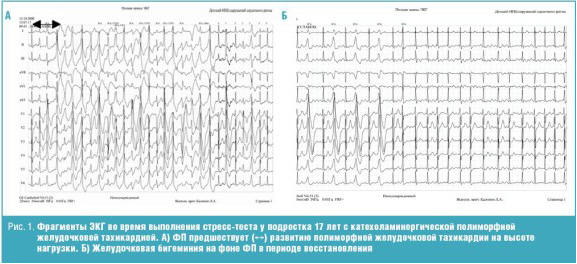
Рис. 1. Фрагменты ЭКГ во время выполнения стресс-теста у подростка 17 лет с катехоламинергической полиморфной желудочковой тахикардией. А) ФП предшествует (↔) развитию полиморфной желудочковой тахикардии на высоте нагрузки. Б) Желудочковая бигеминия на фоне ФП в периоде восстановления
На сегодняшний день известен целый ряд генетических мутаций (преимущественно влияющих на структуру ионных каналов), которые играют роль в развитии аритмий, в том числе ФП и ТП [37–39]. Генетически детерминированные нарушения ритма имеют наибольшее клиническое значение именно в педиатрической практике, поскольку манифестируют в детском возрасте и нередко носят жизнеугрожающий характер. При семейных формах ФП нередко описываются мутации в гене натриевого канала кардиомиоцитов — SCN5A [37], который также поражен при большинстве первичных электрических заболеваний сердца — синдромах короткого и удлиненного интервала QT (LQT3), синдроме Бругада, а также у больных с синдромом слабости синусового узла и дилятационной КМП [39, 40]. Развитие ФП при синдроме короткого интервала QT связывают с укорочением эффективного рефрактерного периода в кардиомиоцитах предсердий [41]. Также описано сочетание катехоламинергической ЖТ, для которой характерно поражение рианодиновых рецепторов кардиомиоцитов (RyR2), с пароксизмами ФП [42]. Авторы связывают развитие наджелудочковых тахиаритмий при этом заболевании с диффузным поражением RyR2 в миокарде не только желудочков, но и предсердий.
Таким образом, как причины ФП и ТП у детей имеют значение ВПС, КМП, заслуживают внимания воспалительные изменения и генетические мутации с поражением ионных каналов кардиомиоцитов. В отличие от взрослых, у существенной части (более 50%) больных в детском возрасте эти аритмии развиваются в отсутствие структурных изменений в миокарде и могут быть расценены как идиопатические.
По клиническому течению выделяют пароксизмальную форму ФП и ТП со спонтанно прекращающимися эпизодами длительностью не более 7 дней (чаще не более 24 часов), устойчивую — персистирующую и постоянную формы [12]. Как пароксизмальная, так и персистирующая формы могут быть рецидивирующими, а впоследствии переходить в постоянную форму ФП. В отличие от взрослых, в большинстве случаев у детей редко диагностируется пароксизмальная форма, а постоянная форма ФП встречается в 64% случаев [43]. Согласно нашим наблюдениям, пароксизмальная форма имела место у 18% детей с ТП и 23% — с ФП, в то время как постоянная форма регистрировалась у 71% детей с ТП и 67% — с ФП (рис. 2 А, Б). Более чем в 50% случаев ФП и ТП сочетаются с другими видами нарушений ритма, наиболее часто с нарушением функции синусового узла и эктопической предсердной тахикардией. В ряде случаев у одного и того же ребенка отмечается сочетание ТП и ФП, при этом, как правило, имеет место непрерывно-рецидивирующий характер аритмии. По мнению G. Mainzer с соавт. детям менее свойственна трансформация фокусной предсердной тахикардии в ФП в связи с меньшей распространенностью миокардиального фиброза, меньшей дисперсией рефрактерности в предсердиях и сравнительно небольшим объемом самих предсердий [35].
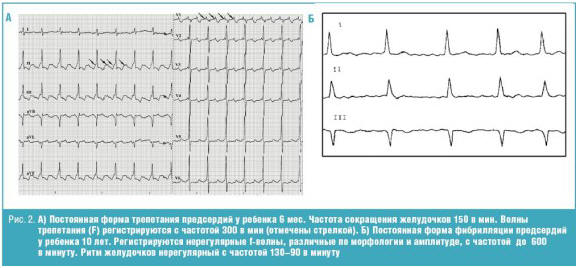
Рис. 2. А) Постоянная форма трепетания предсердий у ребенка 6 мес. Частота сокращения желудочков 150 в мин. Волны трепетания (F) регистрируются с частотой 300 в мин (отмечены стрелкой). Б) Постоянная форма фибрилляции предсердий у ребенка 10 лет. Регистрируются нерегулярные f-волны, различные по морфологии и амплитуде, с частотой до 600 в минуту. Ритм желудочков нерегулярный с частотой 130–90 в минуту
Электрофизиологические механизмы развития аритмий у детей не отличаются от таковых у взрослых [44]. Экспериментально и клинически доказана возможность существования следующих основных механизмов аритмогенеза: циркуляции волны возбуждения по миокарду предсердий, или макрореентри; триггерные зоны, генерирующие импульсы высокой частоты одновременно в нескольких зонах миокарда предсердий; задержанная деполяризация миокарда предсердий и роторный механизм [28, 45, 46]. ТП реализуется путем реципрокной циркуляции электрического импульса вокруг рубцово-измененных участков миокарда или крупных анатомических отверстий в предсердиях (макрореентри) [46]. При ФП могут иметь место все перечисленные механизмы аритмогенеза [28]. Циркуляция возбуждения чаще происходит в зонах пересечения и резкого изменения хода волокон кардиомиоцитов — вокруг анатомических структур, в частности устьев легочных и полых вен и фиброзных колец атриовентрикулярных клапанов [47]. Для реализации ТП и ФП по механизму макрореентри необходим достаточно большой объем предсердий, что объясняет низкую распространность данных нарушений ритма у детей раннего возраста [34]. Субстратом для ФП служит электрическая неоднородность миокарда предсердий, причинами которой могут быть ремоделирование/растяжение, воспаление или фиброзное изменение миокарда [48]. Предполагается, что электрофизиологически ФП поддерживается по роторному механизму [49]. Сверхчастое возбуждение кардиомиоцитов предсердий вызывает их электрическое ремоделирование (укорочение эффективного рефрактерного периода и длины цикла мерцания), что способствует персистированию ФП [50]. Следует отметить, что исчерпывающего понимания механизмов развития ФП до сегодняшнего дня нет, что отчасти объясняет недостаточную эффективность лечения данной аритмии.
Среди других патофизиологических механизмов, для которых подтверждена связь с развитием специфических для этих видов аритмий электрофизиологических нарушений, увеличение скорости внутрипредсердного проведения импульса под влиянием предсердного натрийуретического пептида, что создает условия для развития реципрокных предсердных аритмий, в том числе ФП и ТП [51]. К развитию ФП предрасполагает ремоделирование предсердий с их растяжением вследствие повышения внутрипредсердного давления, что характерно для больных с частыми приступами реципрокной атриовентрикулярной тахикардии. Показано, что степень повышения давления прямо коррелирует со скоростью ретроградного проведения по дополнительному предсердно-желудочковому соединению (ДПЖС) [30, 52]. Большое значение в возникновении и поддержании ФП также придается нарушению функции синусового узла (синдрому слабости синусового узла). При нарушении нормального ритмовождения происходит компенсаторная активация эктопических источников ритма (развивается синдром брадитахикардии) [3, 53]. В свою очередь, ремоделирование кардиомиоцитов синоатриальной области при персистирующей ФП приводит к усугублению дисфункции синусового узла [50], что повышает значение данного патофизиологического механизма этой аритмии. Согласно нашим наблюдениям, нарушение функции синусового узла имело место у 26% детей с мерцательной аритмией.
Немаловажным фактором персистенции ФП являются нарушения вегетативной регуляции сердечной деятельности [54, 55]. Вегетативные кризы (симпатоадреналовые и вагоинсулярные) могут служить провоцирующими факторами для пароксизмов ФП [54]. Экспериментальными исследованиями установлено, что в устьях легочных вен имеются не только волокна рабочего миокарда, но и клетки, обладающие пейсмейкерной активностью [56]. Как и область синусового узла, эти клетки хорошо иннервированы — окружены ганглионарными сплетениями и благодаря этому высокочувствительны к изменениям вегетативного тонуса [57]. Парасимпатическая активация приводит к укорочению эффективного рефрактерного периода в миокарде предсердий, что создает условия запуска ФП при экстрасистолии [58]. Одновременное воздействие симпатических стимулов вызывает выход кальция из саркоплазматического депо, раннюю деполяризацию, которая приводит к экстрасистолии [59]. Холинергический (вагозависимый) характер пароксизмов ФП характерен в большей степени для больных без сопутствующей сердечно-сосудистой патологии и нередко наблюдается у детей, а адренергический — для пациентов со структурными заболеваниями сердца, в том числе с инцизионными аритмиями [60]. У взрослых больных с постоянной формой ФП нередко отмечается гиперсимпатикотония [61].
Многие авторы отмечают достаточно высокую частоту развития ФП у пациентов с гипертиреозом — в 10–15% случаев [62, 63]. В детском возрасте гипертиреоз реже осложняется развитием этой аритмии, однако такие случаи описаны [64]. Наиболее прогностически значимым фактором риска ФП при данном заболевании является снижение сывороточного уровня тиреотропина. Гормоны щитовидной железы изменяют электрофизиологические свойства кардиомиоцитов предсердий, укорачивая их эффективный рефрактерный период и повышая уровень автоматизма пейсмейкерных клеток, в том числе в эктопических очагах [65]. Они оказывают непосредственное действие на ядерные рецепторы клеток, повышают уровень синтеза белков кардиомицитов, таких как тяжелая альфа-цепь миозина, кальциевая АТФаза, калиевые и натриевые каналы, а также бета-адренорецепторы. Таким образом, повышается чувствительность миокарда к симпатической стимуляции, что в совокупности с повышением триггерной активности при гипертиреозе создает условия для развития и поддержания ФП.
Фибрилляция предсердий описана у детей, перенесших хирургические вмешательства на заднем средостении (коррекция пороков развития пищевода, удаление опухолей) [35]. При этом пусковым патофизиологическим механизмом служит резкое изменение внутригрудного давления и давления на предсердия при выполнении торакотомии или травма симпатического ствола, приводящая к нарушению вегетативной регуляции сердечного ритма [66].
Клинические проявления ФП и ТП у детей обусловлены в первую очередь высокой частотой сердечных сокращений (ЧСС) и нарушением физиологического соотношения предсердно-желудочковых сокращений, что сопровождается сердцебиениями, артериальной гипотонией, миокардиальной дисфункцией. При ФП систола предсердий отсутствует, а при ТП является функционально неэффективной, в связи с чем уменьшается наполнение желудочков. Дополнительно высокая частота проведения импульсов на желудочки приводит к нарушению гемодинамики вследствие резкого укорочения фазы диастолического расслабления желудочков и снижения минутного объема сердца [67]. Пароксизмальные формы у детей старшего возраста, как правило, протекают с выраженной клинической симптоматикой: ощущение учащенного сердцебиения, симптомы сердечной недостаточности, кардиалгии, пресинкопальные и синкопальные состояния. К последним приводит не только обусловленная тахикардией артериальная гипотензия, но и посттахикардитические остановки синусового узла, предшествующие восстановлению синусового ритма. У новорожденных и детей младшего возраста быстрее развиваются симптомы сердечной недостаточности; характерно беспокойство ребенка, возможен отказ от еды, рвота. Для детей характерна выраженная вегетативная окраска приступов, проявления которой также зависят от возраста пациентов. У детей младшего возраста отмечаются изменение цвета кожных покровов, повышенное потоотделение, повышение частоты дыхания, резкая слабость. У детей старшего возраста клиническая картина приступа не отличается от таковой у взрослых. При постоянной форме ФП и ТП уменьшение сердечного выброса в связи с отсутствием эффективной систолы предсердий у детей старшего возраста нередко сопровождается повышенной утомляемостью, снижением толерантности к физическим нагрузкам. Именно эти жалобы могут послужить причиной обращения больного или его родителей к специалисту. Для постоянной и персистирующей ФП также характерно ощущение неритмичности сердцебиений, что влияет на развитие у ребенка повышенной тревожности [68]. Исследованиями Ricci S. и Drago F. с соавт. показано, что длительное персистирование ФП и ТП с высокой частотой проведения на желудочки у детей может вызвать снижение сократительной способности миокарда (аритмогенную кардиомиопатию) [1, 3]. При персистирующей и постоянной формах ФП и ТП клинические проявления аритмии у детей зависят, в первую очередь, от частоты проведения импульсов на желудочки. При частоте сокращений желудочков, близкой к возрастной норме, аритмия в детском возрасте практически не ощущается или протекает малосимптомно. Она не приводит к развитию недостаточности кровообращения и редко сопровождается аритмогенной дисфункцией миокарда. Необходимо принимать во внимание, что для детей, особенно раннего возраста, в норме характерны относительно высокие значения ЧСС. Так, у детей первого года жизни по данным ЭКГ-скрининга 95 перцентиль нормальных значений ЧСС составляет 170 уд./мин [16]. Как следствие — дети практически не ощущают наджелудочковые тахиаритмии с ЧСС, близкой к возрастной норме [69]. В совокупности с тем, что дети адекватно формализуют симптомы с возраста 5–6 лет, клиническая картина нарушения ритма у новорожденных, в том числе при пароксизмальных нарушениях ритма с частотой проведения на желудочки до 160–180 в мин, а у детей раннего возраста — до 140 в мин, с высокой вероятностью будет стертой.
Для диагностики фетальных тахиаритмий информативна эхокардиография, которая позволяет оценить ЧСС, вид аритмии и признаки сердечной недостаточности (водянки плода), выявить структурные заболевания сердца как возможную причину аритмии. Эти данные учитываются при принятии решения о методе и сроках родоразрешения, выборе антиаритмической терапии в анте- или постнатальном периоде. Учитывая непредсказуемость ответа на антиаритмическую терапию, ведение детей с фетальными аритмиями остается сложной клинической задачей [70]. Диагностика ТП и ФП в постнатальном периоде не отличается от таковой у взрослых. Необходимо отметить значение метода длительного ЭКГ-мониторирования в выявлении эпизодов мерцательной аритмии у детей из групп риска (оперированные больные с ВПС, дети с КМП, опухолями сердца, предсердными тахикардиями, феноменом и синдромом ВПУ, синдромом короткого интервала QT, катехоламинергической ЖТ), в том числе у детей с синкопальными состояниями и приступами сердцебиений неясной этиологии.
Имеются данные, свидетельствующие о доброкачественном течении ТП у новорожденных и детей первого года жизни со структурно нормальным сердцем: медикаментозное восстановление синусового ритма происходит быстро, и в дальнейшем ТП не рецидивирует, поэтому длительная антиаритмическая терапия не требуется [35]. При ТП у плода описаны случаи спонтанного восстановления синусового ритма после родов, поэтому по мнению Krapp M. [34] и Ortega J. [71] в отношении ТП у новорожденных оправдана выжидательная тактика ведения в течение нескольких часов. В целом, по сравнению со взрослыми, у пациентов детского возраста клиническая картина заболевания менее выражена и нарушения ритма могут длительно протекать бессимптомно [10]. В то же время риск осложнений фибрилляции и трепетания предсердий (тромбоэмболия, внезапная смерть) при этом остается высоким, особенно у детей со структурными поражениями сердца [1, 2]. Это диктует необходимость разработки эффективных методов лечения, в том числе при бессимптомных формах мерцательной аритмии.
Арсенал методов медикаментозного и интервенционного лечения ФП и ТП для детей и взрослых принципиально одинаков. Однако существуют особенности в выборе тактики лечения для пациентов детского возраста. Учитывая достаточно частую ассоциацию ФП у детей и подростков с другими нарушениями ритма сердца и заболеваниями миокарда, по мнению ряда авторов в первую очередь необходимо воздействовать на возможные триггерные факторы [5, 72, 73].
Для контроля ЧСС и восстановления синусового ритма у детей применяются дигоксин (противопоказан у больных с функционирующими ДПЖС), амиодарон и соталол [74]. В ряде случаев обсуждается целесообразность назначения бета-блокаторов. A. Barros с соавт. и M. Krapp с соавт. отмечают невысокую (до 17%) частоту рецидивов ТП после восстановления синусового ритма у детей [34, 75]. На тактику ведения детей с ФП влияет наличие ДПЖС, создающих условия для развития жизнеугрожающих аритмий. Короткий рефрактерный период ДПЖС и наличие множественных дополнительных проводящих путей являются факторами риска внезапной аритмической смерти [9, 20, 52]. Согласно исследованиям V. Santinelli и соавт., у 10% детей с феноменом ВПУ развиваются эпизоды ФП с проведением по ДПЖС, которые более чем в половине случаев переходят в фибрилляцию желудочков [72]. Таким пациентам необходимо интервенционное лечение — абляция ДПЖС для устранения возможности сверхчастого проведения импульса на желудочки [9, 20, 76]. Терапию антиаритмическими препаратами получали 68% детей, наблюдавшихся в нашей клинике. Полное длительное восстановление ритма имело место у 1/3 из этих детей, а наиболее эффективным в плане поддержания синусового ритма оказался соталол. Коррекция гормональных и нейровегетативных нарушений, например повышенных вагусных влияний на сердечный ритм, является дополнительным терапевтическим ресурсом, способным повлиять на течение ФП и ТП. Так, у пациентов с тиреотоксикозом при достижении эутиреоза в 2/3 случаев синусовый ритм восстанавливается без применения антиаритмической терапии [62, 64].
У детей с постоянной формой ФП актуальна электрическая кардиоверсия. Предполагают, что при интервенционном лечении ФП у подростков могут быть эффективными более щадящие вмешательства, чем у взрослых пациентов, — абляция только триггерных зон без обширного воздействия на миокард предсердий. M. Strieper с соавт. сообщают об успешном предотвращении рецидивов пароксизмальной ФП методом абляции фокусной предсердной тахикардии, служившей пусковым механизмом ФП, у трех из четырех наблюдаемых ими подростков [73]. Осторожное отношение к изоляции легочных вен для лечения ФП у детей связано с риском развития стеноза вследствие циркулярных радиочастотных аппликаций. Однако частота данного осложнения не изучена. Для минимизации повреждения миокарда у детей возможно применение метода криоабляции. Детям с ТП может быть рекомендована радиочастотная катетерная абляция каватрикуспидального истмуса или критических зон петель тахикардии. При выявлении симптомов синдрома слабости синусового узла у детей с ФП и ТП, в том числе после проведенного интервенционного лечения, может потребоваться имплантации электрокардиостимулятора. По мнению S. Pizzale устранение реципрокных предсердных тахикардий, в том числе ТП и ФП, жизненно необходимо детям и лицам молодого возраста с катехоламинергической ЖТ, так как у них наджелудочковые тахиаритмии служат триггерным фактором жизнеугрожающей ЖТ [77]. У таких пациентов изоляция легочных вен позволяет не только предотвратить развитие ФП, но и снизить чувствительность миокарда к катехоламинам, поскольку происходит повреждение симпатических нервных окончаний, расположенных вокруг устьев легочных вен [25]. Наиболее резистентными к антиаритмической и электроимпульсной терапии являются инцизионные аритмии у детей после коррекции сложных ВПС [7, 19, 78]. К персистенции ФП и ТП в этих случаях предрасполагают наличие множественных рубцов в миокарде предсердий, растяжение предсердий и увеличение давления в них [71]. При ТП у плода и новорожденного с ВПС и опухолью сердца ответ на антиаритмическую и электроимпульсную терапию вариабелен [75]. Следует отметить, что нередко эффективным в плане контроля ЧСС или в качестве противорецидивной терапии оказывается комбинированное применение интервенционных и медикаментозных методов лечения.
Таким образом, причины развития мерцательной аритмии у взрослых и детей различны. Если у взрослых пациентов циркуляция электрического импульса по предсердиям происходит преимущественно вокруг рубцово?измененных, ишемизированных участков миокарда, то у детей субстратом аритмии служат структурные изменения миокарда предсердий при ВПС, КМП, послеоперационные рубцы и участки дополнительных проводящих путей. Как причина ФП и ТП у детей заслуживают внимания также воспалительные изменения и генетические мутации с поражением ионных каналов кардиомиоцитов. Более чем в половине случаев мерцательная аритмия выявляется у детей без структурных аномалий сердца. На развитие и поддержание ФП и ТП влияют вегетативные и гормональные нарушения. В детском возрасте как при ФП, так и при ТП преобладает постоянная форма аритмии. В отличие от взрослых, детям свойственно малосимптомное течение этих нарушений сердечного ритма. Фактором риска развития фибрилляции желудочков при ФП является наличие быстрых дополнительных проводящих путей — аномалии, широко распространенной в детском и молодом возрасте. Наряду с вероятностью благоприятного прогноза у детей первого года жизни без органической патологии сердца, у детей более старшего возраста мерцательная аритмия склонна к хроническому течению, ассоциируется с нарушениями гемодинамики и риском развития жизнеопасных осложнений. Вариабельность клинико-электрофизиологических вариантов аритмии наряду с малым числом исследований и опубликованных клинических наблюдений не позволяют сделать однозначных заключений о тактике лечения. Сочетанное применение антиаритмических препаратов и интервенционных методов представляется наиболее эффективным. Коррекция выявленных вегетативных и гормональных нарушений является дополнительным ресурсом терапии.
Литература
- Ricci S. Embolism from the heart in the young patient: a short review // Neurol Sci. 2003, May; 24, Suppl 1: S13–14.
- Losay J., Touchot-Kone A., Lambert V. Congenital cardiopathy: indications for anticoagulant treatmen //Arch Mal Coeur Vaiss. 2005, May; 98 (5): 566–570.
- Drago F., Silvetti M. S., Grutter G., De Santis A. Long term management of atrial arrhythmias in young patients with sick sinus syndrome undergoing early operation to correct congenital heart disease // Europace. 2006, Jul; 8 (7): 488–494.
- Bar-Cohen Y., Silka M. J. Sudden cardiac death in pediatrics // Curr Opin Pediatr. 2008, Oct; 20 (5): 517–521.
- Nanthakumar K., Lau Y. R., Plumb V. J., Epstein A. E., Kay G. N. Electrophysiological findings in adolescents with atrial fibrillation who have structurally normal hearts // Circulation. 2004, Jul 13; 110 (2): 117–123. Epub 2004, Jun 14.
- Stulak J. M., Dearani J. A., Puga F. J., Zehr K. J., Schaff H. V., Danielson G. K. Right-sided Maze procedure for atrial tachyarrhythmias in congenital heart disease // Ann Thorac Surg. 2006, May; 81 (5): 1780–1784; discussion 1784–1785.
- Papagiannis J., Maounis T., Laskari C., Theodorakis G. N., Rammos S. Ablation of atrial tachycardias with radiofrequency current after surgical repair of complex congenital heart defects // Hellenic J Cardiol. 2007, Sep-Oct; 48 (5): 268–277.
- Damjanovic M. R., Dordevic-Radojkovic D., Perisic Z., Apostolovic S., Koracevic G., Pavlovic M., Tomasevic M., Jankovic R. Ebstein’s anomaly as a cause of paroxysmal atrial fibrillation // Vojnosanit Pregl. 2008, Nov; 65 (11): 847–850.
- Harahsheh A., Du W., Singh H., Karpawich P. P. Risk factors for atrioventricular tachycardia degenerating to atrial flutter/fibrillation in the young with Wolff-Parkinson-White // Pacing Clin Electrophysiol. 2008, Oct; 31 (10): 1307–1312.
- Di Rocco J. R., During A., Morelli P. J., Heyden M., Biancaniello T. A. Atrial fibrillation in healthy adolescents after highly caffeinated beverage consumption: two case reports // J Med Case Reports. 2011.
- Camm A. J., Kirchhof P., Lip G. Y., Schotten U., Savelieva I., Ernst S., Van Gelder I. C., Al-Attar N., Hindricks G., Prendergast B., Heidbuchel H., Alfieri O., Angelini A., Atar D., Colonna P., De Caterina R., De Sutter J., Goette A., Gorenek B., Heldal M., Hohloser S. H., Kolh P., Le Heuzey J. Y., Ponikowski P., Rutten F. H. European Heart Rhythm Association; European Association for Cardio-Thoracic Surgery, Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC) // Eur Heart J. 2010, Oct; 31 (19): 2369–2429. Epub 2010, Aug 29.
- Fuster V., Ryden L. E., Cannom D. S., Crijns H. J., Curtis A. B., Ellenbogen K. A., Halperin J. L., Kay G. N., Le Huezey J. Y., Lowe J. E., Olsson S. B., Prystowsky E. N., Tamargo J. L., Wann L. S. 2011 ACCF/AHA/HRS Focused Updates Incorporated Into the ACC/AHA/ESC 2006 Guidelines for the Management of Patients With Atrial Fibrillation. A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines Developed in partnership with the European Society of Cardiology and in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society // J Am Coll Cardiol. 2011, Mar 15; 57 (11): e101–198.
- Verma A., Macle L., Cox J., Skanes A. C. CCS Atrial Fibrillation Guidelines Committee. Canadian Cardiovascular Society atrial fibrillation guidelines 2010: catheter ablation for atrial fibrillation/atrial flutter // Can J Cardiol. 2011, Jan-Feb; 27 (1): 60–66.
- Bonhorst D., Mendes M., de Sousa J., Primo J., Adragao P., Andrade S., De Macedo A. M. Epidemiology of atrial fibrillation // Rev Port Cardiol. 2010, Jul-Aug; 29 (7–8): 1207–1217.
- Heemstra H. E., Nieuwlaat R., Meijboom M., Crijns H. J. The burden of atrial fibrillation in the Netherlands // Neth Heart J. 2011, Jul 15.
- Нормативные параметры ЭКГ у детей и подростков. Ассоциация детских кардиологов России. Под ред.: Школьникова М. А., Миклашевич И. М., Калинин Л. А. М., 2010. 232 с.
- Greason K. L., Dearani J. A., Theodoro D. A., Porter C. B., Warnes C. A., Danielson G. K. Surgical management of atrial tachyarrhythmias associated with congenital cardiac anomalies: Mayo Clinic experience // Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu. 2003; 6: 59–71.
- Townsend S. N. Arrhythmias in adults with congenital heart disease // Arch Cardiol Mex. 2007, Apr-Jun; 77, Suppl 2: S2–47, S2–50.
- Mitchell L. B. CCS Atrial Fibrillation Guidelines Committee. Canadian Cardiovascular Society atrial fibrillation guidelines 2010: prevention and treatment of atrial fibrillation following cardiac surgery // Can J Cardiol. 2011, Jan-Feb; 27 (1): 91–97.
- Chiale P. A., Albino E., Garro H. A., Selva H., Levi R. J., Sanchez R. A., Elizari M. V., Alvarez C. B. Supernormal conduction in the anomalous bundles of the Wolff-Parkinson-White syndrome: an overlooked electrophysiologic property with potential clinical implications // J Cardiovasc Pharmacol Ther. 2007, Sep; 12 (3): 181–191.
- Термосесов С. А., Школьникова М. А. Современные методы интервенционного лечения наджелудочковых тахиаритмий у детей // Российский вестник перинатологии и педиатрии. 2005, № 2., с. 26–34.
- Finsterer J., Stollberger C. Atrial fibrillation/flutter in myopathies // Int J Cardiol. 2008, Aug 29; 128 (3): 304–310. Epub 2008, Mar 17.
- Hsu D. T. Cardiac manifestations of neuromuscular disorders in children // Paediatr Respir Rev. 2010, Mar; 11 (1): 35–38. Epub 2009, Nov 18.
- Maury P., Extramiana F., Sbragia P., Giustetto C., Schimpf R., Duparc A., Wolpert C., Denjoy I,. Delay M., Borggrefe M., Gaita F. Short QT syndrome. Update on a recent entity // Arch Cardiovasc Dis. 2008, Nov-Dec; 101 (11–12): 779–786. Epub 2008, Nov 18.
- Sumitomo N., Nakamura T., Fukuhara J., Nakai T., Watanabe I., Mugishima H., Hiraoka M. Clinical effectiveness of pulmonary vein isolation for arrhythmic events in a patient with catecholaminergic polymorphic ventricular tachycardia // Heart Vessels. 2010, Sep; 25 (5): 448–452. Epub 2010, Jul 31.
Статья опубликована в журнале Лечащий Врач
материал MedLinks.ru







