Введение
По данным Всемирной организации здравоохранения, на 2019 г. хроническая обструктивная болезнь легких (ХОБЛ) стала причиной смерти 2,32 млн человек [1]. Хроническое воспаление, прогрессирующая эмфизема, легочная гиперинфляция приводят у больных ХОБЛ к повышению постнагрузки на правый желудочек (ПЖ) за счет увеличения легочного сосудистого сопротивления и к умеренному росту систолического давления в легочной артерии (ЛА), что с течением времени вызывает структурные изменения правых отделов сердца и правожелудочковую недостаточность [2–4]. Болезнь постепенно и неуклонно прогрессирует, что приводит к инвалидизации больных [1]. Основными причинами смерти при ХОБЛ являются прогрессирующая дыхательная и сердечная (правожелудочковая) недостаточность.
Муковисцидоз (МВ) является системным наследственным заболеванием, которое регистрируется с частотой 1:3000–1:6000 новорожденных. Прогрессирование дыхательной недостаточности и сопутствующая гипоксия у больных МВ в 70% случаев сочетаются с нарушениями легочно-сердечной гемодинамики, вплоть до развития хронического легочного сердца [5–7]. Одной из основных причин развития недостаточности ПЖ у больных МВ некоторые считают легочную гипертензию (ЛГ), приводящую к перегрузке правых отделов сердца, однако механизмы декомпенсации сердечной деятельности остаются предметом дискуссий, особенно в случае незначительного повышения давления в ЛА или отсутствия ЛГ [8, 9].
Следует заметить, что диагностика ранних признаков недостаточности кровообращения у больных с хронической легочной патологией непроста, особенно на ранних этапах заболевания, т. к. гемодинамические нарушения маскируются сопутствующей дыхательной недостаточностью.
Цель исследования — эходопплеркардиографическая оценка функционального состояния правых отделов сердца у ХОБЛ и больных со смешанной и легочной формами МВ.
Материал и методы
Всего обследовано 112 больных. Из них 82 были пациенты с ХОБЛ (все мужчины, средний возраст — 54±1,6 года) III стадии по GOLD (The Global Initiative for Chronic Obstructive Lung Disease – Глобальная инициатива по хронической обструктивной болезни легких), смешанный эмфизематозно-бронхитический фенотип, в период ремиссии заболевания. Все пациенты в качестве базисной терапии получали олодатерол + тиотропия бромид 2,5 мкг + 2,5 мкг (Спиолто® Респимат®) по 2 ингаляции 1 р/сут. Остальные 30 пациентов страдали МВ, смешанной формой, преимущественно среднетяжелого течения (19 мужчин и 29 женщин, средний возраст — 28±1,1 года). Контрольную группу составили 40 здоровых добровольцев в возрасте от 18 до 59 лет (средний возраст — 41±3,1 года). В зависимости от наличия ЛГ и признаков недостаточности правых отделов сердца пациентов разделили на 4 группы: в 1-ю группу включили 11 больных МВ с ЛГ в покое (систолическое давление в легочной артерии [СДЛА] выше 30 мм рт. ст.) без признаков недостаточности правых отделов сердца; во 2-ю группу включили 47 больных ХОБЛ с ЛГ в покое (СДЛА выше 30 мм рт. ст.) без признаков недостаточности правых отделов сердца; 3-ю группу составили 19 больных МВ с ЛГ и признаками недостаточности ПЖ; в 4-ю группу вошли 35 мужчин с тяжелым течением ХОБЛ, сопровождающимся ЛГ и правожелудочковой недостаточностью.
Эходопплеркардиографическое (ЭхоДКГ) исследование легочно-сердечной гемодинамики проводили на ультразвуковой диагностической системе VIVID 7 Dimension (GE, США) по стандартной методике [10]. Рассчитывали показатели, характеризующие функциональное состояние правых отделов сердца: конечно-систолический размер (КСР) и конечно-диастолический размер (КДР) ПЖ, толщину миокарда передней стенки ПЖ в систолу
и толщину миокарда передней стенки ПЖ в диастолу (ТМ ПСПЖд), скорость сокращения миокарда и скорость расслабления миокарда ПЖ, фракцию систолического утолщения миокарда передней стенки ПЖ (ФСУт ПСПЖ), фракцию систолического уменьшения площади правого предсердия (ФСУ ПП), СДЛА по градиенту трикуспидальной регургитации с учетом диаметра нижней полой вены и ее коллабирования при дыхании для оценки правопредсердного давления. Систолическую функцию ПЖ оценивали по амплитуде движения кольца трикуспидального клапана, а диастолическую функцию ПЖ — по спектрограммам транстрикуспидального кровотока. При проведении ЭхоДКГ оценивали Е/А — соотношение скоростей раннего и предсердного диастолического потока и E/e’ – соотношение максимальной скорости трансмитрального кровотока и пиковой скорости расслабления миокарда в фазу раннего наполнения желудочков. Использование тканевой допплерографии позволяло определить соответствующие скорости сокращения базального сегмента передней стенки ПЖ.
Для исследования механики дыхания выполняли спирометрию и бодиплетизмографию по стандартным методикам на установке Master Screen (E. Jaeger, Германия). Выполнили оценку следующих показателей легочной вентиляции: форсированная жизненная емкость легких (ФЖЕЛ), объем форсированного выдоха за 1 секунду (ОФВ1), индекс Генслера (ОФВ1/ФЖЕЛ), общая емкость легких и остаточный объем легких. Статистическая обработка материала выполнялась стандартными методами с помощью пакета Statistica for Windows 6.0. Различия считали статистически значимыми при р<0,05.
Результаты и обсуждение
Сердечно-сосудистые заболевания считаются одной из самых важных сопутствующих патологий при ХОБЛ, поскольку риск их развития в 2–3 раза превышает таковой у пациентов без ХОБЛ, с поправками на курение и возраст [11]. Нарушения гемодинамики малого круга кровообращения у больных с хронической патологией легких проявляются в виде повышения легочного сосудистого сопротивления и ЛГ 1-й степени, что впоследствии может привести к структурным изменениям правых камер и правожелудочковой недостаточности.
Как следует из таблицы 1, у больных ХОБЛ отмечалась тенденция к более выраженным изменениям эхокардиографических показателей правых отделов сердца по сравнению с показателями у больных МВ. Так, расчетное СДЛА у больных ХОБЛ во 2-й группе было достоверно выше, а КДР ПЖ — больше, чем у пациентов из 1-й группы, составив 44,9±3,4 мм рт. ст. и 3,26±0,26 см против 36,3±1,73 мм рт. ст. и 2,96±0,09 см соответственно (р<0,01). Наметившиеся проявления диастолической дисфункции миокарда также оказались более выраженными у больных ХОБЛ, чем у пациентов с МВ. Так, показатели Е/А ПЖ и Е/е’ ПЖ, составили 0,70±0,09 и 6,9±1,13 у пациентов из 2-й группы против 0,95±0,05 и 5,7±1,11 у пациентов из 1-й группы соответственно (р<0,01). Следует отметить, что ФСУ ПП у пациентов с ХОБЛ по сравнению с показателем у здоровых добровольцев проявляла тенденцию к статистически недостоверному снижению, а у больных МВ, напротив, к повышению. Амплитуда движения кольца трикуспидального клапана у больных МВ мало отличалась от контрольного значения, а у пациентов с ХОБЛ была существенно ниже.
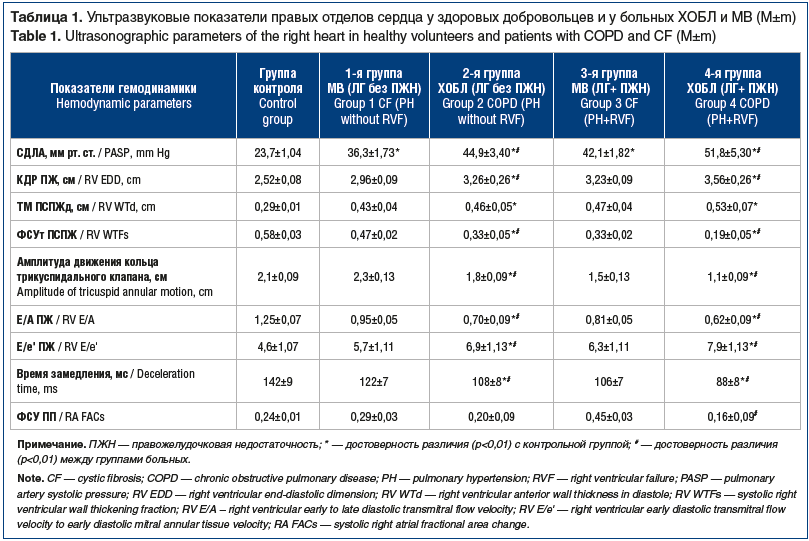
Как следует из таблицы 1, у больных ХОБЛ с сочетанием ЛГ и недостаточности ПЖ отмечались выраженные нарушения правожелудочковой гемодинамики, у пациентов с МВ эти нарушения выявлялись в меньшей степени. Так, расчетное СДЛА у больных ХОБЛ в 4-й группе было существенно повышено относительно нормальных значений, составив 51,8±5,3 мм рт. ст., у пациентов в 3-й группе СДЛА повышалось достоверно менее выраженно — до 42,1±1,82 мм рт. ст. (р<0,01 по сравнению с показателем у пациентов из 4-й группы). Сходные закономерности выявлены и относительно размеров ПЖ.
Наметившиеся у пациентов в первых двух группах проявления диастолической дисфункции миокарда были более выраженными у пациентов с признаками правожелудочковой недостаточности — в 3-й и 4-й группах, причем большая выраженность отмечалась у больных ХОБЛ, чем у пациентов с МВ. Так, у больных из 4-й и 3-й групп показатели Е/А ПЖ и Е/е’ ПЖ составили 0,62±0,09 и 7,9±1,13 против 0,81±0,05 и 6,3±1,11 соответственно (р<0,01).
ФСУ ПП у пациентов из 4-й группы по сравнению с контрольной группой оказалась существенно снижена (0,16±0,09 и 0,24±0,01 соответственно), а у больных из 3-й группы, напротив, повышена до 0,45±0,03. Амплитуда движения кольца ТК у больных из 4-й группы также снизилась в существенно большей степени, чем у пациентов из 3-й группы.
Таким образом, если у больных без существенной гипоксемии, гиперкапнии и хронической интоксикации резервные возможности миокарда ПЖ вполне достаточны, то у лиц с ЛГ, нарушенным газовым составом крови и хроническим воспалительным процессом в легочной ткани ПЖ испытывает повышенную нагрузку, а после исчерпания функциональных резервов происходит формирование хронического легочного сердца [12, 13]. Наблюдались и нарушения функции левого желудочка (ЛЖ) за счет десинхронии межпредсердной перегородки, которая может при этом становиться функционально как бы частью гипертрофированного и дилатированного ПЖ, что, в свою очередь, снижает фракцию выброса ЛЖ и также приводит к формированию левожелудочковой недостаточности [14].
Представленные данные свидетельствуют о том, что диастолическая функция ПЖ обладает меньшими компенсаторными возможностями, в отличие от систолической функции, и при неблагоприятных условиях нарушается в первую очередь [15, 16]. Такое нарушение процессов расслабления ПЖ, проявляющееся в виде более медленного снижения давления в нем, приводит к уменьшению максимальной скорости раннего диастолического наполнения и вызывает не только увеличение длительности, но и уменьшение скорости замедления кровотока в раннюю диастолу у пациентов с хронической патологией легких.
Динамика максимальных скоростей кровотока в фазу раннего и позднего диастолического наполнения E/A ПЖ свидетельствует о состоянии пред- и постнагрузки и позволяет судить об эластичности миокарда, т. е. о его жесткости и растяжимости, от которых зависит величина пассивного наполнения желудочка. Кроме того, изменение временных показателей в фазу быстрого наполнения желудочков позволяет определить скорость сокращения наружной косой и внутренней прямой мышц желудочка, что обеспечивает дальнейшее изменение формы и объема его полости, истончение стенки и степени развития присасывающей силы [17, 18]. К неблагоприятным факторам, вызывающим нарушение диастолической функции в виде замедления релаксации, увеличения жесткости стенок ПЖ, следует отнести хроническую гипоксемию, гиперкапнию, ацидоз, в анамнезе — длительную хроническую интоксикацию у больных ХОБЛ.
По-видимому, можно согласиться с авторами, считающими, что функциональное состояние ПЖ связано в большей степени с выраженностью артериальной гипоксемии и гиперкапнии, характером и длительностью инфекционно-токсических и аутоиммунных воздействий на миокард, а не непосредственно с уровнем давления в МКК [19, 20]. Нормальной компенсаторной реакцией на возрастание постнагрузки на ПЖ являлась тенденция к увеличению некоторых фракционных и скоростных показателей миокарда, сохранности амплитуды движения кольца трикуспидального клапана.
При хронической сердечной недостаточности выделяют два классических типа: систолический диагностируют при фракции выброса ЛЖ менее 45%, диастолический – при фракции выброса ЛЖ более 45%, наличии диастолической дисфункции ЛЖ и клинических признаков хронической сердечной недостаточности. Вероятно, у больных ХОБЛ может первоначально наблюдаться субклиническое снижение сократимости сердца с развитием диастолической дисфункции и относительно сохраненной фракцией изгнания, что следует учитывать при их терапевтическом ведении.
Результаты проведенного исследования показывают, что развитие гипертрофии и недостаточности ПЖ может наблюдаться при относительно невысоких величинах давления в ЛА, когда СДЛА не превышает 40–50 мм рт. ст., гипертрофия и дилатация нередко отмечались одновременно.
Еще одним актуальным вопросом для пациентов с ХОБЛ и сердечно-сосудистой патологией являются эффективность и безопасность использования комбинаций длительно действующих бронхолитиков. Объединенный анализ нескольких крупных исследований показал, что добавление олодатерола к тиотропию не связано с повышением риска сердечно-сосудистых нежелательных явлений, таким образом, комбинация тиотропия/олодатерола является подходящим вариантом терапии даже при наличии сердечно-сосудистых факторов риска [21]. Также в ретроспективном анализе применения комбинации тиотропия/олодатерола по сравнению с монотерапией в долгосрочной перспективе не наблюдалось увеличения ЧСС и систолического и диастолического АД [22]. Таким образом, терапия комбинацией тиотропия/олодатерола является эффективным и безопасным вариантом терапии для пациентов с ХОБЛ и сопутствующей сердечно-сосудистой патологией.
Заключение
Таким образом, правое предсердие у больных МВ способно компенсировать нарушения функции ПЖ. В условиях нарушения диастолической функции ПЖ происходит усиление сократительной способности правого предсердия, которое снижается лишь в фазе выраженной декомпенсации хронического легочного сердца. У больных МВ нарушения диастолической функции правых отделов сердца предшествуют расстройствам систолической функции. У пациентов с ХОБЛ в обеих группах определялись более существенные нарушения структуры и функции ПЖ. Компенсаторные возможности ПЖ и ЛЖ истощались, изменялось межжелудочковое взаимодействие, что создавало условия для прогрессирования сердечной недостаточности и развития хронического легочного сердца.
Благодарность
Редакция благодарит компанию «Берингер Ингельхайм» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgements
The technical edition is supported by Boehringer Ingelheim.
Сведения об авторах:
Титова Ольга Николаевна — д.м.н., профессор, директор НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0003-4678-3904.
Кузубова Наталия Анатольевна — д.м.н., заместитель директора НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0002-1166-9717.
Александров Альберт Леонидович — д.м.н., профессор, руководитель отдела НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0002-9246-5256.
Перлей Виталий Евгеньевич — д.м.н., профессор, ведущий научный сотрудник НИИ пульмонологии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0001-6292-3888.
Гичкин Алексей Юрьевич — к.м.н., врач функциональной диагностики НИИ хирургии ФГБОУ ВО ПСПбГМУ
им. И.П. Павлова Минздрава России; 197022, Россия, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8; ORCID iD 0000-0003-1127-0041.
Контактная информация: Кузубова Наталия Анатольевна, e-mail: kuzubova@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах и методах.
Конфликт интересов отсутствует.
Статья поступила 05.07.2021.
Поступила после рецензирования 28.07.2021.
Принята в печать 20.08.2021.
About the authors:
Olga N. Titova — Dr. Sc. (Med.), Professor, Director of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0003-4678-3904.
Nataliya A. Kuzubova — Dr. Sc. (Med.), Deputy Director of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0002-1166-9717.
Albert L. Aleksandrov — Dr. Sc. (Med.), Professor, Head of Division of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0002-9246-5256.
Vitaliy E. Perlei — Dr. Sc. (Med.), Professor, leading researcher of the Research Institute of Pulmonology, I.P. Pavlov First St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0001-6292-3888.
Aleksey Yu. Gichkin — C. Sc. (Med.), functional diagnostician of the Research Institute of Pulmonology, I.P. Pavlov First
St. Petersburg State Medical University; 6–8, Lev Tolstoy str., St. Petersburg, 197022, Russian Federation; ORCID iD 0000-0003-1127-0041.
Contact information: Nataliya A. Kuzubova, e-mail: kuzubova@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 05.07.2021.
Revised 28.07.2021.
Accepted 20.08.2021.
.
Информация с rmj.ru