Содержание статьи
Хроническая сердечная недостаточность с позиций эпидемиологии
Статистика сердечной недостаточности (СН) хорошо известна, и можно было бы в очередной раз не приводить ее цифры, если бы не тревожная тенденция к сохранению стабильно высокого процента больных с данной патологией. Обновленные Рекомендации Европейского общества кардиологов (European Society of Cardiology, ESC) по диагностике и лечению хронической СН (ХСН) 2021 г. [1] и Клинические рекомендации Минздрава России 2020 г., разработанные Российским кардиологическим обществом при участии Национального общества по изучению сердечной недостаточности и заболеваний миокарда и Общества специалистов по сердечной недостаточности [2], в очередной раз актуализировали данную проблему. Одной из новых позиций данных рекомендаций является введение категории больных с умеренно сниженной (промежуточной) фракцией выброса (ФВ) левого желудочка (ЛЖ) в диапазоне 40–49%, что представляется весьма целесообразным с точки зрения своевременного выявления того пограничного контингента больных ХСН, которые имеют высокий риск перехода в группу с низкой ФВ (менее 40%).
Тем не менее результаты эпидемиологических исследований последних лет, равно как и данные статистики, свидетельствуют о высоком проценте больных ХСН со сниженной ФВ и высоким функциональным классом (ФК). Так, по данным исследований ЭПОХА-ХСН, ЭПОХА-Госпиталь-ХСН и ЭПОХА-Декомпенсация-ХСН, за последние годы распространенность ХСН в РФ выросла практически в 2 раза, количество пациентов с III–IV ФК возросло примерно в 4 раза, а общая смертность больных ХСН составила 25,1%. Таким образом, общее количество больных ХСН в России составляет на сегодняшний день около 5 млн человек [3].
Увеличение количества больных ХСН, несомненно, имеет объективные причины. Это, прежде всего, увеличение продолжительности жизни населения России и, как следствие, доли лиц пожилого и старческого возраста. Немаловажным фактором является также улучшение качества оказания медицинской помощи больным в острой стадии инфаркта миокарда и инсульта, что, в свою очередь, приводит к развитию у них более поздних осложнений, в частности ХСН. Бремя СН для российского общества обусловлено крайне неблагоприятным прогнозом для больных, высокой степенью летальности, высокой частотой госпитализации, что с экономической точки зрения резко увеличивает затраты на лечение и реабилитацию данного контингента больных [4].
Хроническая сердечная недостаточность в свете национальных рекомендаций 2020 г.
В соответствии с национальными рекомендациями 2020 г. СН определяется клинически как синдром, при котором пациенты имеют типичные жалобы (одышка, отеки лодыжек, усталость) и симптомы (повышенное давление в яремной вене, хрипы в легких, периферические отеки), вызванные нарушением структуры и/или функции сердца, что приводит к уменьшению сердечного выброса, и/или повышению внутрисердечного давления в покое или во время нагрузки.
Одна из основных классификаций ХСН базируется на величине ФВЛЖ, в соответствии с которой, как указывалось выше, в настоящее время выделяют 3 категории больных: с сохраненной, промежуточной (средней) и сниженной ФВ (табл. 1) [2].
![Таблица 1. Диагностические критерии ХСН с различными ФВЛЖ [2] Таблица 1. Диагностические критерии ХСН с различными ФВЛЖ [2]](https://medblog.su/wp-content/uploads/2021/12/lechenie-otechnogo-sindroma-u-bolnyh-hronicheskoj-serdechnoj-nedostatochnostyu-uspehi-est-no-problemy-ostayutsya-drobotya-n-v-kaltykova-v-v-pirozhenko-a-a.png)
Расширение представлений о патогенезе ХСН позволяет в настоящее время использовать в лечении больных как традиционные, так и новые препараты, эффективность которых подтверждена результатами многоцентровых клинических исследований и проспективных наблюдений [5–7]. К ним прежде всего относятся нейрогуморальные антагонисты ренин-ангиотензин-альдостероновой (РААС) и симпатоадреналовой (САС) систем, антагонисты минералокортикоидных рецепторов (АМКР), патогенетическая эффективность которых широко обсуждается в литературе [8–10]. Данные препараты имеют большую доказательную базу, свидетельствующую об их способности к улучшению прогноза, увеличению продолжительности жизни и снижению количества госпитализаций у больных ХСН [11–13]. Следует также подчеркнуть возрастающую роль инвазивных и хирургических методов лечения данного контингента больных (сердечная ресинхронизирующая терапия, имплантация кардиовертера-дефибриллятора, трансплантация сердца и др.).
В целом же стратегия лечения ХСН базируется на комплексном подходе, который включает в себя активную титрацию базисной терапии и своевременное подключение хирургических методов, проведение мероприятий по физической и психологической реабилитации с обязательным вовлечением родственников на всех этапах лечения [14].
Современные подходы к лечению отечного синдрома при декомпенсации ХСН
В то же время при декомпенсации ХСН на первый план выходят проявления отечного синдрома — периферические отеки, застой в малом круге кровообращения, одышка, которые требуют эффективной симптоматической терапии. Патогенез отеков при СН представлен на рисунке 1.
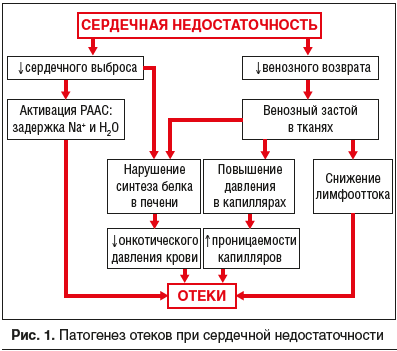
Сердечная недостаточность развивается вследствие снижения сердечного выброса и уменьшения венозного возврата, что приводит к активации РААС, задержке натрия и воды в организме. В свою очередь, уменьшение венозного возврата сопровождается венозным застоем в тканях, повышением давления в капиллярах, снижением лимфооттока и повышением проницаемости капилляров. Параллельно происходит нарушение синтеза белка в печени и снижение онкотического давления крови. Совокупность вышеперечисленных патологических процессов в конечном итоге проявляется формированием отеков.
Симптомы СН, обусловленные задержкой жидкости, служат предикторами риска госпитализации в течение 1 мес. и существенно ухудшают прогноз и качество жизни больного. Соответственно, одним из основных компонентов лечения пациентов с декомпенсированной ХСН является дегидратация диуретическими препаратами, цель которой — скорейшее достижение эуволемического состояния с помощью положительного диуреза при минимуме побочных реакций [15]. Важным является и тот факт, что поддержание эуволемического состояния у больных ХСН во многом обеспечивает успешность терапии бета-блокаторами, ингибиторами ангиотензинпревращающего фермента, блокаторами рецепторов ангиотензина и АМКР.
Таким образом, как указывается в национальных клинических рекомендациях, грамотно скорректированная диуретическая терапия должна обеспечить достижение и поддержание «сухого веса» пациента с помощью адекватных доз препаратов.
В арсенале современного врача диуретики представлены несколькими классами: тиазидные (гидрохлоротиазид, индапамид, хлорталидон), петлевые (фуросемид, торасемид, буметанид (не зарегистрирован в РФ), этакриновая кислота (не зарегистрирована в РФ)), ингибиторы карбоангидразы (ИКАГ) (ацетазоламид) и калийсберегающие (спиронолактон, триамтерен).
В соответствии с рекомендациями алгоритм назначения диуретиков (в зависимости от тяжести ХСН) выглядит следующим образом:
I ФК — не лечить мочегонными (0 препаратов);
II ФК (без клинических признаков застоя) — малые дозы торасемида (2,5–5 мг) (1 препарат);
II ФК (с признаками застоя) — петлевые/тиазидные диуретики + спиронолактон 100–150 мг (2 препарата);
III ФК (поддерживающее лечение) — петлевые диуретики (лучше торасемид) ежедневно в дозах, достаточных для поддержания сбалансированного диуреза, + АМКР (25–50 мг/сут) + ИКАГ (ацетазоламид по 250 мг 3 р/сут в течение 3–4 дней 1 р / 2 нед.) (3 препарата);
III ФК (декомпенсация) — петлевые диуретики (лучше торасемид) + тиазидные + спиронолактон в дозах 100–300 мг/сут + ИКАГ (4 препарата);
IV ФК — петлевые диуретики (торасемид однократно или фуросемид 2 р/сут или в/в капельно в высоких дозах) + тиазидные + АМКР + ИКАГ (ацетазоламид по 250 мг
3 р/сут в течение 3–4 дней 1 р / 2 нед.) + при необходимости механическое удаление жидкости (5 препаратов/воздействий).
Сравнительная характеристика основных петлевых диуретиков — фуросемида и торасемида
Приведенный алгоритм отражает широкое использование петлевых диуретиков у больных ХСН различных ФК [16]. Следует отметить, что в течение длительного времени основным представителем петлевых диуретиков, активно применяемым в амбулаторной и стационарной практике, был фуросемид, который по-прежнему остается классическим препаратом сравнения при проведении рандомизированных клинических исследований.
Несмотря на отчетливо выраженное диуретическое действие, фуросемид обладает целым рядом побочных эффектов, хорошо известных кардиологам и терапевтам. К ним в первую очередь относятся рефлекторное стимулирование активности РААС в ответ на гиповолемию и нарушения электролитного баланса, которые могут стать самостоятельной проблемой у больного ХСН. Показано, в частности, что у пациентов, госпитализированных по поводу декомпенсации ХСН с нарушениями водно-солевого гомеостаза натрия и/или калия, при поступлении в стационар отмечается возрастание относительного риска годичной летальности в 1,43 раза к концу года наблюдения по сравнению с пациентами, имевшими нормальные уровни натрия и калия [17]. Кроме того, фуросемид не обладает способностью замедлять прогрессирование ХСН и улучшать прогноз больных [18, 19].
В настоящее время на первое место по частоте применения в клинической практике для лечения отечного синдрома у больных ХСН вышел торасемид, чьи преимущества подкреплены мощной доказательной базой [20–29].
Одно из ранних исследований, в котором в сравнительном аспекте были продемонстрированы преимущества торасемида перед фурасемидом, было исследование, проведенное M.D. Murray et al. [20]. Исследователями установлено, что у пациентов, получавших торасемид, по сравнению с пациентами, получавшими фуросемид, частота госпитализаций по поводу ХСН была на 15% ниже (39 (32%) в группе торасемида по сравнению с 19 (17%) в группе фуросемида, p<0,01), так же как и частота госпитализаций по поводу всех сердечно-сосудистых причин (71 (59%) и 50 (44%) соответственно, р<0,03). Кроме того, в группе пациентов, получавших торасемид, суммарная продолжительность дней госпитализации была значительно меньше, чем в группе фуросемида, — 106 дней по сравнению с 296 днями (р<0,02). При этом принципиально важно помнить общеизвестный факт, что каждая повторная госпитализация приближает пациента с ХСН к фатальному исходу.
Торасемид был разработан и внедрен в международную клиническую практику в начале 1990-х годов [30, 31].
В известном, уже ставшем классическим, исследовании TORIC (TORasemide in Congestive heart failure), включавшем около 2000 пациентов, торасемид продемонстрировал способность не только снижать клинические проявления ХСН, но и оказывать благоприятное влияние на прогноз [23]. В одном из первых крупных российских исследований ДУЭЛЬ-ХСН, в котором оценивались эффективность и безопасность лечения пациентов с декомпенсированной СН, показано, что лечение торасемидом позволяет быстрее достичь компенсации состояния [24].
Механизм действия торасемида хорошо известен: в его основе лежит обратимое связывание с ко-транспортером Na+/2Cl—/K+, расположенным в апикальной мембране толстого сегмента восходящей петли Генле, в результате чего снижается или полностью ингибируется реабсорбция ионов натрия, что приводит к уменьшению осмотического давления внутриклеточной жидкости и реабсорбции воды. Однако анализ данных литературы позволяет расширить представления о торасемиде как о классическом петлевом диуретике. Доказано, что торасемид обладает целым рядом дополнительных свойств, связанных с возможностью блокады РААС, отчетливыми антиадренергическими и антиальдостероновыми механизмами действия [25, 26]. В частности, в исследовании B. Lopez et al. [25] было впервые показано, что длительное лечение различными петлевыми диуретиками может оказывать неодинаковое влияние на фиброз миокарда у пациентов с ХСН, поскольку у пациентов, получавших торасемид, наблюдалось снижение маркеров фиброза – накопления коллагена в миокарде и синтеза коллагена I типа по сравнению с пациентами, получавшими фуросемид. Авторы предположили, что торасемид может обладать дополнительными кардиорепаративными свойствами, сродни эффектам ингибиторов ангиотензинпревращающего фермента, или антагонистов рецепторов ангиотензина, или β-блокаторов у больных ХСН. Последние, в свою очередь, позволяют нивелировать такие негативные эффекты альдостерона, как фиброз миокарда и сосудов, потеря электролитов (К+, Mg2+), что и обеспечивает, очевидно, улучшение прогноза и качества жизни пациентов [27, 28].
С позиций наличия дополнительных положительных эффектов торасемида трактуют, в частности, результаты своего исследования «ТРИОЛЯ» и Ф.Т. Агеев с соавт. [29]. Ими показано, что диуретическая терапия больных ХСН как торасемидом, так и фуросемидом является успешной, однако клинико-гемодинамическая эффективность торасемида существенно выше, чем у фуросемида, что, с точки зрения авторов, связано с наличием у торасемида антиальдостероновых механизмов влияния на функцию сердца, в т. ч. на процессы синтеза коллагена I типа.
При этом указанными преимуществами обладает именно торасемид немедленного высвобождения, в то время как антифибротические эффекты торасемида замедленного высвобождения (торасемид-PR) сопоставимы с эффектами фуросемида [32].
Немаловажным является тот факт, что торасемид превосходит фуросемид по длительности эффекта и имеет лучшую биодоступность.
Перспективы оптимизации диуретической терапии
Сейчас торасемид выпускается в дозировках 2,5 мг, 5 мг и 10 мг. Дозировка 10 мг применяется для коррекции отечного синдрома, в первую очередь у больных ХСН. В то же время клиническая практика свидетельствует о том, что в подавляющем большинстве случаев декомпенсированным больным требуется значительное увеличение суточной дозы препарата. При этом суточные дозы торасемида 10–20 мг считаются малыми, 20–40 мг — средними, ≥40 мг — большими. В случае необходимости в соответствии с инструкцией по медицинскому применению препарата доза может быть увеличена до 100–200 мг/сут в 1–2 приема. Максимальная суточная доза при застойной СН составляет 200 мг/сут.
При этом, как отмечают ведущие кардиологи, в нашей стране наблюдается негативная тенденция к применению малых доз торасемида, что обусловливает возникновение проблемы недостижения адекватного суточного диуреза у больных с высоким ФК ХСН [33]. Это, в свою очередь, приводит к нарушению водно-электролитного гомеостаза организма, увеличивает пред- и постнагрузку на сердце, усугубляет систолическую и диастолическую дисфункцию миокарда ЛЖ, способствуя, таким образом, прогрессированию ХСН и усугублению ее симптомов [34].
Вне всякого сомнения, эта проблема во многом связана с определенной терапевтической инерцией, которая находит отражение в недостаточной титрации дозы препарата врачами, особенно на уровне амбулаторно-поликлинического звена, и, как следствие, в недостижении оптимального медикаментозного эффекта.
Другим аспектом данной проблемы является снижение комплаентности больного при увеличении количества принимаемых препаратов (рис. 2) [35].
![Рис. 2. Снижение комплаентности пациентов при увеличении количества принимаемых препаратов [34] Рис. 2. Снижение комплаентности пациентов при увеличении количества принимаемых препаратов [34]](https://medblog.su/wp-content/uploads/2021/12/1640483954_437_lechenie-otechnogo-sindroma-u-bolnyh-hronicheskoj-serdechnoj-nedostatochnostyu-uspehi-est-no-problemy-ostayutsya-drobotya-n-v-kaltykova-v-v-pirozhenko-a-a.png)
В многочисленных исследованиях показано, что максимальная комплаентность наблюдается при приеме больными 1–2 препаратов (от 85% до 100%). При приеме 3 препаратов несоблюдение режима терапии отмечается уже у 30% больных, 4 препаратов — у 40%, 6 препаратов — у 55% больных. Практически все больные не соблюдают режим терапии, если они должны принимать
7 и более препаратов.
По данным различных авторов, низкая приверженность лечению встречается в среднем у 20% больных ХСН, в то время как их высокая комплаентность является наиболее важным компонентом лечебных программ, особенно в старшей возрастной группе, и в последние годы расценивается как самостоятельный фактор риска прогрессирования ХСН [36].
Представители практического здравоохранения нередко сталкиваются с той ситуацией, когда декомпенсированному больному ХСН требуется назначение до 6–10 таблеток торасемида в сутки помимо препаратов основных классов, которые в обязательном порядке должны быть назначены таким пациентам, вне зависимости от выраженности отечного синдрома. Одним из оптимальных вариантов решения проблемы гипергидратации и недостаточной комплаентности может явиться применение таблеток торасемида в уникальной большой дозировке 20 мг.
Заключение
В настоящее время увеличение продолжительности жизни населения РФ является одним из приоритетных направлений дальнейшего развития социальной политики государства. Однако увеличение продолжительности жизни подразумевает и обязательное сохранение ее качества у лиц пожилого и старческого возраста. С учетом того, что когорта больных ХСН представлена преимущественно этим возрастным контингентом, в настоящее время значительно возрастает актуальность поиска различных способов оптимизации лечения больных с декомпенсацией ХСН. Диуретики остаются основным классом препаратов, применяемых для лечения отечного синдрома у данного контингента больных. Эффективно используемым петлевым диуретиком с антиальдостероновым, антиадренергическим эффектами и способностью улучшать прогноз при ХСН является торасемид.
Однако вынужденный прием большого количества таблеток и, как следствие, снижение комплаентности терапии не позволяли максимально эффективно использовать торасемид в реальной клинической практике. Другой стороной проблемы является назначение меньших доз, чем это необходимо для полноценного терапевтического эффекта торасемида.
Появление в арсенале врача уникальной в России на сегодняшний день дозировки – 20 мг торасемида (Тригрим) в 1 таблетке в значительной мере способствует решению данной проблемы. Широкая интеграция в схему терапии пациентов с ХСН петлевого диуретика торасемида в дозировке 20 мг позволит не только лучше контролировать отечный синдром у пациентов с застойной СН, но и снизить частоту и продолжительность госпитализаций, тем самым значимо улучшить прогноз у данной группы пациентов.
Благодарность
Редакция благодарит АО «Акрихин» за оказанную помощь в технической редактуре настоящей публикации.
.
Информация с rmj.ru






