Комплексное лечение тоннельных невропатий тазового пояса при патологии поясничного отдела позвоночника
А. Н. Баринов, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Пациенты, обращающиеся за медицинской помощью в связи с периодически возникающим асимметричным онемением и/или парестезиями в тазовой области и/или ногах, в большинстве случаев страдают тоннельными невропатиями: компрессией и нарушением микроциркуляции периферических нервов в анатомически узких фиброзных и фиброзно-костных каналах (тоннелях). Тоннельные невропатии, относящиеся по классификации к мононевропатиям, составляют 1/3 поражений периферических нервов и часто наблюдаются на фоне эндокринных заболеваний (сахарный диабет, гипотиреоз, акромегалия), заболеваний суставов (деформирующий остеоартроз, ревматоидный артрит, подагра), объемных образований самих нервов (шваномма, неврома) и вне нерва (саркома, липома), депозитарных невропатий (амилоидоз), при наследственной склонности к параличам от сдавления, а также при некоторых физиологических изменениях гормонального статуса (беременность, климакс). Около половины таких больных имеют сочетанное поражение нервных стволов помимо дистального еще и на проксимальном уровне: аксоплазматический ток скомпрометирован вследствие дискорадикулярного конфликта, что облегчает возникновение тоннельных невропатий и обозначается в литературе как «синдром двойного аксоплазматического сдавления» (double crush syndrome). Как будет показано ниже, аксоплазматическое сдавление может быть не только двойным, но и тройным, и даже более. Именно поэтому уместнее употреблять термин «множественное аксоплазматическое сдавление» — МАС-синдром. Выявление МАС-синдрома позволяет снизить гипердиагностику спондилогенных радикулопатий и избежать необоснованных нейрохирургических вмешательств на позвоночнике. С другой стороны, понимание роли спондилогенного фактора в развитии периферических тоннельных невропатий дает возможность применения патогенетически обоснованных методов лечения, направленных на восстановление аксоплазматического тока за счет купирования дискорадикулярного конфликта или устранения сдавления проксимальных отделов нерва в составе сосудисто-нервных сплетений.
Существует ряд теорий, объясняющих причину возникновения тоннельных невропатий: дисметаболическая, воспалительная, гормональная, сосудистая, механическая, аномалийная, функциональная и многие другие, однако ни одна из них не может претендовать на роль всеобъемлющей. Вероятно, следует говорить о мультифакториальной природе тоннельных невропатий: для развития данного заболевания необходима генетическая предрасположенность, а для проявлений его — воздействие различных средовых факторов: экзогенных и эндогенных.
К эндогенным относят анатомические варианты строения костей и связок, а также периферических нервов; особенности функционирования двигательного аппарата; сопутствующие эндокринные и метаболические расстройства. К экзогенным — механические и инфекционные факторы.
Во всех существующих теориях развития тоннельных невропатий фигурируют два фактора: декомпенсация в трофических системах нерва (нарушение аксоплазматического тока, кровоснабжение vasae nervorum) и локальные микротравмы периферических нервов. Известно, что по наследству могут передаваться как недостаточность трофических систем периферических нервов, так и узость фиброзно-костных каналов (за счет особенностей строения и двигательного стереотипа). По этой причине неудивительно частое выявление больных тоннельными невропатиями в отдельных семьях с наличием соответствующей патологии.
Патогенез механического поражения периферических нервов достаточно хорошо изучен: особенностью периферических нервов является их устойчивость к изменениям длины — они приспосабливаются к выраженным изменениям положения конечностей с помощью скользящих движений нерва в ложе. Эта адаптация осуществляется вследствие высокоамплитудных, недифференцированных движений, во время которых нерв перемещается внутри ограниченного тоннеля, производя экстраневральное движение. При интраневральных движениях отдельный пучок скользит относительно других в пределах нерва. Патологические процессы, такие как наличие крови в эпиневральном пространстве, отек ложа нерва или интраневрального пространства, а также разволокнение или утолщение в тоннеле окружающей нерв фиброзной ткани (например, при коллагенозах, стенозирующем лигаментите), могут нарушать работу этого механизма. Движения конечностей при этом обусловливают значительный рост напряжения проксимальнее и дистальнее области патологических изменений. Диаметр нерва уменьшается, и интраневральное давление возрастает. Если интраневральное давление превышает давление в эпиневральных артериолах, наступает преходящая ишемия нервных волокон. Это может приводить к формированию отека, усилению воспалительной реакции, нарастанию адгезии и к дальнейшему уменьшению объема скользящего движения нерва или росту напряжения. В нервных стволах, особенно в участках нерва, прилегающих к зоне стенозирования, образуются веретенообразные утолщения; в волокнах ствола происходят различные патоморфологические изменения (от демиелинизации до фрагментации осевых цилиндров и исчезновения аксонов).
Помимо патологии соединительной ткани, диаметр тоннелей, в которых находится нерв, могут существенно менять форсированные движения, стереотипные длительные тонические и статические позиции и привычные характерные позы (сидение в позе «нога на ногу», вызывающее компрессию малоберцового нерва; поза «на корточках», приводящая к микротравматизации 4-го межплюсневого нерва в канале Мортона и т. п.), что способствует возникновению ишемии нерва, особенно если он при этом подвергается компрессии в проксимальном отделе в связи с дисфункцией поясничного отдела позвоночника.
Таким образом, патогенез тоннельных компрессионно-ишемических невропатий включает: 1) увеличение объема периневральных тканей, 2) повышение тканевого давления внутри тоннеля, 3) нарушения кровообращения в компримированном участке, 4) гиперфиксацию нерва. Имеет значение изначальное состояние периферического нерва, подвергающегося компрессии, — тоннельные невропатии легче возникают в случаях, когда аксональные транспортные системы уже скомпрометированы в проксимальном отделе (синдром множественного аксоплазматического сдавления при плексопатии или радикулопатии) или дистально (полиневропатии или множественные мононевропатии) на фоне дефицита аксоплазматического тока и нейротрофических факторов, требующихся для регенерации аксона. При обсуждении патогенеза МАС-синдрома необходимо учитывать не только дискогенное поражение корешков спиномозговых нервов, но также миофасциальные и мышечно-тонические синдромы, вызывающие компрессию сосудисто-нервных стволов. В их генезе указывается на «рассогласование деятельности» волокон в мышце и болезненное сокращение отдельных ее пучков при выполнении неподготовленного движения. Определенная роль в патогенезе мышечно-тонических синдромов отводится «рефлекторным» механизмам — повышению возбудимости сегментарных спинальных структур в ответ на афферентную импульсацию от раздражения рецепторов синувертебрального нерва в области пораженного диска. К другим рефлекторным механизмам, приводящим к формированию мышечно-тонического синдрома, относятся так называемые «висцеромоторные» реакции в виде спазма мышцы в миотоме, соответствующем афферентации от пораженного внутреннего органа («висцеросоматический» рефлекс).
Именно поэтому у каждого конкретного больного для уточнения механизмов патогенеза тоннельного синдрома и подбора оптимальной тактики терапии необходимо учитывать острые, подострые и хронические повреждения на всех возможных уровнях периферической нервной системы, «проявляющие» наследственную или приобретенную узость фиброзно-костного канала.
Клинические проявления тоннельных невропатий включают симптомы нарушения сенсорных, вегетативно-трофических (если нерв смешанный, то и моторных) функций с возможными невропатическими болями в зоне, иннервируемой пораженным нервом, а также ноцицептивными болями в области компрессии нерва — болезненность при поколачивании, растяжении, давлении (статическая гипералгезия). Эти симптомы могут усиливаться после физической нагрузки или в ночное время в связи с нарушением кровоснабжения нерва в области тоннеля. Клинические проявления невропатического болевого синдрома включают симптомокомплекс спонтанных и стимулзависимых болей в зоне иннервации периферического нерва дистальнее зоны тоннельной компрессии. Интенсивные стреляющие, дергающие боли обычно возникают в виде пароксизмов и не бывают постоянными, в то время как жгучие, ноющие боли могут быть постоянными и периодически весьма высокой интенсивности. Во многих случаях боли усиливаются при физической активности, длительной статической нагрузке или охлаждении. Спонтанные боли сопровождаются, как правило, стимулзависимыми болями — аллодинией, статической и динамической гипералгезией. В дебюте заболевания позитивная неврологическая симптоматика (боли, парестезии и онемение) преобладают над симптомами выпадения (негативной невропатической симптоматикой), которые появляются снижением чувствительности различных модальностей, а при вовлечении двигательных волокон — гипорефлексией, слабостью и атрофией мышц. Однако дефицитарные двигательные расстройства встречаются достаточно редко. Чаще всего при МАС-синдроме пациенты жалуются на боли в позвоночнике или в мышцах тазового пояса, варьирующие по выраженности от легкого дискомфорта до высокой интенсивности, которые значительно уменьшаются после отдыха, растирания, разминания и растягивания мышцы. Визуально можно определить изменение контура, «выбухание» мышцы, которая при пальпации может иметь каменистую плотность. Произвольные движения с вовлечением спазмированной мышцы (например, грушевидной) совершаются в неполном объеме из-за выраженной боли. Хроническое течение мышечно-тонических синдромов чаще всего отмечается в тех мышцах, которые испытывают постуральные перегрузки, например, при асимметрии конечностей, таза, выраженном сколиозе, патологии внутренних органов. Боль в этих случаях бывает, как правило, слабой или умеренной интенсивности. Пациенты предъявляют жалобы на ощущение дискомфорта, чувство тяжести после физической нагрузки, которые уменьшаются после разминания мышцы, ее согревания. Болезненность в мышце определяется при ее активном сокращении и обычно отсутствует при растяжении. При компрессии сосудисто-нервных образований при мышечно-тонических синдромах могут возникать иррадиация боли в конечность, а также двигательные, чувствительные и вегетативные нарушения, локализующиеся в зоне иннервации и васкуляризации компримированных нервных и сосудистых образований в рамках МАС-синдрома. При вовлечении артерий и вен возможно развитие сосудистых расстройств, что проявляется побледнением, снижением локальной температуры или появлением цианоза и отечности в области поражения. Однако при изолированном поражении нерва сосудистые и трофические изменения тоже возможны за счет вовлечения автономных волокон, хотя выражены они чаще всего незначительно.
Локализация нарушений чувствительности при всей их топографической типичности весьма варьирует у разных пациентов вследствие преморбидных вариантов сенсорной иннервации кожи, существования зон перекрытия смежными нервами, а также нередкой асимметричности компрессии нервного ствола. То же самое можно сказать и о мышечной слабости, которая нередко носит анталгический, а иногда и психогенный характер. В силу деликатности или непостоянства объективных признаков повреждения нерва, традиционное неврологическое исследование должно быть дополнено специальными клиническими тестами, провоцирующими парестезии и боли, направленными на поиск места компрессии:
- Тест Тинеля — при перкуссии в зоне повреждения над проекцией нерва появляются боли и/или парестезии в области иннервации нерва, дистальнее места перкуссии.
- Тест пальцевой компрессии Гольдберга — аналогично тесту Тинеля производится сдавление большим пальцем или локтем на протяжении 1 минуты седалищного нерва в проекции грушевидной мышцы и т. д. В ответ возникают парестезии и боли по ходу компримированного нерва.
- Турникетный (манжеточный) тест — проксимальнее места предполагаемой компрессии нерва (на бедре или голени) накладывают манжету тонометра и повышают в ней давление до уровня обычного систолического или слегка выше его. Выжидают 1 мин. При наличии тоннельного синдрома появляются парестезии в зоне иннервации компримированного нерва. Этот тест может быть использован и для суждения о степени тяжести заболевания, если измерять время от начала манжетной компрессии до появления парестезии. С равным успехом применим он для контроля за эффективностью лечения.
- Тест поднятия конечностей (элевационный) — при невропатиях ног в положении лежа поднимается поочередно на 1 минуту выпрямленная одна, а затем другая нога. Вследствие уменьшения гидростатического давления в артериях конечностей нарушается кровоснабжение нервов и возникают парестезии.
- Тест форсированных максимальных по объему пассивных движений — выбирают такое направление движения, при котором пораженный нерв оказался бы в еще большей степени компрессии и добавочного натяжения. При подозрении на синдром грушевидной мышцы выполняют пробу Бонне — в положении лежа на животе согнутую в колене ногу отводят в сторону, растягивая грушевидную мышцу, появление боли и парестезий по ходу седалищного нерва свидетельствует о его компрессии в подгрушевидном пространстве. При мералгии Бернгардта–Рота применяют обратный симптом Ласега — переразгибание бедра вызывает тракционную боль в проекции латерального кожного нерва бедра. Механизм всей этой группы пассивных провоцирующих движений, по существу, может быть отнесен к тракции нерва, нередко дополняемой и его гиперангуляцией и компрессией.
Не все вышеописанные тесты бывают положительными даже на поздних стадиях тоннельных невропатий. Поэтому для точной диагностики поражения периферических нервов и наличия МАС-синдрома при дисфункции поясничного отдела позвоночника, определяющей стратегию терапии, необходимо точное знание особенностей наиболее типичных тоннельных синдромов тазового пояса и ног и их связи с корешками спинномозговых нервов.
К тоннельным синдромам тазового пояса относятся:
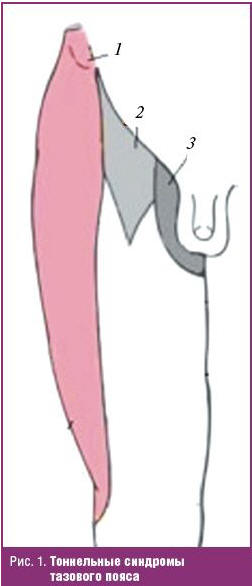
- Парестетическая мералгия Бернгардта–Рота (L2-L3): невропатия наружного кожного нерва бедра вследствие компрессии в тоннеле под паховой (пупартовой) связкой либо на уровне передней верхней ости подвздошной кости (избыточное отложение жира, ношение тугого пояса и др). Проявляется болями и чувствительными нарушениями на переднебоковой поверхности бедра, иногда сопровождающимися нарушением потоотделения и роста волос. Симптом Гольдберга положителен при пальпации паховой складки на 2–3 пальца медиальнее передней верхней ости подвздошной кости (рис. 1).
- Компрессионно-тракционная невропатия подвздошно-пахового нерва (L1) вследствие перерастяжения и компрессии нервов в межмышечных слоях нижних частей брюшной стенки и в области внутреннего отверстия пахового канала паховой грыжей или спаечным процессом после ее удаления. Проявляется болевым синдромом в паховой зоне, иррадиирующим по верхневнутренней поверхности бедра, усиливающимся при напряжении брюшной стенки, а также эректильной дисфункцией у мужчин (в последнем случае этот синдром называется в честь описавших его в 1956 г. невролога Е. Е. Гольдберга и уролога Р. Д. Амеляра). Характерна семенящая походка с наклоном вперед, боль уменьшается при сгибании бедра с ротацией внутрь. При вовлечении в процесс подвздошно-подчревного нерва (Th12-L1) характерны боли в области крестцово-подвздошного сочленения, имитирующие сакроилеит (рис. 1).
- Синдром Мейджи–Лайона — тракционная невропатия бедренно-полового нерва (L1-L2) в месте его перегиба через крестцово-остистую связку или седалищную ость. Проявляется болями в аногенитальной и ягодичной области и на передневнутренней поверхности верхней трети бедра, усиливающимися при ходьбе, в положении сидя, при дефекации. Проба на растяжение крестцово-остистой связки (приведение согнутого бедра к противоположному плечу) провоцирует боль (рис. 1). Каузалгию паховогенитальной зоны (синдром Мументалеров) большинство зарубежных авторов относят к психосоматической патологи.
- Промежностная невралгия (S2-S4) или синдром велосипедиста — компрессия внутреннего срамного нерва в ишиоректальной ямке между седалищной костью и внутренней запирательной мышцей в канале д’Алкока. При одностороннем поражении характерны боли и чувствительные нарушения в промежности, усиливающиеся в положении стоя, эректильная дисфункция. При двустороннем поражении присоединяются нарушения функции наружных сфинктеров.
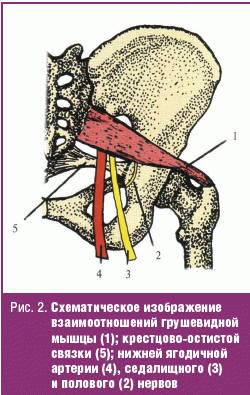
- Синдром грушевидной мышцы — компрессия седалищного нерва (L4-S3) между грушевидной мышцей и крестцово-остистой связкой проявляется болевым синдромом преимущественно по задней поверхности ноги, чувствительными и двигательными нарушениями в области иннервации большеберцового и малоберцового нервов. Характерна положительная проба Бонне (см. выше). Это один из самых частых тоннельных синдромов тазового пояса, встречающихся в практике вертеброневрологов (рис. 2).
- Cиндром запирательного канала — компрессия запирательного нерва (L2-L4) в запирательном канале за счет фиброза, остефитов лонных костей, грыжи канала, травматического отека мягких тканей проявляется болями и чувствительными нарушениями на внутренней поверхности коленного сустава (феномен Хаушипа–Ромберга), спазмами или парезом приводящих мышц бедра — при ходьбе в фазе, когда нога находится в воздухе, наблюдается избыточное отведение стопы.
- Компрессионная невропатия подкожного бедренного нерва (L1-L4) в «подпортняжном» или гунтеровском (Хантеровском) канале бедра проявляется болями и чувством тяжести в дистальной части бедра и голени, нарастающими при ходьбе, а также чувствительными нарушениями и снижением секреции потовых желез на внутренней стороне голени.
Для объективной оценки тяжести поражения и процессов восстановления функций нерва, особенно на ранних стадиях заболевания при отсутствии объективной неврологической симптоматики, применяются нейрофизиологические исследования: стимуляционная электронейромиография (ЭНМГ), количественное сенсорное тестирование. При ЭНМГ определяется снижение амплитуды и скорости проведения импульса по двигательным и чувствительным волокнам и увеличение резидуальной латенции в месте компрессии нерва и дистальнее.
Относительно новой, но весьма перспективной методикой оценки морфологических изменений в периферических нервах является ультразвуковая диагностика. Для ультразвуковых исследований используются датчики с частотой 7–17 МГц. Изображение нерва имеет ряд характерных признаков: в поперечной проекции он выглядит как овальное или округлое образование с четким гиперэхогенным контуром и внутренней гетерогенной упорядоченной структурой («соль — перец», «медовые соты»), а в продольной проекции нерв лоцируется в виде линейной структуры с четким эхогенным контуром, в составе которой правильно чередуются гипо- и гиперэхогенные полосы — «электрический кабель». В процессе сканирования оценивают анатомическую целостность нервного ствола, его структуру, четкость контуров нерва и состояние окружающих тканей. Метод ультразвуковой диагностики позволяет не только выявлять объемные новообразования (шванномы, невриномы и т. п.), вызывающие повреждение нерва, но и оценивать подвижность нерва в тоннеле при динамических пробах, наличие рубцово-спаечных изменений, воспалительного отека или, наоборот, атрофии нерва при сопоставлении с нервом интактной конечности. Данные ультразвуковой диагностики полезны для определения тактики терапии: невролиза — при спаечном процессе, патогенетического воздействия на процессы реиннервации — при атрофии, блокад с глюкокортикоидами — при воспалительном отеке, блокад с анестетиками и нестероидными противовоспалительными средствами (НПВС) (раствор 8 мг Ксефокама с 4 мл 2% Лидокаина или 5 мл 0,5% Новокаина) в миофасциальные триггеры в структуре МАС-синдрома или в «заинтересованные» мышцы (например, в грушевидную). Кроме того, ультразвуковой контроль малоинвазивных лечебно-диагностических воздействий (параневральных и паравертебральных блокад) позволяет проводить их с максимальной точностью, а следовательно — эффективностью.
В целях проверки диагностического предположения о наличии компрессии нерва ex juvantibus используются блокады с местными анестетиками параневрально в точки наибольшей болезненности («ловушечный пункт») или в точки предполагаемого сдавления, находимые по топографическим ориентирам. Купирование парестезии и болей свидетельствует о том, что диагноз поставлен правильно. Проба отличается высокой чувствительностью при условии точного выполнения техники блокады, но не самой высокой специфичностью. Плацебо-эффект блокад при синдроме психогенных акропарестезий исключается при использовании 0,9% раствора NaCl вместо анестетика.
Для того чтобы лечение тоннельного синдрома было эффективным, необходимо понять причину и механизмы возникновения компрессии и применить комплексный подход к терапии. Радикальным методом лечения большинства тоннельных синдромов является оперативное вмешательство, которое заключается в рассечении тканей, сдавливающих нерв, и в создании оптимальных условий для нервного ствола, предупреждающих его травматизацию. Наличие грубых выпадений двигательных и чувствительных функций, быстрое нарастание симптоматики с развитием контрактур является абсолютным показанием к операции. Однако в подавляющем большинстве случаев прибегнуть к операции больных вынуждает безуспешность консервативного лечения, а не абсолютные показания, что особенно часто наблюдается при МАС-синдромах, когда источник проксимальной компрессии нерва не установлен и не подвергается терапевтическому воздействию.
С позиции клинической практики необходимо заметить, что даже задержка восстановительных процессов в нерве в течение нескольких месяцев не является показанием к оперативному лечению, так как в подавляющем числе наблюдений проводимая больным консервативная терапия не адекватна ни этиологической предиспозиции, ни патогенетическим механизмам развития компрессии нерва. Прежде всего, для успешной консервативной терапии необходима фиксация конечности в функционально-выгодном положении — необходимо прекратить физическое воздействие в области компрессии. Для этого существуют специальные ортопедические приспособления: ортезы, бандажи, лангеты, которые позволяют добиться иммобилизации именно в зоне повреждения. При наличии МАС-синдрома необходимо воздействие на всех уровнях поражения аксональных транспортных систем, в том числе и на вертебральном, что также может требовать введения в триггерные зоны «заинтересованных» мышц, компримирующих сосудисто-нервные стволы, растворов анестетика (2% Лидокаина или 0,5% Новокаина) и 8 мг Ксефокама путем локальных инфильтраций (блокад). Показана также эффективность курса сакральных эпидуральных блокад с использованием раствора 8 мг Ксефокама в 16 мл 0,25% Лидокаина в качестве патогенетической терапии дискорадикулярного конфликта в структуре хронических радикулопатий, играющих ключевую роль в развитии МАС-синдрома (рис. 3).
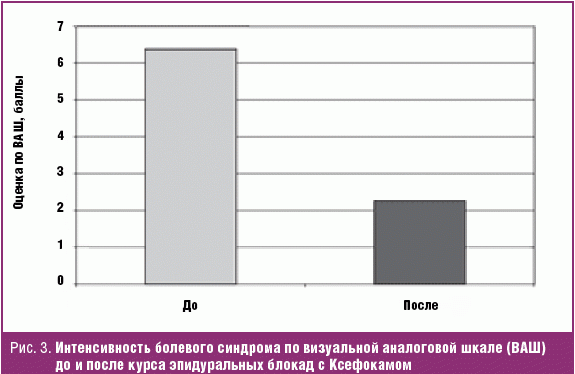
Вторым направлением успешного консервативного лечения тоннельных невропатий и профилактики возникновения последующих тоннельных синдромов является этиотропная терапия, направленная на восстановление нарушенного метаболизма в поврежденном нерве при эндокринных, инфекционных и дизимунных поражениях периферической нервной системы.
Самым коротким и действенным путем для купирования боли при наличии у врача необходимых манипуляционных навыков являются медикаментозные блокады. Инъекции глюкокортикоидов непосредственно в соответствующие каналы или ткани, окружающие нерв, являются методом патогенетического лечения тоннельных невропатий. Применение глюкокортикоидов обосновано противовоспалительным и противоотечным действием непосредственно в тканях, в которые они вводятся, а также ремиелинизирующим действием при локальных аутоиммунных поражениях периферических нервов. Однако необходимо учитывать и возможное системное действие гормонов, поэтому в начале терапии целесообразно применение растворов короткодействующих глюкокортикоидов для оценки не только эффективности, но и безопасности этого вида лечения, а при отсутствии значимых побочных явлений (отеки, дисменорея, неконтролируемая гипергликемия и/или артериальная гипертензия и т. п.) и в случае недостаточной эффективности препаратов короткого действия возможно осторожное применение микрокристаллических суспензий. Альтернативной методикой являются компрессы с Димексидом (5,0 мл), анестетиками (2 мл 0,5% Новокаина или 2% Лидокаина), глюкокортикоидами (2 мл суспензии гидрокортизона) или НПВС (8 мг лиофилизата Ксефокама) и витаминами группы В (раствор Нейробиона 3 мл) на 20–30 минут в области повреждения нерва.
Для симптоматической терапии невропатического болевого синдрома при тоннельных невропатиях применяются антиконвульсанты, трициклические антидепрессанты и трансдермальные системы с Лидокаином. Антидепрессанты повышают активность эндогенной подавляющей боль (антиноцицептивной) системы мозга за счет повышения концентрации ключевого нейромедиатора антиноцицептивной системы — норадреналина. Антиконвульсанты со своей стороны эффективно «успокаивают» расторможенные ноцицептивные структуры головного и спинного мозга, подавляя периферическую и центральную сенситизацию, являющуюся основным патогенетическим механизмом формирования невропатической боли при поражении периферических нервов.
Для патогенетической терапии тоннельных невропатий в зависимости от преобладающих механизмов поражения нервов также могут применяться антиоксиданты (альфа-липоевая кислота), ингибиторы холинестеразы (Прозерин, Ипидакрин), вазоактивные препараты (Пентоксифиллин, гингко билоба и др.), репаранты (Солкосерил, Актовегин). В качестве физиотерапевтических мероприятий наиболее эффективны массаж дистальнее и проксимальнее места компрессии, ультразвук с глюкокортикоидами на область компрессии, электрофорез с лидазой и ударно-волновая терапия высокой частоты и низкой интенсивности. Используются методики мануальной терапии (неоперативный невролиз), позволяющие воздействовать на механизм гиперфиксации нерва за счет уменьшения рубцово-спаечного процесса в тоннеле.
Для активации регенеративных процессов в периферических нервах успешно применяется нейротропный комплекс, содержащий большие дозы витаминов группы В (В1, В6, B12). Эффективность комбинированного препарата Нейробион для парентерального введения (В1 — 100 мг, В6 — 100 мг, В12 — 1 мг) изучалась с помощью ретроспективного анализа (S. Worschhauser и соавт.) 1082 пациентов с различными болевыми синдромами. Оценка имеющихся данных позволила констатировать, что вне зависимости от диагноза 481 пациент получал лечение Нейробионом в ампулах без использования каких-либо других лекарственных средств. В 78% всех случаев лечения Нейробионом в ампулах, независимо от сопроводительной терапии, был описан положительный результат. Помимо высокой эффективности, Нейробион отличается высокой безопасностью ввиду того, что не содержит Лидокаин, способный вызывать тяжелые аллергические реакции. Однако отсутствие анестетиков в составе препарата может снижать комплаенс пациентов ввиду болезненности процедуры инъекции. При отсутствии указаний на непереносимость местных анестетиков, Нейробион может быть смешан с любым из них (0,5% Новокаином, 2% Лидокаином или 7,5% Наропином).
Применение витамина В12 способствует не только ремиелинизации, но и снижению интенсивности болевого синдрома. Пиридоксин в составе Нейробиона участвует в синтезе сфингозина — структурного элемента мембраны нервного волокна и нейромедиаторов (серотонина, норадреналина). Таким образом, оба нейротропных компонента улучшают скорость проведения нервного импульса, улучшают его репаративные свойства. Доказано патогенетическое воздействие тиамина на улучшение аксоплазматического тока и восстановление трофической функции нейрона.
Лечение тоннельных невропатий целесообразно начинать с парентерального введения Нейробиона (ежедневно по 3 мл внутримышечно, курс 6–12 инъекций), а после достижения клинического улучшения для обеспечения стабильного патогенетического действия, направленного на восстановление функции нерва, перейти на прием таблетированной формы 3 раза в сутки в течение 1–3 месяцев.
Понимание патогенетических механизмов развития тоннельной невропатии у каждого конкретного пациента обусловливает индивидуальный подбор этиотропной, патогенетической и симптоматической терапии, способной не только облегчить состояние больного (уменьшить выраженность болевого синдрома, купировать воспаление и отек, улучшить вегетативно-трофические функции), но и предотвратить появление повторных компрессий периферических нервов. Прогноз пациента с тоннельной невропатией зависит от своевременного начала терапии, до наступления необратимых метаболических процессов в нерве, а также атрофии и контрактур в иннервируемых мышцах.
Литература
- Алексеев В. В., Баринов А. Н., Кукушкин М. Л., Подчуфарова Е. В., Строков И. А., Яхно Н. Н. Боль: руководство для врачей и студентов / Под ред. Н. Н. Яхно, М.: МедПресс. 2009. 302 с.
- Баринов А. Н. Невропатическая боль: клинические рекомендации и алгоритмы // Врач. 2012, № 9, с. 17–23.
- Баринов А. Н. Тоннельные невропатии: обоснование патогенетической терапии // Врач. 2012, № 4, с. 31–37.
- Бублик Л. А. с соавт. Эпидуральные блокады при выраженном корешковом и болевом синдроме, обусловленном патологией межпозвонковых дисков поясничного отдела позвоночника, с применением Ксефокама и лидокаина // Международный неврологический журнал. 2006, № 1 (5), с. 12–17.
- Данилов А. Б. Витамины группы В в лечении боли // Лечащий Врач. 2009, № 9, с. 1–3.
- Еськин Н. А., Матвеева Н. Ю., Приписнова С. Г. Ультразвуковое исследование периферической нервной системы // SonoAce-Ultrasound. 2008, № 18, с. 65–75.
- Мельцер Р. И., Ошукова С. М., Иванова И. У. Нейрокомпрессионные синдромы: Монография. Петрозаводск: ПетрГУ. 2002. 134 с.
- Миронов С. П., Еськин Н. А., Голубев В. Г. и др. Ультразвуковая диагностика патологии сухожилий и нервов конечностей // Вестник травматологии и ортопедии. 2004. № 3. с. 3–4.
- Яхно Н. Н., Баринов А. Н., Подчуфарова Е. В. Невропатическая и скелетно-мышечная боль. Современные подходы к диагностике и лечению // Клиническая медицина. 2008. Т. 86, № 11. С. 9–15.
- Eckert M., Schejbal P. Therapy of neuropathies with a vitamin B combination // Fortschr Med. 1992, Oct 20; 110 (29): 544–548.
- Gelberman R. H., Szabo R. M., Williamson R. V. et al. Sensibility testing in peripheral-nerve compression syndromes. An experimental study in humans // J Bone Joint Surg Am. 1983; Jun, 65 (5): 632–638.
- Graham R. G., Hudson D. A., Solomons M. A prospective study to assess the outcome of steroid injections and wrist splinting for the treatment of carpal tunnel syndrome // Plast Reconstr Surg. 2004; 113 (2): 550–556.
- Jarvik J. G., Comstock B. A., Kliot M., Turner J. A., Chan L., Heagerty P. J. et al. Surgery versus non-surgical therapy for carpal tunnel syndrome: a randomised parallel-group trial // Lancet. 2009; Sep 26, 374 (9695): 1074–1081.
- Kwon B. C., Jung K. I., Baek G. H. Comparison of sonography and electrodiagnostic testing in the diagnosis of carpal tunnel syndrome // J Hand Surg [Am]. 2008; Jan, 33 (1): 65–71.
- Lo S. F. Clinical characteristics and electrodiagnostic features in patients with carpal tunnel syndrome, double crush syndrome, and cervical radiculopathy // Rheumatol Int. 2012; 01 May, 32 (5): 1257–1263.
- Pomerance J., Zurakowski D., Fine I. The cost-effectiveness of nonsurgical versus surgical treatment for carpal tunnel syndrome // J Hand Surg Am. 2009; Sep, 34 (7): 1193–1200.
- Schmid A. B. The double crush syndrome revisited — a Delphi study to reveal current expert views on mechanisms underlying dual nerve disorders // Man Ther. 2011; 01 Dec, 16 (6): 557–562.
- Violante F. S., Armstrong T. J., Fiorentini C. et al. Carpal tunnel syndrome and manual work: a longitudinal study // J Occup Environ Med. 2007; 49 (11): 1189–1196.
- Upton А., McComas А. The Double Crush in Nerve-Entrapment Syndromes // Lancet. 1973, 18, p. 359–362.
Статья опубликована в журнале Лечащий Врач
материал MedLinks.ru






