Содержание статьи
Введение
В основе развития таких сердечно-сосудистых заболеваний (ССЗ), как ишемическая болезнь сердца (ИБС), острое нарушение мозгового кровообращения, периферический атеросклероз, лежат нарушения липидного обмена (НЛО): дислипидемии, гиперхолестеринемии [1]. Согласно данным многоцентрового популяционного исследования INTERHEART именно дислипидемия является наиболее распространенным модифицируемым фактором кардиоваскулярного риска [2]. В Российской Федерации длительное время существовала проблема неизученности фактической распространенности различных НЛО и эффективности холестеринснижающей терапии в реальной клинической практике [3], что в итоге привело к инициации Министерством здравоохранения в 2012 г. крупного многоцентрового эпидемиологического исследования по оценке распространенности ССЗ и их факторов риска в 13 регионах России (ЭССЕ-РФ) [4]. Согласно результатам этого исследования доля трудоспособного населения страны с НЛО составляет в среднем 57,6%, достигая в отдельных регионах 67,6% [5]. В Кемеровской области распространенность НЛО составляет 45,6%, увеличиваясь с возрастом независимо от половой принадлежности [6], что актуализирует потребность в ее активном выявлении и ранней коррекции.
Согласно действующим рекомендациям адекватность снижения сердечно-сосудистого риска на фоне проводимого холестеринснижающего лечения оценивается по достижению целевых значений показателей липидного спектра соответственно стратификации риска развития ССЗ, определяемого персонифицированно для каждого пациента [7]. Однако существует категория больных, имеющих семейную гиперхолестеринемию (СГХС), у которых применение стандартной терапии малоэффективно. При этом СГХС выступает одним из широко распространенных в мире генетических заболеваний [8] и характеризуется повышением уровня общего холестерина (ХС) в 2–2,5 раза по сравнению с нормой за счет Хс липопротеинов низкой плотности (Хс-ЛПНП). При этом у больных с СГХС уровень атерогенного Хс может превышать 4,9 ммоль/л (в норме не более 3 ммоль/л у здоровых взрослых). Опасность заболевания состоит в том, что без лечения у таких пациентов регистрируют раннее агрессивное развитие атеросклероза (3–4-я де-када жизни), ранние инфаркты, инсульты, развитие стеноза аорты и внезапную смерть. Причиной СГХС считают мутации и образование дефектов генов рецепторов Хс-ЛПНП (LDLR), а также генов, кодирующих белок-адаптер (LDLRAP или ARH), кодирующих синтез апопротеина-В (апо-В), и гена фермента пропротеиновой конвертазы субтилизин-кексинового типа (PCSK9). Мутации (гомозиготные и гетерозиготные) могут затрагивать один ген или сразу два гена (так называемая двойная гетерозиготность) [7]. Считается, что распространенность гетерозиготной формы СГХС среди представителей европеоидной расы составляет 1:500, гомозиготной формы — 1:1 000 000 [7–9]. По косвенным данным ЭССЕ-РФ, распространенность гетерозиготной формы СГХС в РФ составляет 1:108, гомозиготной формы — 1:300 000 [6, 7]. В большинстве случаев заболевание остается недиагностированным даже в развитых странах Европейского союза. Для выявления пациентов с СГХС используются так называемые голландские критерии (Dutch lipid clinic network criteria, DLCNC) [7, 8].
На сегодняшний день в России нет стандартизированной специализированной сети липидных центров и/или кабинетов. Имеются отдельные центры на базе крупных клиник и научных центров (Москва, Санкт-Петербург, Новосибирск, Самара, Казань). В Кемерово липидный центр на базе ГБУЗ «КККД» функционирует с сентября 2016 г. В это же время был сформирован липидный центр в Сургуте на базе ОКД «ЦД и ССХ». Оба центра работают в тесном научно-практическом сотрудничестве и применяют единые критерии отбора пациентов на специализированную консультацию. Маршрутизация пациентов в липидном центре г. Кемерово представлена на рисунке 1.
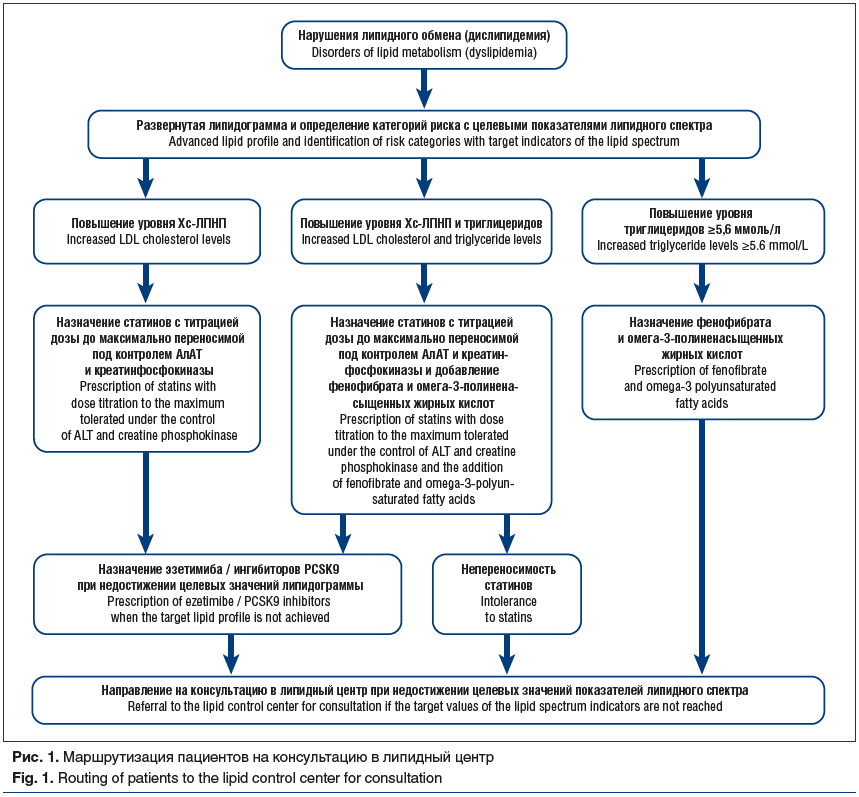
На консультацию в липидный центр направляются следующие пациенты:
с высокой гиперхолестеринемией (общий Хс в крови >7,5 ммоль/л, или Хс-ЛПНП >4,9 ммоль/л, или триглицериды >5 ммоль/л), требующей подбора высокодозированной и/или комбинированной терапии липидснижающими препаратами;
с ранним анамнезом сердечно-сосудистых заболеваний и/или реваскуляризаций сосудистых бассейнов (до 55 лет), требующих «агрессивной» вторичной профилактики;
с подозрением на непереносимость липидснижающей терапии из-за развития побочных эффектов или с ее недостаточной эффективностью.
Относительно таких пациентов обсуждается необходимость включения в холестеринснижающую терапию новых групп лекарственных препаратов, эффективно снижающих проатерогенные показатели липидограммы, например, ингибиторов PCSK9. К таковым относятся: полностью человеческий моноклональный иммуноглобулин G2 (IgG2) эволокумаб (Репата, «Амджен», США) и полностью человеческое моноклональное антитело иммуноглобулин G1 (IgG1) алирокумаб. Эволокумаб селективно и с высокой степенью аффинности связывается с PCSK9 и ингибирует связывание циркулирующей PCSK9 с рецептором ЛПНП (Р-ЛПНП) на поверхности клеток печени, таким образом предотвращая PCSK9-
опосредованный распад Р-ЛПНП. В результате повышения экспрессии Р-ЛПНП в печени снижается сывороточная концентрация Хc-ЛПНП.
За два года на консультативный прием липидолога в Кемерово направлен 691 пациент. У 307 (44%) пациентоввыявлены тяжелые НЛО, у 233 (34%) из них — с крайне высоким риском сердечно-сосудистых осложнений и недостижением целевых значений показателей липидограммы. У 33 (4,8%) пациентов диагностирована вероятная и определенная СГХС, у 41 (5,9%) пациента подтверждена непереносимость статинов.
Кардиолог-липидолог, определив, что в результате терапии статинами в максимально переносимой дозировке не достигаются целевые значения показателей липидограммы, обозначенные в национальных рекомендациях (у пациентов очень высокого риска Хс-ЛПНП <1,4 ммоль/л; у пациентов высокого риска Хс-ЛПНП <1,8 ммоль/л) [7], оптимизирует холестерин-снижающую терапию, чаще всего за счет дополнительного назначения эзетимиба в дозе 10 мг (класс рекомендаций I, уровень доказательности B), что может обеспечить дополнительное снижение уровня Хс-ЛПНП на 15–30%. Пациентам высокого и очень высокого риска с повышенным содержанием триглицеридов (1,5–5,6 ммоль/л) на фоне приема статинов показаны фибраты и при недостаточном их эффекте или при непереносимости фибратов —
омега-3 жирные кислоты этиловых эфиров 2 г 2 р./сут (класс рекомендаций IIa, уровень доказательности B).
Если же при высоком или очень высоком сердечно-сосудистом риске не достигаются целевые значения Хс-ЛПНП, должен быть рассмотрен вопрос о назначении ингибиторов PCSK9 (класс рекомендаций I, уровень доказательности A).
Данные доказательной медицины по применению эволокумаба
Крупное (27 564 пациента, средний возраст — 63 года, 69% больных получали высокоинтенсивную статинотерапию) международное рандомизированное клиническое исследование FOURIER было посвящено оценке эффективности ингибитора PCSK9 эволокумаба (подкожное введение 420 мг 1 р./мес. или 140 мг каждые 2 нед.) в отношении уровня Хс-ЛПНП и сердечно-сосудистых конечных точек у пациентов очень высокого сердечно-сосудистого риска с недостижением целевых значений Хс-ЛПНП на фоне использования статинотерапии и эзетимиба. Было показано, что при дополнительном назначении эволокумаба в активной группе исследования, помимо снижения уровня
Хс-ЛПНП на 59% и повышения содержания Хс-ЛПВП на 8,1% [10], уменьшилась частота сердечно-сосудистых конечных точек на 18% (в группе эволокумаба было зарегистрировано 2192 конечные точки, в группе плацебо — 2714) и не увеличивался риск развития сахарного диабета, в т. ч. у пациентов с метаболическим синдромом [11].
При этом 2669 (10%) пациентов достигли значений Хс-ЛПНП менее 0,5 ммоль/л, 8003 (31%) больных — 0,5–1,3 ммоль/л, 3444 (13%) — 1,3–1,8 ммоль/л, 7471 (29%) — 1,8–2,6 ммоль/л и 4395 (17%) — 2,6 ммоль/л и выше. Была выявлена значимая прямая связь между снижением содержания Хс-ЛПНП и уменьшением частоты сердечно-сосудистых событий (связь низких значений Хс-ЛПНП менее 0,2 ммоль/л с меньшей частотой первичной конечной точки (сердечно-сосудистая смерть, инфаркт миокарда (ИМ), инсульт, госпитализация по поводу нестабильной стенокардии, коронарная реваскуляризация миокарда) (р=0,0012) и с меньшей частотой вторичной конечной точки (сердечно-сосудистая смерть, ИМ или инсульт) (р=0,0001) [12].
В субанализе исследования FOURIER по оценке эффективности эволокумаба у пациентов с недавно (в течение 12 мес. до включения в исследование, n=5711) перенесенным ИМ по сравнению с теми, кто перенес ИМ в более отдаленные сроки (n=16 609), было выявлено, что в течение трех лет частота конечных точек была закономерно выше при недавно перенесенном ИМ, однако абсолютное снижение риска первичной конечной точки в этой группе на фоне применения эволокумаба составило 3,7% в отличие от 1,1% в группе эволокумаба при отдаленном ИМ [13].
Показательно, что терапия эволокумабом в отношении профилактики инсультов была более эффективной в группе первичной профилактики, чем в группе вторичной профилактики [14]. Так, частота повторных инсультов у пациентов в исследовании FOURIER составила 3,5% в группе эволокумаба и 4% в группе плацебо, тогда как в группе первичной профилактики частота инсультов составила 1% и 1,4% в соответствующих группах [15]. Следует отметить, что эволокумаб в исследовании EBBINGHAUS (Evaluating PCSK9 Binding Antibody Influence on Cognitive Health in High Cardiovascular Risk Subjects) продемонстрировал отсутствие влияния на когнитивную функцию у пациентов (n=1204), включенных в исследование FOURIER, в т. ч. в группе пациентов, достигших значений ХС-ЛПНП <1 ммоль/л [16].
В исследовании эффектов эволокумаба у пациентов с острым коронарным синдромом (EVOlocumab for Early Reduction of LDL-cholesterol Levels in Patients With Acute Coronary Syndromes, EVOPACS, n=308) среднее значение Хс-ЛПНП в группе эволокумаба (высокоинтенсивная терапия статинами и эволокумабом) снизилось с 3,61 до 0,79 ммоль/л к 8-й нед. терапии, в группе плацебо (высокоинтенсивная терапия статинами) — с 3,42 до 2,06 ммоль/л. В группе эволокумаба содержания Хс-ЛПНП <1,8 ммоль/л удалось достигнуть у 95,7% пациентов, в группе плацебо — только у 37,6%. При этом частота нежелательных явлений и сердечно-сосудистых событий в группах была одинаковой, т. е. применение эволокумаба является эффективным и безопасным в раннем госпитальном периоде лечения острого коронарного синдрома [17].
В исследовании GLAGOV у пациентов с ангиографическим подтверждением ишемической болезни сердца на фоне терапии статинами дополнительное назначение эволокумаба сопровождалось значительным снижением (на 0,95%, р<0,001) процентного объема атеромы в коронарной артерии, по данным внутрикоронарного ультразвукового исследования, после 76 нед. терапии по сравнению с показателями в группе плацебо [18].
Известно также, что применение эволокумаба сопровождается стабилизацией атеросклеротической бляшки за счет утолщения фиброзной капсулы у пациентов с острым коронарным синдромом [19].
Несмотря на доказанную высокую эффективность и безопасность ингибиторов PCSK9, в реальной клинической практике даже в странах Европейского союза имеется значительное недоиспользование возможностей препаратов этой группы для достижения у большинства пациентов с НЛО с высоким и очень высоким риском целевых значений показателей липидограммы в соответствии с действующими клиническими рекомендациями, что связано с социально-экономическим аспектом данной терапии [20].
Задачей функционирования липидных центров является, в частности, повышение доступности современной липидснижающей терапии для пациентов, у которых не удается достичь целевых значений показателей липидограммы на фоне приема статинов [21].
На сегодняшний день практическое использование эволокумаба в России насчитывает единичные случаи. В липидном центре г. Кемерово идет активное накопление данных по использованию ингибиторов PCSK9. Представляем первый собственный опыт применения эволокумаба.
Собственный опыт применения эволокумаба
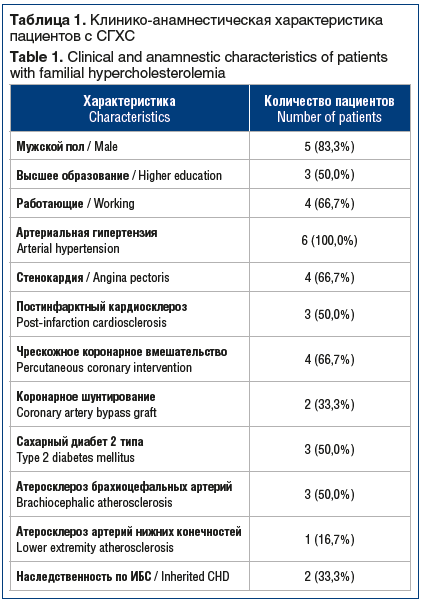
В проспективное рандомизированное исследование исходно были включены 6 пациентов, из них 5 мужчин, в возрасте 49±5,8 года. Пациенты были госпитализированы для обследования и лечения в кардиологическое отделение НИИ КПССЗ с тяжелыми НЛО. Все пациенты — с вероятным диагнозом СГХС (7 [5; 8] баллов по DLCNC) с очень высоким сердечно-сосудистым риском (табл. 1).
До проведения подкожной инъекции ингибитора PCSK9 эволокумаба у всех пациентов натощак кубитальным катетером забирали венозную кровь для оценки параметров липидограммы (общий Хс, Хс-ЛПНП, Хс-ЛПВП, триглицериды, апо-белки) и проведения других лабораторных исследований (общий анализ крови, глюкоза, печеночные маркеры цитолиза и холестаза, креатинин, коагулограмма). В вечерние часы в первый день госпитализации всем пациентам подкожно вводили эволокумаб. В ранние утренние часы натощак повторно забирали кровь для проведения исследований в том же объеме, что и при поступлении. В этот же день пациентов выписывали на амбулаторный этап лечения. Через 2 нед. проводили повторную госпитализацию с подкожным введением эволокумаба и двукратной оценкой параметров липидограммы и биохимических показателей, характеризующих безопасность применения лекарственного препарата (оценка функции почек, печени, гемостаза, ионного и углеводного обмена).
В рамках первичной госпитализации проводилась эхокардиография с оценкой параметров внутрисердечной гемодинамики. Никто из пациентов не имел тяжелой сердечной недостаточности. Медиана фракции выброса левого желудочка составляла 63,5 [55; 68]%.
Все пациенты получали комбинированную холестеринснижающую терапию статинами в максимально переносимых дозировках (аторвастатин до 80 мг, розувастатин до 40 мг) и эзетимибом (10 мг). Кроме того, пациенты принимали ацетилсалициловую кислоту, β-адреноблокаторы, ингибиторы ангиотензинпревращающего фермента — по 4 (66,7%) человека, антагонисты кальция — 3 (50%), сартаны — 2 (33,3%) человека, нитраты и диуретики — по 1 (16,7%) человеку.
В исследуемой группе все пациенты успешно прошли две госпитализации для оценки эффективности и безопасности терапии эволокумабом. Исходные значения липидограммы, а также результаты первого введения эволокумаба через 2 нед. после первичной госпитализации представлены в таблице 2.
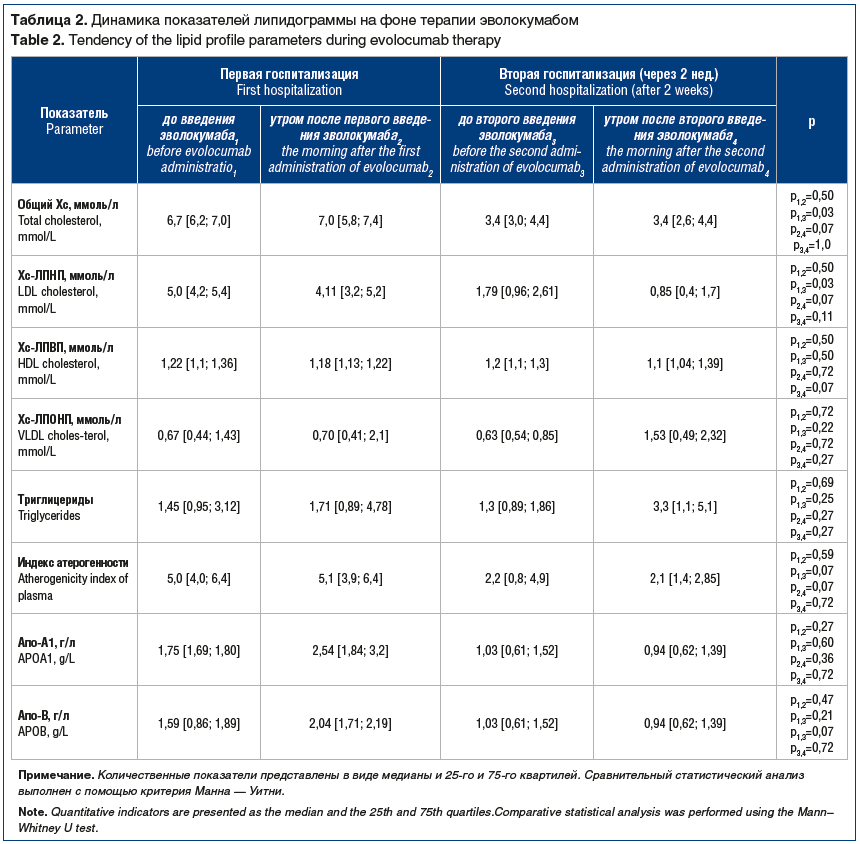
Уже через 2 нед. после первого введения эволокумаба выявлено значительное снижение индекса атерогенности, снижение уровня Хс-ЛПНП на 67%. Лечение эволокумабом не оказало значимого влияния на лабораторные показатели безопасности (табл. 3).

Таким образом, дополнительное назначение эволокумаба пациентам с НЛО высокого и очень высокого риска, получающим максимально переносимую дозу статинов и эзетимиб и не достигающим на этом фоне целевых значений липидограммы, показало свою эффективность — значимое снижение уровня Хс-ЛПНП (на 67% от исходных значений). Для сохранения эффекта необходимо длительное применение препарата. При этом эволокумаб безопасен, не вызывает развития органных дисфункций. Документы всех пациентов, прошедших лечение эволокумабом в липидном центре г. Кемерово, направлены в Министерство здравоохранения Кузбасса для получения адресной региональной помощи. В настоящее время 2 пациента в г. Кемерово получают ингибиторы PCSK9 в рамках адресной помощи. В липидном центре г. Сургута
4 пациента продолжают прием эволокумаба в рамках региональной адресной помощи больным с тяжелыми НЛО.
Заключение
Лидирующее место среди причин смертности в развитых странах занимают сердечно-сосудистые заболевания, ассоциированные с атеросклерозом. Основной фактор риска развития атеросклероза — НЛО. Существует категория пациентов с тяжелыми НЛО (включая СГХС), у которых стандартная холестеринснижающая терапия оказывается недостаточно эффективной для достижения целевых значений показателей липидограммы. У пациентов высокого и очень высокого риска это ухудшает прогноз из-за увеличения риска развития сердечно-сосудистых событий. В таких случаях методом выбора для интенсификации холестеринснижающей терапии являются новые липидснижающие препараты — ингибиторы PCSK9, например эволокумаб (Репата). Липидные центры могут стать организационной основой маршрутизации пациентов с тяжелыми НЛО для повышения доступности современной, эффективной лекарственной терапии.
Сведения об авторах:
Барбараш Ольга Леонидовна — д.м.н., профессор, член-корр. РАН, директор НИИ КПССЗ, 650002, Россия, г. Кемерово, Сосновый бульвар, д. 6; заведующая кафедрой кардиологии и сердечно-сосудистой хирургии, ФГБОУ ВО КемГМУ Минздрава России, 650029, Россия, г. Кемерово, ул. Ворошилова, д. 22а; ORCID iD 0000-0002-4642-3610.
Кашталап Василий Васильевич — д.м.н., доцент, заведующий отделом клинической кардиологии, НИИ КПССЗ, 650002, Россия, г. Кемерово, Сосновый бульвар, д. 6; профессор кафедры кардиологии и сердечно-сосудистой хирургии ФГБОУ ВО КемГМУ Минздрава России, 650029, Россия, г. Кемерово, ул. Ворошилова, д. 22а; ORCID iD 0000-0003-3729-616Х.
Федорова Наталья Васильевна — к.м.н., кардиолог-липидолог, заведующая клинико-диагностическим отделением, НИИ КПССЗ, 650002, Россия, г. Кемерово, Сосновый бульвар, д. 6; ORCID iD 0000-0002-3841-8539.
Седых Дарья Юрьевна — к.м.н., научный сотрудник лаборатории патологии кровообращения отдела клинической кардиологии, НИИ КПССЗ, 650002, Россия, г. Кемерово, Сосновый бульвар, д. 6; ORCID iD 0000-0001-7058-2008.
Урванцева Ирина Александровна — к.м.н., главный врач, ОКД «ЦД и ССХ», 628416, Россия, г. Сургут, пр. Ленина, д. 69/1; заведующая кафедрой кардиологии медицинского института, БУ ВО «Сургутский государственный университет», 628412, Россия, г. Сургут, пр. Ленина, д. 1; ORCID iD 0000-0002-5545-9826.
Воробьев Антон Сергеевич — к.м.н., кардиолог-липидолог, ведущий научный сотрудник научно-образовательного центра, доцент кафедры кардиологии медицинского института, БУ ВО «Сургутский государственный университет», 628412, Россия, г. Сургут, пр. Ленина, д. 1; ORCID iD 0000-0002-4279-7578.
Контактная информация: Седых Дарья Юрьевна, e-mail: md-sedih@mail.ru. Прозрачность финансовой деятельности: материал для статьи взят из базы данных наблюдательного регистрового исследования стационарного этапа ведения пациентов с тяжелыми нарушениями липидного обмена в рамках выполнения поискового научного исследования НИИ КПССЗ 2020_419_23 «Комплексное лечение пациентов с наследственными формами нарушений липидного обмена с применением ЛНП-афереза и медикаментозной терапии», финансируемого Министерством науки и высшего образования Российской Федерации. Конфликт интересов отсутствует. Статья поступила 08.09.2020, поступила после рецензирования 22.09.2020, принята в печать 06.10.2020.
About the authors:
Olga L. Barbarash — Dr. of Sci. (Med.), Professor, Corresponding Members of the Russian Academy of Sciences, Head of the Research Institute for Complex Issues of Cardiovascular Diseases: 6, Sosnovy Bulvar, Kemerovo, 650002, Russian Federation; Head of the Department of Cardiology and Cardiovascular Surgery, Kemerovo State Medical Univeristy: 22A, Voroshilova str., Kemerovo, 650029, Russian Federation; ORCID iD 0000-0002-4642-3610.
Vasily V. Kashtalap — Dr. of Sci. (Med.), Associate Professor, Head of the Department of Clinical Cardiology, Research Institute for Complex Issues of Cardiovascular Diseases: 6, Sosnovy Bulvar, Kemerovo, 650002, Russian Federation; Professor of the Department of Cardiology and Cardiovascular Surgery, Kemerovo State Medical University: 22A, Voroshilova str., Kemerovo, 650029, Russian Federation; ORCID iD 0000-0003-3729-616X.
Natalia V. Fedorova — Cand. of Sci. (Med.), cardiologist-lipidologist, Head of the Clinical and Diagnostic Department, Research Institute for Complex Issues of Cardiovascular Diseases: 6, Sosnovy Bulvar, Kemerovo, 650002, Russian Federation; ORCID iD 0000-0002-3841-8539.
Darya Yu. Sedykh — Cand. of Sci. (Med.), researcher of the Laboratory of Cardiovascular Pathology of the Department of Clinical Cardiology, Research Institute for Complex Issues of Cardiovascular Diseases: 6, Sosnovy Bulvar, Kemerovo, 650002, Russian Federation; ORCID iD 0000-0001-7058-2008.
Irina A. Urvantseva — Cand. of Sci. (Med.), Chief Medical Officer, Yugra Cardiology and Cardiovascular Surgery Center: 69/1, Lenina prospect, Surgut, 628416, Russian Federation; Head of the Department of Cardiology of the Medical Institute, Surgut State University: 1, Lenina prospect, Surgut, 628412, Russian Federation; ORCID iD 0000-0002-5545-9826.
Anton S. Vorobyov — Cand. of Sci. (Med.), cardiologist-lipidologist, Leading Researcher of the Research and Educational Center, Associate Professor of the Department of Cardiology of the Medical Institute, Surgut State University: 1, Lenina prospect, Surgut, 628412, Russian Federation; ORCID iD 0000-0002-4279-7578.
Contact information: Darya Yu. Sedykh, e-mail: md-sedih@mail.ru. Financial Disclosure: the material for the article is taken from the database of an observational registry study on inpatient basis of patient management with severe lipid metabolism disorders as part of an exploratory research at the Research Institute for Complex Issues of Cardiovascular Diseases 2020_419_23 “Complex treatment of patients with hereditary forms of lipid metabolism disorders using LDL apheresis and drug therapy”, funded by the Ministry of Science and Higher Education of the Russian Federation. There is no conflict of interests. Received 08.09.2020, revised 22.09.2020, accepted 06.10.2020.
.
Информация с rmj.ru





