Введение
Появление новой коронавирусной инфекции (COVID-19) не только оказало влияние на жизнь и здоровье населения, но и сыграло огромную роль в изменении эпидемиологических процессов распространения острых респираторных инфекций (ОРИ).
Многими авторами отмечается снижение роли ОРИ в структуре детской заболеваемости во время развития пандемии COVID-19, особенно в его дебюте. Так, в рамках Сиэтловского исследования гриппа показано снижение уровня заболеваемости гриппом и другими респираторными инфекциями во время начала развития пандемии COVID-19 [1]. Авторы считают, что на сложившуюся ситуацию оказали влияние как циркуляция нового вируса, так и противоэпидемические меры, вводимые во всех странах. Изменения чаще всего касались вируса гриппа, респираторно-синцитиального вируса (РС-вирус), риновируса и энтеровирусов. Имеются схожие данные о снижении уровня заболеваемости гриппом в различных странах: так, в Канаде в 2021 г. отмечалась исторически низкая заболеваемость гриппом, в США также зарегистрирована самая низкая частота встречаемости гриппа начиная с 1997 г. [2, 3]. Схожая ситуация выявлена в Мексике, Бангладеш и Австралии [4, 5]. Имеются данные о странах, где заболеваемость гриппом в 2021–2022 гг. сохранялась на прежнем уровне — Китай, Бразилия, Аргентина, но при этом отмечено изменение характерной сезонности циркуляции гриппа с повышением заболеваемости в летние месяцы.
Ряд исследователей приводят данные, что циркуляция риновирусов и респираторных энтеровирусов также снизилась на фоне развития пандемии, но затем очень быстро (в течение года) вернулась к доковидным показателям [2, 6]. Регистрируется снижение активности РС-вируса, аденовируса, сезонного коронавируса, парагриппа и метапневмовируса, особенно среди детского населения [7]. Данные по бокавирусной инфекции разнятся: имеются исследования, где показано снижение выявления данного возбудителя в детской популяции, в других же говорится о сохранении прежнего уровня заболеваемости [8, 9].
В свою очередь, снижение активности респираторных вирусов привело к снижению распространенности инвазивных инфекций, вызванных Streptococcus pneumoniae. В США и Германии показано снижение уровня заболеваемости пневмониями, не связанными напрямую с COVID-19 [9, 10].
Цель исследования: изучить региональные особенности изменения этиологии ОРИ, приводивших к госпитализации детей в период 2020–2024 гг.
Содержание статьи
Материал и методы
Проведен анализ этиологической структуры ОРИ у госпитализированных детей с клиническими проявлениями поражения верхних и нижних дыхательных путей в период с 2020 по 2024 г. Этиология заболеваний подтверждалась анализом полимеразно-цепной реакции (ПЦР) мазков из зева и носа на SARS-CoV-2 (регистрационное удостоверение реагента № РЗН 2022/18677), ПЦР-анализом «Респираторный скрин» (регистрационное удостоверение реагента № РЗН 2023/19859, вирусы гриппа, парагриппа, РС-вирус, риновирусы, аденовирусы, метапневмовирусы, коронавирусы, бокавирусы), ПЦР-анализом мазка из зева на Mycoplasma pneumoniae и иммуноферментным анализом с определением иммуноглобулинов класса М (IgM) к M. pneumoniae (savyon diagnostics версия М1262-01Е 09-07/09). За годы наблюдения было получено 13 213 положительных результатов. В рамках исследования DeMaRes в лаборатории молекулярной диагностики НИИ антимикробной химиотерапии ФГБОУ ВО «СГМУ» Минздрава России было проведено исследование 108 образцов ДНК M. pneumoniae с целью выявления мутаций, приводящих к формированию резистентности к макролидам.
Результаты и обсуждение
Первые случаи COVID-19 в Воронежском регионе зарегистрированы в марте 2020 г. Значительный подъем заболеваемости COVID-19 пришелся на май 2020 г. При этом в данный период отмечалось снижение роли других респираторных вирусных инфекций и микоплазмоза у госпитализированных детей (рис. 1).
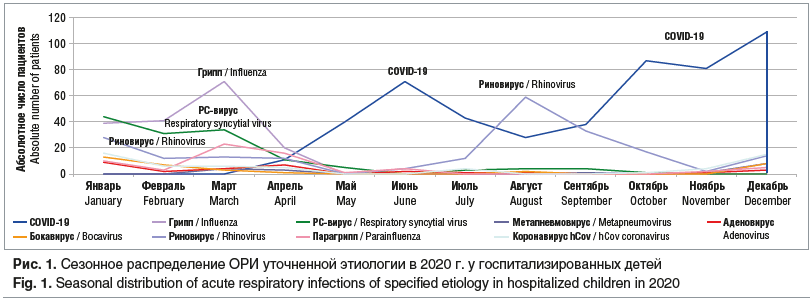
Исключение составила риновирусная инфекция, которая сохраняла свою активность при незначительном снижении COVID-19. При этом отмечалось изменение ее привычной, представленной в литературе зимне-весенней сезонности с увеличением госпитализации детей в летние месяцы, пик пришелся на август [9, 10].
В первом полугодии 2021 г., при проведении активных противоэпидемических мероприятий, отмечена незначительная активация парагриппозной и бокавирусной инфекций, с изменением их сезонности. Согласно данным литературы в допандемический период пик госпитализации детей с парагриппом приходился на февраль [9, 10], а в 2021 г. нами зарегистрировано смещение сезонности на март — апрель. К лету 2021 г. выявляется окончательная адаптация риновирусной и РС-инфекций к пандемическому вирусу и начиная с августа отмечается совместная циркуляция возбудителей (рис. 2).
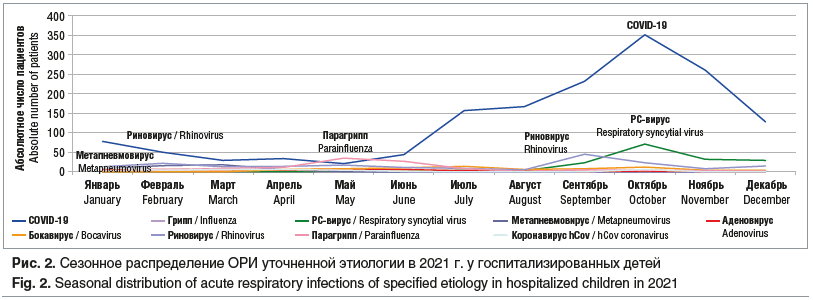
Респираторный микоплазмоз практически не регистрировался. Также в 2020–2021 гг. у госпитализированных детей крайне редко выявлялся грипп.
На 2022 г. пришлась рекордная заболеваемость COVID-19, что связано с распространением штамма «омикрон». В данных условиях продолжает регистрироваться сохранение активности риновирусной инфекции, начинается адаптация парагриппозной и аденовирусной инфекций с переходом их привычной сезонности на летний период. В конце 2022 г. с сохранением привычного эпидемического сезона регистрируется рост заболеваемости гриппом (рис. 3).
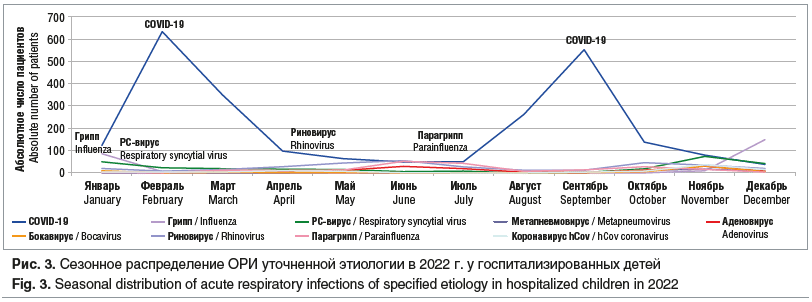
Чаще стала диагностироваться микоплазменная инфекция, число госпитализированных детей в регионе с респираторным микоплазмозом приблизилось к допандемическим показателям 2018–2019 гг.
Таким образом, только к концу 2022 г. произошла адаптация возбудителей респираторных инфекций к подавляющей циркуляции SARS-CoV-2. В 2023 г. с февраля по май происходит постепенное снижение госпитализации детей с COVID-19. Начиная с этого периода в Воронежском регионе стала резко нарастать роль микоплазменной инфекции в этиологической структуре инфекций у госпитализированных детей с поражением нижних дыхательных путей, и в течение 6 мес. респираторный микоплазмоз занял лидирующее положение (рис. 4).
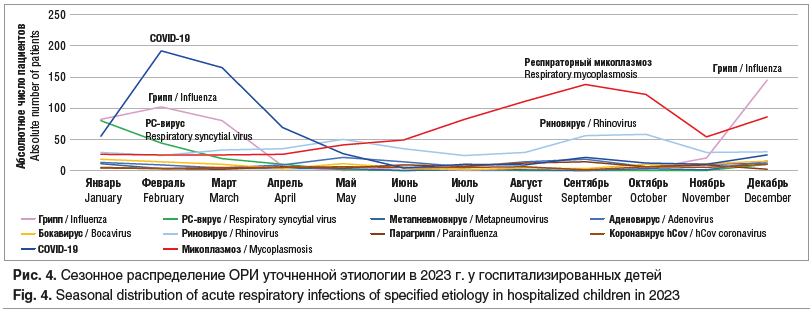
Микоплазменная инфекция имеет эпидемиологическую цикличность с подъемами заболеваемости каждые 3–5–7 лет [11]. До пандемии новой коронавирусной инфекции повышенная заболеваемость респираторным микоплазмозом в Воронежском регионе с развитием вспышек в организованных детских коллективах регистрировалась в 2013–2015 гг. [12].
Согласно данным литературы микоплазменная инфекция имеет осенне-зимнюю сезонность. Так, О.В. Островская и соавт. [13] показывают повышение выявляемости микоплазм начиная с последних месяцев лета и до февраля — марта с пиком в сентябре. Схожие показатели получены и в нашем исследовании, проведенном в 2013 г. [12]. В 2023 г. выявлено расширение сезонности инфекции до летне-осеннего периода — подъем заболеваемости начался в мае с пиком в августе — октябре. При этом по результатам исследования DeMaRes[1] 83,3% изолятов M. pneumoniae имели мутацию в рРНК A2058G, которая обусловливает высокий уровень резистентности к макролидам с 14-членным кольцом.
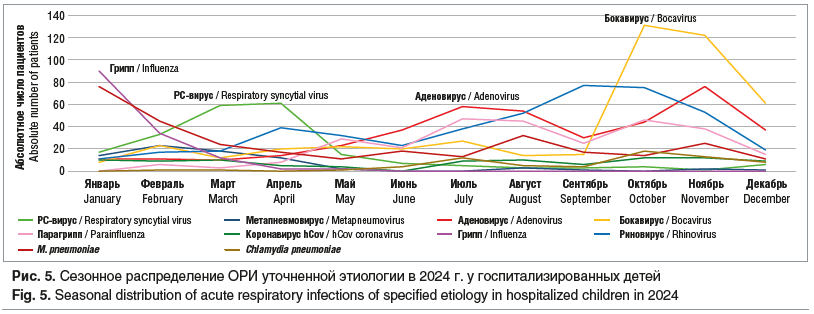
В эпидемический сезон 2024 г. SARS-CoV-2 полностью перешел в группу сезонных респираторных вирусов, и впервые в регионе мы отметили значительно возросшую роль бокавирусной инфекции в осенний период как этиологического фактора, приводящего к госпитализации детей с поражением респираторного тракта. Бокавирусная инфекция в регионе диагностируется с 2014 г., но только в 2024 г. отмечено возрастание ее выявляемости у госпитализированных детей в 4,4 раза, что в полтора раза больше числа всех детей, госпитализированных в год с COVID-19. В этот эпидемический сезон активизировалась аденовирусная инфекция, которая стала чаще диагностироваться у детей не только с респираторными проявлениями, но и с вирусными диареями (рис. 5).
Данное исследование демонстрирует разнообразие циркулирующих респираторных возбудителей, что указывает на целесообразность использования в лечении ОРИ у детей этиотропных препаратов широкого спектра действия. Среди препаратов широкого спектра противовирусного действия, показанных для лечения и профилактики гриппа и других острых респираторных вирусных инфекций (ОРВИ) у детей, обращают на себя внимание отечественные лекарственные средства нового класса — биологические препараты, полученные на основе градуальной технологии и выпускаемые компанией ООО «НПФ «Материа Медика Холдинг» (https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15/). К ним относятся противовирусные препараты на основе аффинно очищенных антител к интерферону γчеловека — Анаферон® детский в таблетках для рассасывания (5000 ЕМД (единиц модифицирующего действия) в 1 таблетке; РУ: ЛП-N (000035) — (РГ-RU)), показанный к применению для профилактики и лечения гриппа и других ОРВИ у детей от 1 мес. до 18 лет, и Анаферон® детский в каплях для приема внутрь (10000 ЕМД в 1 мл; РУ: ЛП-N (000019) — (РГ-RU)), применяемый для лечения ОРИ верхних дыхательных путей у самых маленьких — от 1 года до 4 лет[2],[3]. Для лечения ОРВИ, включая грипп, у детей от 6 мес. применяется препарат Эргоферон® в таблетках для рассасывания, содержащий помимо аффинно очищенных антител к интерферону γ антитела к CD4 и гистамину (по 10000 ЕМД каждого в 1 таблетке; РУ: ЛП-N (000031) — (РГ-RU))[4]. Стоит отметить, что в отличие от многих противовирусных препаратов данный препарат обладает противовоспалительным и антигистаминным действием, что важно в контексте иммунопатогенеза ОРВИ/гриппа у маленьких пациентов, включая особые группы детей с рекуррентными инфекциями, отягощенными аллергологическим анамнезом4 [14, 15]. Эффективность препаратов доказана не только в отношении вирусов гриппа и других возбудителей ОРВИ, но и для препарата Анаферон® детский в таблетках для рассасывания — против возбудителей острых кишечных вирусных инфекций (ОКВИ) (рота- и калицивируса), инфекционного мононуклеоза и ветряной оспы, а также для препарата Эргоферон® — против возбудителей ОКВИ и SARS-CoV-2. Применение данных препаратов снижает концентрацию вирусов в тканях2,4.
В метаанализах рандомизированных клинических исследований (РКИ), двойных слепых плацебо-контролируемых РКИ препаратов Анаферон® детский и Эргоферон® продемонстрированы их клиническая эффективность вне зависимости от этиологического агента и благоприятный профиль безопасности при лечении ОРВИ, включая грипп, а также при профилактическом приеме в соответствии с показаниями [14–22]. Профилактический прием препарата Анаферон® детский по 1 таблетке в течение 1 мес. в 2,6 раза уменьшает количество детей с недостаточностью IgA в сыворотке крови (с 41,3 до 15,8%), частоту нарушений со стороны клеточного звена иммунитета, а также способствует улучшению респираторного микробиома: почти в 2 раза уменьшилась доля детей с выделением β-гемолитического стрептококка группы А, в 5 раз — золотистого стафилококка и в 3 раза — дрожжеподобных грибов рода Candida [21]. Стоит также отметить, что в масштабной наблюдательной программе «ЭкспертиЗА», проведенной в эпидемическом сезоне 2024/2025 гг. с участием 9888 детей в возрасте от 6 мес. в условиях реальной практики, продемонстрирована «отсроченная» эффективность препарата Эргоферон® — благодаря особенностям реализации механизма действия через естественный иммунитет 85% детей не заболели ОРВИ/гриппом через 1 мес. после окончания терапии этим препаратом эпизода данного заболевания, а 71% — через 3 мес. [22]. При этом в лечении ОРВИ/гриппа вне зависимости от этиологии 84% пациентов обошлись монотерапией препаратом Эргоферон®, который в среднем позволял купировать лихорадку за 2,6 дня, сокращая длительность заболевания до 4 дней. Полученные в данном исследовании результаты свидетельствуют о реальной возможности минимизации политерапии/полипрагмазии при ОРВИ/гриппе у детей при использовании препарата, а также о его вкладе в иммунореабилитацию.
Мощная доказательная база препаратов Анаферон® детский и Эргоферон® позволила им занять достойную позицию в введенных в действие в июле 2025 г. клинических рекомендациях «Грипп» (возрастная группа: дети) с наивысшим уровнем убедительности рекомендаций и достоверности данных — А1[5]. Особенности механизма действия препаратов в сочетании с доказанной клинической эффективностью и благоприятным профилем безопасности позволяют рекомендовать их к широкому применению для профилактики и лечения гриппа и других ОРВИ у детей с самого раннего возраста в соответствии с показаниями.
Заключение
Стремительное распространение нового пандемического вируса в 2020 г. привело к долгосрочной смене ведущих респираторных патогенов в популяции. После значимого снижения доли привычных респираторных возбудителей происходило постепенное восстановление их значимости, начиная с РНК-содержащих вирусов (риновирусы, РС-вирусы), с изменением их привычной сезонности в регионе. В последующие эпидемические сезоны восстановилось распространение вирусов гриппа и парагриппа при снижении роли SARS-CoV-2 в госпитализации детей. Микоплазменная инфекция активизировалась в 2023 г. с расширением эпидемического сезона и резкого скачка заболеваемости среди детского населения. В 2024 г. более активными стали ДНК-содержащие вирусы (аденовирусы, бокавирусы). Пандемия COVID-19 и проводимые противоэпидемические мероприятия оказали значимое влияние на привычную циркуляцию респираторных возбудителей и этиологическую структуру респираторных инфекций в регионе. Изучение региональных особенностей респираторных инфекций как в эпидемиологическом, так и в клиническом разрезе важно для выбора оптимальной терапии ОРИ у детей с использованием препаратов широкого спектра действия, в том числе противовирусных препаратов на основе аффинно очищенных антител.
СВЕДЕНИЯ ОБ АВТОРАХ:
Кокорева Светлана Петровна — д.м.н., доцент, заведующая кафедрой детских инфекционных болезней ФГБОУ ВО ВГМУ им. Н.Н. Бурденко Минздрава России; 394036, Россия, г. Воронеж, ул. Студенческая, д. 10; ORCID iD 0000-0002-3387-9803
Разуваев Олег Александрович — к.м.н., доцент кафедры детских инфекционных болезней ФГБОУ ВО ВГМУ им. Н.Н. Бурденко Минздрава России; 394036, Россия, г. Воронеж, ул. Студенческая, д. 10; ORCID iD 0000-0002-3648-5076
Макарова Алла Вячеславовна — к.м.н., доцент кафедры детских инфекционных болезней ФГБОУ ВО ВГМУ им. Н.Н. Бурденко Минздрава России; 394036, Россия, г. Воронеж, ул. Студенческая, д. 10; ORCID iD 0000-0001-6901-314X
Котлова Вероника Борисовна — к.м.н., доцент кафедры детских инфекционных болезней ФГБОУ ВО ВГМУ им. Н.Н. Бурденко Минздрава России; 394036, Россия, г. Воронеж, ул. Студенческая, д. 10; ORCID iD 0000-0002-0520-2977
Контактная информация: Разуваев Олег Александрович, e-mail: oleg.razuvaev@gmail.com
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 01.10.2025.
Поступила после рецензирования 24.10.2025.
Принята в печать 20.11.2025.
ABOUT THE AUTHORS:
Svetlana P. Kokoreva — Dr. Sc. (Med.), Assistant Professor, Head of the Department of Pediatric Infections, N.N. Burdenko Voronezh State Medical University; 10, Studencheskaya str., Voronezh, 394036, Russian Federation; ORCID iD 0000-0002-3387-9803
Oleg A. Razuvaev — C. Sc. (Med.), Assistant Professor of the Department of Pediatric Infections, N.N. Burdenko Voronezh State Medical University; 10, Studencheskaya str., Voronezh, 394036, Russian Federation; ORCID iD 0000-0002-3648-5076
Alla V. Makarova — C. Sc. (Med.), Assistant Professor of the Department of Pediatric Infections, N.N. Burdenko Voronezh State Medical University; 10, Studencheskaya str., Voronezh, 394036, Russian Federation; ORCID iD 0000-0001-6901-314X
Veronika B. Kotlova — C. Sc. (Med.), Assistant Professor of the Department of Pediatric Infections, N.N. Burdenko Voronezh State Medical University; 10, Studencheskaya str., Voronezh, 394036, Russian Federation; ORCID iD 0000-0002-0520-2977
Contact information: Oleg A. Razuvaev, e-mail: oleg.razuvaev@gmail.com
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 01.10.2025.
Revised 24.10.2025.
Accepted 20.11.2025.
[1] Исследование DeMaRes 2021. (Электронный ресурс.) URL: https://amrcloud.net/ru/project/demares/ (дата обращения: 02.09.2025).
[2] Общая характеристика лекарственного препарата Анаферон детский, таблетки для рассасывания. (Электронный ресурс.) URL: https://lk.regmed.ru/Register/EAEU_SmPC (дата обращения: 30.10.2025).
[3] Общая характеристика лекарственного препарата Анаферон детский, капли для приема внутрь. (Электронный ресурс.) URL: https://lk.regmed.ru/Register/EAEU_SmPC (дата обращения: 30.10.2025).
[4] Общая характеристика лекарственного препарата Эргоферон, таблетки для рассасывания. (Электронный ресурс.) URL: https://lk.regmed.ru/Register/EAEU_SmPC (дата обращения: 30.10.2025).
[5] Клинические рекомендации. Грипп (возрастная группа: дети). 2025. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/preview-cr/249_2 (дата обращения: 15.09.2025).
Информация с rmj.ru






