Андрей Борисович Данилов, д.м.н., профессор кафедры нервных болезней ИПО ФГАОУ ВО Первый МГМУ им.. И.М. Сеченова Минздрава России (Сеченовский Университет) выступил с докладом о новых взглядах на остеохондроз.


А.Б. Данилов отметил, что остеохондроз — не единственная причина боли в спине. Зачастую пациентов подталкивают к дополнительным, возможно, ненужным инструментальным методам исследования (рентгенография, МРТ и др.), результаты которых плохо коррелируют с неврологической симптоматикой и не дают ответа на вопрос о причинно-следственных связях морфологических и структурных изменений и болевого синдрома.. По мнению зарубежных авторов, остеохондроз — это дегенерация межпозвонкового диска (ДМД) [1]. ДМД является основным источником боли в спине и корешковой боли. Детальное выяснение патогенеза ДМД способствует разработке эффективных методов лечения боли в спине.. Патогенез ДМД очень сложен. Доказано, что он включает в себя апоптоз клеток, аутофагию, провоспалительный «цитокиновый шторм» и повышенный катаболизм матрикса. Накопление стареющих клеток в дегенеративно измененном диске предполагает пагубную роль старения клеток в патогенезе ДМД. С одной стороны, стареющие клетки диска теряют репликативную способность, что влечет за собой постепенное снижение количества функциональных клеток.. С другой стороны, у стареющих клеток диска изменяется набор секретируемых веществ, что меняет характер окружающей микросреды на воспалительный.. Они уменьшают производство внеклеточного матрикса и усиливают его деградацию.. Провоспалительные цитокины, секретируемые стареющими клетками диска, включая TNF-α, IL-1α/β, IL-17, IL-6, COX-2 и хемокины, могут способствовать старению соседних клеток диска и инфильтрации иммунных клеток, а затем усиливать воспаление в микросреде дегенеративно-измененного диска.. Таким образом, стареющие клетки диска претерпевают фенотипические изменения и нарушают баланс между анаболизмом и катаболизмом внеклеточного матрикса в дисках. В результате дегенерация диска ускоряется [2, 3]. Дальнейшее усиление воспалительной реакции происходит за счет инфильтрации иммуноцитов, а также неоваскуляризации и прорастания нервов в структурно дефектные ткани диска. На заключительном этапе происходит сенсибилизация нервных окончаний и модуляция активности болевого канала дорсального корешкового ганглия медиаторами воспаления и нейротрофинами, что приводит к боли.
Профессор А.Б. Данилов подчеркнул, что дискогенная боль четко локализована, носит аксиальный характер, не иррадиирует. Как остановить этот процесс разрушения? К сожалению, возможности организма крайне ограничены, снижение содержания хондроитина сульфата в диске прямо пропорционально степени его деградации.
Изучение воспалительных механизмов дискогенной боли является весьма перспективным направлением, прежде всего, с точки зрения развития терапевтических возможностей.
Подходы к патогенетической терапии боли в спине включают (рис. 1):
генно-инженерную терапию;
антикатаболические препараты (TIMPs);
N-пептид;
ингибиторы NF-kB;
блокаторы SASP (хондроитин, агрекан);
терапию стволовыми клетками [4].
![Рис. 1. Предполагаемый биохимический каскад в процессе старения диска и потенциальные терапевтические мишени [4] Рис. 1. Предполагаемый биохимический каскад в процессе старения диска и потенциальные терапевтические мишени [4]](https://medblog.su/wp-content/uploads/2021/12/1639228168_74_dva-vzglyada-na-problemu-osteoartrita-i-osteohondroza-sravnenie-podhodov-k-terapii-postreliz.png)
Среди перечисленных подходов на сегодняшний день только блокаторы SASP (в т.ч. хондропротекторы) доступны для реальной клинической практики.. Патогенетическая терапия — это способ предупредить дегенерацию диска, процессы воспаления и, соответственно, дать возможность пациенту жить без боли. Хондропротекторы являются не только патогенетической терапией, но и обладают стратегическим действием — защищают человека от многих проблем будущего, в частности, предупреждая дегенеративные изменения в суставах. Компания «Промомед» производит биоактивный хондропротектор с уникальным составом — АМБЕНЕ®Био, который эффективно справляется с болью всего за 1 курс терапии — 10 инъекций по 2 мл через день. Как показали результаты исследования И.В. Меньшиковой и В.И. Сороцкой (2021), после первого курса АМБЕНЕ®Био наблюдается значимое уменьшение боли при движении на 40–57%, боли в покое на 54–71%, причем положительные изменения сохраняются в течение последующих 6 мес. [5].
Высокая эффективность препарата АМБЕНЕ®Био и его модулирующее хондропротективное действие обусловлены синергией четырех компонентов: хондроитина сульфата, полипептидов, 15 аминокислот, микро- и макроэлементов (рис.. 2) [6]. Профессор А.Б. Данилов отметил, что длительный терапевтический эффект препарата в течение 6 мес. достигается благодаря современной технологии его производства.
![Рис. 2. Состав и эффекты комплексного препарата АМБЕНЕ®Био [6] Рис. 2. Состав и эффекты комплексного препарата АМБЕНЕ®Био [6]](https://medblog.su/wp-content/uploads/2021/12/1639228168_990_dva-vzglyada-na-problemu-osteoartrita-i-osteohondroza-sravnenie-podhodov-k-terapii-postreliz.png)
В конце своего выступления А.Б. Данилов подчеркнул, что для реализации персонализированного подхода к терапии недостаточно иметь только клинические рекомендации, необходимо учитывать очень много факторов, связанных с самим пациентом, к которым относятся индивидуальный фенотип боли, возраст, пол, психика, сон, физическая активность, когнитивные функции, социальные факторы, коморбидность.
Продолжил сессию Александр Михайлович Лила, д..м.н., профессор, директор ФГБНУ НИИР им. В..А. Насоновой, который представил доклад о персонализированном подходе к терапии пациентов с остеоартритом (ОА).

Согласно современным рекомендациям комплексное лечение больных ОА включает немедикаментозные и медикаментозные методы, при этом профессор А.М. Лила обратил внимание на ряд факторов, которые практикующий врач должен учитывать, принимая пациента с данной нозологией..
Факторы, определяющие терапию ОА:
локализация процесса (к основным локализациям первичного ОА относятся мелкие суставы кистей, коленные, тазобедренные суставы);
возраст, пол, общий статус, коморбидные состояния;
рентгенологические стадии остеоартрита;
фенотип ОА (табл. 1);
![Таблица 1. Фенотипы ОА коленного сустава [7] Таблица 1. Фенотипы ОА коленного сустава [7]](https://medblog.su/wp-content/uploads/2021/12/1639228168_677_dva-vzglyada-na-problemu-osteoartrita-i-osteohondroza-sravnenie-podhodov-k-terapii-postreliz.png)
эффективность предшествующей терапии;
готовность пациента выполнять врачебные рекомендации.
А.М. Лила подчеркнул, что создание классификации, основанной на фенотипировании пациентов в зависимости от преобладающих патофизиологических изменений, является основополагающим фактором как для индивидуального подбора терапии, так и для перехода от недостаточно эффективного симптоматического лечения к более эффективному болезнь-модифицирующему.
А.М. Лила представил два концептуальных подхода к фенотипированию ОА, предложенных F. Berenbaum [8]: движение «сверху вниз» (top-down), который основан на уже известных фактах о заболевании, и движение «снизу вверх» (step-up), который предполагает поиск фенотипа на основе сложных статистических методов (рис. 3) [9].
![Рис. 3. Подходы к фенотипированию ОА [9] Рис. 3. Подходы к фенотипированию ОА [9]](https://medblog.su/wp-content/uploads/2021/12/1639228168_846_dva-vzglyada-na-problemu-osteoartrita-i-osteohondroza-sravnenie-podhodov-k-terapii-postreliz.png)
Отдельного внимания заслуживают пожилые пациенты с наличием двух и более заболеваний, которые называют «коморбидными заболеваниями» или «коморбидными состояниями». У этой группы пациентов обязательно должны учитываться фармакокинетические и фармакодинамические лекарственные взаимодействия.
Профессор А.М. Лила подчеркнул, что для лечения ОА у пациентов с коморбидными состояниями должны использоваться лекарственные препараты с благоприятным профилем безопасности. К таким препаратам следует отнести симптоматические препараты замедленного действия (symptomatic slow acting drugs for osteoarthritis, SYSADOAs), в т.ч. АМБЕНЕ®Био, обладающие собственным анальгетическим эффектом, участвующие в подавлении катаболического воспаления, лежащего в основе прогрессирования ОА [10].
Кроме того, отдельное внимание стоит уделять нефармакологическим методам лечения ОА: лечебной физкультуре, использованию роботизированных экзоскелетов.
В заключение своего выступления А.М. Лила подчеркнул, что симптом-модифицирующая терапия должна быть назначена каждому пациенту как можно раньше после постановки диагноза ОА.
Завершил сессию Алексей Юрьевич Феклистов, м.н.с. лаборатории остеопороза отдела метаболических заболеваний костей и суставов, заместитель главного врача ФГБНУ НИИР им. В.А. Насоновой,

c докладом, в котором впервые представил результаты клинического исследования, проведенного под руководством НИИ ревматологии в пяти клинических центрах России, по оценке эффективности и безопасности препарата Амбене®Био (КОЛИБРИ).
Критериями включения в исследование были:
возраст старше 18 лет;
ОА коленных, тазобедренных или мелких суставов кистей I–III рентгенологической стадии по Kellgren — Lawrence;
боль при движении более 40 мм по визуально-аналоговой шкале (ВАШ);
прием стабильной дозы НПВП не менее чем за 4 нед. до начала исследования;
подписанное информированное согласие;
желание и способность пациента принять участие в исследовании.
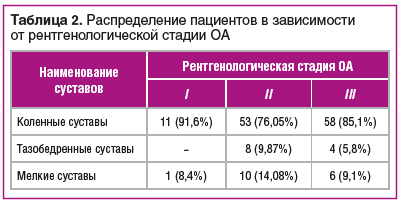
В исследовании 155 пациентов (92% женщин, 8% мужчин) получали терапию препаратом комплексного действия Амбене®Био. Пациенты с ОА коленных суставов составили 54%, с генерализованным ОА — 31%, ОА мелких суставов — 12%, ОА тазобедренных суставов — 3%. Большинство пациентов имели II–III стадию заболевания (табл. 2).
Схемы применения препарата представлены в таблице 3.

Результаты лечения пациентов оценивали по ВАШ боли в покое и при движении, индексам AUSCAN, WOMAC через 12 мес. (табл. 4).
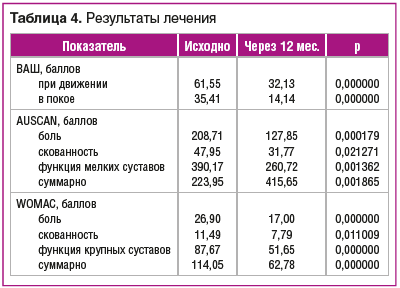
Результаты многоцентрового клинического исследования эффективности и безопасности препарата АМБЕНЕ®Био доказали, что терапия с его использованием у больных ОА мелких и крупных суставов позволяет добиться уменьшения выраженности болевого синдрома, улучшения функции суставов и обеспечивает замедление прогрессирования ОА у пациентов. Применение АМБЕНЕ®Био дает возможность снизить потребность в НПВП и сократить их прием, что особенно важно для коморбидных пациентов, при этом препарат хорошо переносится. Анальгетический и хондропротективный эффект препарата наблюдался уже после первого курса терапии и сохранялся до 6 мес. после его окончания. Короткая схема терапии (по 2 мл через день курсом 10 инъекций) позволяет быстро и эффективно достигнуть длительного терапевтического эффекта.
В заключение своего выступления А.Ю. Феклистов особо подчеркнул, что результаты клинического исследования «КОЛИБРИ» позволяют рассматривать препарат АМБЕНЕ®Био как эффективное средство для терапии пациентов с ОА крупных и мелких суставов, обладающее благоприятным профилем безопасности. А выпуск новой дозировки 2 мл дает возможность проводить лечение коротким курсом (10 инъекций) и получить длительный эффект.
Мероприятие проведено при поддержке ГК «Промомед»
.
Информация с rmj.ru