Введение
В офтальмохирургии с каждым днем появляются новые технологии и методики, позволяя достичь высоких результатов в лечении заболеваний глаз, обеспечивая пациентам успешное восстановление зрения и улучшение качества их жизни. Для терапии глаукомы, заболеваний сетчатки и стекловидного тела применяются не только хирургические, но и лазерные методы лечения, играющие важную роль в офтальмологии. Например, они успешно используются для селективной лазерной трабекулопластики, иридэктомии и гониопунктуры при глаукоме [1, 2]. Особенно эффективными оказываются процедуры, включающие использование СО2-лазера. Этот тип лазерного оборудования позволяет достичь высокой точности и контроля реза во время операций, что особенно важно при таких сложных вмешательствах, как лечение глаукомы [3]. В витреоретинальной хирургии обычно применяется зеленый лазер с длиной волны (λ) 532 нм, который используется в основном для эндокоагуляции сетчатки. Некоторые заболевания глаз, такие как пролиферативная витреоретинопатия и диабетическая ретинопатия, сопровождаются образованием патологических мембран на поверхности сетчатки и прорастанием в них новообразованных сосудов. Это приводит к ряду осложнений в виде кровоизлияний под сетчатку и в полость стекловидного тела, тракционной отслойке сетчатки [4], что может быть неблагоприятным для зрения пациента.
Актуальность разработки новых инструментов для удаления преретинальных образований, позволяющих не повреждать сетчатку, трудно переоценить. Механические инструменты, такие как пинцеты, вертикальные и горизонтальные ножницы, шпатели и скраперы, петли, долгое время были основными инструментами в хирургии данного профиля. Но их применение не уменьшает риск интраоперационных осложнений, таких как кровоизлияния в витреальную полость [4] и формирование ятрогенных разрывов сетчатки, последствиями которых могут быть отслойка сетчатки [5, 6] и субретинальное кровоизлияние [7]. Для предотвращения осложнений, вызванных излишним тракционным воздействием на ткань сетчатки при удалении патологических мембран, необходимо разработать методику, минимизирующую механическое воздействие на слои сетчатки. Кроме того, важно снизить термические повреждения при коагуляции источников кровотечения. В данном случае лазерные технологии могут стать перспективной альтернативой механическим инструментам.
В литературе отмечается, что использование лазерного излучения для разрезания биологических тканей обеспечивает точность, сравнимую с механическими инструментами [8]. Лазеры с длиной волны в ультрафиолетовом и инфракрасном (ИК) диапазоне обладают уникальной способностью проникать в биологические ткани, что и послужило основой для создания термина «лазерный нож». Лазеры ИК-диапазона ранее использовались только в военных и промышленных целях, теперь их потенциал в области медицины начинает расширяться и активно исследоваться [9–11]. Исследования показывают, что ИК-излучение обладает уникальными свойствами. Благодаря спектральному поглощению воды и белков, находящемуся на уровне 3 и 6–8 мкм соответственно, открываются новые возможности применения лазера в медицине: в данном диапазоне можно проводить абляцию биологических тканей с высокой эффективностью [12].
За счет вышеперечисленного, на наш взгляд, лазерные источники среднего ИК-диапазона могут занимать определенную нишу и в общей хирургии, и в офтальмохирургии — в частности, для осуществления прецизионных резов, абляции как патологических, так и нормальных тканей глаза. При этом существует вероятность получить незначительное коллатеральное повреждение в зоне абляции. Для подтверждения или опровержения вынесенной гипотезы необходимо было провести ряд экспериментов. Перед проведением исследования необходимо было тщательно изучить потенциальные риски и возможную пользу от воздействия лазерного излучения среднего ИК-диапазона в эксперименте (на ткани свиных глаз). Нам удалось установить, что длина волны 3000 нм определенным образом воздействует на склеру, сосудистую оболочку глаза и сетчатку. Результаты нашего исследования показали, что данное лазерное излучение способно проводить рассечение склеры и сосудистой оболочки глаза с минимальным коллатеральным повреждением [13]. На следующем этапе эксперимента необходимо оценить воздействие данного лазера на ткани кадаверных глаз и сравнить его при аналогичных параметрах с применяющимся в настоящее время в витреоретинальной хирургии лазером с λ=532 нм для определения эффективности и безопасности применения данного лазера с λ=3000 нм.
Цель исследования: проанализировать и сравнить воздействие на структуры глаза лазерного излучения с λ=3000 и 532 нм.
Содержание статьи
Материал и методы
В качестве источника ИК-излучения использовали лазерный скальпель среднего ИК-диапазона 2–8 мкм для прецизионной хирургии, разработанный в ГОИ им. С.И. Вавилова. В качестве лазера с λ=532 нм использовали лазерный стенд контроля оптических элементов и оптико-электронных систем в ультрафиолетовом и видимом диапазоне (на базе ГОИ им. С.И. Вавилова).
Для целей данного эксперимента был выбран специфический диапазон λ, который может оказать значительное воздействие на биологические ткани. Эксперимент проведен с использованием рабочейλ=3000 нм. Лазерное излучение с λ=532 нм, используемое в витреоретинальной хирургии для эндолазеркоагуляции сетчатки, было использовано для сравнения в данном исследовании.
Эксперимент проводили на кадаверных глазах. После энуклеации глаза помещали в транспортировочный контейнер при температуре 3 °С. На месте проведения эксперимента осуществляли подготовку тканей глаза к облучению. Методика описана ранее [13]. На сегодняшний день используемая лазерная установка не оснащена волноводом, что ограничивает возможности проведения экспериментов. Именно из-за отсутствия данной системы проведение экспериментов ограничено воздушной средой, иначе вода полностью поглощает ИК-излучение, не позволяя достичь необходимого воздействия на структуры глазного яблока. Для успешной реализации исследования дополнительно убирали остаточную влагу с поверхности облучаемых тканей. В промежутках между лазерным воздействием на ткани их орошали раствором BSS (balanced salt solution — солевой сбалансированный раствор) с целью предотвращения пересыхания и сохранения их структуры. Такой подход позволял добиться оптимальных результатов при воздействии на ткани лазерным излучением.
Для стандартизации результатов исследования использовали одинаковые параметры лазерного излучения для лазера с различной λ (3000 и 532 нм): энергия (Е) излучения — 1, 2 и 3 мДж; частота (ν) излучения — 100 и 1000 Гц. Воздействие лазерным излучением осуществляли в виде одиночных импульсов (ν=100 Гц) и непрерывным режимом (ν=1000 Гц).
Для оценки воздействия на ткани глаза использовались методы фото-, видеофиксации и данные сканирующего электронного микроскопа EVO LS10 (Zeiss, Германия).
После выполнения лазерной коагуляции образцов сразу же начинали фиксацию в глютаровом альдегиде на 1 сут. Затем приступали к разрезанию зафиксированных образцов микротомным лезвием Accu-Edge (Sakura Seiki Co, Япония). После этого образцы постепенно обезвоживали, используя различные концентрации спирта от 20 до 97%. Не использовали процесс сушки в обход критической точки углекислого газа, вместо него проводили напыление металлами для предотвращения исчезновения части вещества в газе и избежания излишней конденсации образцов (что было необходимо для решения морфометрических задач).
Исследования были осуществлены при низком вакууме (EP, 70 Па), где напряжение составляло 21 кВ, а ток на образце достигал 94 пА. Съемка была сделана в режиме обратно-рассеянных электронов. Разрешение изображений было 3072 на 2304 пикселя с плотностью 1,8 мкм/пиксель при увеличении в 100 пикселей, 1,3 мкм/пиксель при увеличении в 200 пикселей и 898,9 нм/пиксель при увеличении в 300 пикселей. Наблюдения проводились с использованием рабочего расстояния от 7 до 12 мм.
При помощи программного обеспечения GNU Image Manipulation Program, позволяющего редактировать изображения, выполнять манипуляции с графикой и создавать новые визуальные эффекты, были проанализированы полученные изображения после электронной микроскопии в формате TIF. Проведены расчеты глубины, диаметра коагулята и ширины коллатерального повреждения.
Результаты исследования
Вследствие отсутствия соответствующего волновода и специального наконечника эксперимент проводили в воздушной среде. В результате взаимодействия с жидкостью обнаружено, что лазерное излучение с λ=3000 нм не проходит сквозь нее без потерь — оно поглощается, вызывая формирование пузырьков на поверхности границы раздела сред. Такое поглощение не оказывает негативного влияния на внутренние структуры глаза, находящиеся под слоем воды, включая сетчатку, хориоидею и склеру (рис. 1). Чтобы добиться желаемого эффекта от лазерного излучения на ткань в жидкой среде, крайне важно расположить источник излучения как можно ближе к целевой области. После проведения эксперимента на кадаверных глазах выявлены признаки аутолиза сетчатки, что объясняется временным промежутком более 12 ч между удалением глаз и началом исследования. В процессе удаления стекловидного тела оставить сетчатку без повреждений зачастую не удавалось, и даже использование единичных лазерных импульсов с мощностью в 1 мДж при λ=3000 и 532 нм приводило к дефекту на всю толщину сетчатки. Это подчеркивает сложность процедуры, несмотря на ее кажущуюся простоту.

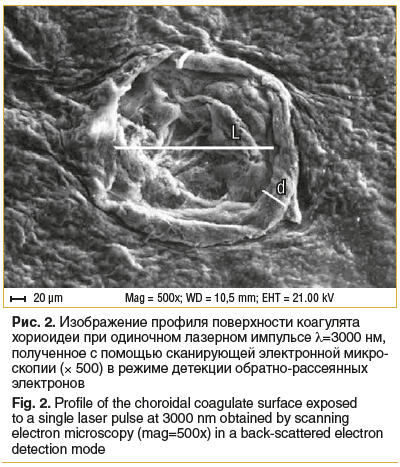
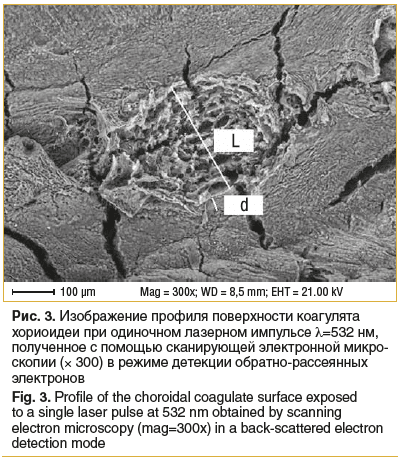
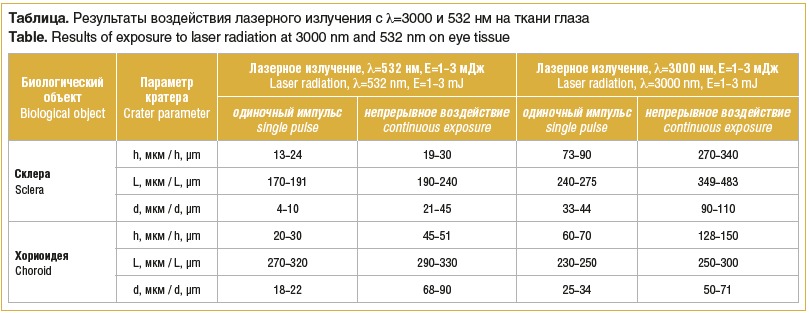
При воздействии на хориоидею излучением λ=3000 нм в режиме одиночного импульса (рис. 2) глубина (h) кратера составила 60–70 мкм, ширина (L) кратера — 230–250 мкм, зона коллатерального повреждения (d) — 25–34 мкм. При воздействии на хориоидею излучением λ=532 нм в режиме одиночного импульса (рис. 3) h составила 20–30 мкм, L — 270–320 мкм, d — 18–22 мкм.
При воздействии на склеру излучением λ=3000 нм в режиме одиночного импульса (рис. 4) h составила 73–90 мкм, L — 240–275 мкм, d — 33–44 мкм. При воздействии на склеру излучением λ=532 нм в режиме одиночного импульса (рис. 5) h составила 13–24 мкм, L — 170–191 мкм, d — 4–10 мкм.


При воздействии на хориоидею излучением λ=3000 нм в непрерывном режиме (рис. 6, 7) h составила 128–150 мкм, L — 250–300 мкм, d — 50–71 мкм. При воздействии излучением λ=532 нм на хориоидею в непрерывном режиме (рис. 8) h составила 45–51 мкм, L — 290–330 мкм, d — 68–90 мкм.



При воздействии на склеру излучением λ=3000 нм в непрерывном режиме (рис. 9) h составила 270–340 мкм, L — 349–483 мкм, d — 90–110 мкм. При воздействии на склеру излучением λ=532 нм в непрерывном режиме h составила 19–30 мкм, L — 190–240 мкм, d — 21–45 мкм.

Данные о коллатеральном повреждении в зоне коагулята в тканях глаза, полученного при разных видах излучения, представлены в таблице.
Обсуждение
В нашем исследовании мы изучили влияние лазерного скальпеля среднего ИК-диапазона 2–8 мкм для прецизионной хирургии на ткани кадаверных глаз в сравнении с лазерным излучением 532 нм. Мы провели анализ данных об абляции и коллатеральном повреждении, выявив важные особенности воздействия лазерного излучения на ткани глаза в газовоздушных условиях. Особое внимание мы уделили лазеру с λ=3000 нм, который, по нашему мнению, открывает новые возможности для применения в медицине, в частности в офтальмохирургии. Мы поставили перед собой цель изучить перспективы использования данного лазера в различных областях, включая витреоретинальную хирургию и хирургию глаукомы, особенно в контексте выкраивания склерального лоскута. В рамках исследования было осуществлено сравнение воздействия лазерного излучения с λ=3000 нм на ткани глаза с действием широко применяемого в офтальмологии лазерного излучения с λ=532 нм. Мы обнаружили интересные различия и сходства в реакции тканей на разные типы лазеров, что может иметь важное значение для развития современной офтальмологии. Кроме того, помимо общего анализа эффективности лазера, мы также уделяли внимание вопросу безопасности его применения и потенциальным осложнениям в случае возможного внедрения в клиническую практику.
Лазер Er (Erbium/Эрбий): YAG (Yttrium Aluminum Garnet / Иттрий-алюминиевый гранат) имеет рабочую длину волны 2,94 мкм, что максимально соответствует длине волны, применяемой нами в эксперименте. G.A. Peyman et al. [14] были пионерами в использовании Er:YAG-лазера с λ=2,94 мкм в качестве инструмента исследования воздействия лазерного излучения среднего ИК-диапазона на структуры заднего отрезка глаза. Под руководством профессора D.J. D`Amico [15] в 1994 г. были предприняты первые шаги в изучении воздействия Er:YAG-лазера на сетчатку энуклеированных глаз кроликов. Было отмечено, что использование одиночных импульсов лазерного излучения на сетчатку в воздушной среде вызывало образование кратеров, h которых напрямую зависела от плотности потока Е. Уже на первых этапах исследования было выявлено, что минимальная h кратера, достигаемая при воздействии лазера, составляла 30 мкм и прямо коррелировала с плотностью потока Е в размере 1,3 Дж/см2. Тем самым исследование пролило свет на важные параметры воздействия лазерного излучения на сетчатку и его потенциальные последствия. Ретинотомия, то есть образование кратера, пронизывающего всю толщину сетчатки, наблюдалась при плотности потока Е, равной 3,9 Дж/см2. Интересно, что при изучении диапазона d было выявлено, что ее ширина варьируется от 15 до 40 мкм. По результатам исследований стало ясно, что аддитивный эффект возникает в результате последовательного воздействия множественными импульсами. Этот результат говорит о значительной изменчивости процессов, происходящих в тканях глаза при воздействии на них таких импульсов. По мнению авторов, проведение частичной абляции наружных слоев сетчатки может послужить моделью для абляции эпиретинальных образований. Открытие такой модели имеет огромный потенциал в сфере хирургии заднего отрезка глаза, открывая новые возможности для развития новых лечебных методик и технологий [15].
По результатам нашего исследования ретинотомии удалось достигнуть при воздействии одиночными импульсами с Е=1 мДж при λ=3000 и 532 нм. Так как при воздействии лазерным излучением с λ=532 нм и Е=100 мДж на сетчатку во время эндолазеркоагуляции при операции мы достигаем формирования коагулята белого цвета без сквозного дефекта в сетчатке, то данные эксперимента указывают на развитие аутолиза в сетчатке кадаверных глаз, чем и объясняется образование сквозного дефекта даже при Е=1 мДж. Исследование показывает, что использование λ=3000 нм может быть эффективным средством для лечения патологий на поверхности сетчатки, особенно при снижении Е до уровня ниже 1 мДж. Следовательно, требуется проведение дальнейших исследований в этом направлении. Необходимо глубже изучить влияние различных параметров лазерного излучения in vitro, в том числе проведение качественной оценки воздействия ИК-лазера диапазона 2–8 мкм на сетчатку глаза. Только после этого можно переходить к исследованию in vivo, что поможет получить полноценные данные об эффективности и безопасности использования данного метода в медицине. Необходимо иметь в виду, что выбор параметров лазерного излучения играет ключевую роль в успешном проведении хирургических процедур на сетчатке глаза. Оптимальное сочетание λ, мощности лазера и времени воздействия обеспечивает желаемый эффект без негативных последствий для пациента.
T. Hutchens et al. [16] провели исследования в области лазерной хирургии, создав эндозонд для Er:YAG-лазера с уникальной конструкцией. В данном эндозонде был использован полый волновод с пятью сапфировыми микросферами на конце, что привело к значительному улучшению характеристик лазерного излучения. Излучение на конце волновода позволяло добиться абляции с h 10–20 мкм, что намного ниже, чем данные, полученные нами. Создатели эндозонда также интегрировали в него дополнительное освещение, что способствовало улучшению визуализации в зоне проведения операции. Увеличение толщины эндозонда, обусловленное добавлением освещения, привело к расширению возможностей использования данного инструмента в хирургии глаза. Новый дизайн эндозонда позволил повысить точность и эффективность процедур, но при этом привел к увеличению размеров склеротомических отверстий, что несколько не соответствует современной тенденции в микрохирургии, нацеленной на уменьшение размеров входных отверстий. По мнению авторов, использование Er:YAG-лазера с разработанными ими эндозондами может стать перспективной альтернативой традиционным механическим инструментам во время витреоретинальной хирургии. Внедрение данной технологии позволит повысить эффективность операций и улучшить результаты лечения пациентов, открывая новые возможности в области офтальмологии.
S. Borirakchanyavat et al. [17] эксперимент проводили на глазах кроликов, изучали эффективность применения Ho:YAG-лазера с λ=2 мкм для рассечения шварт стекловидного тела. По результатам исследования было установлено, что для проведения ретинотомии требуется плотность Е на уровне 190 Дж/см2, а кончик зонда должен находиться на расстоянии до 1,5 мм от поверхности сетчатки. Также стоит отметить, что зона коллатерального термического повреждения, выявленная в работе, оказалась в пределах от 150 до 450 мкм, что значительно выше, чем в нашем исследовании.
Важно отметить, что воздействие лазерным излучением на сосудистую оболочку и склеру глаза может вызывать значительные изменения в их структуре. Результаты исследований показали, что при использовании лазера с λ=3000 нм наблюдается значительное увеличение h, L кратера и d по сравнению с таковыми при использовании лазера 532 нм. Более того, эти результаты не зависят от того, используется одиночный импульс или непрерывное воздействие. Такая проникающая способность лазерного излучения с λ=3000 нм демонстрирует его высокую эффективность в разрезании ткани. Это открывает новые перспективы для его применения в хирургии, включая эндорезекцию опухолей сетчатки, сосудистой оболочки, а также в склерэктомии и склеротомии при антиглаукомных процедурах. Подобные исследования открывают возможности для разработки более точных и эффективных методов лазерной хирургии глаза. Витреоретинальная хирургия представляет собой сложную область медицины, где даже малейшие повреждения сосудистой оболочки могут привести к серьезным геморрагическим осложнениям во время операции, что усложняет вмешательство, увеличивает его продолжительность и негативно сказывается на результате лечения. Коллатеральное повреждение сосудистой оболочки при работе лазером λ=3000 нм оказывает положительное воздействие на гемостаз, что весьма значимо для успешного проведения операций. Считается, что способность данного лазера проводить разрезы ткани с одновременной коагуляцией краев разреза значительно увеличивает эффективность оперативного вмешательства, минимизируя риск возникновения геморрагических осложнений и снижая время восстановления пациента после операции. Таким образом, применение лазера с λ=3000 нм в витреоретинальной хирургии может значительно повысить успешность операций и улучшить функциональные результаты лечения благодаря его способности к точному и эффективному воздействию на ткани. Исследования in vivo играют важную роль в понимании взаимосвязи между зоной коллатерального повреждения тканей и контракционным эффектом. Чем меньше эта зона, тем меньше риск развития в дальнейшем пролиферативных тканей. Расширение исследований in vivo позволит более точно определить оптимальные методы исключения коллатерального повреждения для минимизации контракционного эффекта.
Результаты нашей работы показали интересные закономерности влияния различных импульсов на h кратеров в сосудистой оболочке глаза. В ходе экспериментов было обнаружено, что после одиночного импульса с Е=3 мДж кратер достигал h 67 мкм, а при множественных импульсах с такой же Е — 150 мкм. Кроме того, влияние импульсов также вызывало образование зоны коллатерального повреждения шириной от 25 до 71 мкм в зависимости от количества импульсов. Эти результаты ставят под сомнение возможность сквозного рассечения сосудистой оболочки глаза при использовании лазерного излучения, учитывая толщину хориоидеи, которая у людей старше 50 лет составляет 230–250 мкм [18, 19]. Поэтому при текущих параметрах лазерного воздействия рассечение хориоидеи in vivo, скорее всего, не будет сквозным. Однако с увеличением интенсивности излучения существует возможность достичь сквозного рассечения сосудистой оболочки глаза, минимизируя при этом ущерб для окружающих тканей. При пересадке ретинального пигментного эпителия важно учитывать возможность эффективного гемостаза за счет коллатерального термического повреждения на этапе выкраивания комплекса пигментный эпителий — хориоидея. Когда речь идет о минимизации повреждений окружающих тканей в ходе лечения, важно понимать, что использование лазера позволяет уменьшить зону коллатерального повреждения, не уменьшая при этом размер выкраиваемого лоскута. Кроме того, при эндорезекции опухолевого очага сосудистой оболочки глаза, особенно при ее парамакулярном расположении, использование лазерного скальпеля окажется крайне эффективным. Эта техника позволит ограничивать зону удаления опухоли и свести риск повреждения окружающих тканей до минимума. Таким образом, использование технологий лазерного рассечения в офтальмологии открывает новые перспективы для лечения заболеваний глаз и повышает эффективность медицинского вмешательства.
Наши результаты показали, что при работе с лазерным излучением λ=3000 нм размеры кратера и зона коллатерального повреждения в склеральной оболочке статистически значимо превышают подобные показатели в хориоидее. Обратная картина наблюдается для лазерного излучения с λ=532 нм. Скорее всего, это связано с тем, что лазерное излучение с λ=532 нм хорошо поглощается пигментом в хориоидее, а в склере меньше воды, за счет чего излучение с λ=3000 нм лучше проникает в ткань.
Т. Klink et al. [20] провели эксперимент с использованием Er:YAG-лазера для выкраивания склерально-роговичного лоскута на энуклеированных свиных глазах. Они использовали следующие параметры работы лазера: Е — в диапазоне от 75 до 80 мДж, длительность импульса — от 50 до 250 мс, частота — от 5 до 70 Гц. При таких настройках лазера d склеры составила 10–30 мкм. Несмотря на то, что Е в их исследовании была намного ниже — от 1 до 3 мДж, чем в других работах, и частота была в 100 раз выше, результаты их исследования показали в 3 раза большую глубину реза ткани. Это указывает на то, что для увеличения глубины реза ткани лазерным скальпелем и одновременного сокращения зоны термического повреждения можно использовать стратегию увеличения Е и частоты при одновременном снижении длительности импульса излучения. Такие выводы актуализируют возможности использования высокоэнергетических лазеров в хирургической практике для точных манипуляций с тканями при минимальном воздействии на окружающие структуры. Глубокие и точные разрезы, как показывает исследование, могут быть достигнуты путем тщательной настройки параметров лазерного воздействия.
Заключение
Исследование, проведенное нами, сфокусировалось на оценке воздействия различных длин волн лазерного излучения на оболочки кадаверных глаз. Мы провели анализ эффектов лазерного излучения с λ=3000 и 532 нм, сравнили их и выявили различия между ними. Оказалось, что при использовании лазерного излучения с λ=3000 нм наблюдается более значительное воздействие на ткани глаза, чем при использовании λ=532 нм. Согласно нашим результатам при работе с лазером λ=3000 нм наблюдается увеличение h, L, d тканей глаза (включая сетчатку, сосудистую оболочку и склеру), по сравнению с лазером λ=532 нм при примерно одинаковых параметрах работы. При воздействии на склеру разница в размерах кратера больше, чем при воздействии на хориоидею. Это связано с тем, что в склере процентное содержание воды меньше, чем в сосудистой оболочке глаза, а пик спектрального поглощения воды находится в спектре 3 мкм. Глубина кратера при воздействии на оболочки глаза излучениемλ=3000 нм и E=3 мДж составляет 150–350 мкм. При увеличении энергии и частоты излучения можно добиться сквозного реза, таким образом, лазерным излучением в среднем ИК-диапазоне и при определенных параметрах работы лазера можно достигнуть сквозного рассечения оболочек глаза. Например, полнослойное разрезание сетчатки может быть использовано при проведении ретинотомии; хориоидеи — при пересадке пигментного эпителия сетчатки, эндовитреальном удалении внутриглазных ново-образований; склеры — при выкраивании склерального лос-кута. На сегодняшний день, судя по данным эксперимента, абляцию патологических эпиретинальных мембран сделать не представляется возможным, поэтому дальнейшие исследования в этом направлении необходимы для оптимизации параметров лазерного излучения, средств доставки лазерного излучения к оболочкам глаза, что может существенно повысить эффективность офтальмологических операций.
СВЕДЕНИЯ ОБ АВТОРАХ:
Юсеф Юсеф — д.м.н., профессор, директор ФГБНУ «НИИГБ им. М.М. Краснова»; 119021, Россия, г. Москва, ул. Россолимо, д. 11А, Б; ORCID iD 0000-0003-4043-456X
Петрачков Денис Валериевич — к.м.н., заведующий отделом «Инновационные витреоретинальные технологии» ФГБНУ «НИИГБ им. М.М. Краснова»; 119021, Россия, г. Москва, ул. Россолимо, д. 11А, Б; ORCID iD 0000-00034757-5584
Коробов Егор Николаевич — к.м.н., младший научный сотрудник отдела «Инновационные витреоретинальные технологии» ФГБНУ «НИИГБ им. М.М. Краснова»; 119021, Россия, г. Москва, ул. Россолимо, д. 11А, Б; ORCID iD 0000-0003-3254-4451
Новиков Иван Александрович — старший научный сотрудник отдела «Лаборатория фундаментальных исследований в офтальмологии» ФГБНУ «НИИГБ им. М.М. Краснова»; 119021, Россия, г. Москва, ул. Россолимо, д. 11А, Б; ORCID iD 0000-0003-4898-4662
Контактная информация: Коробов Егор Николаевич, e-mail: egorkorobov1991@mail.ru
Источник финансирования: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 12.02.2025.
Поступила после рецензирования 07.03.2025.
Принята в печать 01.04.2025.
ABOUT THE AUTHORS:
Yusef Yusef — Dr. Sc. (Med.), Professor, Director of M.M. Krasnov Research Institute of Eye Diseases; 11A, B, Rossolimo str., Moscow, 119021, Russian Federation; ORCID iD 0000-0003-4043-456X
Denis V. Petrachkov — C. Sc. (Med.), Head of the Department of Advanced Vitreoretinal Technologies, M.M. Krasnov Research Institute of Eye Diseases; 11A, B, Rossolimo str., Moscow, 119021, Russian Federation; ORCID iD 0000-00034757-5584
Egor N. Korobov — C. Sc. (Med.), Junior Scientific Officer at the Department of Advanced Vitreoretinal Technologies, M.M. Krasnov Research Institute of Eye Diseases; 11A, B, Rossolimo str., Moscow, 119021, Russian Federation; ORCID iD 0000-0003-3254-4451
Ivan A. Novikov — Senior Scientific Officer at the Department of Laboratory of Fundamental Researches in Ophthalmology, M.M. Krasnov Research Institute of Eye Diseases; 11A, B, Rossolimo str., Moscow, 119021, Russian Federation; ORCID iD 0000-0003-4898-4662
Contact information: Egor N. Korobov, e-mail: egorkorobov1991@mail.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 12.02.2025.
Revised 07.03.2025.
Accepted 01.04.2025.
материал rmj.ru
