Содержание статьи
Введение
Пресбиопия, или возрастное ослабление аккомодации глаза, представляет собой физиологический процесс, патогенетическую основу которого связывают с постепенным изменением эластичности хрусталика и ремоделированием цилиарной мышцы [1, 2]. Пресбиопия представляет собой глобальную медико-социальную проблему, наблюдаемую у 80% населения в возрасте старше 40 лет. В условиях общего старения населения и увеличения продолжительности активной жизни прогрессирующая неспособность к фокусировке на близком расстоянии становится значимым фактором, снижающим профессиональную деятельность, повседневную независимость и качество жизни в целом [3–5].
Современные клинические подходы, включая прогрессивные очковые и контактные линзы, а также интраокулярные и лазерные хирургические вмешательства, направлены на оптическую компенсацию симптомов, но не воздействуют на биологические механизмы старения аккомодационного аппарата. В этой связи закономерен устойчивый научный интерес к поиску фармакологических агентов, способных уменьшать влияние пресбиопических изменений (с помощью миотиков) [6, 7] либо модулировать биохимические и биомеханические свойства хрусталика, тем самым потенциально замедляя или корригируя пресбиопические изменения. Одним из таких перспективных соединений является пиреноксин (пиреноксин натрия) — вещество, изначально предложенное для профилактики и лечения начальных стадий катаракты. Предполагаемый механизм его действия связан с ингибированием карбонильного стресса и гликозилирования белков хрусталика, а также со стабилизацией сульфгидрильных групп, что в совокупности может препятствовать денатурации кристаллинов и потере прозрачности [8]. Логично предположить, что подобная стабилизация белковой матрицы способна также влиять на эластические свойства хрусталика, а следовательно, и на его аккомодационную функцию.
Однако, несмотря на теоретические предпосылки и установленную роль пиреноксина в биохимической стабилизации хрусталика [9], эмпирические данные о его непосредственном влиянии на аккомодационные ресурсы у человека крайне ограниченны и противоречивы. Большинство существующих исследований сфокусировано на его антикатарактном эффекте, в то время как динамика объективных и субъективных аккомодационных параметров на фоне его применения изучена недостаточно [10–12].
Таким образом, существует очевидная потребность в проведении контролируемых клинических исследований, направленных на оценку возможности фармакологической модуляции аккомодации с помощью пиреноксина. Получение достоверных данных о его эффективности в данном контексте позволило бы не только расширить представления о механизмах действия препарата, но и оценить его потенциальное место в комплексной стратегии профилактики и коррекции ранних проявлений пресбиопии. Данное исследование является планомерным продолжением изучения возможностей фармакологического воздействия на аккомодационную функцию.
Цель исследования: оценка динамики аккомодационных ресурсов у пациентов в возрасте 30–55 лет на фоне 3-месячного курса инстилляций 0,005% офтальмологического раствора пиреноксина.
Материал и методы
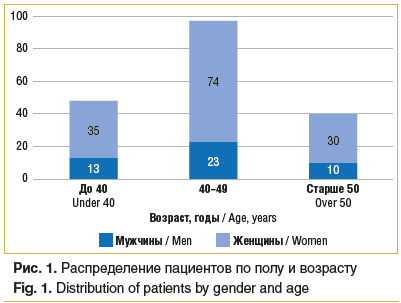
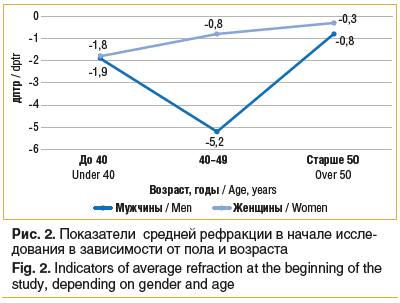
Было проведено проспективное многоцентровое исследование с участием 185 пациентов (370 глаз) в возрасте от 30 до 55 лет (средний возраст 43,8±6,5 года) с признаками начальной катаракты (минимальное, незначительное снижение прозрачности хрусталика без снижения максимальной корригированной остроты зрения) и пресбиопии. Распределение по возрасту: младше 40 лет — 48 человек (96 глаз, 26%), 40–49 лет — 97 человек (194 глаза, 52%), старше 50 лет — 40 человек (80 глаз, 22%). Большинство обследованных — 139 (75%) — женщины (рис. 1). Средняя рефракция в начале исследования у мужчин — -3,3 дптр, у женщин — -0,9 дптр (рис. 2). Основная жалоба пациентов при обращении за амбулаторной медицинской помощью к офтальмологу — постепенное снижение зрения вблизи без использования средств оптической коррекции для чтения.
Критерии невключения: астигматизм, наличие рефракционной хирургии в анамнезе, любые офтальмологические заболевания (кроме аномалий рефракции), а также анизометропия более 2,0 дптр.
До начала исследования от всех пациентов было получено информированное добровольное согласие.
Возрастные изменения хрусталика представляют собой континуум структурно-биохимических процессов, объединяемых в современной литературе понятием «синдром дисфункции хрусталика» (Dysfunctional Lens Syndrome, DLS) [13]. Ключевыми проявлениями DLS являются как снижение эластичности хрусталика с формированием пресбиопии, так и прогрессирующее помутнение его вещества, приводящее к развитию возрастной катаракты. Пиреноксин применяется при начальных формах возрастной катаракты как средство, направленное на замедление белковой агрегации и окислительных повреждений в ткани хрусталика. С учетом общности патогенетических механизмов катарактогенеза и возрастного снижения аккомодационной способности представляется обоснованным изучение потенциального влияния пиреноксина не только на динамику прозрачности, но и на функциональные свойства хрусталика, включая параметры аккомодации и эластичности. Таким образом, настоящее исследование направлено на оценку влияния пиреноксина на функциональные проявления DLS с использованием препарата в рамках показаний, разрешенных инструкцией по применению.
Всем участникам исследования назначали инстилляции 0,005% раствора пиреноксина по 1 капле 3 р/сут в течение 90 дней в оба глаза, а также соответствующую очковую коррекцию для чтения.
Для оценки аккомодации использовали следующие показатели:
-
ближайшую точку ясного зрения (БТЯЗ, punctum proximum): определялась по стандартной методике с полной оптической коррекцией;
-
запас аккомодации: оценивался путем определения максимальной силы рассеивающей линзы, при которой сохранялось чтение текста № 4 (стандартный оптотип для близи) в условиях полной коррекции аметропии;
-
сферический эквивалент клинической рефракции.
Всех пациентов обследовали дважды: до начала терапии и после завершения 90-дневного курса лечения.
В ходе исследования все пациенты применяли офтальмологический раствор пиреноксина согласно стандартной инструкции. Прием других препаратов, способных влиять на аккомодационную функцию, был исключен. В течение всего периода наблюдения не изменяли используемую оптическую коррекцию и привычный режим зрительных нагрузок.
Все полученные в ходе исследования данные были обработаны с использованием программного пакета IBM SPSS Statistics, версия 26.0 (IBM Corp., США) и Microsoft Excel 2019 (Microsoft Corp., США). Количественные данные, включая возраст, показатели клинической рефракции (сферический эквивалент), расстояние до БТЯЗ (см) и запас аккомодации (дптр), представлены в виде среднего арифметического (M) и стандартного отклонения (SD) – M±SD, поскольку распределение значений после проверки с помощью критерия Шапиро — Уилка было признано соответствующим нормальному (p>0,05). Качественные данные описаны в виде абсолютных частот и процентных долей.
Для оценки динамики аккомодационных параметров до и после 90-дневного курса терапии пиреноксином применяли парный t-критерий Стьюдента (paired samples t-test). Данный параметрический тест был выбран в связи с нормальным распределением данных и проведением измерений в одной и той же группе пациентов в двух временных точках.
Уровень статистической значимости (p-value) устанавливали на уровне <0,05. Все p-значения рассчитаны для двусторонней гипотезы. Величину эффекта для парного t-критерия оценивали с помощью коэффициента d Коэна, интерпретируемого как малый эффект (d ≈ 0,2), средний эффект (d ≈ 0,5) и большой эффект (d ≈ 0,8).
Для оценки достаточности размера выборки был проведен расчет апостериорной (достигнутой) мощности теста (post-hoc power analysis) с использованием программного модуля G*Power 3.1.9.7. Анализ выполняли для парного t-критерия на основе фактически полученных средних значений, стандартных отклонений и размера выборки (185 пациентов, 370 глаз). Приемлемым уровнем мощности считалось значение ≥0,80 (80%).
Все данные были собраны в единую электронную базу с двойным вводом для минимизации ошибок. Анализ проводился на совокупности глаз (370 глаз), что соответствует методологии, применяемой в аналогичных офтальмологических исследованиях для оценки функциональных параметров. Дополнительно был выполнен чувствительный анализ на уровне пациентов (n=185) для исключения потенциального влияния внутрипарной корреляции глаз, который подтвердил основные выводы.
Результаты исследования
По завершении 90-дневного курса терапии были получены следующие данные по ключевым аккомодационным показателям (рис. 3).
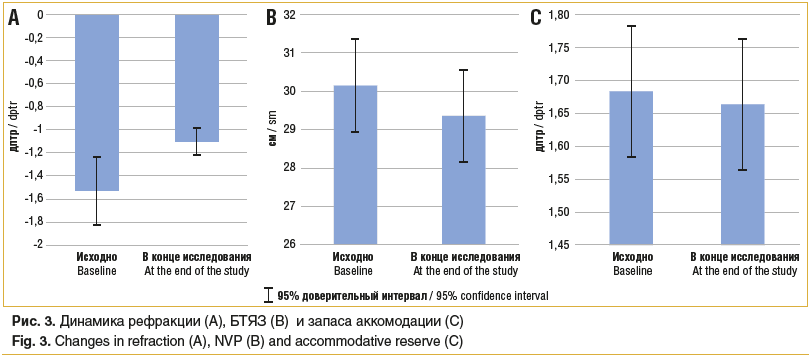
Динамика клинической рефракции. Наблюдалась тенденция к незначительному сдвигу средней рефракции в сторону эмметропии (-1,10 дптр по сравнению с исходными -1,53 дптр), однако данное изменение не достигло статистической значимости.
Динамика БТЯЗ. Зафиксировано статистически значимое, но клинически маловыраженное уменьшение расстояния до БТЯЗ на 2,5% (29,36 см против исходных 30,15 см).
Динамика запаса аккомодации. Средний показатель запаса аккомодации не продемонстрировал отрицательной динамики, оставшись на прежнем уровне и варьируя в пределах погрешности метода (1,66 дптр против исходных 1,68 дптр).
Полученные результаты свидетельствуют о клиническом влиянии 3-месячного курса пиреноксина на аккомодационный ответ у пациентов с признаками начальной катаракты и начальными проявлениями пресбиопии. Выявленная слабая динамика БТЯЗ не сопровождалась приростом запаса аккомодации, но гораздо важнее именно сам факт сохранения аккомодационной функции на прежнем уровне, а не ее очевидное возрастное снижение. Таким образом, при назначении пиреноксина в клинической практике по поводу начальной катаракты нельзя исключать сопутствующую коррекцию пресбиопических жалоб.
Обсуждение
Результаты настоящего проспективного многоцентрового исследования демонстрируют определенное влияние 3-месячного курса инстилляций 0,005% раствора пиреноксина на ключевые параметры аккомодации у пациентов 30–55 лет с признаками начальной катаракты и начальными проявлениями пресбиопии.
Полученные данные указывают на диссоциацию между статистической значимостью и клинической релевантностью изменений. Зафиксированное смещение БТЯЗ в среднем на 0,79 см (2,5%) является статистически значимым, но может не ощущаться пациентом, хотя принципиально важным является не достижение улучшения, а именно сохранение функции аккомодации. Практически незаметное для пациента изменение этого параметра не коррелирует с субъективным улучшением зрительного комфорта вблизи. Более важным результатом является отсутствие достоверной динамики в показателях запаса аккомодации, который является интегральным показателем функциональных возможностей аккомодационной системы. Его стабильность на протяжении всего периода наблюдения свидетельствует о том, что пиреноксин в использованном режиме дозирования оказывает стабилизирующее воздействие на физиологический механизм аккомодации.
Эти выводы согласуются с результатами исследований фармакологических агентов для коррекции пресбиопии [9, 14, 15]. Отсутствие выраженного эффекта в отношении аккомодационных параметров позволяет предположить, что основное действие пиреноксина в контексте возрастных изменений может быть связано не со стимуляцией аккомодационного аппарата, а с процессами стабилизации метаболизма и биомеханических свойств хрусталика. Данный препарат, направленный на улучшение эластичности хрусталика или тонуса цилиарной мышцы, демонстрирует минимальный и/или непостоянный клинический эффект в краткосрочной перспективе. Подобная картина, наблюдаемая и в настоящем исследовании, подчеркивает сложность фармакологического воздействия на инволюционный процесс, в основе которого лежат многокомпонентные изменения как в хрусталике (упрощение архитектоники волокон, увеличение размеров ядра), так и в цилиарной мышце.
Основной предполагаемый механизм действия пиреноксина связан с антиоксидантной активностью и ингибированием карбонильного стресса, ведущего к агрегации и денатурации белков кристаллинов. Таким образом, его первичная точка приложения — биохимическая стабилизация структуры хрусталика, а не непосредственное воздействие на аккомодационный аппарат. Полученные нами результаты косвенно подтверждают эту гипотезу: отсутствие динамики запаса аккомодации позволяет предположить, что 3-месячный курс терапии не изменил вязкоэластических свойств хрусталика в степени, достаточной для влияния на его деформационную способность. Вероятно, для проявления потенциального биомеханического эффекта, теоретически способного повлиять на амплитуду аккомодации, требуются более длительные сроки применения.
Важным ограничением нашего исследования является отсутствие контрольной группы, получавшей плацебо. Это не позволяет полностью исключить влияние регрессии к среднему или эффекта плацебо на минимальное, но статистически значимое изменение БТЯЗ. Кроме того, использованные методы оценки аккомодации (определение БТЯЗ и запаса аккомодации) являются субъективными и зависимыми от условий проведения и усилия пациента. Включение в будущие протоколы объективных методов, таких как автоматическая рефрактометрия в условиях стимуляции аккомодации или оптическая когерентная томография для оценки морфологии хрусталика и цилиарного тела, позволило бы получить более точные и воспроизводимые данные.
Заключение
Проведенное проспективное многоцентровое исследование позволило оценить влияние 3-месячного курса инстилляций 0,005% раствора пиреноксина на аккомодационные возможности пациентов в возрасте 30–55 лет с начальными признаками катаракты и пресбиопии. Полученные результаты свидетельствуют о возможности влияния данной терапевтической схемы на ключевые функциональные параметры аккомодационной системы у так называемых «ранних» пресбиопов с начальными признаками катаракты.
Анализ данных показал, что, несмотря на статистически значимое, но минимальное смещение БТЯЗ, показатель запаса аккомодации оставался стабильным на протяжении всего периода наблюдения, несмотря на общевозрастные тенденции к снижению функциональных показателей. Это указывает на то, что пиреноксин в исследованном режиме применения оказывает стабилизирующее воздействие на физиологический механизм аккомодации даже в краткосрочной перспективе. Основной предполагаемый механизм действия препарата связан с биохимической стабилизацией белковых структур хрусталика.
Таким образом, на основании настоящего исследования 0,005% раствор пиреноксина у пациентов указанной возрастной группы с начальными признаками катаракты может способствовать сохранению аккомодационной функции и, возможно, стабилизации пресбиопических симптомов в рамках 3-месячного курса лечения. Авторы рекомендуют использовать шире термин «синдром дисфункционального хрусталика» как отправную точку для собственных наблюдений за пациентами с начальными проявлениями катаракты и первыми пресбиопическими симптомами. Такой подход открывает перспективы для принципиальной возможности медикаментозного решения проблемы.
Потенциальная терапевтическая роль пиреноксина, вероятно, связана не с непосредственным воздействием на аккомодацию, а с долгосрочными процессами, направленными на поддержание метаболического гомеостаза, эластичности и прозрачности хрусталика. Для верификации этой гипотезы и определения возможных отсроченных эффектов препарата на биомеханические свойства аккомодационного аппарата необходимы дальнейшие рандомизированные плацебо-контролируемые исследования. Ключевыми направлениями для будущих научных работ должны стать:
-
увеличение продолжительности наблюдения (до 6–12 мес. и более) для оценки возможного кумулятивного эффекта;
-
внедрение объективных инструментальных методов диагностики, таких как аккомодография или оптическая когерентная томография, позволяющих количественно оценить изменения толщины хрусталика и динамику состояния цилиарной мышцы;
-
формирование дизайна исследований, включающего контрольные группы (плацебо и/или группы сравнения с другими профилактическими схемами), для повышения уровня доказательности получаемых результатов.
Благодарность врачам, принявшим участие в исследовании: Комаха М.В., Журавлева О.В., Сипина Ю.В., Комаровских Е.В., Муратова Е.О., Негрей Т.В. , Мосиенко Е.А., Имамутдинова Э.М., Жданова А.А., Зиновьева Г.М., Пронина Е.А., Гречаниченко Н.А., Сергиенко С.В., Нагорнова Н.Д., Олейников К.Е., Петрова Е.В., Рытик Н.П., Костина Н.Е., Жданова А.А., Панфилова Т.А., Романенкова С.А., Чиканова А.Н., Новикова Т.А., Чередниченко О.Г.
Gratitude to the doctors who took part in the study: Komakha M.V., Zhuravleva O.V., Sipina Yu.V., Komarovskikh E.V., Muratova E.O., Negrey T.V., Mosienko E.A., Imamutdinova E.M., Zhdanova A.A., Zinovieva G.M., Pronina E.A., Grechanichenko N.A., Sergienko S.V., Nagornova N.D., Oleynikov K.E., Petrova E.V., Rytik N.P., Kostina N.E., Zhdanova A.A., Panfilova T.A., Romanenkova S.A., Chikanova A.N., Novikova T.A., Cherednichenko O.G.
Сведения об авторах:
Борисов Федор Григорьевич — врач-офтальмолог филиала КДЦ ГБУЗ МО МОНИКИ им. М.Ф. Владимирского в г. Реутов; 129110, Россия, г. Москва, ул. Щепкина, д. 61/2; ORCID iD 0009-0005-2783-9935
Лоскутов Игорь Анатольевич — д.м.н., заведующий научным отделом и кафедрой офтальмологии и оптометрии ГБУЗ МО МОНИКИ им. М.Ф. Владимирского; 129110, Россия, г. Москва, ул. Щепкина, д. 61/2; ORCID iD 0000-0003-0057-3338
Абакаров Сапиюлла Анварович — к.м.н., научный сотрудник офтальмологического отделения для взрослых ГБУЗ МО МОНИКИ им. М.Ф. Владимирского; 129110, Россия, г. Москва, ул. Щепкина, д. 61/2; ORCID iD 0009-0000-9204-9781
Контактная информация: Борисов Федор Григорьевич, e-mail: oftborisov@gmail.com
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 22.12.2025.
Поступила после рецензирования 12.01.2026.
Принята в печать 30.01.2026.
материал rmj.ru
