Введение
Глаукома остается ведущей патологией в структуре причин инвалидности по профилю «офтальмология», несмотря на доступность гипотензивных препаратов и совершенствование лазерных и хирургических антиглаукомных методик [1–4].
При всех преимуществах операций перфорирующего типа непроникающие операции отличаются в первую очередь малым количеством осложнений и более щадящей техникой [5–9] и направлены на частичное улучшение оттока по основному дренажному пути без создания прямого сообщения с передней камерой глаза.
Однако их эффективность значительно снижается при далеко зашедшей и терминальной стадиях глаукомного процесса, что требует тщательного наблюдения за пациентами и использования методик, позволяющих прогнозировать гипотензивный эффект с целью сохранения зрительных функций [10]. Повышенный интерес к непроникающим операциям сконцентрировал внимание офтальмологов на методах исследования, позволяющих изучить морфологические структуры дренажной системы, участвующие в фильтрации водянистой влаги. Такими исследованиями в настоящее время являются оптическая когерентная томография (ОКТ) и ультразвуковая биомикроскопия (УБМ) [11, 12].
Оптическая когерентная томография глаза — это информативный и безопасный метод оценки морфофункционального состояния зоны антиглаукомной операции. Высокая разрешающая способность позволяет детально визуализировать все структуры зоны вмешательства, оценить их морфометрические характеристики и оптическую плотность тканей [12]. В то же время стоит отметить, что ОКТ не входит в стандарт оснащения дневного стационара и офтальмологического отделения в соответствии с приложением № 14 приказа Минздрава России от 12 ноября 2012 г. № 902Н1. Это обстоятельство затрудняет широкое использование данного метода в практической деятельности офтальмолога.
Ультразвуковая биометрия была разработана в 1990 г. Методика позволяет прижизненно исследовать структуры переднего сегмента глаза и оценивать состоятельность сформированных оперативным способом путей оттока внутриглазной жидкости (ВГЖ) после антиглаукомных операций [13].
В основе УБМ лежит концепция отражения ультразвуковых волн тканями глаза. Ее разрешающая способность составляет 25–50 мкм. Изменение акустической рефлективности с высоким разрешением в режиме реального времени позволяет показать изменения плотности структур и границы разделов тканей через изменения уровня яркости сигнала [14].
Так, например, в исследовании [14] были проанализированы данные УБМ после непроникающей глубокой склерэктомии (НГСЭ) в сроки от 1 года до 10 лет после операции. Установлено, что в послеоперационном периоде дренажная система сохраняла фильтрующие функции на фоне компенсации ВГД, а появление акустически негативных щелей — тоннелей — создавало картину образования других путей движения ВГЖ. В то же время у ряда пациентов была зафиксирована ретенция ВГЖ с нарушением офтальмотонуса, обусловленная формированием толстого склерального лоскута и кровоизлияниями в зону операции. При помощи УБМ в дренажной зоне был выявлен пролиферативный процесс, которые был запущен, вероятно, низкой фильтрующей функцией трабекуло-десцеметовой мембраны [14].
Наше исследование направлено на изучение акустических структур, участвующих в оттоке водянистой влаги в разные сроки после непроникающей операции хирургической резекции склеры (ХРС), что позволит прогнозировать длительное сохранение склерального оттока. Способ лечения, предложенный О.А. Румянцевой и Е.А. Корчугановой, обеспечивает улучшение оттока водянистой влаги через склеру по увеосклеральному пути и позволяет снизить повышенное внутриглазное давление (ВГД) у больных с далеко зашедшей и терминальной стадиями первичной открытоугольной глаукомы (ПОУГ) [15–17].
Цель исследования: оценить функциональную состоятельность сформированных путей оттока водянистой влаги (при помощи УБМ) у пациентов с ПОУГ и ВПГ после ХРС.
Содержание статьи
Материал и методы
В группу исследования вошло 67 пациентов (67 глаз) с ПОУГ и 17 пациентов (17 глаз) с ВПГ III и IV стадии, перенесших ХРС. Исследование одобрено комитетом по этике научных исследований РНИМУ им. Н.И. Пирогова Минздрава России (протокол № 161 от 30.01.2017).
Критерии невключения: высокая миопия, системные заболевания соединительной ткани и склериты.
Пациентам проводилось комплексное офтальмологическое обследование, включающее стандартные методики для изучения гидродинамики и зрительных функций (биомикроофтальмоскопия, визометрия, компьютерная периметрия, тонометрия по Маклакову и тонография).
Техника проведения ХРС подробно описана нами ранее [18].
Для визуального подтверждения склерального оттока нами использовалась УБМ, которая позволила оценить морфологические структуры зоны операции и прогнозировать гипотензивный эффект. Исследование выполняли на приборе HiScan (OPTIKON, Италия) в положении лежа на спине после предварительной эпибульбарной анестезии раствором 0,4% оксибупрокаина. В конъюнктивальный свод помещали силиконовую глазную чашечку, заполненную контактной средой (физиологический раствор) для более точной передачи ультразвуковых волн в глаз. Далее в иммерсионную среду погружали головку ультразвукового излучателя и располагали ее таким образом, чтобы расстояние до роговицы не превышало 1 мм. Медленное перемещение датчика относительно исследуемых структур по 4 меридианам позволило получить меридиональные срезы. В ходе исследования оценивали и фиксировали акустические признаки хирургически сформированных зон фильтрации ВГЖ — интрасклеральное пространство (эхогенность акустической щели) и высоту фильтрационной подушки (ФП; расстояние от конъюнктивы до дна склерального ложа в центральной его части).
Исследование проводили в ранние (через 4 нед.) и отдаленные (через 24 и 36 мес.) сроки после ХРС.
Статистический анализ данных проведен на персональном компьютере при помощи электронных таблиц MS Excel 2010 и пакета прикладных программ SPSS Statistics 13 с оценкой критерия достоверности (р) по Стьюденту и критерия согласия Пирсона (χ2).
Результаты исследования
В рамках настоящей статьи необходимо напомнить, что после ХРС у пациентов с ПОУГ и ВПГ удалось нормализовать гидродинамику глаза: снизить уровень ВГД на 83,6 и 64,7% соответственно, (p≤0,05) и усилить коэффициент легкости оттока у пациентов с ПОУГ на 0,07±0,006 мм3/мин/мм рт. ст., с ВПГ — на 0,08±0,007 мм3/мин/мм рт. ст. (p<0,05), что позволило ослабить медикаментозный гипотензивный режим (на 35,9 и 33,2% соответственно) [18].
Проведенный анализ акустических характеристик тканей в зоне ХРС позволил определить признаки функциональной активности дренажной системы и выявить соотношения структур в зоне оперативного пособия.
Согласно данным УБМ, выполненной спустя 4 нед. после ХРС, у всех прооперированных пациентов сформировалась разлитая, несколько рыхлая ФП, высота ее у пациентов с ПОУГ составила в среднем 0,49±0,06 мм, с ВПГ — 0,42±0,03 мм (уровень ВГД в среднем составил 19,0±0,25 и 21,2±1,05 мм рт. ст. соответственно). При УБМ визуализировалось интрасклеральное пространство как акустическая щель средней плотности (рис. 1).
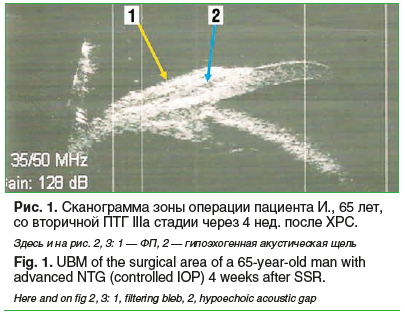
Спустя 24 мес. после ХРС ФП была выражена, среднее значение ее высоты у пациентов с ПОУГ составило 0,55±0,02 мм, с ВПГ — 0,46±0,04 мм, а среднее значение уровня ВГД было равно 18,00±0,31 и 20,1±0,65 мм рт. ст. соответственно. Интрасклеральное пространство в обеих группах регистрировалось в виде акустической щели с низкой эхогенностью (рис. 2). Выявленная картина свидетельствовала о беспрепятственной фильтрации водянистой влаги через истонченную склеру и заполняемости ВГЖ интрасклерального пространства.
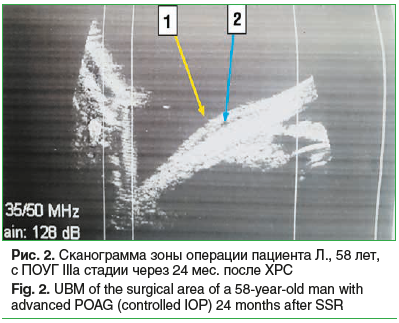
К концу срока наблюдения (36 мес.) у большинства пациентов ФП характеризовалась тенденцией к уплощению, ее высота у пациентов с ПОУГ в среднем составила 0,40±0,06 мм, у пациентов с ВПГ — 0,34±0,02 мм на фоне компенсированного ВГД. При УБМ в обеих группах визуализировалась гипоэхогенная акустическая щель (рис. 3). Результаты, полученные в отдаленные сроки, свидетельствовали о сохранении процесса фильтрации на фоне менее выраженной ФП. Статистически значимых различий высоты ФП и степени эхогенности интрасклерального пространства между группами ПОУГ и ВПГ на всем протяжении наблюдения выявлено не было (p>0,1).
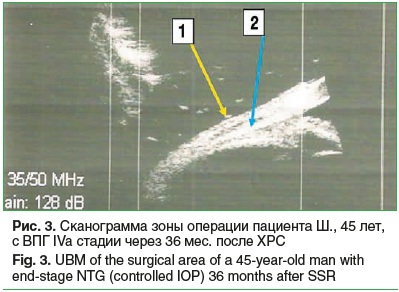
Обсуждение
При проведении УБМ (по данным сканограмм) спустя 1 мес. после ХРС у всех прооперированных пациентов наблюдалась акустическая щель (или интрасклеральное пространство) со средней степенью эхогенности. Через 24 и 36 мес. после оперативного лечения при УБМ визуализировалась гипоэхогенная акустическая щель, что указывает на беспрепятственную фильтрацию водянистой влаги.
Ранее было показано, что после НГСЭ отмечается генерализация пролиферативного процесса во всех зонах дренажной системы с переходом в его завершающую стадию — фиброзирование (нарастание акустической плотности структур) на фоне декомпенсации офтальмотонуса [19].
В ходе настоящего исследования по изучению состояния склерального оттока после ХРС не получено данных, свидетельствующих об увеличении эхогенности интрасклерального пространства в отдаленный период наблюдения как о возможном индикаторе пролиферации тканей глаза. Данное обстоятельство, вероятно, связано с тем, что при непроникающей ХРС иссекаются эписклера, богатая кровеносными сосудами, и теноновая оболочка. Предложенная оперативная тактика позволяет снизить риски избыточного рубцевания и сохранить беспрепятственную фильтрацию водянистой влаги через истонченную склеру в зоне хирургического воздействия. Причем такой механизм увеосклерального оттока в зоне проекции цилиарного тела и эхогенность структур глаза после ХРС идентичны у пациентов с ПОУГ и ВПГ [15].
Выводы
-
Впервые с помощью методики УБМ в отдаленные сроки (до 3 лет) после ХРС были получены достоверные признаки формирования ФП и оценено состояние зоны фильтрации водянистой влаги у пациентов с ПОУГ и ВПГ.
-
По данным УБМ после ХРС происходит беспрепятственная активная фильтрации водянистой влаги через склеру, что подтверждается наличием выраженной акустической щели, свидетельствующей о достаточной заполняемости ВГЖ интрасклерального пространства.
-
Метод УБМ показал свою информативность и возможность его применения в амбулаторных условиях. При повышении эхогенности акустической щели (интрасклерального пространства) или снижении высоты ФП в отдаленные сроки наблюдения после оперативного лечения следует установить более тщательный контроль за уровнем ВГД и, при необходимости, корректировать тактику ведения с целью сохранения зрительных функций.
1Приказ Министерства здравоохранения РФ от 12 ноября 2012 г. № 902н «Об утверждении порядка оказания медицинской помощи взрослому населению при заболеваниях глаза, его придаточного аппарата и орбиты» (в ред. приказов Минздрава России от 09.06.2020 № 558н, от 01.02.2022 № 44н).
Сведения об авторах:
Казанцева Ангелина Юрьевна — младший научный сотрудник научно-исследовательской лаборатории глаукомы и дистрофических заболеваний глаза РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-2542-3734.
Корчуганова Елена Александровна — д.м.н., старший научный сотрудник научно-исследовательской лаборатории глаукомы и дистрофических заболеваний глаза РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0001-5147-0385.
Контактная информация: Казанцева Ангелина Юрьевна, e-mail: bronvis@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 15.01.2024.
Поступила после рецензирования 07.02.2024.
Принята в печать 04.03.2024.
About the authors:
Angelina Yu. Kazantseva — junior researcher of the Research Laboratory of Glaucoma and Eye Dystrophic Diseases, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0002-2542-3734.
Elena A. Korchuganova — Dr. Sc. (Med.), senior researcher of the Research Laboratory of Glaucoma and Eye Dystrophic Diseases, Pirogov Russian National Research Medical University; 1, Ostrovityanov str., Moscow, 117437, Russian Federation; ORCID iD 0000-0001-5147-0385.
Contact information: Angelina Yu. Kazantseva, e-mail: bronvis@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 15.01.2024.
Revised 07.02.2024.
Accepted 04.03.2024.
материал rmj.ru
