Введение
В последние десятилетия в структуре кислотозависимых заболеваний наметился четкий тренд к увеличению числа лиц с гастроэзофагеальной рефлюксной болезнью (ГЭРБ) [1]. Во многом данный факт эксперты связывают с полиэтиологичностью заболевания и высокой частотой встречаемости в популяции факторов риска. Наиболее изученными на сегодняшний день факторами, ассоциированными с развитием ГЭРБ, являются факторы генетики и эпигенетики [2]. Среди последних следует отметить избыточную массу тела, ожирение, курение, прием ряда лекарственных препаратов, приводящих к расслаблению нижнего пищеводного сфинктера (НПС), грыжу пищеводного отверстия диафрагмы (ГПОД), беременность [3–5]. Кроме того, в последние годы получены данные о том, что новым фактором риска ГЭРБ могут стать различные бариатрические вмешательства, которые приобретают особую популярность на фоне значимого увеличения числа лиц с ожирением. В частности, данные метаанализа 9 исследований, опубликованных в период с июля 2017 г. по июнь 2022 г., продемонстрировали, что лапароскопическая рукавная гастрэктомия повышает вероятность ГЭРБ в 3,61 раза, а к концу 5-летнего периода наблюдения за пациентами после перенесенного вмешательства заболевание диагностируется у 64,3% из них [6].
Необходимо подчеркнуть, что реализация указанных факторов направлена, прежде всего, на формирование моторно-эвакуаторной дисфункции органов гастроэзофагеальной зоны, включая несостоятельность НПС, высокий градиент давления между желудком и пищеводом, ослабление двигательной активности дистального отдела пищевода и связанное с ним замедление клиренса, нарушение процессов аккомодации и антродуоденальной координации [1]. Вместе с тем с позиций определения дальнейшего прогноза течения заболевания крайне важным является учет факторов агрессии и защиты слизистой оболочки пищевода с оценкой риска развития эрозивной формы заболевания, пищевода Барретта и ассоциированной с ним аденокарциномы пищевода. Предполагается, что именно снижение протективных свойств (резистентности) слизистой оболочки пищевода, т. е. возможности противостоять воздействию повреждающих компонентов рефлюксата, и лежит в основе прогрессирования ГЭРБ [7].
Установлено, что соляная кислота и пепсин при персистирующем гастроэзофагеальном рефлюксе (ГЭР), а в ряде случаев также желчные кислоты, лизолецитин и трипсин у пациентов с дуоденогастроэзофагеальным рефлюксом (ДГЭР), приводят к повреждению белков плотных контактов и, как следствие, целостности эпителиального барьера слизистой оболочки пищевода, в результате чего агрессивные молекулы проникают в более глубокие слои эпителиальной выстилки с развитием вторичных воспалительных реакций и опосредованных иммунными клетками процессов перекисного окисления липидов. В свою очередь, хроническое воспаление сопровождается нарушением клеточного обновления и увеличением пролиферативной активности с гиперплазией клеток базального слоя слизистой оболочки пищевода, что в условиях сохраняющегося ГЭР или ДГЭР ассоциировано с повреждением вновь формирующихся эпителиоцитов, нарушением их созревания и дифференцировки, накоплением мутаций в клеточной популяции, в том числе регулирующих синтез онкогенных белков [7, 8]. Совокупность воспалительных процессов и повышенный пролиферативный потенциал выступают основой для формирования цилиндроклеточной метаплазии кишечного типа (пищевод Барретта) с последующим прогрессированием структурных изменений эпителия до аденокарциномы пищевода [8, 9]. Таким образом, можно говорить о реализации модели «хроническое воспаление — метаплазия — рак», подобной каскаду P. Correa в условиях хронического воспаления при гастрите.
В соответствии с Монреальским консенсусом (2006 г.) среди классических клинических проявлений ГЭРБ выделяют те, которые характеризуются наличием только симптомов (рефлюксный синдром, синдром боли в грудной клетке), а также те, при которых наряду с жалобами выявляются признаки повреждения пищевода или осложнения заболевания (эрозивно-язвенный эзофагит, стриктура, пищевод Барретта, аденокарцинома пищевода) [10]. Хорошо известно, что изжога и отрыжка кислым являются самыми частыми и типичными симптомами ГЭРБ, однако они не позволяют верифицировать форму заболевания, поскольку их частота и выраженность не определяются наличием эрозий слизистой оболочки или осложнений [11, 12], в связи с чем российские эксперты настаивают на том, что всем пациентам с подозрением на ГЭРБ должно быть назначено эндоскопическое исследование [13].
Результаты эпидемиологических исследований свидетельствуют о том, что на долю эрозивной ГЭРБ приходится 48–65% всех случаев заболевания [14, 15]. При этом эксперты указывают на возможную недооценку распространенности данной формы ГЭРБ, вероятно, ее встречаемость может быть намного выше, поскольку зачастую еще до проведения эндоскопического исследования пациенты с целью купирования имеющихся симптомов самостоятельно начинают принимать лекарственные препараты, способствующие заживлению эрозивно-язвенных дефектов и затрудняющие их диагностику, прежде всего ингибиторы протонной помпы (ИПП) [16].
Факторы риска эрозивной формы ГЭРБ
Согласно данным, полученным в нашем центре ранее, к факторам риска формирования эрозивной формы ГЭРБ относятся мужской пол, дебют заболевания в возрасте младше 30 лет, избыточная масса тела и ожирение, курение, наличие сопутствующих заболеваний, таких как ГПОД, неалкогольная жировая болезнь печени (НАЖБП) или сахарный диабет [17]. В подтверждение этому — результаты метаанализа 114 обсервационных исследований с общим числом участников 759 100, согласно которому из 29 изученных факторов значимыми в отношении повышенного риска эрозивного эзофагита стали возраст ≥60 лет (отношение шансов (ОШ) 2,03, 95% доверительный интервал (ДИ) 1,81–2,28), принадлежность к европеоидной расе (ОШ 1,67, 95% ДИ 1,40–1,99), длительность анамнеза ГЭРБ ≥5 лет (ОШ 1,27, 95% ДИ 1,14–1,42), ожирение (ОШ 1,78, 95% ДИ 1,61–1,98), абдоминальное ожирение (ОШ 1,29, 95% ДИ 1,18–1,42), сахарный диабет (ОШ 1,24, 95% ДИ 1,17–1,32), артериальная гипертензия (ОШ 1,16, 95% ДИ 1,09–1,23), дислипидемия (ОШ 1,15, 95% ДИ 1,06–1,24), гипертриглицеридемия (ОШ 1,42, 95% ДИ 1,29–1,57), ГПОД (ОШ 4,07, 95% ДИ 3,21–5,17) и НАЖБП (ОШ 1,26, 95% ДИ 1,18–1,34) [18].
На наш взгляд, повышение риска развития эрозивно-язвенного эзофагита у коморбидных пациентов с ГЭРБ, имеющих различные метаболические расстройства в анамнезе, обусловлено частой встречаемостью среди них ДГЭР на фоне сопутствующей патологии гепатобилиарной системы [19]. Высокую распространенность смешанного по составу рефлюксата среди больных с эрозивным рефлюкс-эзофагитом и пищеводом Барретта отмечают и другие исследователи [20].
В последние годы в качестве еще одного фактора прогрессирующего течения ГЭРБ и формирования эрозивного рефлюкс-эзофагита в гендерном аспекте рассматривается изменение гормонального профиля. Предполагается, что меньшая распространенность осложненных форм ГЭРБ среди женщин репродуктивного возраста связана с эпителийпротективным эффектом эстрогенов, который утрачивается после менопаузы, и это подтверждается той же частотой эрозивного рефлюкс-эзофагита среди пациентов в возрасте старше 50 лет независимо от пола [21]. В эксперименте показано, что введение женского полового гормона 17β-эстрадиола способствует усилению барьерной функции пищевода посредством усиления экспрессии белка окклюдина и уменьшения межэпителиальных промежутков в слизистой оболочке [22].
Факторы риска и скрининг пищевода Барретта
По данным отдельных эпидемиологических исследований, с развитием пищевода Барретта ассоциированы возраст старше 50 лет (ОШ 1,53, 95% ДИ 1,05–2,25), еженедельные симптомы ГЭРБ (ОШ 2,33, 95% ДИ 1,34–4,05), абдоминальное ожирение (ОШ 1,98, 95% ДИ 1,52–2,57), курение (ОШ 1,99, 95% ДИ 1,21–3,29), наличие пищевода Барретта или аденокарциномы пищевода у родственников первой и второй линии родства (ОШ 12,23, 95% ДИ 3,34–44,76) [23, 24]. Основываясь на этих результатах, многие международные профильные сообщества рекомендуют проводить скрининг пищевода Барретта у больных ГЭРБ, имеющих указанные факторы риска или их сочетание (см. таблицу).
![Таблица. Рекомендации по скринингу пищевода Барретта среди пациентов с ГЭРБ [13, 23, 24] Table. Recommendations for screening Barrett’s esophagus in patients with GERD [13, 23, 24] Таблица. Рекомендации по скринингу пищевода Барретта среди пациентов с ГЭРБ [13, 23, 24] Table. Recommendations for screening Barrett’s esophagus in patients with GERD [13, 23, 24]](https://medblog.su/wp-content/uploads/2025/01/Gastroezofagealnaya-reflyuksnaya-bolezn-kak-optimizirovat-vedenie-bolnyh-Livzan-MA.png)
Подходы к курации пациентов с прогрессирующим течением ГЭРБ
Прогрессирующий характер течения ГЭРБ подчеркивает важность максимальной реализации возможностей как немедикаментозной, так и медикаментозной терапии на всех этапах курации больного. Крайне сложно переоценить роль немедикаментозных методов при ГЭРБ, где отдельное внимание уделяется выявлению и коррекции модифицируемых факторов риска заболевания, включая отказ от курения, нормализацию массы тела у пациентов с избыточной массой тела и ожирением, при возможности — замену или отмену лекарственных препаратов, способствующих рефлюксу, и др. [25]. Пациенту рекомендованы сон с приподнятым головным концом кровати или использование антирефлюксной (клиновидной) подушки, ограничение подъема тяжестей, работы в наклон, исключение ношения тугих поясов и корсетов, горизонтального положения в течение 1,5 ч после приема пищи, перерыв не менее 3 ч между ужином и сном.
Диетотерапия также представляет собой неотъемлемый компонент курации больного, что нашло свое отражение во всех клинических рекомендациях экспертных сообществ по лечению ГЭРБ [11, 13, 26]. Согласно современным представлениям рацион питания должен подбираться индивидуально, на основе анализа дневника питания, с учетом оценки реакции «употребление продукта — появление симптома». Одновременно с этим всем больным рекомендуется ограничение потребления продуктов, которые могут приводить к расслаблению НПС (кофе, алкоголь, шоколад, мята, цитрусовые, острая пища), тормозить опорожнение желудка (жирная пища) или повышать внутрибрюшное давление (газированные напитки, продукты, повышающие газообразование в кишечнике, и др.) [27].
В соответствии с клиническими рекомендациями РГА ключевыми целями терапии ГЭРБ, помимо купирования симптомов заболевания, являются повышение качества жизни пациентов, заживление эрозивно-язвенных поражений слизистой оболочки пищевода и предупреждение развития осложнений [13]. Вместе с тем существенное значение, помимо достижения клинической и эндоскопической ремиссии, имеет достижение гистологической ремиссии, в частности редукции воспалительных изменений и нормализации пролиферативного потенциала слизистой оболочки пищевода, поскольку именно эти стигмы определяют скорость прогрессирования рефлюкс-эзофагита и риск формирования осложнений [7].
К лекарственным препаратам, используемым для терапии пациентов с ГЭРБ и зарегистрированным на российском фармацевтическом рынке, относят влияющие на кислотопродукцию (ИПП, Н2-гистаминоблокаторы) или снижающие агрессивность рефлюксата (альгинаты, антациды); нормализующие моторику верхних отделов пищеварительного тракта (прокинетики); способствующие повышению протективных свойств слизистой оболочки пищевода (эзофагопротектор).
Следует подчеркнуть, что, несмотря на то, что в основе развития ГЭРБ первично лежат нарушения моторики, ведущей группой лекарственных препаратов, которая позволяет достичь всех целей терапии заболевания и должна быть назначена всем пациентам, являются ИПП. Препараты данной группы подавляют секрецию соляной кислоты в желудке, в результате чего не только уменьшается объем рефлюксата, но и снижается повреждающий потенциал пепсина и желчных кислот в его составе [28].
При неполном ответе на терапию ИПП необходимо оценить приверженность больного лечению, убедиться в диагнозе ГЭРБ и рассмотреть возможность расширения терапии [29].
Потребность в расширении терапевтических возможностей связана с тем, что примерно у 40% пациентов с ГЭРБ регистрируется смешанный состав рефлюксата [30]. Этим определяется обоснованность курсового назначения прокинетиков и эпителийпротективной терапии [13]. Прокинетики влияют на первичный механизм формирования ГЭРБ, т. е. регулируют моторно-эвакуаторную функцию органов гастроэзофагеальной зоны, включая тонус НПС, пищеводный клиренс, аккомодацию желудка и антродуоденальную координацию [31]. Однако несмотря на это, прокинетические агенты не являются терапией первой линии, их применение лимитировано побочными эффектами препаратов, поэтому они применяются курсами продолжительностью 4–8 нед. в составе комплексной терапии вместе с ИПП.
Кроме того, пациенты, полностью не ответившие на терапию ИПП, нуждаются в назначении эзофагопротектора для повышения резистентности слизистой оболочки пищевода к воздействию агрессивных молекул рефлюксата [13]. Медицинское изделие Альфазокс представляет собой биоадгезивную формулу на основе глюкозаминов гиалуроновой кислоты и хондроитина сульфата, которые с помощью биоадгезивного носителя полоксамера 407 равномерно распределяются на поверхности эпителиальных клеток, способствуя их защите и восстановлению. Он может применяться как в виде монотерапии, так и в составе комбинированной терапии совместно с ИПП. Согласно инструкции по применению Альфазокс может быть рекомендован пациенту с ГЭРБ по 1 пакетику-саше после основных приемов пищи и перед сном, возможно назначение между приемами пищи каждые 8 ч в течение светового дня и перед сном или в соответствии с индивидуальными рекомендациями врача[1].
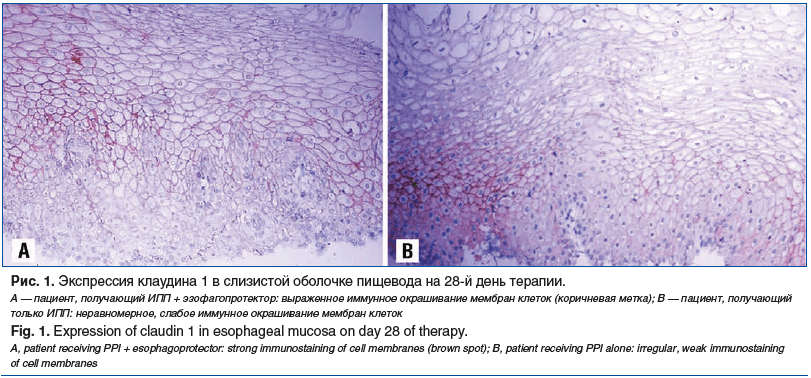
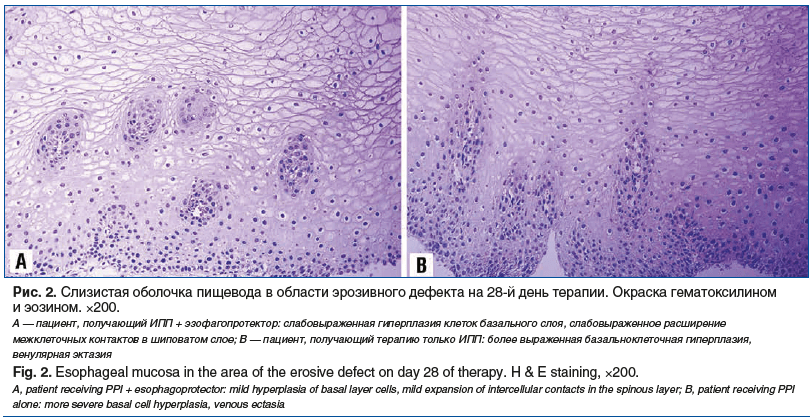
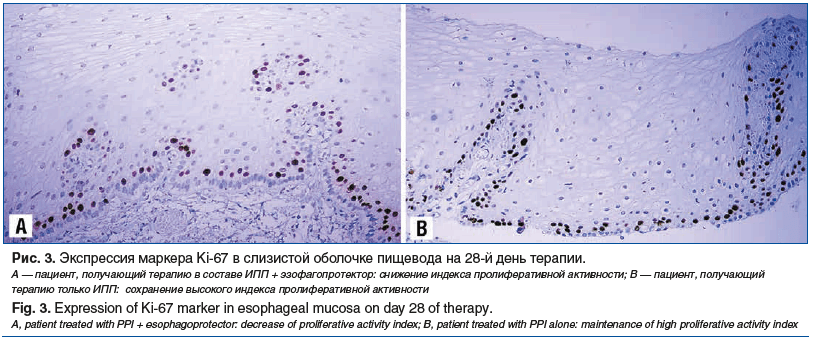
В нашем исследовательском центре имеется собственный опыт применения Альфазокса у пациентов с эрозивной формой ГЭРБ, у которых при комбинированной терапии в составе ИПП и эзофагопротектора уже к 28-му дню удалось достичь достоверно более эффективного купирования симптомов и более быстрой эпителизации слизистой оболочки пищевода по сравнению с таковыми на фоне монотерапии ИПП. При этом наиболее интересные, на наш взгляд, данные были получены при анализе биопсийного материала. Так, в группе пациентов, получавших комбинированную терапию с Альфазоксом, на 28-й день отмечена статистически значимо более высокая экспрессия белков плотных контактов класса клаудинов типа 1 и 4 (рис. 1), что способствовало уменьшению морфологических признаков рефлюкс-эзофагита (рис. 2) и восстановлению пролиферативного потенциала слизистой оболочки, который оценивали с помощью маркера Ki-67 (рис. 3) [32].
В 2022 г. опубликованы данные метаанализа, посвященного оценке эффективности комбинированной терапии эзофагопротектором Альфазокс и ИПП у пациентов с эрозивной формой ГЭРБ [34]. Из 39 исследований, отобранных в пяти базах данных (PubMed, EMBASE, Cochrane, РИНЦ, Google), в соответствии с критериями включения/исключения в итоговый анализ вошли три с общим числом участников 181. Результаты метаанализа продемонстрировали, что эффективность комбинированной терапии эзофагопротектором и ИПП через 4 нед. лечения превосходит таковую при монотерапии ИПП в отношении эпителизации эрозивных дефектов слизистой оболочки пищевода (р=0,003), однако сопоставима в плане купирования изжоги (р=0,287).
Как уже было отмечено выше, основной целью терапии больного ГЭРБ считается достижение не только клинической и эндоскопической, но и гистологической ремиссии, т. е. полное купирование симптомов, отсутствие эрозивных дефектов слизистой оболочки пищевода и редукция морфологических стигм рефлюкс-эзофагита [7]. При этом ключевым фактором профилактики прогрессирования заболевания, развития осложнений и обострений должно быть именно достижение гистологической ремиссии. С этих позиций оправданным представляется курсовое назначение эзофагопротектора с целью защиты слизистой оболочки пищевода и после заживления эрозий, если невозможно устранить факторы риска прогрессирующего течения заболевания.
Заключение
Важным с точки зрения прогноза и определения дальнейшей тактики курации при ГЭРБ представляется выявление и, при возможности, своевременная коррекция факторов риска по развитию эрозивного рефлюкс-эзофагита, пищевода Барретта и ассоциированной с ним аденокарциномы пищевода. Следует отметить, что повышение защитных свойств эпителиального барьера пищевода наряду с кислотосупрессивной терапией представляет собой неотъемлемый компонент лечебной стратегии при ведении пациентов с ГЭРБ, прежде всего, имеющих высокий риск прогрессирующего течения заболевания и формирования осложнений. Комплексная терапия ИПП и эзофагопротектором обеспечивает защиту слизистой оболочки пищевода, способствует более значимому уменьшению воспаления, позволяет достичь более быстрого и полного заживления эрозий, а также повышает эффективность профилактики грозных осложнений и прогрессирующего течения заболевания.
СВЕДЕНИЯ ОБ АВТОРАХ:
Ливзан Мария Анатольевна — член-корреспондент РАН, д.м.н., профессор, заведующая кафедрой факультетской терапии и гастроэнтерологии, ректор ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-6581-7017.
Гаус Ольга Владимировна — к.м.н., доцент кафедры факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0001-9370-4768.
Мозговой Сергей Игоревич — д.м.н., доцент, профессор кафедры патологической анатомии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0002-6733-5572.
Бордин Дмитрий Станиславович — д.м.н., заведующий отделом патологии поджелудочной железы, желчных путей и верхних отделов пищеварительного тракта ГБУЗ МКНЦ им. А.С. Логинова ДЗМ; 111123, Россия, г. Москва, ул. Новогиреевская, д. 1, корп. 1; профессор кафедры пропедевтики внутренних болезней и гастроэнтерологии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; профессор кафедры общей врачебной практики и семейной медицины ФГБОУ ВО Тверской ГМУ Минздрава России; 170100, Россия, г. Тверь, ул. Советская, д. 4; ORCID iD 0000-0003-2815-3992.
Гавриленко Дарья Александровна — ординатор 1-го года обучения по специальности «терапия» кафедры
факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России; 644099, Россия, г. Омск, ул. Ленина, д. 12; ORCID iD 0000-0001-5245-7190.
Контактная информация: Гаус Ольга Владимировна, e-mail: gaus_olga@bk.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 20.02.2024.
Поступила после рецензирования 19.03.2024.
Принята в печать 11.04.2024.
ABOUT THE AUTHORS:
Maria A. Livzan — Dr. Sc. (Med.), Professor, Corresponding Member of the Russian Academy of Sciences, Head of the Department of Faculty Therapy and Gastroenterology, rector, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-6581-7017.
Olga V. Gaus — C. Sc. (Med.), Assistant Professor of the Department of Faculty Therapy and Gastroenterology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0001-9370-4768.
Sergei I. Mozgovoy — Dr. Sc. (Med.), Associate Professor, Professor of the Department of Pathological Anatomy, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0002-6733-5572.
Dmitriy S. Bordin — Dr. Sc. (Med.), Head of the Department of Pancreatic, Biliary, and Upper Gastrointestinal Disorders, A.S. Loginov Moscow Clinical Scientific Center; 1, build., 1, Novogireevskaya str., Moscow, 111123, Russian Federation; professor of the Department of Propaedeutics of Internal Diseases and Gastroenterology, Russian University of Medicine; 4, Dolgorukovskaya str., Moscow, 127006, Russian Federation; professor of the Department of General Medical Practice and Family Medicine, Tver State Medical University; 4, Sovetskaya str., Tver, 170100, Russian Federation; ORCID iD 0000-0003-2815-3992.
Darya A. Gavrilenko — 1st year resident of the Department of Faculty Therapy and Gastroenterology, Omsk State Medical University; 12, Lenin str., Omsk, 644099, Russian Federation; ORCID iD 0000-0001-5245-719.
Contact information: Olga V. Gaus, e-mail: gaus_olga@bk.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 20.02.2024.
Revised 19.03.2024.
Accepted 11.04.2024.
Информация с rmj.ru