Введение
Использование алкоголя является основным фактором риска бремени болезней во всем мире, на которые приходится почти 10% смертей среди населения в возрасте 15–49 лет. Согласно статистике около 20–30% россиян регулярно злоупотребляют алкоголем. Со злоупотреблением алкоголем связано примерно 70% регистрируемых в России случаев гепатита и цирроза печени[1]. Согласно данным статистики Всемирной организации здравоохранения употребление алкоголя ежегодно приводит к 2,6 млн случаев смерти (4,7% от общего числа смертей в год), а еще 0,6 млн случаев смерти обусловлено употреблением психоактивных веществ. Важно отметить, что 2 млн случаев смерти связаны с употреблением алкоголя1. Прямая связь между смертностью по причине патологии печени и употреблением спиртосодержащих напитков подтверждается практически во всех странах мира[2].
В настоящее время не теряет актуальности проблема изучения препаратов, имеющих гепатопротективные свойства [1], которые за короткий период способны нивелировать последствия алкогольной зависимости, повысить устойчивость печени к действию токсических веществ, а следовательно, снизить риски преждевременной смертности, особенно молодого населения. В связи с этим особого внимания заслуживают природные соединения класса терпенов, обладающие широким спектром фармакологической активности и низкой токсичностью. Выявлено большое разнообразие терапевтических свойств терпенов, таких как противоопухолевые, антимикробные, противопаразитарные, спазмолитические, противовоспалительные, иммуномодулирующие, антиаллергические [2–9].
Терпеноиды (изопреноиды) — один из самых крупных классов природных соединений, состоящих из изопреновых звеньев, формула: С5Н8. В зависимости от их количества органические углеводороды разделяются на моно-, сескви-, ди-, три-, тетра- и политерпеноиды. Ранние исследования свойств терпенов, входящих в состав биологически активных добавок (БАД), показали, что они обладают антимикробным, противовоспалительным, ранозаживляющим, гиполипидемическим, антиатеросклеротическим и корригирующим действием при метаболическом синдроме1 [4–7].
В ходе экспериментальных исследований при моделировании алкогольного поражения печени были доказаны гепатопротективные свойства терпенов. Перед нами стояла задача в ходе клинической практики подтвердить эти свойства, а именно действие терпенов на нормализацию биохимических показателей липидного и углеводного обмена в крови; снижение выраженности гидропической и зернистой дистрофии гепатоцитов и фибротических изменений в печени. Кроме того, известно, что терпены обладают иммуномодулирующей и антиапоптотической активностью, а также положительно влияют на желчевыделительную систему, оказывая холеретическое, холекинетическое и литолитическое действие [1, 4].
Цель исследования: оценка эффективности и переносимости терпеносодержащей БАД ВитаТерпен Актив® в лечении пациентов с хроническим алкогольным гепатитом (ХАГ).
Содержание статьи
Материал и методы
На базе терапевтического отделения ФГБУ «Клиническая больница» (г. Москва) проведено неинтервенционное открытое неконтролируемое исследование. Отбор пациентов в протокол клинического исследования проводили с учетом критериев включения: мужчины и женщины в возрасте от 28 до 75 лет, страдающие ХАГ; превышение верхнего лимита нормы содержания аланинаминотрансферазы (АЛТ) как минимум в 3 раза. Критерии невключения: стеатогепатит неалкогольной этиологии; цирроз печени; тяжелая соматическая патология в стадии декомпенсации; эндокринные заболевания (диффузный токсический зоб с тиреотоксикозом, миксидема, синдром Кушинга, ожирение, акромегалия и др.); легочные обструктивные заболевания, тяжелые гнойные процессы; злокачественные опухоли; прием гепатотоксических лекарств; беременные женщины; наркоманы и лица с индивидуальной непереносимостью компонентов БАД.
Пациенты находились на стационарном лечении по поводу ХАГ или сердечно-сосудистой патологии. У пациентов с сердечно-сосудистой патологией в ходе обследования был поставлен диагноз ХАГ. Пациенты подписывали информированное согласие на получение дополнительно к немедикаментозному (коррекция образа жизни, лечебная физкультура, физиотерапия) и медикаментозному (согласно клиническим рекомендациям) лечению терпеносодержащей БАД ВитаТерпен Актив® в виде липосомальной формы (порошок), в состав которого входит набор терпеноидов пихты сибирской (Abies sibirika L.), витамин Е, витамин С и льняное масло. После выписки пациенты продолжали лечение БАД на амбулаторном этапе с последующими контрольными исследованиями.
В исследование включено 20 человек, которым назначен БАД ВитаТерпен Актив® по 3 капсулы в сутки (75 мг/кг массы тела) после еды в течение 1 мес. Возраст пациентов колебался от 28 до 75 лет (в среднем 54,1±6,2 года), большинство были мужчины — 12 (65%). Все пациенты злоупотребляли алкоголем в среднем в течение 12,5 года (от 5 до 30 лет). Употребляли алкоголь в течение 5–10 лет 10 (50%) пациентов, 11–20 лет — 7 (35%), 21–30 лет — 2 (10%), более 30 лет — 1 (5%).
Из анамнеза: длительность ХАГ составила в среднем 5 лет (от впервые выявленного до 10-летней давности). У 9 (45%) пациентов заболевание длилось менее 1 года, у 10 (50%) — от 1 года до 5 лет, у 1 (5%) — более 5 лет.
Сопутствующие заболевания: хронический панкреатит алкогольного генеза — 9 (45%) пациентов, язвенная болезнь двенадцатиперстной кишки — 1 (5%), гастроэзофаге-альная рефлюксная болезнь — 5 (25%), хронический бескаменный холецистит — 3 (15%), хронический бронхит — 2 (10%), ишемическая болезнь сердца — 5 (25%), гипертоническая болезнь — 7 (35%), сахарный диабет 2 типа — 2 (10%) и аденома предстательной железы — 1 (5%). Все болезни были в стадии ремиссии и не требовали дополнительного лечения.
Оценку эффективности лечения проводили по результатам оценки нескольких показателей до и после лечения:
данные УЗИ (структура органов) печени и селезенки;
данные биохимического анализа крови: содержание АЛТ, аспартатаминотрансферазы (АСТ), общего билирубина, щелочной фосфатазы (ЩФ), γ-глутамилтранспептидазы (ГГТ), креатинина;
данные анализа крови;
индекс фиброза печени, определяемый по дискриминантной счетной шкале Боначини (показатели МНО, число тромбоцитов и соотношение АЛТ/АСТ);
клинический симптомокомплекс (боли и/или ощущение тяжести в животе, тошнота и рвота, отрыжка и вздутие живота, послабление стула, запор).
В ходе статистической обработки проводили сравнение двух выборок (до и после лечения). Различия считали статистически значимыми на уровне значимости 95% при р<0,05. Для качественных показателей применяли абсолютные и процентные значения, для количественных показателей рассчитывали среднее арифметическое и среднее квадратичное отклонение (M±m).
Результаты и обсуждение
Одним из критериев эффективности терапии служили данные УЗИ печени и селезенки: исходно размеры печени у 16 (80%) пациентов были увеличены, у 4 (20%) — в пределах нормы, у всех больных были признаки жировой инфильтрации печени. Селезенка у больных была не увеличена. По данным УЗИ у больных после месячного курса терапии препаратом размеры печени и селезенки остались прежними.
Динамика показателей биохимии крови представлена в таблице 1.
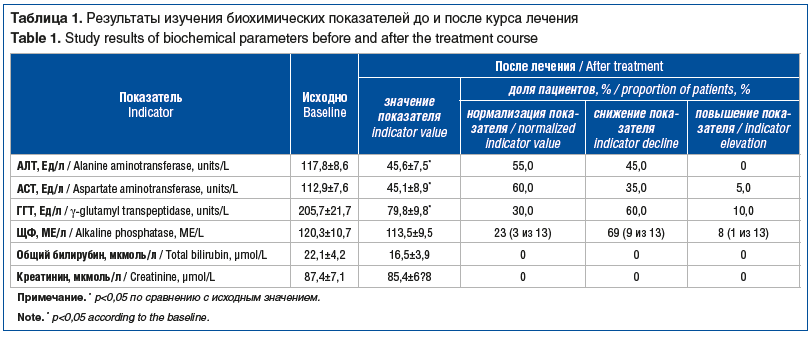
Как видно из таблицы 1, исходно у всех пациентов отмечалось повышение уровня АЛТ, АСТ и ГГТ. По окончании курса лечения констатировали следующую динамику.
Показатели АЛТ: у 11 (55%) больных наблюдалась полная нормализация показателя, у 9 (45%) — снижение в среднем с 3,8 до 1,7 нормы.
Показатели АСТ: у 12 (60%) пациентов наблюдалась нормализация показателя, у 7 (35%) — снижение уровня АСТ в среднем с 2,9 до 1,3 нормы и у 1 (5%) пациента — повышение содержания АСТ в среднем до 1,4 нормы (статистический разброс).
Показатели ГГТ: у 6 (30%) пациентов наблюдалась нормализация показателя, у 12 (60%) — снижение показателя в среднем с 7,8 до 1,8 нормы и у 2 (10%) — повышение содержания ГГТ в среднем до 1,2 нормы.
Уровень ЩФ исходно был повышен у 13 (65%) пациентов. После лечения у 3 (23%) пациентов наблюдалась нормализация показателя, у 9 (69%) — снижение показателя в среднем с 4,6 до 1,9 нормы и у 1 (8%) пациента — повышение показателя в среднем с 1,2 до 1,4 нормы.
Показатели общего билирубина и креатинина на фоне проводимой терапии колебались в пределах нормальных значений.
По данным общего анализа крови, показатели эритроцитов, лейкоцитов, тромбоцитов, СОЭ и гемоглобина исходно и после лечения изменялись в пределах нормальных значений.
Динамика индекса фиброза печени (ИФ) представлена в таблице 2.
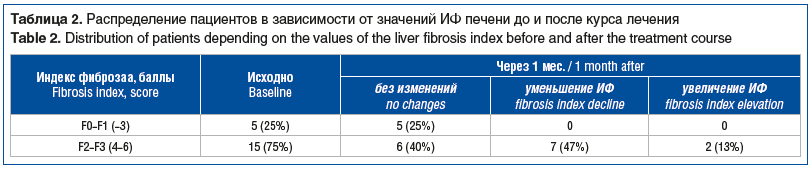
Как видно из таблицы 2, исходно у пациентов фиксировали слабый, умеренный и выраженный фиброз. После месячного курса терапии слабый фиброз отмечался у 5 (25%) пациентов, умеренный и выраженный фиброз — у 15 (75%), однако в последних случаях ИФ не изменялся у 6 (40%) из 15 пациентов, уменьшался у 7 (47%) из 15 пациентов и повышался у 2 (13%) из 15 пациентов, однако данные носили недостоверный характер.
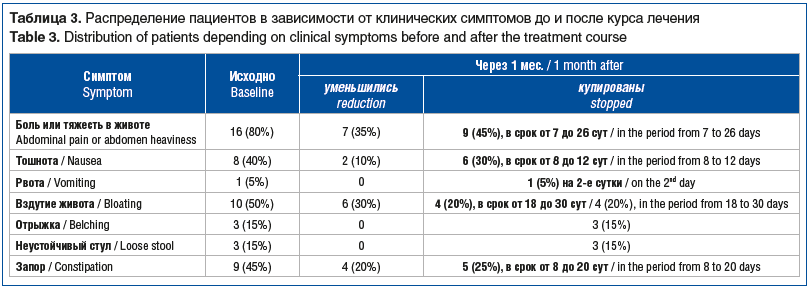
Как следует из таблицы 3, у пациентов от начала приема БАД клинические симптомы стали уменьшаться в срок от 2 до 18 сут и полностью купировались к окончанию курса терапии. Следует отметить, что у 3 (15%) из 20 пациентов течение ХАГ сопровождалось кожным зудом. На фоне комплексного лечения кожный зуд полностью купировался в срок от 2 до 4 сут.
Пациенты оценивали переносимость и безопасность БАД как очень хорошую и хорошую, нежелательных лекарственных и аллергических реакций на компоненты БАД не отмечено.
Заключение
В настоящем исследовании впервые изучали эффективность и безопасность терпеносодержащей БАД ВитаТерпен Актив® в дозе 1 капсула 3 р/сут после еды в течение 1 мес. для лечения больных ХАГ.
Получены следующие результаты:
снижение показателей цитолиза (АЛТ, АСТ) и холестаза (за исключением ЩФ, общего билирубина, ГГТ) через 1 мес. у 90–100% пациентов, при этом у 55% данные носили статистически значимый характер;
у 10% пациентов лечение не оказало эффекта, и это может быть связано как с недостаточностью суточной дозы, так и с недостаточной продолжительностью лечения;
индекс фиброза печени снизился, но недостоверно, у 7 (47%) из 15 пациентов, у остальных 8 (53%) из 15 пациентов существенной динамики не претерпел (это может быть связано с коротким курсом лечения — всего 1 мес.);
клинические проявления заболевания отмечены у 80% пациентов. По окончании курса лечения у всех они уменьшились или купировались полностью. Обращает на себя внимание полное купирование кожного зуда в срок от 2 до 4 сут.
Пациенты оценивали переносимость и безопасность препарата как очень хорошую и хорошую, побочных эффектов не отмечено.
Таким образом, можно сделать вывод, что терпеносодержащая БАД ВитаТерпен Актив® обладает гепатопротективными свойствами и может быть рекомендована как дополнение к комплексной терапии ХАГ.
Сведения об авторах:
Петухова Светлана Вячеславовна — к.м.н., заведующая терапевтическим отделением ФГБУ «Клиническая больница»; 107150, Россия, г. Москва, ул. Лосиноостровская, д. 45, корп. 2, вн. тер. г. муниципального округа Метрогородка.
Зверков Игорь Владимирович — д.м.н., профессор кафедры гастроэнтерологии ФГБУ «ЦГМА»; 121359, Россия, г. Москва, ул. Маршала Тимошенко, д. 19, стр. 1А; ORCID iD 0000-0001-6210-1955.
Бибова Ольга Ахатовна — директор по маркетингу ООО «Инитиум-Фарм»; 121357, Россия, г. Москва, Кутузовский пр-т, д. 69/6.
Рашитова Элина Ленаровна — врач-ординатор гематолог ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, 117198, Россия, г. Москва, ул. Саморы Машела, д. 1; ORCID iD 0000-0003-1450-8254.
Контактная информация: Рашитова Элина Ленаровна, e-mail: elina.rashitova@gmail.com.
Источник финансирования: исследование проведено при поддержке ООО «Инитиум-Фарм» на безвозмездной основе.
Конфликт интересов: Бибова О.А. является представителем компании ООО «Инитиум-Фарм». Сотрудник компании не участвовал в разработке и проведении исследования; сборе, анализе и интерпретации данных.
Статья поступила 15.07.2024.
Поступила после рецензирования 06.08.2024.
Принята в печать 29.08.2024.
About the authors:
Svetlana V. Petukhova — C. Sc. (Med.), Head of the Department of Therapy, Clinical Hospital; 45, build. 2, Losinoostrovskaya str., intracity territory of Metrogorodok federal city, Moscow, 107150, Russian Federation.
Igor V. Zverkov — Dr. Sc. (Med.), Professor of the Department of Gastroenterology, Central State Medical Academy; 19, build. 1A, Marshal Timoshenko str., Moscow, 121359, Russian Federation; ORCID iD 0000-0001-6210-1955.
Olga A. Bibova — Marketing Director, Initium-Pharm LLC; 69/6, Kutuzovsky Ave., Moscow, 121357, Russian Federation.
Elina L. Rashitova — resident hematologist, Dmitry Rogachev National Medical Research Center for Children’s Hematology, Oncology and Immunology; 1, Samora Mashela str., Moscow, 117198, Russian Federation; ORCID iD 0000-0003-1450-8254.
Contact information: Elina L. Rashitova, e-mail: elina.rashitova@gmail.com.
Financial Disclosure: the study was conducted with the support of Initium-Pharm LLC on a gratuitous basis.
Conflict of interest: Bibova O.A. is representative of Initium-Pharm LLC. The company’s employee did not participate in the development and conduct of the study, as well as collection, analysis and interpretation of data.
Received 15.07.2024.
Revised 06.08.2024.
Accepted 29.08.2024
[1] Клинические рекомендации. Алкогольная болезнь печени (АБП) у взрослых 2023. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/schema/711_1 (дата обращения: 19.07.2024).
[2] Каждый год употребление алкоголя и психоактивных веществ уносит жизни более 3 млн человек, большинство из которых составляют мужчины (Электронный ресурс.) URL: https://www.who.int/ru/news/item/25-06-2024-over-3-million-annual-deaths-due-to-alcohol-and-drug-use… (дата обращения: 19.07.2024).
Информация с rmj.ru

