Содержание статьи
- 1 Введение
- 2 Параметры исследования
- 3 Критерии включения
- 4 Критерии невключения
- 5 Определение ЛП(а)
- 6 Прямое секвенирование генов LDLR, APOB, PCSK9 по методу Sanger
- 7 Полигенный индекс
- 8 Ген АРОЕ
- 9 NGS
- 10 Статистический анализ
- 11 Результаты исследования
- 12 Особые группы клинического наблюдения
- 13 Пациенты с геСГХС
- 14 Влияние инклисирана на уровень ЛП(а) в сыворотке крови
- 15 Обсуждение
- 16 Выводы
Введение
Основной причиной смертности в Российской Федерации и в мире являются сердечно-сосудистые заболевания (ССЗ) атеросклеротической этиологии [1–3]. Ключевым модифицируемым фактором риска этих заболеваний является повышение уровня холестерина (ХС) атерогенных фракций, в частности липопротеинов низкой плотности (ЛПНП), липопротеинов невысокой плотности (неЛПВП), триглицеридов (ТГ), а также обсуждаемого в последние годы липопротеина (а) (ЛП(а)) [4] Доказанной терапевтической мишенью первичной и вторичной профилактики атеросклеротических ССЗ является ХС ЛПНП, повышение уровня которого в крови корректируется путем назначения препаратов первой линии — ингибиторов гидроксиметилглутарилкоэнзим А-редуктазы (ГМГ-КоА редуктазы), т. е. статинов, с доказанной эффективностью и достаточной безопасностью1 [1]. За последние 20 лет целевой уровень ХС ЛПНП неоднократно пересматривали, устанавливая все более низкие значения с целью предупреждения сердечно-сосудистых осложнений [3, 4]. Наряду с этим появилась проблема достижения этих целей, поэтому как в отечественных, так и в зарубежных клинических рекомендациях по коррекции нарушений липидного обмена особое внимание уделено комбинированной гиполипидемической терапии1 [1, 5]. Поиск стратегий по снижению концентрации ХС ЛПНП привел к разработке препарата инклисиран, первой в своем классе малой интерферирующей РНК, которая предотвращает трансляцию пропротеиновой конвертазы субтилизин/кексин типа 9 (PCSK9) в гепатоцитах [6]. Это повышает рециркуляцию и количество рецепторов ХС ЛНПН на мембране гепатоцитов, что усиливает захват ХС ЛНПН, снижая их концентрацию в крови [6]. Первые проведенные двойные слепые рандомизированные контролируемые исследования инклисирана III фазы (ORION-9, ORION-10 и ORION-11) показали значительное снижение уровня ХС ЛПНП — примерно на 50% по сравнению с плацебо как после инициальной инъекции, так и после инъекции через 3 мес. и далее 1 раз в 6 мес. в течение 18 мес. [7–9]. Министерство здравоохранения Российской Федерации в 2022 г. одобрило использование инклисирана для лечения гиперхолестеринемии (гетерозиготной семейной (ГеСГХС) и несемейной) или смешанной дислипидемии, что также нашло отражение в клинических рекомендациях «Нарушения липидного обмена»1.
Так, в соответствии с данными рекомендациями, назначение инклисирана (с высоким классом и уровнем доказательности) рекомендовано:
пациентам с очень высоким риском и недостижением целевого уровня ХС ЛПНП <1,4 ммоль/л на фоне максимально переносимых доз статина, в комбинации с эзетимибом с целью вторичной профилактики ССЗ;
пациентам с экстремальным или очень высоким риском с уровнем ХС ЛПНП >5,0 ммоль/л в качестве инициального назначения, в комбинации со статином в максимально переносимой дозе и эзетимибом;
пациентам с очень высоким риском, без СГХС и с недостижением целевого уровня ХС ЛПНП <1,4 ммоль/л на фоне максимально переносимых доз статина, с/без эзетимиба с целью первичной профилактики ССЗ;
пациентам с непереносимостью любой дозы статина, которые на фоне приема эзетимиба не достигли целевого уровня ХС ЛПНП;
пациентам с сахарным диабетом (СД) 2 типа высокого и очень высокого сердечно-сосудистого риска с недостаточным снижением уровня ХС ЛПНП на фоне приема максимально переносимых доз статинов и эзетимиба для достижения целевого уровня ХС ЛПНП и снижения риска сердечно-сосудистых осложнений;
пациентам с ишемическим инсультом или транзиторной ишемической атакой с целью достижения целевого значения ХС ЛПНП.
Назначение инклисирана нашло отражение в критериях оценки качества медицинской помощи пациентам с нарушениями липидного обмена, когда его применение необходимо в случаях отсутствия достижения целевого уровня ХС ЛПНП через 8±4 нед. как на фоне максимально переносимых доз статина, так и на фоне максимально переносимых доз статина и эзетимиба1. Однако опыт реального применения инклисирана в Российской Федерации невелик и представлен единичным исследованием [10]. Поэтому был предпринят анализ данных собственного клинического опыта применения этого препарата.
Цель исследования: анализ применения инклисирана в условиях реальной клинической практики для первичной и вторичной профилактики атеросклеротических ССЗ у больных с дислипидемией.
Материал и методы
Дизайн исследования
Проведено ретроспективное когортное исследование с анализом данных 22 пациентов, получивших первую (инициальную) и вторую (через 3 мес. от инициальной) дозы инклисирана по 284 мг подкожно в соответствии с инструкцией к препарату в период с 1 февраля по 20 сентября 2023 г. Исследование выполнено в соответствии с требованиями Хельсинкской декларации Всемирной медицинской ассоциации (в ред. 2013 г.). Протокол исследования одобрен локальным этическим комитетом (протокол № 03/2023 от 19.01.2023), все пациенты подписали информированное согласие.
Параметры исследования
Проведен сбор данных пациентов: пол, возраст, анамнез ССЗ атеросклеротической этиологии и СГХС, текущий прием гиполипидемических препаратов, непереносимость статинов, факторы риска ССЗ, включая артериальную гипертензию, СД 1 и 2 типа, статус курения. СГХС определяли как подтверждение патогенного варианта после генетического тестирования или как совпадение с клиническими критериями С. Брума, либо как соответствие шкале Голландских липидных клиник1. Среди пациентов, исходно принимавших статины, была дополнительно выделена группа, получающая высокоинтенсивную терапию (аторвастатин >40 мг или розувастатин >20 мг в сутки) в соответствии с действующими отечественными рекомендациями1. Пациенты, принимавшие комбинированную гиполипидемическую терапию статином и эзетимибом, были также проанализированы отдельно, как и пациенты с непереносимостью статинов, которую определяли по наличию побочных эффектов, препятствующих либо их назначению, либо дальнейшему увеличению дозы. Исходно (перед началом лечения инклисираном) всем пациентам был проведен физикальный осмотр и забор крови натощак для оценки липидного спектра и уровня ТГ (как стандартным биохимическим методом, так и методом электрофореза), содержания ЛП(а), клинического анализа крови, уровня креатинина, мочевины и электролитов, функциональных проб печени и щитовидной железы.
Особенности фармакодинамики инклисирана обусловливают наибольшее ожидаемое снижение уровня ХС ЛПНП после первой инъекции примерно к 60-му дню и после второй инъекции — к 150-му дню [11], поэтому через 2 и 4 мес. от начала терапии инклисираном проводили контрольное исследование крови: липидный спектр, ТГ, ЛП(а), функциональные пробы печени, креатинин, мочевина, клинический анализ крови. У пациентов с гипертриглицеридемией для расчета концентрации ХС ЛПНП ориентировались на уровень ЛПНП, полученный методом электрофореза. Также протокол исследования подразумевал регистрацию побочных реакций и случаев прекращения лечения.
Критерии включения
В исследование включали всех пациентов в возрасте 18 лет, которым в центре диагностики и лечения нарушений липидного обмена ФГБОУ ВО ПСПбГМУ им. акад. И.П. Павлова Минздрава России последовательно была инициирована терапия инклисираном в период с 1 февраля по 20 сентября 2023 г. в соответствии с рекомендациями Минздрава России «Нарушения липидного обмена» (2023 г.) в качестве дополнения к диете, в комбинации со статинами в максимально переносимой дозе и другой гиполипидемической терапией, получаемой пациентом не менее 4 нед. до начала терапии инклисираном. В случае непереносимости или при наличии противопоказаний к назначению статинов инклисиран применялся с другой гиполипидемической терапией или в виде монотерапии.
Критерии невключения
В исследование не включали пациентов со вторичными причинами гиперхолестеринемии, а также получающих инклисиран в рамках клинических исследований, пациентов с доказанной гомозиготной СГХС и тех, кто получал терапию гуманизированными моноклональными антителами к PCSK9. Не включали пациентов с тяжелой печеночной недостаточностью класса С по шкале Чайлд — Пью [12].
Лабораторные исследования
Исследование липидов и биохимических показателей крови
Стандартные биохимические показатели и липидный состав крови (ОХ, ТГ, ХС ЛПНП, ХС ЛПВП) определяли в сыворотке с использованием наборов ThermoFisher SCIENTIFIC на анализаторе Konelab фотометрическим методом.
Электрофорез липидов проводили на оборудовании для горизонтального электрофореза в агарозе Hydrasis II (Sebia, Франция) в соответствии с рекомендациями производителя. Для определения ХС в составе липидных фракций использовали реактивы HDL/LDL Cholesterol Direct (Sebia, Франция), основанные на ферментативном методе выявления ХС с последующей денситометрией продукта реакции. Для исследования ТГ и других липидов в составе ЛП использовали реактивы Hydragel Lipo+Lpa (Sebia, Франция), основанные на колориметрическом окрашивании липидов колорогенным красителем с последующей денситометрией. Для количественного измерения ТГ и ХС использовали автоматический биохимический анализатор и реактивы компании BioSystems (Испания). Расчет содержания ХС и ТГ в составе липидных фракций осуществляли с использованием программного обеспечения Phoresis (Sebia, Франция), тип дислипидемии интерпретировали в соответствии с классификацией Фридериксона D. Fredrickson (1965 г.) или классификацией ВОЗ (2000 г.) [13].
Определение ЛП(а)
Для оценки содержания ЛП(a) использовали метод лазерной кинетической нефелометрии на автоматическом анализаторе белков (Siemens Healtheeners, Германия), с набором реактивов в соответствии с инструкциями производителя.
Молекулярно-генетические методы
Экстракция ДНК
Выделение ДНК осуществляли методом высаливания из лейкоцитов венозной крови пациентов. Далее проводили оценку концентрации выделенной ДНК и наличия контаминации в элюате с помощью соотношения A260/A280 с использованием спектрофотометра BioDrop UV/VIS (SERVA, Германия). Образец считали высокоочищенным, если оптическое поглощение образца A260/280 находилось в диапазоне от 1,8 до 2,0. Оптимальной концентрацией образцов считали показатели от 50 нг/мкл. Образцы ДНК хранили при температуре -20 °С.
Прямое секвенирование генов LDLR, APOB, PCSK9 по методу Sanger
Для генотипирования СГХС использовали прямое секвенирование 2–6, 8–10, 13–14-го экзонов гена LDLR; 26-го экзона гена APOB; 1, 3, 4, 7, 8, 12-го экзонов гена PCSK9 по методу Sanger. На первом этапе проводили полимеразную цепную реакцию (ПЦР) с помощью ДНК-амплификатора T100 Thermal Cycler (Bio-Rad, США). ПЦР выполняли с использованием набора реактивов Encyclio Plus PCR kit («Евроген», Россия). Условия ПЦР подбирали самостоятельно. Для визуализации результатов амплификации и определения наличия ПЦР-продукта был использован метод горизонтального электрофореза в 1,5% агарозном геле. Очищенные продукты ПЦР секвенировали с помощью набора реактивов ABI PRISM BigDye Terminator v3.1 (Thermo Scientific, США). Далее продукт был очищен и идентифицирован с помощью капиллярного электрофореза с использованием генетического анализатора «Нанофор-5» («Синтол», Россия). Полученные данные про-анализированы посредством программного обеспечения Mutation Surveyor (SoftGenetics, США).
Полигенный индекс
Полигенный индекс риска СГХС основывается на оценке точечных полиморфизмов в генах CELSR2, APOB, ABCG8, LDLR и APOE. Генотипирование однонуклеотидных полиморфизмов (SNP) rs629301 гена CELSR2, rs1367117 гена APOB, rs4299376 гена ABCG8, rs6511720 гена LDLR, rs429358 и rs7412 гена APOE осуществляли с помощью ПЦР в реальном времени с использованием коммерческих наборов «ТестГен» (Россия) согласно инструкции производителя. Реакционная смесь объемом 10 мкл включала деионизованную воду, смесь для ПЦР, Taq-полимеразу и ДНК исследуемого образца в разведении до 30 нг/мкл. Амплификацию и анализ результатов осуществляли с использованием анализатора LightCycler 96 (ROCHE, Швейцария/Германия). Далее полученные результаты были интерпретированы в виде суммы аллелей риска с помощью SNP-коэффициентов, разработанных в 2013 г. на основании наиболее распространенных вариантов, повышающих уровень ЛПНП [14].
Ген АРОЕ
Для обнаружения аллелей E2, E3, E4 гена APOE было проведено генотипирование однонуклеотидных полиморфизмов rs429358 и rs7412 с помощью ПЦР в реальном времени с использованием коммерческих наборов «ТестГен» (Россия) согласно инструкции производителя. Реакционная смесь объемом 10 мкл включала деионизованную воду, смесь для ПЦР, Taq-полимеразу и ДНК исследуемого образца в разведении до 30 нг/мкл. Амплификацию и анализ результатов осуществляли с использованием анализатора LightCycler 96 (ROCHE, Швейцария/Германия).
NGS
Для проведения NGS-секвенирования была разработана панель урацилсодержащих праймеров Prep&Seq™ U-target (ООО «ПАРСЕК ЛАБ», Россия). Панель праймеров включала кодирующие последовательности (CDSs), промоторы и близкие интронные области для 3 генов: APOB — 1 промотор, 29 экзонов (захват интронов ± 20 нуклеотидов), LDLR — 1 промотор, 18 экзонов (захват интронов ± 20 нуклеотидов) и PCSK9 — 1 промотор, 12 экзонов (захват интронов ± 20 нуклеотидов).
Процесс создания библиотек включает следующие основные этапы: таргетное обогащение геномной ДНК с использованием урацилсодержащих панелей праймеров, отрезание праймеров с восстановлением концов, лигирование адаптерных последовательностей и амплификацию библиотек.
На первом этапе проводится таргетное обогащение ДНК методом мультиплексной ПЦР с использованием панелей, урацилсодержащих праймеров Prep&Seq™ U-panel. Амплификация проводилась с помощью ДНК-амплификатора T100 Thermal Cycler (Bio-Rad, США). Далее ампликоны, полученные в ходе мультиплексной ПЦР, подвергаются отрезанию праймеров с ферментативной модификацией концов. Завершающим шагом первого этапа является лигирование адапторной последовательности к ампликонам. На втором этапе проводится очистка продуктов лигирования с помощью модуля очистки Prep&Seq™ Beads MultiClean (ООО «ПАРСЕК ЛАБ», Россия), в состав которого входят магнитные частицы. Далее осуществляются амплификация библиотек и итоговая очистка после обогащения на магнитных частицах.
Завершающим этапом подготовки образцов является количественная оценка амплифицированных библиотек с помощью флуориметра Qubit 4 (Thermo Fisher Scientific) с использованием набора Qubit ssDNA Assay Kit для количественного определения ДНК. Оптимальной концентрацией образцов считали показатели в диапазоне от 1 до 5 нг/мкл. Приготовленные образцы ДНК секвенировали на платформе Illumina MiSeq (Illumina, США).
Анализ полученных данных каждого образца осуществляли индивидуально с использованием программного обеспечения, предоставляемого производителем реагентов (ООО «ПАРСЕК ЛАБ», Россия).
Обнаружение делеций и дупликаций гена LDLR с помощью мультиплексной амплификации лигазно-связанных проб (MLPA)
Для обнаружения протяженных делеций и дупликаций промотора и экзонов гена LDLR был проведен анализ методом MLPA с использованием коммерческого набора SALSA MLPA KIT P062 (MRCHolland, Нидерланды), содержащего 33 зонда: 20 зондов к гену LDLR, 1 фланкирующий зонд к гену SMARCA4, расположенному выше гена LDLR, и 12 эталонных зондов. Смесь зондов также содержит 9 контрольных фрагментов, которые образуют короткие продукты, отражающие качество реакции лигирования и количество ДНК. Амплификацию проводили с помощью ДНК-амплификатора T100 Thermal Cycler (Bio-Rad, США). Флуоресцентно меченные фрагменты были разделены и идентифицированы с помощью капиллярного электрофореза с использованием генетического анализатора «Нанофор-5» («Синтол», Россия). Полученные данные проанализированы с помощью программного обеспечения GeneMarker® (SoftGenetics, США). Для проведения анализа был использован один отрицательный контроль, который позволял сравнивать исследуемые образцы для оценки относительного количества амплифицированных зондов.
Статистический анализ
Статистический анализ данных проводили с использованием статистического пакета программ SPSS, версия 17.0 (SPSS Inc., США). Количественные показатели оценивали на предмет соответствия нормальному распределению с помощью критерия Шапиро — Уилка. Количественные показатели, имеющие нормальное распределение, описывались с помощью средних арифметических величин (M) и стандартных отклонений (SD), границ 95% доверительного интервала (95% ДИ). В случае отсутствия нормального распределения количественные данные описывали с помощью медианы (Me) и нижнего и верхнего квартилей (Q1; Q3). При сравнении трех и более зависимых совокупностей, распределение которых отличалось от нормального, использовали непараметрический критерий Фридмана с апостериорными сравнениями с помощью критерия Коновера — Имана с поправкой Холма.
Результаты исследования
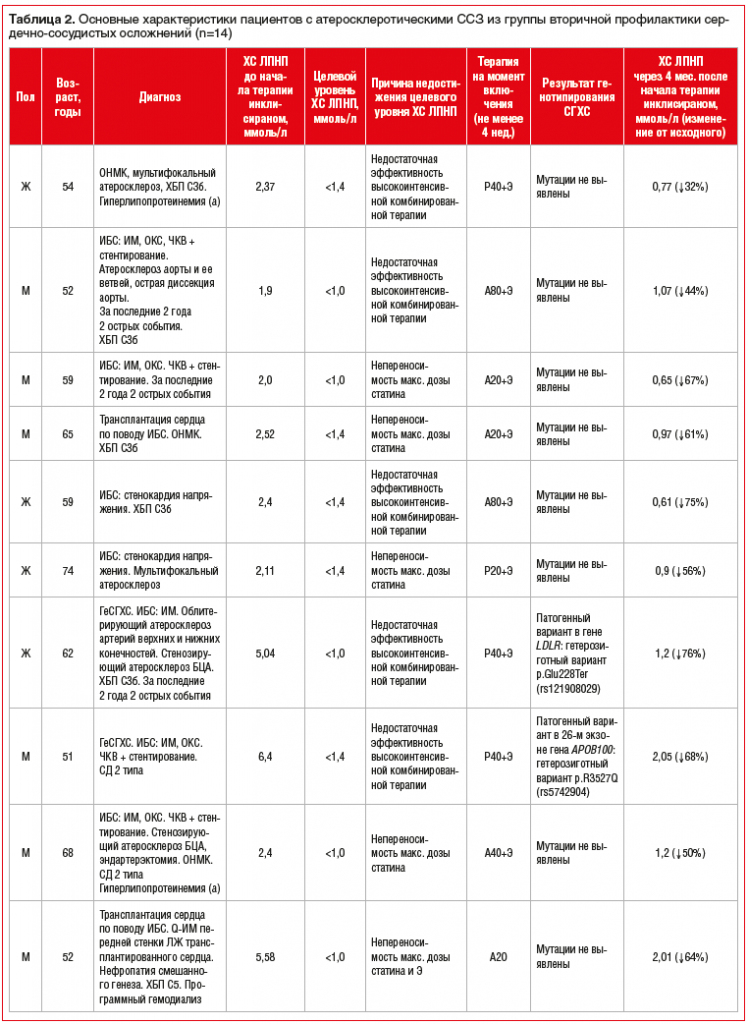
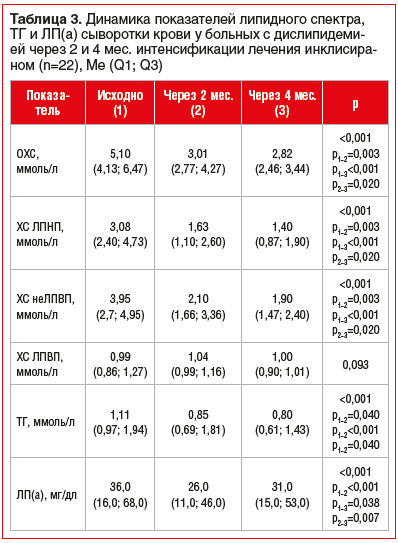
В исследование были включены 22 пациента, которые за указанный период наблюдения получили первую и вторую дозы инклисирана. Возраст обследованных, большинство из которых были мужчины — 13 (59%) человек, составил от 36 до 74 лет (средний возраст 61 (51; 62) год). Основные клинические диагнозы и исходные характеристики пациентов из группы первичной профилактики ССЗ представлены в таблице 1, из группы вторичной профилактики ССЗ — в таблице 2.
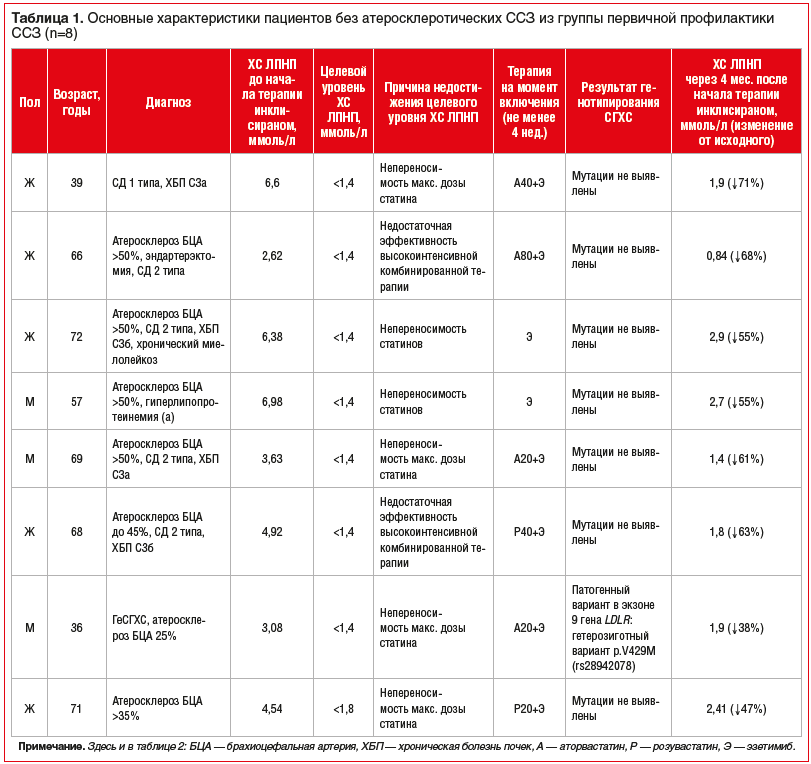
При анализе исходных характеристик установлено, что 3 (13,6%) пациента имели полную непереносимость статинов, которая у 2 пациентов проявлялась рабдомиолизом и у 1 — клинически значимым повышением уровня трансаминаз. Терапию статинами получали 19 (86,4%) человек, из которых у 11 (50%) отмечена непереносимость максимальных доз статина в виде значимого повышения уровня транс-аминаз. Высокоинтенсивную терапию статинами чаще получали женщины, чем мужчины: 8 (73%) против 3 (27%) (р<0,001). Терапию статинами в средних дозах в данном исследовании получали только мужчины по причине непереносимости высокоинтенсивных доз (8 (100%) человек).
Терапию эзетимибом в составе как комбинированной гиполипидемической терапии, так и монотерапии (3 пациента с непереносимостью статинов: 2 мужчины и 1 женщина) получал 21 (95,5%) пациент. У 1 (4,5%) человека в анамнезе была отмечена непереносимость эзетимиба в виде диареи и вздутия живота.
На протяжении всего периода наблюдения регулярной терапии статинами и/или эзетимибом придерживались все 22 пациента, что делает достоверными результаты оценки эффективности терапии инклисираном.
В группе первичной профилактики ССЗ наблюдали 8 пациентов, из которых 7 имели очень высокий сердечно-сосудистый риск (ССР) и 1 — умеренный ССР, обусловленные такими состояниями, как СД 1 типа, атеросклеротическое поражение БЦА, ГеСГХС (см. табл. 1).
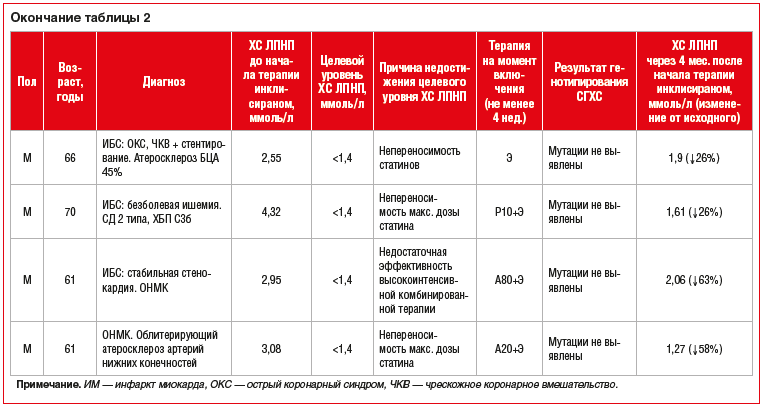
В группе вторичной профилактики ССЗ наблюдали 14 пациентов, из которых 9 имели очень высокий ССР и 5 — экстремальный ССР, обусловленные такими состояниями, как ишемическая болезнь сердца (ИБС), острое нарушение мозгового кровообращения (ОНМК), транзиторная ишемическая атака (ТИА), СД 2 типа, атеросклеротическое поражение БЦА и артерий нижних конечностей, ГеСГХС (см. табл. 2). По данным анамнеза в связи с тяжестью течения ИБС двум пациентам была проведена трансплантация сердца, у одного из пациентов имеется терминальная стадия ХБП, он дополнительно получает заместительную почечную терапию (программный гемодиализ).
Для оценки показателей липидного профиля и содержания ТГ сыворотки крови использовали стандартный фотометрический метод, сравнивая его показатели с данными, полученными методом электрофореза, значимых различий результатов между двумя этими методами оценки получено не было, вероятно, по причине отсутствия больных с выраженной гипертриглицеридемией. В таблицах указаны данные, полученные стандартным фотометрическим методом.
В обследованной группе пациентов исходные показатели липидного профиля не соответствовали целевым значениям для пациентов с высоким и очень высоким ССР. Через 2 и 4 мес. после начала терапии инклисираном наблюдали значимое и стойкое снижение показателей липидного профиля (рис. 1, табл. 3), что подтверждает известный факт снижения инклисираном концентрации ЛПНП не менее чем на 50% по данным исследований группы ORION [9].
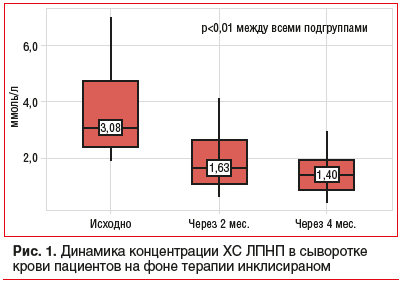
На фоне терапии инклисираном значимого снижения достигли в отношении не только ХС ЛПНП, но и ХС неЛПВП и ТГ (рис. 2, 3).
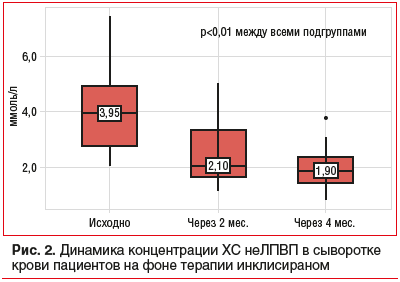
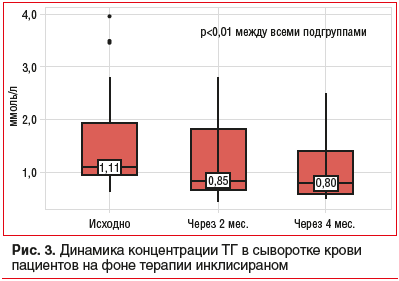
Индивидуальные ответы на лечение инклисираном представлены в таблицах 1 и 2, демонстрируя широкий диапазон снижения уровня ХС ЛПНП в пределах от 26 до 76% от исходного уровня. Медиана ХС ЛПВП в ходе наблюдения значимо не изменилась (см. табл. 3), а медиана концентрации ТГ снизилась с 1,11 до 0,61 ммоль/л (p<0,001).
Различия в степени снижения уровня ХС ЛПНП к 4-му месяцу лечения инклисираном были выявлены в обследованной когорте больных в зависимости от пола. Так, у женщин уровень ХС ЛПНП снизился на 60,3%, а у мужчин — на 52,4% (р=0,004). Такая особенность может объясняться тем, что в данной выборке пациентов терапию высокоинтенсивными дозами статинов значимо чаще получали женщины, что было отмечено выше.
Снижение уровня ХС ЛПНП при добавлении к терапии инклисирана было значимым, но зависело от сопутствующей терапии статинами и эзетимибом. Так, к 4-му месяцу наблюдения наибольшего снижения уровня ХС ЛПНП достигли пациенты, получавшие высокоинтенсивные или максимальные дозы статинов в комбинации с эзетимибом 10 мг (60,3% снижения); несколько менее выраженно, но также значимо снижался уровень ХС ЛПНП у тех пациентов, которые исходно получали средние дозы статинов в комбинации с эзетимибом (53,1% снижения); наименьшего эффекта достигли те, кто исходно получал только эзетимиб по причине непереносимости статинов (45,3% снижения). Различия между группами пациентов с тремя различными стратегиями гиполипидемической терапии исходно были значимы (р<0,05), различия в снижении уровня ХС ЛПНП в каждой группе по сравнению с исходным уровнем было также статистически значимым (р<0,05).
К 4-му месяцу лечения инклисираном 16 (72,7%) пациентов достигли снижения уровня ХС ЛПНП на 50% и более по сравнению с исходным уровнем, а 10 (45,5%) пациентов достигли уровня ХС ЛПНП <1,4 ммоль/л.
Анализ стандартных биохимических параметров оценки функции печени (аланинаминотрансфераза, аспартатаминотрансфераза, лактатдегидрогеназа, щелочная фосфатаза) и почек (креатинин, мочевина, скорость клубочковой фильтрации (СКФ)) и клинического анализа крови не показал существенных различий в течение периода наблюдения.
Нежелательное явление (НЯ) за весь период наблюдения было зарегистрировано у 1 (4,5%) из 22 пациентов. Это была умеренная реакция в виде гиперемии кожи в месте инъекции после первого введения препарата, при его повторном назначении на 3-й месяц у этого же пациента подобной реакции не наблюдали. Данное НЯ разрешилось самостоятельно в течение 2 ч.
Особые группы клинического наблюдения
Среди особых клинических случаев наблюдения следует отметить результаты терапии инклисираном у пациентов с трансплантированным сердцем и у пациентов с ГеСГХС, а также его влияние на уровень ЛП(а) в сыворотке крови.
Пациенты с трансплантированным сердцем
Особого внимания в проведенном анализе заслуживают 2 случая интенсификации гиполипидемической терапии посредством назначения инклисирана у пациентов в отдаленном периоде после трансплантации сердца. Эффективность данной стратегии была оправдана как с позиций эффективности, так и с позиций безопасности, обеспечив снижение уровня ХС ЛПНП к 4-му месяцу наблюдения более 50% от исходного уровня в обоих клинических наблюдениях (табл. 2).
Так, один из пациентов, мужчина 65 лет с трансплантацией сердца (2011 г.) по поводу ИБС, с указаниями на ОНМК по ишемическому типу (2008 г.), ХБП С3б ст. смешанной этиологии (атеросклероз и применение ингибиторов кальциневрина) и рядом тяжелых сопутствующих состояний, повышающих ССР до очень высокого уровня, исходно и более 10 лет получал терапию средней дозой аторвастатина — 20 мг (по причине непереносимости высокоинтенсивной дозы) в комбинации с эзетимибом 10 мг, при этом имея нецелевой для своей категории ССР (<1,4 ммоль/л) уровень ХС ЛПНП в крови, который на момент обращения составил 2,52 ммоль/л. При дообследовании данных в пользу СГХС получено не было. Необходимость назначения PCSK9 таргетной терапии не вызывала сомнения. К 4-му месяцу терапии инклисираном у этого пациента достигнуто снижение уровня ХС ЛПНП на 61%, которое составило в абсолютных значениях 0,97 ммоль/л. Клинических и лабораторных данных в пользу развития НЯ у этого пациента получено не было.
Второй пациент — мужчина 52 лет с трансплантацией сердца (октябрь 2022 г.) по поводу ИБС, с указаниями на перенесенный трансмуральный ИМ передней стенки левого желудочка трансплантированного сердца (октябрь 2022 г.), с нефропатией смешанного генеза и ХБП С5, получающий в связи с этим программный гемодиализ, а также страдающий рядом тяжелых сопутствующих состояний, повышающих его ССР до экстремального уровня. Данный пациент исходно и более 2 лет получал монотерапию средней дозой аторвастатина — 20 мг (по причине непереносимости высокоинтенсивной дозы статина и эзетимиба), при этом имея нецелевой для своей категории ССР (<1,0 ммоль/л) уровень ХС ЛПНП в крови, который на момент обращения составил 5,58 ммоль/л. При дообследовании данных в пользу СГХС получено не было. Необходимость назначения PCSK9 таргетной терапии не вызывала сомнения. На фоне терапии инклисираном у этого пациента достигнуто снижение уровня ХС ЛПНП на 64%, что составило в абсолютных значениях 2,01 ммоль/л и стало для него историческим минимумом. Клинических и лабораторных данных в пользу развития НЯ у этого пациента получено не было.
Пациенты с геСГХС
Эффективность терапии инклисираном у пациентов с ГеСГХС по сравнению с обследованными без доказанных мутаций генов липидного обмена была сопоставимой и значимо не различалась, приводя к 4-му месяцу лечения к снижению уровня ХС ЛПНП на 60,6 и 58,8% соответственно (р>0,05).
Влияние инклисирана на уровень ЛП(а) в сыворотке крови
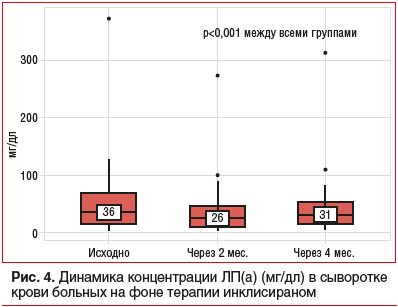
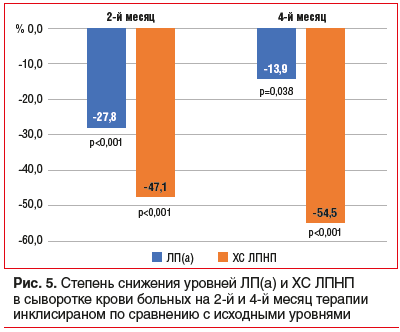
Содержание ЛП(а) было проанализировано у всех пациентов исходно и в динамике, у всех больных оно снизилось ко 2-му месяцу терапии инклисираном на 27,8% (р<0,001), а при исследовании его содержания через 1 мес. после второй инъекции (4-й месяц) было чуть менее существенным, но также статистически значимым — 13,9% (р=0,038) (рис. 4, 5).
Обсуждение
Недостаточные клиническая эффективность и приверженность лечению, а также частые дозозависимые побочные эффекты статинов представляют собой основные ограничения при лечении больных с атерогенными дислипидемиями в реальной клинической практике [5]. Около 50% пациентов прекращают терапию статинами менее чем через 1 год от ее начала [15]. Другие гиполипидемические средства, разрешенные для использования в России, такие как эзетимиб и омега-3-полиненасыщенные жирные кислоты, являются дополнением к основной терапии статинами, однако в ряде случаев применяются в качестве единственных средств1. Такие препараты для лечения атерогенных дислипидемий, как бемпедоевая кислота, секвестранты желчных кислот, ингибиторы микросомального триглицерид-переносящего белка (ломитапид), антисмысловые олигонуклеотиды к протеину апоВ-100 (мипомерсен), в нашей стране не зарегистрированы [2, 4, 5]. Появление в России моноклональных антител к PCSK9 расширило возможности терапии таких пациентов. Несмотря на свою эффективность, препараты данной группы малодоступны вследствие высокой стоимости, особенностей хранения и транспортировки, строгих критериев приемлемости для их использования во многих странах [16]. Регистрация препарата инклисиран в России дает возможность более широкого выбора препаратов для управления дислипидемией — не только для тех пациентов, которые имели непереносимость или ограничения к использованию гуманизированных моноклональных антител к PCSK9, но и для первичного назначения в составе комбинированной терапии со статинами и/или эзетимибом, а также в случаях непереносимости статинов у пациентов с ССР. Кроме того, пациенты могут учитывать экономическую составляющую лечения этим классом препаратов1.
Результаты проведенного нами исследования позволили оценить опыт применения препарата инклисиран у пациентов с дислипидемией с целью первичной и вторичной профилактики ССЗ в условиях реальной клинической практики, назначенного на основании отечественных клинических рекомендаций. Продолжительность периода наблюдения за когортой пациентов была ограничена применением первых двух доз инклисирана в соответствии с инструкцией к препарату, по которой пациенты будут продолжать лечение и далее в режиме 1 раз в 6 мес. Установлено, что двукратная подкожная инъекция инклисирана к 4-му месяцу лечения снижает уровень ХС ЛПНП на 54,5% [9, 11]. Снижение уровня ХС ЛПНП более 50% от исходного не зависело от пола, однако у женщин было более существенным, чем у мужчин, что в нашем наблюдении может объясняться лучшей переносимостью и более высокой частотой назначения высокоинтенсивной терапии статинами женщинам, чем мужчинам, из-за непереносимости ими высоких доз статинов. Общие результаты и закономерности, полученные в настоящем исследовании, согласуются с данными исследований ORION-10 и ORION-11, которые показали снижение среднего уровня ХС ЛПНП примерно на 50% [8, 9].
Кроме того, в нашей работе значимо более выраженное снижение уровня ХС ЛПНП было достигнуто пациентами при назначении инклисирана в дополнение к высокоинтенсивной терапии статинами, что подчеркивает патогенетическую важность сочетания двух стратегий для обеспечения биологического синергизма: снижение концентрации свободного PCSK9, повышающего концентрацию рецепторов ЛПНП, с терапией, повышающей транскрипцию рецептора ЛПНП и сопровождающейся ингибированием ферментативного синтеза эндогенного ХС в печени, при этом общий эффект заключается в увеличении клиренса циркулирующего ХС ЛПНП [5, 6]. Как показали ранее проведенные исследования, сочетание ингибиторов PCSK9 с высокоинтенсивной терапией статинами может привести к снижению уровня ХС ЛПНП до 75–80%1 [9]. Поэтому необходимо подчеркнуть высокую клиническую значимость поддержания приверженности лечению и продолжения приема пациентами исходной гиполипидемической терапии. В нашем исследовании все пациенты сохранили высокую комплаентность на протяжении всего периода исследования, однако 36,4% обследованных имели непереносимость только высоких доз статинов, а 13,6% — абсолютную непереносимость, что согласуется с более ранними исследованиями [17]. Для многих пациентов инъекция инклисирана 2 раза в год является более удобным и менее обременительным вариантом лечения, который может способствовать соблюдению режима и в целом добиться большего снижения уровня ХС ЛПНП в будущем [6]. Одобрение инклисирана для применения в учреждениях амбулаторной медицинской помощи в совокупности может привести к увеличению числа пациентов, достигающих сложных терапевтических целей.
К 4-му месяцу лечения инклисираном достигнуто снижение уровня ОХС, ХС неЛПВП, ТГ и ЛП(а). Об этой тенденции на протяжении всего периода наблюдения сообщалось при анализе вторичных конечных точек в исследованиях ORION-10 и ORION-11 [8, 9]. Сходство этих результатов свидетельствует об их воспроизводимости в реальных клинических условиях.
Нежелательное явление — гиперемия в месте инъекции, вероятность развития которой была связана с назначением инклисирана, возникла у 1 пациента, не соответствовала критериям серьезности и не требовала отмены препарата. В исследованиях ORION-3, -9, -10 и -11 частота возникновения реакций в месте инъекции варьировала от 3 до 17% [7–9, 18]. В исследовании U. Makhmudova et al. [19], объединившем результаты работы 14 липидных клиник Германии в рамках программы The German Inclisiran Network, умеренную реакцию в месте инъекции наблюдали в 3% случаев, серьезных НЯ зарегистрировано не было. Возможно, что невысокая частота подобного явления связана с тем, что пациенты сообщают не обо всех легких реакциях в месте инъекции. Ни один пациент в представленном исследовании не прекратил лечение после назначения 2 доз инклисирана, что способствует высокой эффективности лечения. В крупных рандомизированных клинических исследованиях и отдельных наблюдательных исследованиях [7, 8, 18] подтвержден благоприятный профиль безопасности инклисирана.
Следует отметить высокую эффективность инклисирана у пациентов с ГеСГХС, что согласуется с результатами исследования ORION-9 [7].
Уникальными данными, полученными в ходе исследования, следует считать наблюдение за пациентами, получившими инклисиран в отдаленном периоде после трансплантации сердца, наблюдения за которыми ранее в литературе описаны не были. Согласно действующим рекомендациям Международного сообщества трансплантации сердца и легких (The International Society of Heart and Lung Transplantation, ISHLT) от 2010 г. всем пациентам после трансплантации сердца вне зависимости от их пола и возраста рекомендовано пожизненное добавление гиполипидемической терапии из-за высокого риска развития болезни коронарных сосудов пересаженного сердца, развития и/или прогрессии атеросклероза периферических сосудов [20]. Гиполипидемическая терапия также снижает риск развития криза отторжения сердечного трансплантата. Первой линией терапии являются статины в редуцированных дозах из-за высокого риска миопатии и миозита, а также почечной и/или печеночной дисфункции [20]. Ко второй линии гиполипидемической терапии у реципиентов сердца относятся следующие препараты: эзетимиб — для коррекции повышения уровня ХС ЛПНП, фенофибрат и омега-3 полиненасыщенные жирные кислоты — для коррекции гипертриглицеридемии [20].
В 2019 г. Европейское общество кардиологов (European Society of Cardiology, ESC) совместно с Европейским обществом атеросклероза (European Atherosclerosis Society, EAS) опубликовало клинические рекомендации по ведению дислипидемии, согласно которым статины являются первой линией терапии для всех пациентов с трансплантатами и должны быть инициированы в минимальных дозах (класс рекомендаций IIa, уровень доказательности B) [5]. Дальнейшая титрация препарата должна проводиться с осторожностью и с учетом лекарственных взаимодействий (в том числе под контролем концентрации в крови ингибиторов кальциневрина) [20]. В случае непереносимости статинов или их неэффективности при максимально переносимой дозе в качестве альтернативы или второй линии терапии рекомендовано применение эзетимиба [5]. Согласно рекомендациям при развитии гипертриглицерид-емии у таких пациентов показано применение фенофибрата в дополнение к терапии статинами (класс рекомендаций IIb, уровень доказательности B) [5]. Опубликованы оригинальные статьи и клинические случаи в журналах Q1, показывающие эффективность ингибиторов PCSK9 в схеме гиполипидемической терапии у пациентов с трансплантатами [21, 22]. Однако необходимы контроль иммуносупрессивной терапии, оценка почечной и печеночной функций и маркеров воспаления в динамике на фоне проводимой терапии. Тяжелая почечная дисфункция со снижением СКФ <30 мл/мин/1,73 м2 и наличие выраженной ангиоэдемы затрудняют применение ингибиторов PCSK9 в данном случае ввиду недостаточности данных [20].
Рекомендации по кардиоваскулярной профилактике (2023 г.), созданные совместно Российским кардиологическим обществом, Национальным обществом профилактической кардиологии и Российским обществом профилактики неинфекционных заболеваний, включили в группу высокого риска развития дислипидемии пациентов после трансплантации почек и сердца [3].
Согласно действующим Национальным клиническим рекомендациям «Трансплантация сердца, наличие трансплантированного сердца, отмирание и отторжение трансплантата сердца» от 2021 г.:
взрослым реципиентам сердца, независимо от уровней холестерина, рекомендовано назначение средств из группы ГМГ-КоА-редуктазы (статинов) (уровень убедительности А, уровень достоверности доказательств 2).
Рекомендовано назначать начальные дозы статинов ниже, чем рекомендуемые для профилактики нежелательных событий в общей популяции, в связи с учетом особенностей лекарственного взаимодействия (уровень убедительности А, уровень достоверности доказательств 2).
Ингибиторы ГМГ-КоА-редуктазы рекомендованы детям и подросткам с высоким риском развития болезни коронарных артерий сердечного трансплантата (БКАПС) (уровень убедительности В, уровень достоверности доказательств 3).
Пациентам после трансплантации сердца рекомендован прием статинов в связи с тем, что он снижает риск развития БКАПС и улучшает выживаемость без нежелательных событий, включая снижение риска развития злокачественных новообразований и улучшение общей выживаемости (уровень убедительности А, уровень достоверности доказательств 2).
Инклисиран не является субстратом, ингибитором или индуктором ферментов цитохрома Р450 (CYP450), поэтому не ожидается, что этот препарат будет иметь значимые клинические взаимодействия с другими лекарственными препаратами, в том числе с иммуносупрессорами [6, 7]. Ключевой причиной целесообразности использования инклисирана являются опубликованные данные исследований ORION-7 и ORION-1, в которых было продемонстрировано эффективное и безопасное в краткосрочном наблюдении применение препарата у пациентов с тяжелой ХБП со снижением СКФ <30 мл/мин/1,73 м2 [18, 23].
Вместе с тем проведенное исследование имеет ряд ограничений. Во-первых, результаты представляют опыт липидной клиники только одного центра. Во-вторых, размер представленной выборки небольшой, поэтому и частота побочных эффектов может не соответствовать ранее известной. Также малый размер выборки не позволяет перенести полученные результаты на уровень популяции. Кроме того, небольшой период наблюдения ограничивает оценку эффективности препарата и не позволяет дождаться терапевтического пика эффекта инклисирана. Для оценки долгосрочной эффективности и устойчивости благоприятных эффектов инклисирана необходимы более длительные наблюдения и исследования.
Выводы
Двукратное назначение инклисирана в дополнение к стандартной комбинированной гиполипидемической терапии пациентам умеренного, высокого, очень высокого и экстремального ССР эффективно, безопасно и позволяет снизить уровень ХС ЛПНП более чем на 50% от исходных значений, с высокой частотой достижения целевых уровней в рамках как вторичной, так и первичной профилактики ССО.
Двукратное назначение инклисирана при доказанной абсолютной непереносимости статинов у пациентов, находящихся на монотерапии эзетимибом, показало высокую эффективность и безопасность — среднее снижение уровня ХС ЛПНП отмечали на уровне 45,3%.
Инклисиран эффективен и безопасен для пациентов с ГеСГХС, что сопоставимо с пациентами без данного нарушения.
Инклисиран в стандартной дозе был эффективен и безопасен у пациента, получающего программный гемодиализ на фоне терминальной ХБП.
Инклисиран эффективен и безопасен для коррекции дислипидемии у пациентов в отдаленном периоде после трансплантации сердца.
Отмечены дополнительные клинически значимые эффекты инклисирана — снижение концентраций ЛП(а) и ТГ сыворотки крови.
Информация с rmj.ru