Введение
Численность больных сахарным диабетом (СД) в мире за последние 10 лет увеличилась более чем в 2 раза и к концу 2019 г. превысила 463 млн человек. Согласно прогнозам Международной диабетической федерации к 2030 г. СД будет страдать 578 млн человек, а к 2045 г. — 700 млн человек [1].
В РФ на 01.01.2023 на диспансерном учете состояло 4 962 762 человека (3,31% населения РФ), из них с СД 1 типа (СД1) — 5,58% (277,1 тыс.), с СД 2 типа (СД2) — 92,33% (4,58 млн), с другими типами СД — 2,08% (103 тыс.) [2].
Результаты первого национального эпидемиологического кросс-секционного исследования NATION, проведенного в 2013–2015 гг., продемонстрировали, что «реальная распространенность СД2 среди населения оказалась в 2 раза выше и составила 5,4%, причем у 54% СД был ранее не диагностирован» [3]. Таким образом, реальная численность пациентов с СД в РФ составляет не менее 10 млн человек (около 7% населения). Неуклонные темпы роста распространенности СД2 представляют чрезвычайную угрозу [4].
Сахарный диабет 2 типа является не только глобальной медицинской, но и экономической проблемой для РФ. Большую часть затрат (53,5%), связанных с СД2, составляют потери валового внутреннего продукта вследствие нетрудоспособности больных СД. Прямые медицинские затраты составляют 37,7% общей стоимости болезни, из которых 57% приходится на лечение осложнений СД и сопутствующих заболеваний, тогда как на долю сахароснижающей терапии — всего 10% [5]. Современные подходы к ведению пациентов с СД2
С момента установления диагноза уже на первом этапе лечения СД2, помимо соблюдения диеты и физической активности, пациентам необходимо назначение медикаментозной сахароснижающей терапии. С этой целью на протяжении многих десятилетий для лечения СД2 применялись «классические» пероральные сахароснижающие препараты (ССП) — метформин и препараты из группы производных сульфонилмочевины (ПСМ).
Метформин неизменно остается лекарственным средством, относящимся к стартовой терапии СД2, что обосновано имеющейся доказательной базой, свидетельствующей в пользу его эффективности и безопасности, включая низкий риск гипогликемии на фоне выраженного сахароснижающего эффекта, нейтральность по отношению к массе тела и наличие плейотропных эффектов. Своевременное назначение данного препарата позволяет достоверно снизить риск развития микро- и макрососудистых осложнений заболевания [6].
Препараты ПСМ позволяют достаточно быстро достигать целевых уровней гликемии у пациентов с СД2 за счет их прямого стимулирующего действия на β-клетки поджелудочной железы, приводящего к высвобождению запасов инсулина из внутриклеточных гранул и выбросу инсулина в кровь. Низкая стоимость ПСМ, а также отсутствие альтернативных ССП в течение долгих лет определяли их доминирующее положение в терапии СД2. По данным фармакоэпидемиологического анализа, в 2015 г. в Москве лечение ПСМ получали 87% пациентов с СД2 [7]. Важно учитывать, что по сравнению с другими группами неинсулиновых ССП применение ПСМ ассоциировано с более высоким риском развития гипогликемических состояний. Другим существенным недостатком ПСМ является тот факт, что постоянная стимуляция β-клеток у пациентов с СД2, имеющих уже на момент дебюта заболевания их сниженную секреторную активность, приводит к более раннему истощению β-клеток. Медикаментозно вызываемая при применении ПСМ постоянная гиперинсулинемия способствует усилению периферической инсулинорезистентности — ведущего механизма развития СД2 [8].
В течение двух последних десятилетий были достигнуты существенные успехи в оказании специализированной медицинской помощи пациентам с СД2 благодаря внедрению в клиническую практику новых классов ССП, включая ингибиторы дипептилпептидазы 4-го типа (иДПП-4). В то же время, по данным Федерального регистра сахарного диабета, большинство пациентов с СД2 продолжает получать препараты более традиционных классов, даже при наличии высокого сердечно-сосудистого риска [9].
Действие препаратов, относящихся к группе иДПП-4, основано на инсулинзависимой модуляции выработки инсулина и глюкагона. Их применение характеризуется высоким профилем безопасности, включая крайне низкий риск развития гипогликемических состояний у пациентов с СД2. Проведенные исследования, посвященные оценке влияния различных представителей класса иДПП-4 на показатели гликемии, продемонстрировали их высокую эффективность у различных категорий пациентов, включая лиц с ожирением, наличием диабетической нефропатии и среди пациентов пожилого возраста [10, 11].
Для анализа эффективности и безопасности применения современных ССП в реальную клиническую практику активно внедряются технологии непрерывного мониторинга уровня глюкозы (НМГ), которые позволяют более подробно оценить колебания уровня глюкозы (оценивается уровень глюкозы в межклеточной жидкости) в течение заданного временного диапазона (обычно не менее 14 дней). При этом устанавливаемый на кожу датчик получает информацию об уровне глюкозы каждые 1–5 мин. В связи с внедрением данных технологий появились и новые подходы к оценке качества контроля гликемии: время в целевом диапазоне (time-in-range, TIR), а также время в диапазонах выше и ниже целевого, которое выражается в процентах (24 ч в сутках принимаются за 100%). Кроме того, данные технологии позволяют оценить вариабельность гликемии, а также частоту, глубину и продолжительность гипогликемических состояний, развивающихся в течение периода наблюдения, которые могут быть не зафиксированы самим пациентом. Практическая значимость оценки вариабельности гликемии обусловлена тем, что данный показатель ассоциирован как с риском развития гипогликемических состояний, так и с риском развития микро- и макрососудистых осложнений СД.
Вызывает определенный интерес использование НМГ для изучения особенностей гликемического контроля у пациентов, получающих терапию пероральными ССП различных классов. Представляется интересным оценить показатели вариабельности гликемии, а также частоту и глубину гипогликемических состояний, возникающих у пациентов, получающих препараты ПСМ, а также возможности по улучшению данных показателей при переводе данных пациентов на терапию иДПП-4.
С 2020 г. в России появился новый представитель класса иДПП-4 — эвоглиптин (Эводин® производства ООО «ГЕРОФАРМ», Россия). Данный препарат продемонстрировал высокую эффективность и безопасность в терапии больных СД2 [12]. В частности, в сравнительном исследовании ЭВОКОМБИ были продемонстрированы не меньшая эффективность и безопасность, чем у ситаглиптина, при добавлении к монотерапии метформином в русско-корейской популяции пациентов [13]. В настоящее время препарат активно внедряется в клиническую практику, что и стало основанием для проведения данного пилотного исследования.
Собственный опыт применения иДПП-4 эвоглиптина
Набор пациентов проводился на базе клиники эндокринологии ФГАОУ ВО Первый Московский государственный медицинский университет им. И.М. Сеченова Минздрава России (Сеченовский Университет) и на базе эндокринологического отделения ГБУЗКО «Калужская областная клиническая больница» с октября 2022 г. по март 2023 г.
Межвузовский комитет по этике постановил, что рассматриваемая работа соответствует требованиям этических стандартов (протокол № 14–22 от 07.07.2022).
В данной работе мы представляем собственный опыт применения иДПП-4 эвоглиптина (Эводин®) и оценку его влияния на показатели вариабельности уровня глюкозы и времени в целевом диапазоне, а также безопасности в отношении риска развития гипогликемических состояний по сравнению с препаратами из группы ПСМ у пациентов с СД2 в условиях реальной клинической практики.
Под наблюдением находились пациенты мужского и женского пола в возрасте от 18 до 80 лет с СД2, получающие ПСМ в среднетерапевтических или максимальных дозировках в комбинации с метформином; нуждаюшиеся в терапии эвоглиптином в рамках рутинной клинической практики, имеющие уровень НbАс1 от 6,0–7,5% и не имеющие признаков тяжелых гематологических, иммунологических, дыхательных, урогенитальных, желудочно-кишечных, печеночных, почечных, эндокринных, метаболических, обменных, психиатрических, дерматовенерологических заболеваний, нарушения питания, коллагенозов, скелетно-мышечных, злокачественных и подобных заболеваний, аллергии или операции, о которых известно из анамнеза, по результатам физикального осмотра и/или лабораторных анализов, а также не имеющие тяжелых когнитивных нарушений, в том числе тяжелой энцефалопатии с явлениями деменции, пациенты, не злоупотребляющие алкоголем, беременные женщины.
Наблюдение осуществлялось при амбулаторном приеме пациентов. Специальных процедур, выходящих за рамки стандартов лечения и рутинной клинической практики, за исключением сбора данных на каждого участника программы с помощью индивидуальной регистрационной карты (ИРК), не проводилось. Все лечебные и диагностические процедуры, включая проведение НМГ, выполнялись только в соответствии с обычной практикой, стандартами лечения и одобренными инструкциями по применению.
В ходе наблюдения пациенты должны были посещать своего врача в соответствии с собственным планом лечения. Результаты обследований после 2, 6 и 8 нед. наблюдения регистрировались в специально разработанной ИРК.
Общая продолжительность наблюдения 1 пациента составила около 8 нед. Оценка состояния пациента проводилась в ходе 3 очных визитов к лечащему врачу и включала анализ первичной медицинской документации (амбулаторная карта пациента, выписные эпикризы из историй болезни, оценка состояния компенсации углеводного обмена (HbA1c, гликемический профиль)), общий осмотр, в том числе измерение массы тела и роста пациента, объема талии, анализ проводимой терапии СПП, проведение флеш-мониторинга «Фристайл Либре», смену проводимой терапии ССП.
Вариабельность гликемии, время в целевом диапазоне, частота и продолжительность гипогликемических состояний оценивались с помощью использования НМГ (флеш-мониторинг «Фристайл Либре»).
Наблюдение пациентов осуществляли по следующему графику:
В начале наблюдения пациенту выдавали датчик «Фристайл Либре», проводили его установку и обучали пациента использованию НМГ.
-
Через 2 нед. проводили осмотр пациента, собирали анамнез за прошедшие 2 нед., отменяли ПСМ и назначали эвоглиптин, давали рекомендации о следующем визите через 4 нед.
-
Через 6 нед. от начала наблюдения проводили осмотр пациента, собирали анамнез за прошедшие 4 нед. Пациенту выдавали датчик «Фристайл Либре», проводили его установку.
-
Через 8 нед. от начала наблюдения также проводили осмотр пациента, собирали анамнез за прошедшие 2 нед.
Результаты наблюдения
Под наблюдением находились 7 пациентов с СД2 (1 мужчина и 6 женщин).
Все пациенты на момент начала наблюдения получали комбинированную терапию с использованием двух классов ССП: метформина и препарата сульфонилмочевины. Доза метформина у 5 пациентов составляла 2000 мг/сут, 1 пациент получал метформин в дозе 1500 мг/сут и еще 1 — в дозе 1700 мг/сут. В качестве ПСМ чаще всего использовался гликлазид МВ (4 пациента в дозе 60 мг/сут и 1 — в дозе 30 мг/сут), 1 пациент получал глимепирид в дозе 2 мг/сут и 1 — глибенкламид в дозе 7,5 мг/сут.
Общая характеристика пациентов на момент взятия под наблюдение отражена в таблице 1.
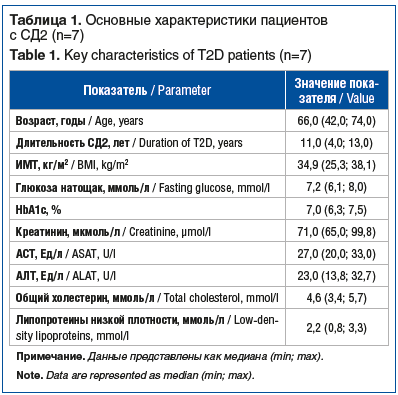
Чаще всего пациентам устанавливался целевой уровень НbА1с 7,5% (n=3). Целевой уровень НbА1с 7,5 и 6,5% был установлен у 2 пациентов. При этом на момент включения 4 пациента находились в целевом диапазоне по уровню НbА1с, 3 пациента имели уровень НbА1с выше целевого. Таким образом, если оценивать качество проводимой сахароснижающей терапии только на основании достижения уровня НbА1с, 4 (57,1%) из 7 пациентов демонстрировали высокую эффективность получаемой терапии ССП на этапе взятия под наблюдение.
Оценка качества гликемического контроля с позиции безопасности в отношении гипогликемических состояний, базирующаяся на опросах пациентов, продемонстрировала, что пациенты в период получения ПСМ изредка отмечали легкие гипогликемии (табл. 2). Тяжелых гипогликемий зарегистрировано не было.

Основные параметры качества гликемического контроля и безопасности в отношении гипогликемических состояний на фоне терапии с использованием ПСМ и после перевода на терапию иДПП-4 были также оценены с помощью НМГ.
Результаты проведенного мониторинга продемонстрированы в таблице 3.
По результатам статистического анализа с использованием инструментов непараметрической статистики для зависимых выборок (критерий Уилкоксона) не выявлено статистически значимых различий по основным сравниваемым показателям (см. табл. 3), что, вероятнее всего, связано с небольшим объемом выборки (n=7).
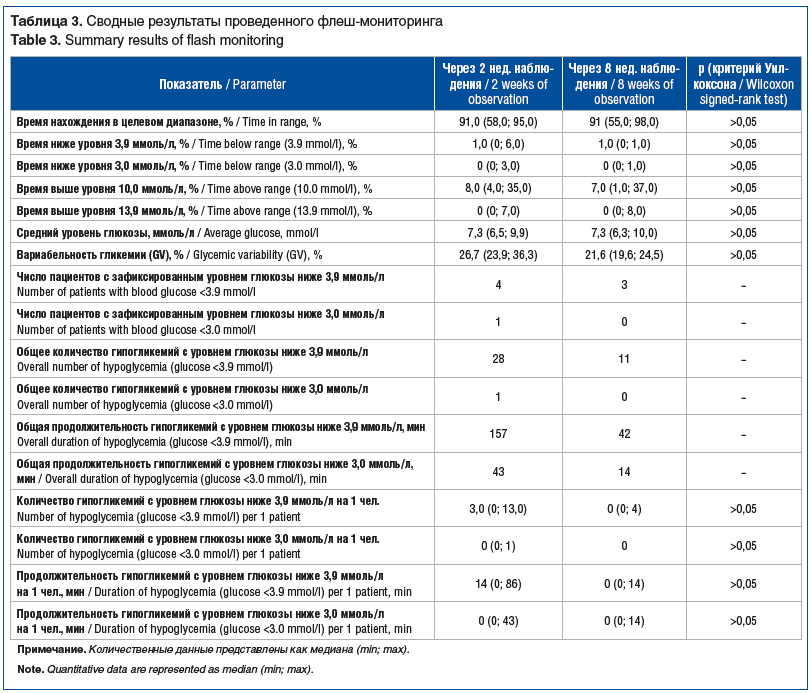
Однако отмечается выраженная тенденция снижения общего числа зафиксированных с помощью НМГ гипогликемических состояний с 28 до 11, суммарного показателя времени, проведенного в диапазоне ниже 3,9 ммоль/л, со 157 до 42 мин, и времени, проведенного в диапазоне ниже 3,0 ммоль/л, с 43 до 14 мин.
Содержание статьи
Клиническое наблюдение
Пациентка Р., 74 года, поступила в клинику эндокринологии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет) с диагнозом: сахарный диабет 2 типа. Диабетическая микроангиопатия: непролиферативная ретинопатия OU. Диабетическая нейропатия, дистальный тип, сенсорная симметричная форма. Гипертоническая болезнь III стадии, 2-й степени, риск 4. ОНМК от 2018 г. Экзогенно-конституциональное ожирение I стадии. Дислипидемия. Целевой уровень гликированного гемоглобина <8%.
При поступлении пациентка предъявляла жалобы на общую слабость, сухость во рту, эпизоды повышения гликемии натощак до 8 ммоль/л, в течение дня до 10 ммоль/л, снижение остроты зрения, боли в коленных и тазобедренных суставах, повышение АД до 170/90 мм рт. ст.
В 2016 г. (68 лет) при плановом обследовании выявлена гликемия натощак 23 ммоль/л, диагностирован СД2, назначена базис-болюсная инсулинотерапия (название препаратов и дозы не помнит). В 2018 г. пациентка переведена на прием гликлазида МВ 60 мг, метформина 1000 мг/сут. В 2021 г. доза метформина была увеличена до 2000 мг, на этом фоне гликемия в течение дня до 8 ммоль/л. В октябре 2022 г. у пациентки выявлена непролиферативная диабетическая ретинопатия. При оценке функционального состояния почек от 2023 г.: СКФ 53,5 мл/мин, альбумин-креатиновое соотношение в утренней порции мочи 1,5 мг/моль, что соответствует диабетической нефропатии, хроническая болезнь почек С3аА1. В 2017 г. у пациентки диагностирована диабетическая полинейропатия, дистальный тип, сенсорная симметричная форма.
Данные НМГ с 02.11.2022 по 15.11.2022 (на фоне приема метформина 1000 мг 2 р/сут, гликлазида МВ 60 мг утром): время нахождения датчика в активном состоянии 99%, средний уровень глюкозы 6,5 ммоль/л, вариабельность глюкозы (коэффициент вариации) — 36,3% (цель <36%), среднее время нахождения в целевом диапазоне 3,9–10,0 ммоль/л (82%), время в диапазоне >10 ммоль/л (9%), в диапазоне <3,9 ммоль/л (6%), <3 ммоль/л (3%) (рис. 1). На основании полученных данных выявлено 13 эпизодов гипогликемии (преимущественно в ночное время и редкие гипогликемии около 16–18 ч), средняя длительность гипогликемий 107 мин.
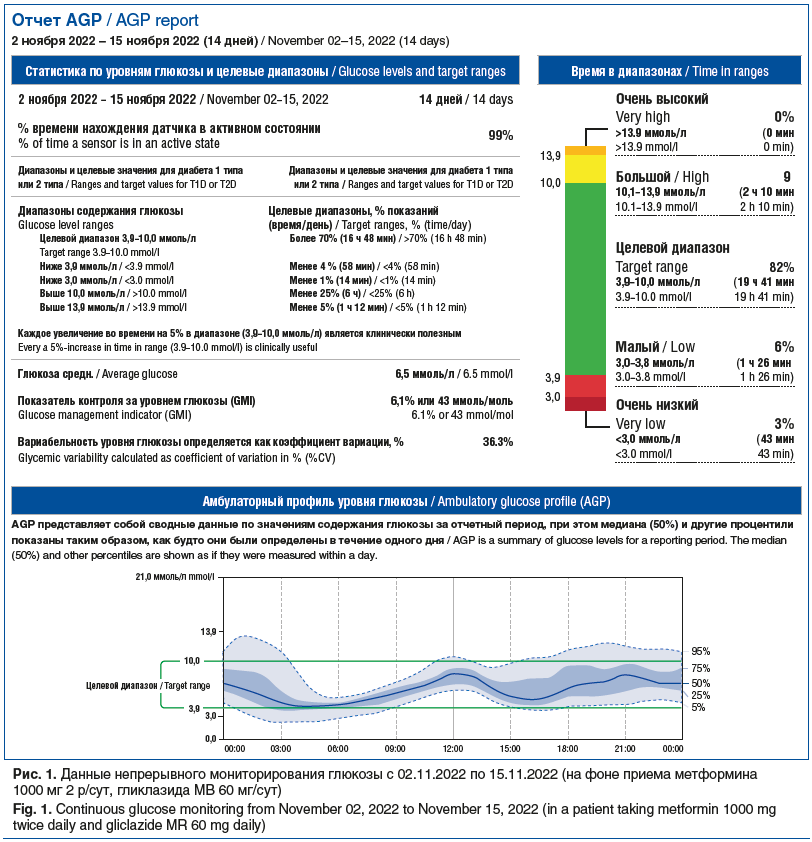
С 15.11.2022 пациентка была переведена на прием эвоглиптина 5 мг, метформина 1000 мг 2 р/сут. Данные НМГ с 13.12.2022 по 26.12.2022: время нахождения датчика в активном состоянии 99%, средний уровень глюкозы 7,3 ммоль/л, коэффициент вариации 22,4%, среднее время нахождения в целевом диапазоне 3,9–10,0 ммоль/л (92%), время нахождения в диапазоне >10 ммоль/л (7%), в диапазоне <3,9 ммоль/л (1%), <3 ммоль/л (0%) (рис. 2).
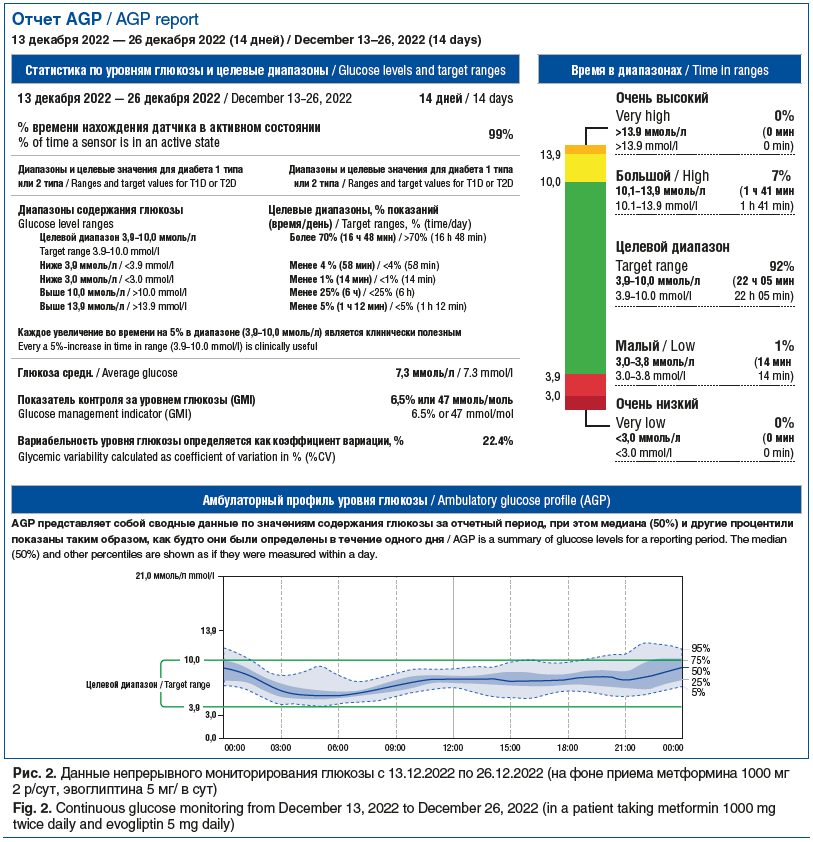
На основании данных НМГ выявлено 3 эпизода снижения глюкозы <3,9 ммоль/л в ночное и раннее утреннее время, средняя длительность гипогликемий 83 мин. Гипогликемических состояний с уровнем <3 ммоль/л выявлено не было.
Таким образом, у пациентки пожилого возраста с отягощенным сердечно-сосудистым анамнезом, при сопоставимом расчетном значении НbА1с (6,1% исходно против 6,5% по окончании наблюдения) на фоне проведенной коррекции сахароснижающей терапии достигнуто снижение частоты и длительности гипогликемий; увеличение времени пребывания в целевом диапазоне глюкозы, снижение вариабельности уровня глюкозы.
Обсуждение
Согласно действующим алгоритмам, регламентирующим подходы к мониторингу пациентов с СД2, ключевым инструментом для оценки качества гликемического контроля до настоящего времени является уровень НbА1с. Между тем широкое использование в терапии таких пациентов ряда препаратов, увеличивающих риск гипогликемии (препараты инсулина, ПСМ), предполагает необходимость использования и других инструментов оценки качества гликемического контроля. Результаты проведенной нами работы наглядно демонстрируют, что нахождение НbА1с в целевом диапазоне и отсутствие репортируемых пациентом гипогликемических состояний вовсе не является гарантией безопасности проводимой терапии, так как пациент может иметь бессимптомные гипогликемические состояния, значимо увеличивающие риск сердечно-сосудистых катастроф.
Высокая стоимость и, как следствие, низкая доступность флеш-мониторинга не позволяют сделать его рутинным методом оценки качества гликемического контроля у больных СД2 вследствие крайне высокой распространенности данного заболевания.
Одним из подходов, способных существенно снизить риск гипогликемических состояний у пациентов с СД2 (в том числе бессимптомным), может быть постепенный отказ от использования ПСМ в пользу ССП, не вызывающих гипогликемий, к которым относятся инновационные препараты, включая иДПП-4 [14]. Единственным существенным фактором, определяющим широкое использование ПСМ в настоящее время, является их низкая стоимость. Таким образом, перспективу повышения безопасности терапии ССП определяет появление на российском фармацевтическом рынке препаратов, сопоставимых по сахароснижающей активности с ПСМ, но безопасных в отношении гипогликемических состояний. Именно возможность использования подобного подхода к терапии СД2 была изучена в нашей работе.
Выводы
-
Пациенты, использующие в терапии СД2 препараты ПСМ, имеют более высокую вероятность гипогликемических состояний с неярко выраженной клинической симптоматикой либо без таковой.
-
Перевод пациентов, получавших терапию ПСМ, на препараты из группы иДПП-4 может быть ассоциирован со снижением частоты и продолжительности гипогликемий.
-
При переводе пациентов, получавших терапию ПСМ, на препараты из группы иДПП-4 была продемонстрирована тенденция к снижению показателей вариабельности гликемии.
-
Появление на российском рынке современных, доступных препаратов из группы иДПП-4 отечественного производства (в частности, эвоглиптина), может стать фактором, способным существенно повлиять на безопасность терапии СД2 в отношении рисков развития гипогликемических состояний и снижения риска развития сердечно-сосудистых осложнений.
Данный проект был проведен в качестве пилотного, полученные результаты требуют дальнейшего подтверждения в более масштабных исследованиях.
Сведения об авторах:
Калашникова Марина Федоровна — д.м.н., профессор кафедры эндокринологии № 1 института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0002-7924-8687.
Лиходей Наталья Вячеславовна — врач-эндокринолог клиники эндокринологии им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0002-4680-0746.
Малолеткина Екатерина Станиславовна — к.м.н., врач-эндокринолог клиники эндокринологии, ассистент кафедры эндокринологии № 1 института клинической медицины им. Н.В. Склифосовского Первого МГМУ им. И.М. Сеченова (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-9881-5459.
Теплов Евгений Викторович — заведующий отделением эндокринологии ГБУЗКО «Калужская областная клиническая больница»; 248007, Россия, г. Калуга, ул. Вишневского, д. 1; ORCID iD 0000-0000-0000-0000.
Вавильченкова Кристина Сергеевна — врач-эндокринолог поликлинического отделения ГБУЗКО «Калужская областная клиническая больница»; 248007, Россия, г. Калуга, ул. Вишневского, д. 1; ORCID iD 0000-0000-0000-0000.
Глинкина Ирина Владимировна — к.м.н., доцент кафедры эндокринологии №1 института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-8505-5526.
Контактная информация: Калашникова Марина Федоровна, e-mail: marina_kalash@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 31.07.2023.
Поступила после рецензирования 21.08.2023.
Принята в печать 11.09.2023.
About the authors:
Marina F. Kalashnikova — Dr. Sc. (Med.), professor of the Department of Endocrinology No. 1, N.V. Sklifosovskiy Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0002-7924-8687.
Natalia V. Likhodey — endocrinologist of the Clinics of Endocrinology of the N.V. Sklifosovskiy Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0002-4680-0746.
Ekaterina S. Maloletkina — C. Sc. (Med.), endocrinologist of the Clinics of Endocrinology, assistant of the Department of Endocrinology No. 1, N.V. Sklifosovskiy Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8, Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0001-9881-5459.
Evgeniy V. Teplov — Head of the Department of Endocrinology, Kaluga Regional Clinical Hospital; 1, Vishnevskiy str., Kaluga, 248007, Russian Federation; ORCID iD 0000-0000-0000-0000.
Kristina S. Vavil’chenkova — endocrinologist of the Outpatient Department, Kaluga Regional Clinical Hospital; 1, Vishnevskiy str., Kaluga, 248007, Russian Federation; ORCID iD 0000-0000-0000-0000.
Irina V. Glinkina — C. Sc. (Med.), associate professor of the Department of Endocrinology No. 1, N.V. Sklifosovskiy Institute of Clinical Medicine, I.M. Sechenov First Moscow State Medical University (Sechenov University); 8 Build. 2, Trubetskaya str., Moscow, 119991, Russian Federation; ORCID iD 0000-0001-8505-5526.
Contact information: Marina F. Kalashnikova, e-mail: marina_kalash@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 31.07.2023.
Revised 21.08.2023.
Accepted 11.09.2023.
Информация с rmj.ru