Содержание статьи
Введение
Сердечно-сосудистые заболевания (ССЗ) являются основной причиной смертности во всем мире, включая и Республику Беларусь (РБ) [1]. Особенности образа жизни и различные факторы риска обусловливают высокую распространенность данной группы заболеваний.
В основе ССЗ лежит атеросклероз, ведущую роль в развитии которого играет дисфункция эндотелия (ДЭ) и дислипидемия. Сосудистый эндотелий является основной мишенью для множества факторов риска, большая часть из которых относится к модифицируемым. Дислипидемия — один из наиболее мощных факторов риска развития ДЭ [2]. Учитывая распространенное мнение о ДЭ как о самой ранней стадии атеросклероза [3], необходимо проводить лабораторные и инструментальные исследования для лучшего понимания функций эндотелия с последующей возможностью ранней профилактики ССЗ.
Нарушения липидного обмена имеют большое значение в развитии атеросклероза. Гиперхолестеринемия запускает механизм атерогенеза, началом которого является ДЭ с последующим каскадом событий [4]. Развитию дислипидемии может способствовать избыточное потребление насыщенных жирных кислот (НЖК). Согласно «Требованиям к продовольственному сырью и пищевым продуктам» в РБ доля НЖК в питании должна составлять не более 10% калорийности от общего дневного рациона, что соответствует примерно 15 г в сутки (постановление МЗ РБ от 21 июня 2013 г. № 52). При наличии гиперхолестеринемии потребление НЖК следует снижать более интенсивно (<7% от потребляемой калорийности). Однако в РБ, как и во многих странах, потребление НЖК превосходит рекомендуемые нормы. Метаанализ, выполненный Q. Wang et al. [5], показал, что избыточное потребление НЖК повышает риск развития ишемической болезни сердца в возрасте 25–34 лет на 19% (относительный риск 1,19, 95% доверительный интервал 1,09–1,30).
В исследовании STEPS в 2016 г. [6] в РБ гиперхолестеринемия диагностирована у 11,2% респондентов в возрасте 18–29 лет. К сожалению, в 2020 г. отмечена тенденция к росту дислипидемии, которая диагностирована уже у 15,8% респондентов (18,9% мужчин и 11,9% женщин) данной возрастной группы [7]. Среди студентов-медиков гиперхолестеринемия была выявлена у 16,7% обследованных [8].
Хорошо известен факт влияния рациона питания на липидный состав плазмы крови. Наиболее наглядно это было продемонстрировано в исследовании «Северная Карелия» [9], в котором коррекция рациона питания привела к снижению уровня общего холестерина (ОХ) в крови с ≥6,5 ммоль/л до 5,2 ммоль/л.
В последнее десятилетие значительно возросло использование пальмового масла (ПМ) в продуктах питания. Являясь растительным маслом, оно приравнивается к животным жирам по высокому содержанию НЖК, 45% из которых составляет пальмитиновая кислота (C16:0) [10, 11]. По данным ряда исследований [12–14], избыточное потребление ПМ расценивается как фактор риска развития ССЗ. Согласно комплексному обзору метаанализов [15] замена масел, богатых полиненасыщенными жирными кислотами (ПНЖК), на ПМ значительно повышала уровень холестерина липопротеинов низкой плотности (ХС ЛПНП). Обзор ряда научных работ [16–18] также свидетельствует о том, что избыточное потребление ПМ увеличивает уровень ОХ и ХС ЛПНП.
Учитывая, что главной причиной, запускающей механизм атерогенеза, является ДЭ, которая формируется под влиянием многих факторов, важно учитывать влияние избыточного потребления насыщенных жиров на формирование дислипидемии и раннее развитие ДЭ с целью своевременной первичной профилактики атеросклероза у лиц молодого возраста.
Цель исследования: оценить изменения функции эндотелия сосудов и уровней липидов крови при дифференцированном потреблении сливочного (СМ) и ПМ у молодых здоровых добровольцев.
Материал и методы
В исследование было включено 137 молодых здоровых добровольцев в возрасте 20,1±0,6 года, которые обедали в столовой ГрГМУ. Критериями исключения являлись наличие хронических заболеваний сердечно-сосудистой системы, желудочно-кишечного тракта, сахарного диабета, и противопоказаний к использованию ПМ либо СМ.
Рандомно все добровольцы были разделены на 5 групп. Группа контроля (ГК) (n=34) не получала масло дополнительно, остальные 4 группы получали добавленное во второе блюдо масло 5 дней в неделю на протяжении 12 нед.: группа СМ (ГС) (n=30) — 25 г СМ, группа ПМ (ГП) (n=32) — 25 г ПМ, ГП-1 (n=20) — 15 г ПМ и ГП-2 (n=21) — 7,5 г ПМ.
Всем добровольцам проводилось стандартное физикальное обследование. Забор венозной крови в условиях процедурного кабинета проводился натощак при помощи вакуумных систем. Оценка показателей липидного профиля: ОХ, ХС ЛПНП, холестерина липопротеинов высокой плотности (ХС ЛПВП), триглицеридов (ТГ) проводилась с использованием реагентов компании «Диасенс» (РБ) на момент включения в исследование и через 12 нед. Коэффициент атерогенности (КА) рассчитывался по формуле: КА = ОХ — ЛПВП/ЛПВП.
Эндотелийзависимую вазодилатацию (ЭЗВД) оценивали при включении в исследование и при его завершении с помощью аппаратно-программного комплекса «Импекард-М» (РБ) путем проведения пробы с реактивной гиперемией реографическим методом. Вычисляли относительное изменение максимальной объемной скорости кровенаполнения (Δdz/dt, %) в течение 1 мин после декомпрессии. Δdz/dt>12% расценивали как референсное значение, значение Δdz/dt<12% — как проявление ДЭ [19]. Скорость распространения пульсовой волны (СРПВ) определялась автоматизированно (импедансным способом) в виде определения времени запаздывания периферической реовазограммы (лучевая артерия) относительно центральной (сонная артерия). СРПВ расценивалась как соответствующая норме, если ее значение не превышало 10,2 м/с, как повышенная — при значении >10,2 м/с [20, 21].
Статистический анализ полученных данных проводили с использованием пакета программ Statistica 10.0. Проверку на нормальность распределения проводили с помощью теста Колмогорова — Смирнова и критерия Лиллиефорса (при p<0,05 распределение признака считали отличающимся от нормального). Полученные результаты представлены в виде среднего значения и стандартного отклонения (M±SD) при нормальном распределении, в виде медианы и нижнего и верхнего квартилей (Ме (LQ; UQ)) при распределении, отличающемся от нормального. Две независимые группы сравнивали с помощью U-критерия Манна — Уитни. Проводился непараметрический корреляционный анализ по Спирмену. Различия считали статистически значимыми при p≤0,05.
Результаты исследования
Исходно группы обследованных были сопоставимы по ЭЗВД, СРПВ и частоте сердечных сокращений (ЧСС) (см. таблицу). После 12 нед. наблюдения ЭЗВД стала достоверно хуже в группах ГС (p=0,017) и ГП (p=0,018) по сравнению с исходной величиной, но между группами не различалась. В группах ГК, ГП-1 и ГП-2 ЭЗВД достоверно не изменилась (p>0,05). Динамика снижения ЭЗВД была наибольшей в группе ГП, однако достоверно не отличалась от ГС. Исходно ДЭ установлена у 56% обследованных в ГК, у 63% в ГС, у 59% в ГП, у 87% в ГП-1 и у 86% в ГП-2. При измерении через 12 нед. ДЭ выявлена у 97% обследованных ГК, а также ГП и ГС, у 65% в ГП-1 и у 71% в ГП-2. В ГК, ГС и ГП при контрольном обследовании ДЭ встречалась достоверно (p<0,05) чаще, чем в ГП-1. СРПВ и ЧСС в анализируемых группах достоверно не изменились (p>0,05) после 12 нед. наблюдения. Величина СРПВ и ее динамика, а также ЧСС в группах после 12 нед. наблюдения не различалась (p>0,05).
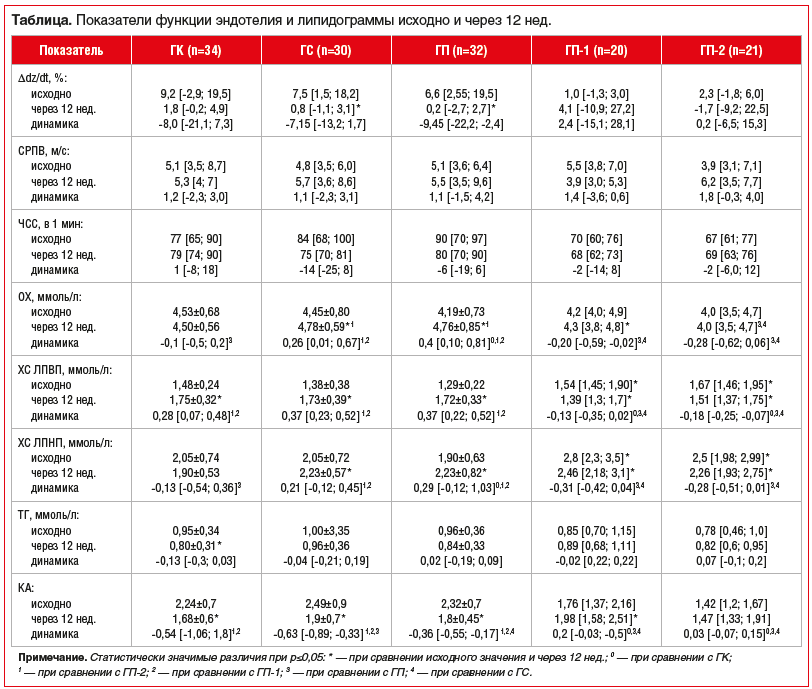
Исходно группы обследованных были сопоставимы по уровню ОХ и ТГ. Уровень ХС ЛПВП и ЛПНП был ниже (p<0,05) в ГП по сравнению с ГП-1 и ГП-2.
Через 12 нед. наблюдения повышение уровней ОХ, ХС ЛПНП и ХС ЛПВП (p<0,05) по сравнению с исходными значениями произошло в ГП и ГС. Увеличение уровня ХС ЛПВП (р<0,05) зафиксировано в ГК. В ГП-1 произошло повышение уровня ОХ (p<0,05), снижение уровней ХС ЛПВП и ХС ЛПНП (р<0,05). Изменений уровня ОХ в ГК и ГП-2 (p>0,05) не наблюдалось. Уровень ТГ не изменился (p>0,05) в группах, получавших нагрузку как ПМ, так и СМ, но стал ниже в ГК (р<0,05). Уровень ОХ на момент завершения исследования был ниже (р<0,05) в ГП-2 по сравнению с ГС и ГП. Уровень ХС ЛПНП был ниже (р<0,05) в ГК по сравнению с ГП-1.
Через 12 нед. наблюдения динамика уровня ОХ в крови была наибольшей в ГП. В ГС динамика ОХ была достоверно (р<0,05) больше, чем в ГП-1 и ГП-2. Динамика уровня ХС ЛПВП была достоверно ниже в группах ГП-1 и ГП-2 по сравнению с группами ГК, ГС и ГП. Динамика ХС ЛПНП была наибольшей в ГП и достоверно различалась с группами ГК, ГП-1 и ГП-2. Уровень ТГ снизился в группах ГК, ГС и ГП-1. Прирост уровня ТГ был выявлен в ГП и ГП-2. Различий в динамике уровня ТГ в исследуемых группах не установлено (p>0,05). КА достоверно повысился в ГП-1 и снизился в группах ГК, ГС, ГП (вероятно, за счет повышения уровня ХС ЛПВП).
В группе ГП-1 получена отрицательная корреляционная связь между уровнем ОХ, измеренным через 12 нед., и ЭЗВД (R=-0,57, р=0,03). Это свидетельствует о негативном влиянии повышенного уровня ОХ на функцию эндотелия даже у лиц молодого возраста. Вместе с тем отсутствие взаимосвязей при обследовании через 12 нед. в ГП можно объяснить полифакторностью развития ДЭ.
Для установления количества ПМ, свыше которого прогнозируется рост показателей липидограммы, был выполнен регрессионный анализ. В результате получено, что потребление 15,03 г и более ПМ в сутки может приводить к росту уровня ОХ (R2=0,31; F(1,64)=0,48; p<0,000001), потребление 15,43 г и более ПМ в сутки — к росту уровня ХС ЛПНП (R2=0,10; F(1,66)=7,45; p<0,008). Однако потребление 14,9 г и более ПМ в сутки может повышать уровень ХС ЛПВП (R2=0,50; F(1,66)=65,08; p<0,0000001).
Обсуждение
Повышение показателей ОХ, ХС ЛПНП у здоровых добровольцев при потреблении как СМ, так и ПМ позволяет нам расценивать эти масла как фактор развития дислипид-емии. Полученные нами данные схожи с результатами 2 исследований [22, 23], включавших суммарно 636 151 участника и продемонстрировавших, что жиры, находящиеся в СМ, приводят к повышению уровня ХС ЛПНП. Аналогичные данные имеются и относительно потребления ПМ — выявлено повышение уровней ОХ и ХС ЛПНП в сыворотке крови у лиц, потреблявших ПМ [12, 13]. В еще одном исследовании [9], сравнивавшем влияние ПМ и подсолнечного масла на показатели липидограммы, было подтверждено увеличение уровней ОХ, ХС ЛПНП и ЛПВП в группах, потреблявших ПМ. Согласно данным M.P. Bonham et al. [24], изучавших влияние применения ПМ и рапсового масла, было показано, что потребление ПМ приводило к повышению уровня ХС ЛПНП и ЛПВП в плазме крови, что согласуется с нашими данными.
В исследовании [25], оценивающем эффект потребления 3 различных растительных масел (оливкового, соевого и ПМ), не было выявлено различий в неблагоприятном воздействии приема данных жиров на функцию эндотелия сосудов, однако все они вызывали повышение уровня ТГ в плазме крови у здоровых людей. С учетом того, что дислипидемия лежит в основе развития ДЭ, представляется целесообразным и необходимым проводить превентивную профилактику у молодых лиц, избыточно потребляющих насыщенные жиры.
Заключение
Избыточное (25 г) потребление в сутки СМ либо ПМ на протяжении 12 нед. здоровыми добровольцами способствует ухудшению ЭЗВД на фоне достоверного повышения уровней ОХ, ХС ЛПНП и ЛПВП. При ежедневном употреблении ПМ в количестве 15 г уровень ОХ в крови отрицательно взаимосвязан с ЭЗВД, что можно расценивать как фактор риска формирования ДЭ.
Ежедневное потребление ПМ на протяжении 12 нед. здоровыми молодыми людьми приводит к следующим изменениям в липидограмме: в количестве 14,9 г и более повышает уровень ХС ЛПВП, 15,0 г и более — уровень ХС ЛПНП, а 15,4 г и более — уровень ОХ в плазме крови. Наибольший прирост уровня ХС ЛПНП отмечен при потреблении ПМ в количестве 25 г в день.
Информация с rmj.ru






